文档内容
第 39 讲 反应热的测定与计算
[复习目标] 1.了解中和反应反应热测定的原理及操作。2.掌握盖斯定律的内容及意义,并
能进行有关反应热的计算。
考点一 中和反应反应热的测定
1.概念
在25 ℃和101 kPa下,在稀溶液中,强酸和强碱发生中和反应生成____________时所放出
的热量。
2.测定原理
ΔH=-
c=4.18 J·g-1·℃-1=4.18×10-3 kJ·g-1·℃-1;n为生成HO的物质的量。稀溶液的密度用
2
1 g·mL-1进行计算。
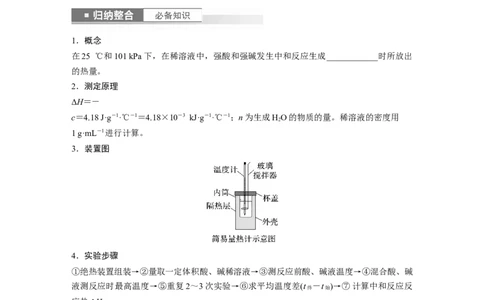
3.装置图
4.实验步骤
①绝热装置组装→②量取一定体积酸、碱稀溶液→③测反应前酸、碱液温度→④混合酸、碱
液测反应时最高温度→⑤重复2~3次实验→⑥求平均温度差(t -t )→⑦计算中和反应反
终 始
应热ΔH。
思考 (1)在中和反应反应热的测定实验中,使用弱酸或弱碱会使测得的中和反应反应热数
值 ________( 填 “ 偏 高 ” “ 不 变 ” 或 “ 偏 低 ” ) , 其 原 因 是
________________________________
_______________________________________________________________________________
。
(2)有两组实验:①50 mL 0.50 mol·L-1盐酸和50 mL 0.55 mol·L-1NaOH溶液,②60 mL 0.50
mol·
L-1盐酸和50 mL 0.55 mol·L-1NaOH溶液。实验①②反应放出的热量______(填“相等”或“不相等”,下同),测得的中和反应反应热_______________________________________,
原因是________________________________________________________________________
________________________________________________________________________。
1.已知H+(aq)+OH-(aq)===HO(l) ΔH=-57.3 kJ·mol-1,则HSO 和Ba(OH) 反应的ΔH
2 2 4 2
=2×(-57.3) kJ·mol-1( )
2.在测定中和反应反应热的实验中,应把NaOH溶液分多次倒入( )
3.为测定反应H+(aq)+OH-(aq)===HO(l)的ΔH,也可以选用0.1 mol·L-1NaHSO 溶液和
2 4
0.1 mol·L-1 NaOH溶液进行实验( )
4.实验时可用铜丝搅拌器代替玻璃搅拌器( )
1.中和反应是放热反应,下列关于中和反应反应热测定的说法错误的是( )
A.等温条件下,试管中进行的中和反应,反应体系向空气中释放的热量就是反应的热效应
B.测定中和反应反应热时,需要快速的将两种溶液混合
C.测定中和反应反应热时,最重要的是要保证实验装置的隔热效果
D.不同的酸碱反应生成1 mol液态水释放的热量可能不相同
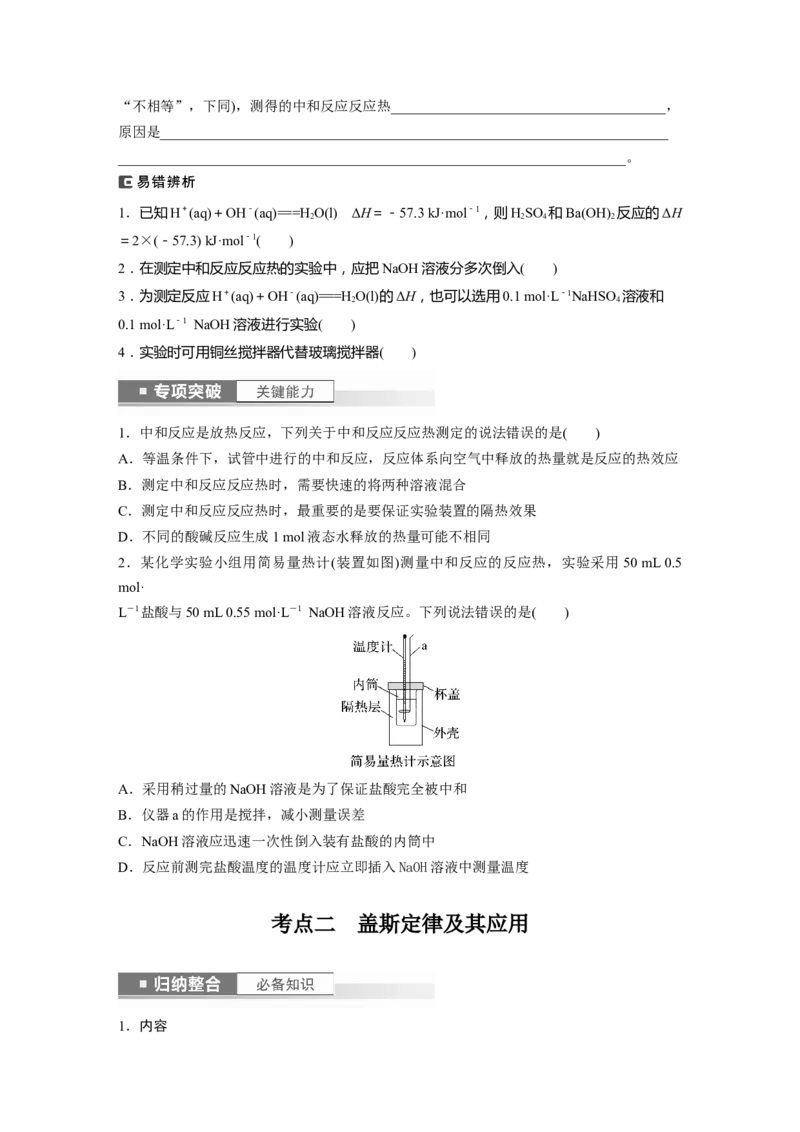
2.某化学实验小组用简易量热计(装置如图)测量中和反应的反应热,实验采用 50 mL 0.5
mol·
L-1盐酸与50 mL 0.55 mol·L-1 NaOH溶液反应。下列说法错误的是( )
A.采用稍过量的NaOH溶液是为了保证盐酸完全被中和
B.仪器a的作用是搅拌,减小测量误差
C.NaOH溶液应迅速一次性倒入装有盐酸的内筒中
D.反应前测完盐酸温度的温度计应立即插入NaOH溶液中测量温度
考点二 盖斯定律及其应用
1.内容一个化学反应,不管是一步完成的还是分几步完成的,其反应热是相同的。即化学反应的反
应热只与反应体系的____________有关,而与____________无关。
2.意义
间接计算某些反应的反应热。
3.应用
转化关系 反应热间的关系
aA――→B;A――→B ΔH=____________
1
AB ΔH=________
1
ΔH=____________
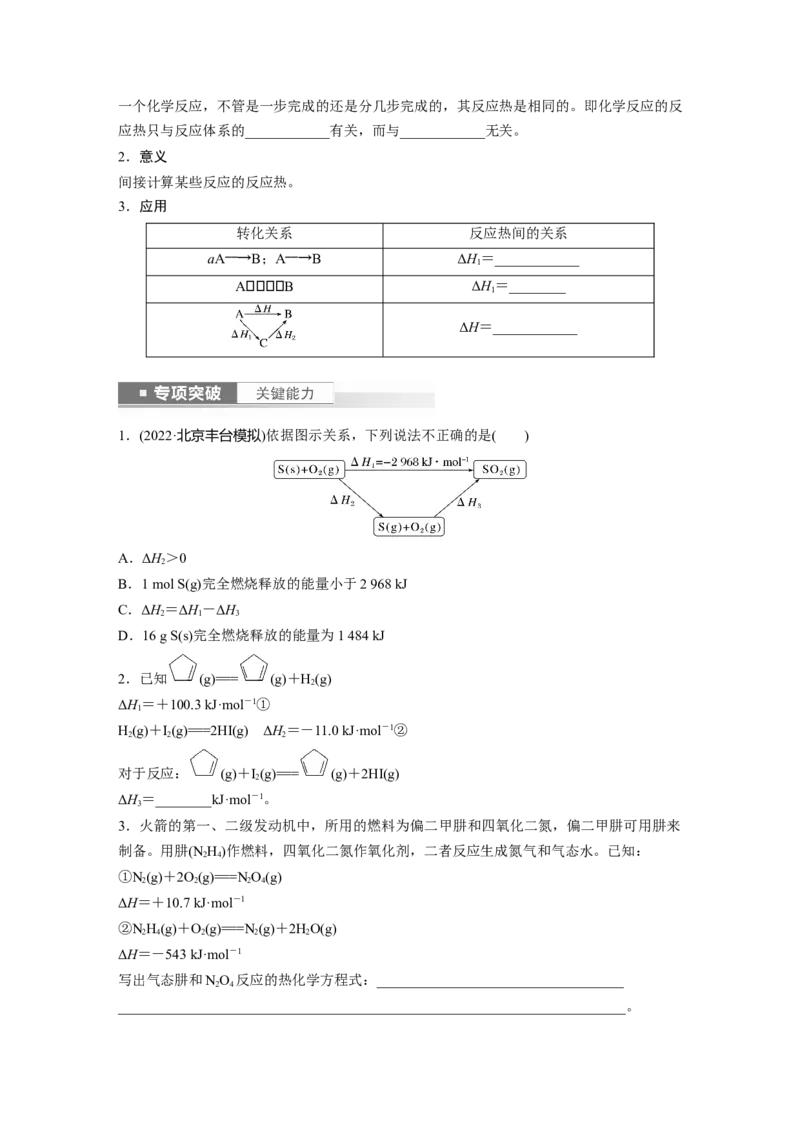
1.(2022·北京丰台模拟)依据图示关系,下列说法不正确的是( )
A.ΔH>0
2
B.1 mol S(g)完全燃烧释放的能量小于2 968 kJ
C.ΔH=ΔH-ΔH
2 1 3
D.16 g S(s)完全燃烧释放的能量为1 484 kJ
2.已知 (g)=== (g)+H(g)
2
ΔH=+100.3 kJ·mol-1①
1
H(g)+I(g)===2HI(g) ΔH=-11.0 kJ·mol-1②
2 2 2
对于反应: (g)+I(g)=== (g)+2HI(g)
2
ΔH=________kJ·mol-1。
3
3.火箭的第一、二级发动机中,所用的燃料为偏二甲肼和四氧化二氮,偏二甲肼可用肼来
制备。用肼(N H)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
2 4
①N(g)+2O(g)===NO(g)
2 2 2 4
ΔH=+10.7 kJ·mol-1
②NH(g)+O(g)===N(g)+2HO(g)
2 4 2 2 2
ΔH=-543 kJ·mol-1
写出气态肼和NO 反应的热化学方程式:___________________________________
2 4
________________________________________________________________________。“三步”确定热化学方程式或ΔH
考点三 反应热大小的比较
1.根据反应物量的大小关系比较反应焓变的大小
①H(g)+O(g)===HO(g) ΔH
2 2 2 1
②2H(g)+O(g)===2HO(g) ΔH
2 2 2 2
反应②中H 的量更多,因此放热更多,|ΔH|<|ΔH|,但ΔH<0,ΔH<0,故ΔH____ΔH。
2 1 2 1 2 1 2
2.根据反应进行的程度大小比较反应焓变的大小
③C(s)+O(g)===CO(g) ΔH
2 3
④C(s)+O(g)===CO(g) ΔH
2 2 4
反应④中,C完全燃烧,放热更____,|ΔH|<|ΔH|,但ΔH<0,ΔH<0,故ΔH____ΔH。
3 4 3 4 3 4
3.根据反应物或生成物的状态比较反应焓变的大小
⑤S(g)+O(g)===SO (g) ΔH
2 2 5
⑥S(s)+O(g)===SO (g) ΔH
2 2 6
方法一:图像法,画出上述两反应能量随反应过程的变化曲线。
由图像可知:|ΔH|>|ΔH|,但ΔH<0,ΔH<0,故ΔH____ΔH。
5 6 5 6 5 6
方法二:通过盖斯定律构造新的热化学方程式。
由反应⑤-反应⑥可得S(g)===S(s) ΔH=ΔH-ΔH<0,故ΔH____ΔH。
5 6 5 6
4.根据特殊反应的焓变情况比较反应焓变的大小⑦2Al(s)+O(g)===Al O(s) ΔH
2 2 3 7
⑧2Fe(s)+O(g)===Fe O(s) ΔH
2 2 3 8
由反应⑦-反应⑧可得2Al(s)+Fe O(s)===2Fe(s)+Al O(s) ΔH=ΔH -ΔH ,已知铝热反
2 3 2 3 7 8
应为________,故ΔH<0,ΔH<ΔH。
7 8
1.(2022·石家庄模拟)已知几种离子反应的热化学方程式如下:
①H++OH-===HO(l) ΔH;
2 1
②Ba2++SO===BaSO(s) ΔH;
4 2
③NH ·H O+H+===NH+HO(l) ΔH;
3 2 2 3
④Ba2++2OH-+2H++SO===BaSO(s)+2HO ΔH。
4 2 4
下列有关判断正确的是( )
A.ΔH>0,ΔH<0 B.ΔH<ΔH
2 3 2 4
C.ΔH<ΔH+ΔH D.ΔH>ΔH
4 1 2 1 3
2.室温下,将1 mol的CuSO ·5H O(s)溶于水会使溶液温度降低,热效应为ΔH ,将1 mol
4 2 1
的CuSO (s)溶于水会使溶液温度升高,热效应为 ΔH ;CuSO ·5H O受热分解的化学方程式
4 2 4 2
为CuSO ·5H O(s)===CuSO (s)+5HO(l),热效应为ΔH。下列判断正确的是( )
4 2 4 2 3
A.ΔH>ΔH B.ΔH<ΔH
2 3 1 3
C.ΔH+ΔH=ΔH D.ΔH+ΔH>ΔH
1 3 2 1 2 3
3.对于反应a:C H(g)C H(g)+H(g),反应b:2CH(g)C H(g)+2H(g),当升高温
2 4 2 2 2 4 2 4 2
度时平衡都向右移动。①C(s)+2H(g)===CH(g) ΔH ;②2C(s)+H(g)===C H(g) ΔH ;
2 4 1 2 2 2 2
③2C(s)+2H(g)===C H(g) ΔH 。则①②③中ΔH 、ΔH 、ΔH 的大小顺序排列正确的是(
2 2 4 3 1 2 3
)
A.ΔH>ΔH>ΔH
1 2 3
B.ΔH>ΔH>2ΔH
2 3 1
C.ΔH>2ΔH>ΔH
2 1 3
D.ΔH>ΔH>ΔH
3 2 1
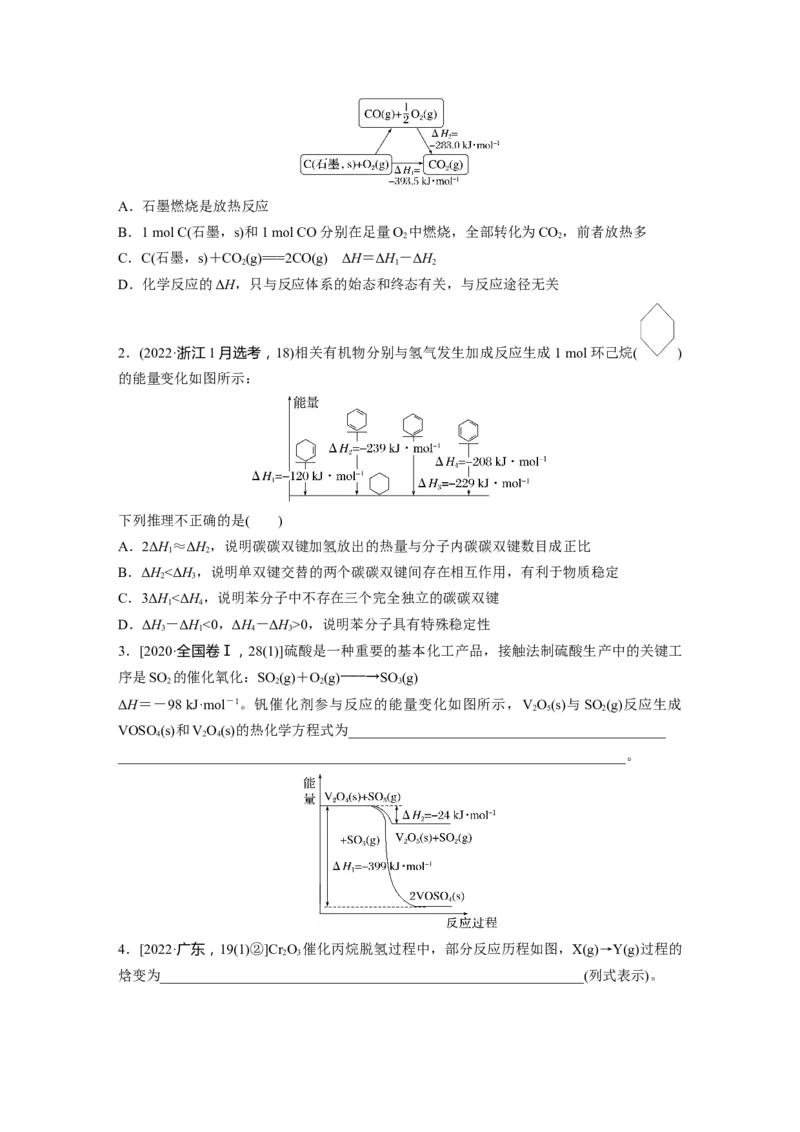
1.(2020·北京,12)依据图示关系,下列说法不正确的是( )A.石墨燃烧是放热反应
B.1 mol C(石墨,s)和1 mol CO分别在足量O 中燃烧,全部转化为CO,前者放热多
2 2
C.C(石墨,s)+CO(g)===2CO(g) ΔH=ΔH-ΔH
2 1 2
D.化学反应的ΔH,只与反应体系的始态和终态有关,与反应途径无关
2.(2022·浙江1月选考,18)相关有机物分别与氢气发生加成反应生成1 mol环己烷( )
的能量变化如图所示:
下列推理不正确的是( )
A.2ΔH≈ΔH,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
1 2
B.ΔH<ΔH,说明单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定
2 3
C.3ΔH<ΔH,说明苯分子中不存在三个完全独立的碳碳双键
1 4
D.ΔH-ΔH<0,ΔH-ΔH>0,说明苯分子具有特殊稳定性
3 1 4 3
3.[2020·全国卷Ⅰ,28(1)]硫酸是一种重要的基本化工产品,接触法制硫酸生产中的关键工
序是SO 的催化氧化:SO (g)+O(g)――――→SO (g)
2 2 2 3
ΔH=-98 kJ·mol-1。钒催化剂参与反应的能量变化如图所示,VO(s)与SO (g)反应生成
2 5 2
VOSO(s)和VO(s)的热化学方程式为_____________________________________________
4 2 4
________________________________________________________________________。
4.[2022·广东,19(1)②]Cr O 催化丙烷脱氢过程中,部分反应历程如图,X(g)→Y(g)过程的
2 3
焓变为____________________________________________________________(列式表示)。5.[2022·湖北,19(1)]已知:
①CaO(s)+HO(l)Ca(OH) (s) ΔH=-65.17 kJ·mol-1
2 2 1
②Ca(OH) (s)Ca2+(aq)+2OH-(aq) ΔH=-16.73 kJ·mol-1
2 2
③Al(s)+OH-(aq)+3HO(l)[Al(OH) ]-(aq)+H(g) ΔH=-415.0 kJ·mol-1
2 4 2 3
则CaO(s)+2Al(s)+7HO(l)===Ca2+(aq)+2[Al(OH) ]-(aq)+3H(g)的ΔH =_______kJ·mol-
2 4 2 4
1。