文档内容
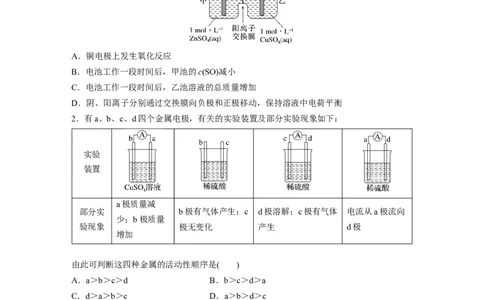
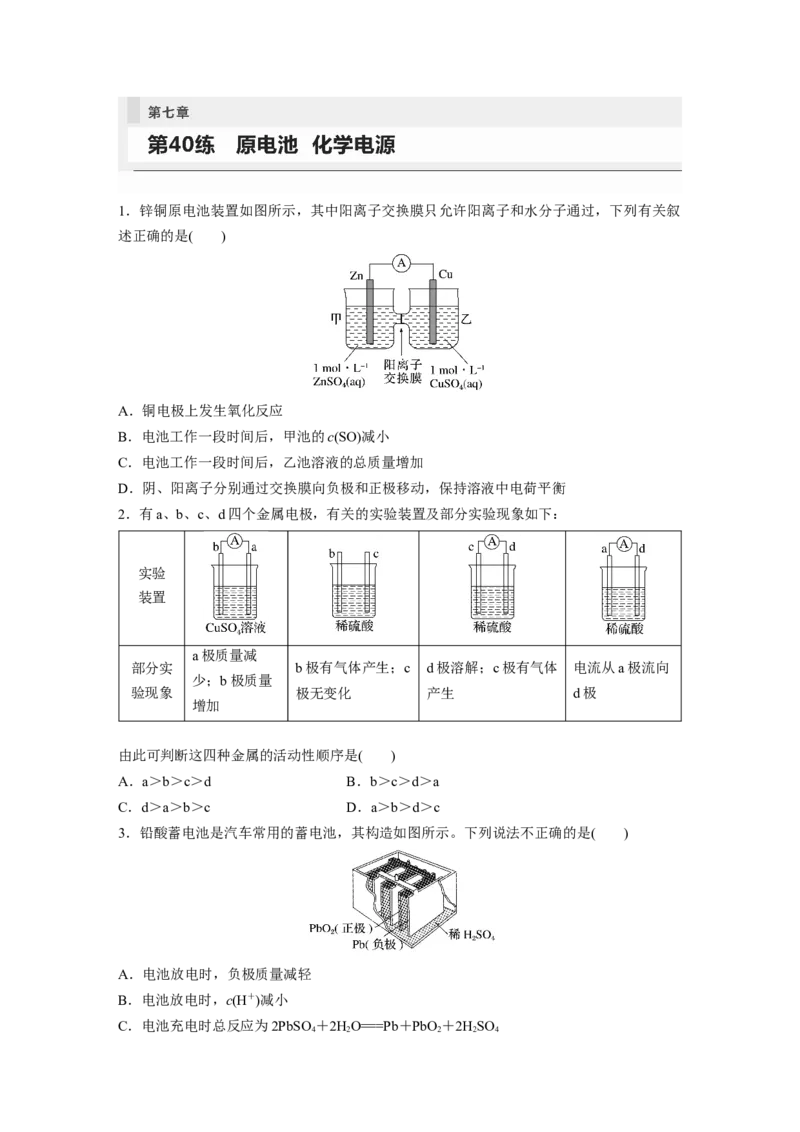
1.锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙
述正确的是( )
A.铜电极上发生氧化反应
B.电池工作一段时间后,甲池的c(SO)减小
C.电池工作一段时间后,乙池溶液的总质量增加
D.阴、阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
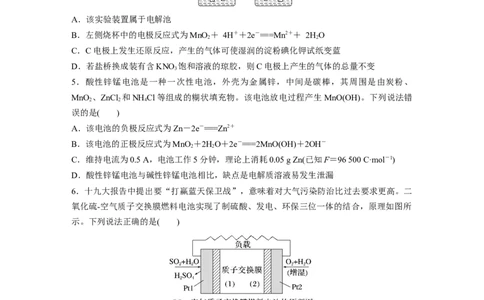
2.有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
实验
装置
a极质量减
部分实 b极有气体产生;c d极溶解;c极有气体 电流从a极流向
少;b极质量
验现象 极无变化 产生 d极
增加
由此可判断这四种金属的活动性顺序是( )
A.a>b>c>d B.b>c>d>a
C.d>a>b>c D.a>b>d>c
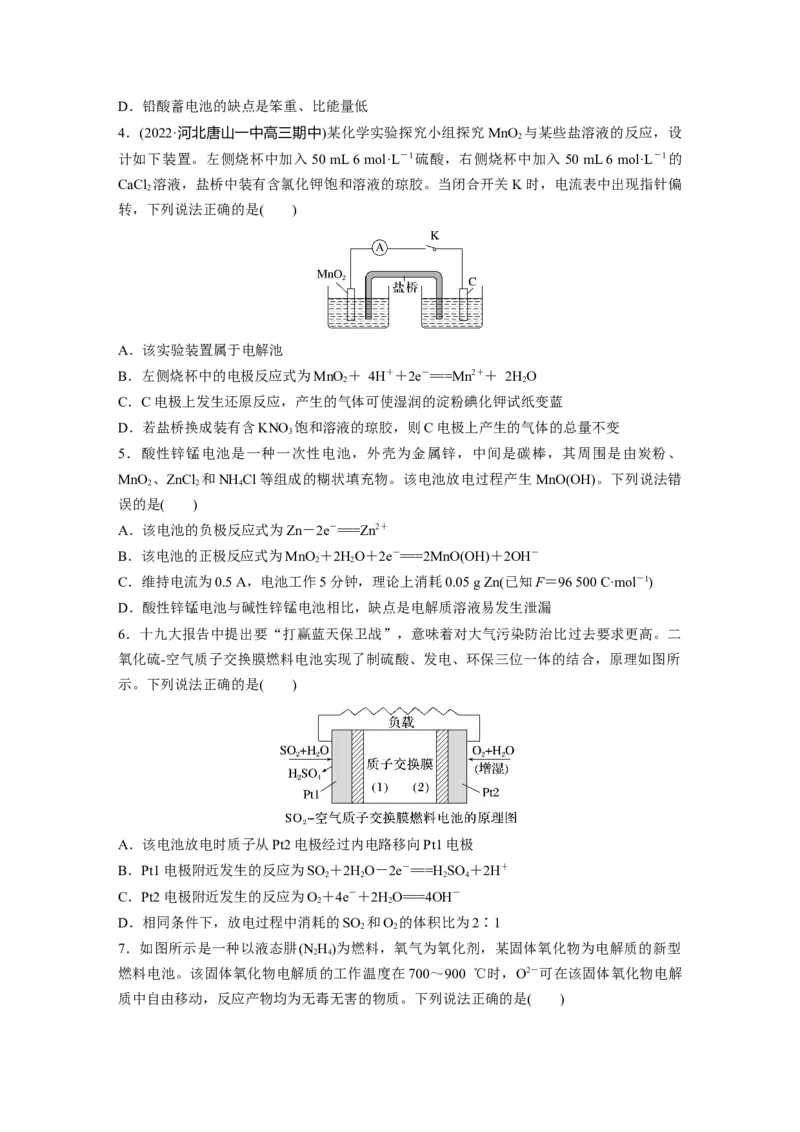
3.铅酸蓄电池是汽车常用的蓄电池,其构造如图所示。下列说法不正确的是( )
A.电池放电时,负极质量减轻
B.电池放电时,c(H+)减小
C.电池充电时总反应为2PbSO +2HO===Pb+PbO +2HSO
4 2 2 2 4D.铅酸蓄电池的缺点是笨重、比能量低
4.(2022·河北唐山一中高三期中)某化学实验探究小组探究MnO 与某些盐溶液的反应,设
2
计如下装置。左侧烧杯中加入 50 mL 6 mol·L-1硫酸,右侧烧杯中加入50 mL 6 mol·L-1的
CaCl 溶液,盐桥中装有含氯化钾饱和溶液的琼胶。当闭合开关K时,电流表中出现指针偏
2
转,下列说法正确的是( )
A.该实验装置属于电解池
B.左侧烧杯中的电极反应式为MnO + 4H++2e-===Mn2++ 2HO
2 2
C.C电极上发生还原反应,产生的气体可使湿润的淀粉碘化钾试纸变蓝
D.若盐桥换成装有含KNO 饱和溶液的琼胶,则C电极上产生的气体的总量不变
3
5.酸性锌锰电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是由炭粉、
MnO 、ZnCl 和NH Cl等组成的糊状填充物。该电池放电过程产生 MnO(OH)。下列说法错
2 2 4
误的是( )
A.该电池的负极反应式为Zn-2e-===Zn2+
B.该电池的正极反应式为MnO +2HO+2e-===2MnO(OH)+2OH-
2 2
C.维持电流为0.5 A,电池工作5分钟,理论上消耗0.05 g Zn(已知F=96 500 C·mol-1)
D.酸性锌锰电池与碱性锌锰电池相比,缺点是电解质溶液易发生泄漏
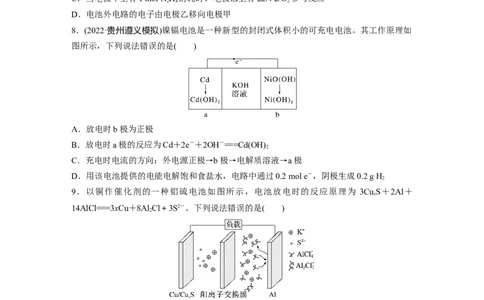
6.十九大报告中提出要“打赢蓝天保卫战”,意味着对大气污染防治比过去要求更高。二
氧化硫-空气质子交换膜燃料电池实现了制硫酸、发电、环保三位一体的结合,原理如图所
示。下列说法正确的是( )
A.该电池放电时质子从Pt2电极经过内电路移向Pt1电极
B.Pt1电极附近发生的反应为SO +2HO-2e-===HSO +2H+
2 2 2 4
C.Pt2电极附近发生的反应为O+4e-+2HO===4OH-
2 2
D.相同条件下,放电过程中消耗的SO 和O 的体积比为2∶1
2 2
7.如图所示是一种以液态肼(N H)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型
2 4
燃料电池。该固体氧化物电解质的工作温度在700~900 ℃时,O2-可在该固体氧化物电解
质中自由移动,反应产物均为无毒无害的物质。下列说法正确的是( )A.电池内的O2-由电极乙移向电极甲
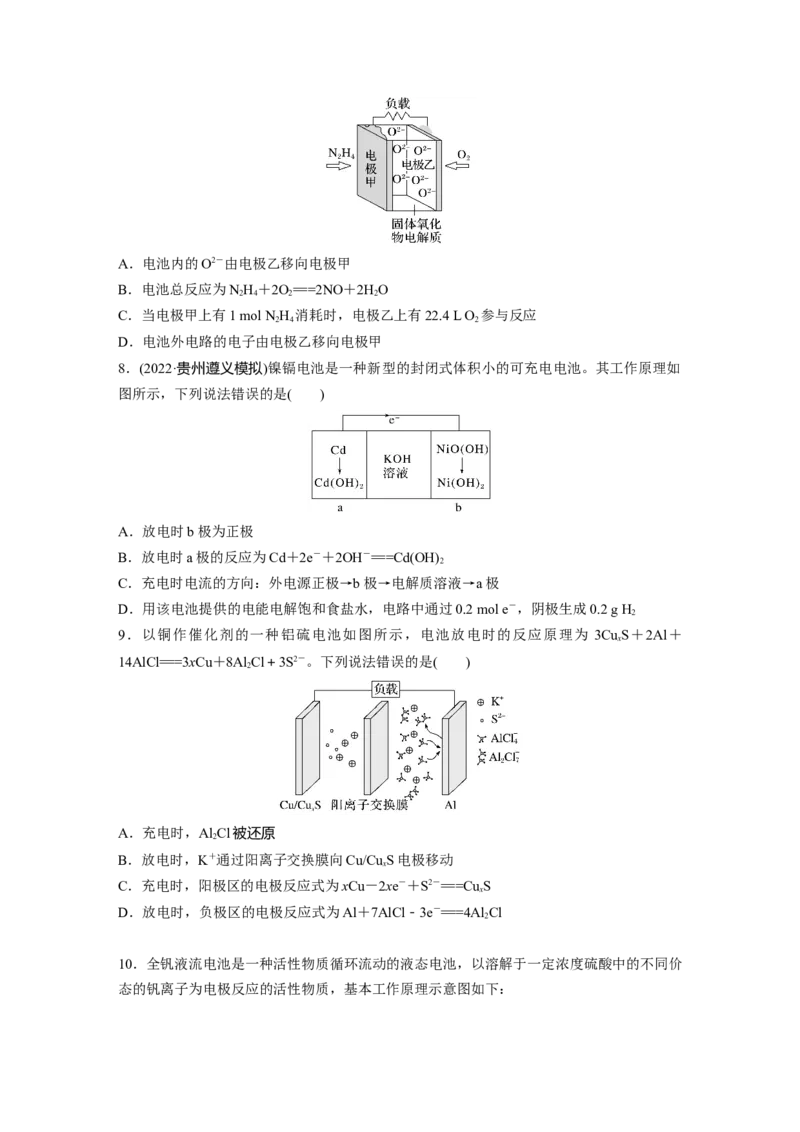
B.电池总反应为NH+2O===2NO+2HO
2 4 2 2
C.当电极甲上有1 mol N H 消耗时,电极乙上有22.4 L O 参与反应
2 4 2
D.电池外电路的电子由电极乙移向电极甲
8.(2022·贵州遵义模拟)镍镉电池是一种新型的封闭式体积小的可充电电池。其工作原理如
图所示,下列说法错误的是( )
A.放电时b极为正极
B.放电时a极的反应为Cd+2e-+2OH-===Cd(OH)
2
C.充电时电流的方向:外电源正极→b极→电解质溶液→a极
D.用该电池提供的电能电解饱和食盐水,电路中通过0.2 mol e-,阴极生成0.2 g H
2
9.以铜作催化剂的一种铝硫电池如图所示,电池放电时的反应原理为 3CuS+2Al+
x
14AlCl===3xCu+8Al Cl+3S2-。下列说法错误的是( )
2
A.充电时,Al Cl被还原
2
B.放电时,K+通过阳离子交换膜向Cu/CuS电极移动
x
C.充电时,阳极区的电极反应式为xCu-2xe-+S2-===CuS
x
D.放电时,负极区的电极反应式为Al+7AlCl-3e-===4Al Cl
2
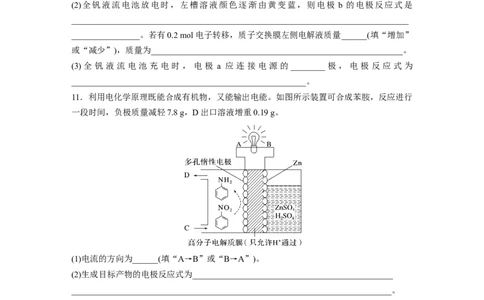
10.全钒液流电池是一种活性物质循环流动的液态电池,以溶解于一定浓度硫酸中的不同价
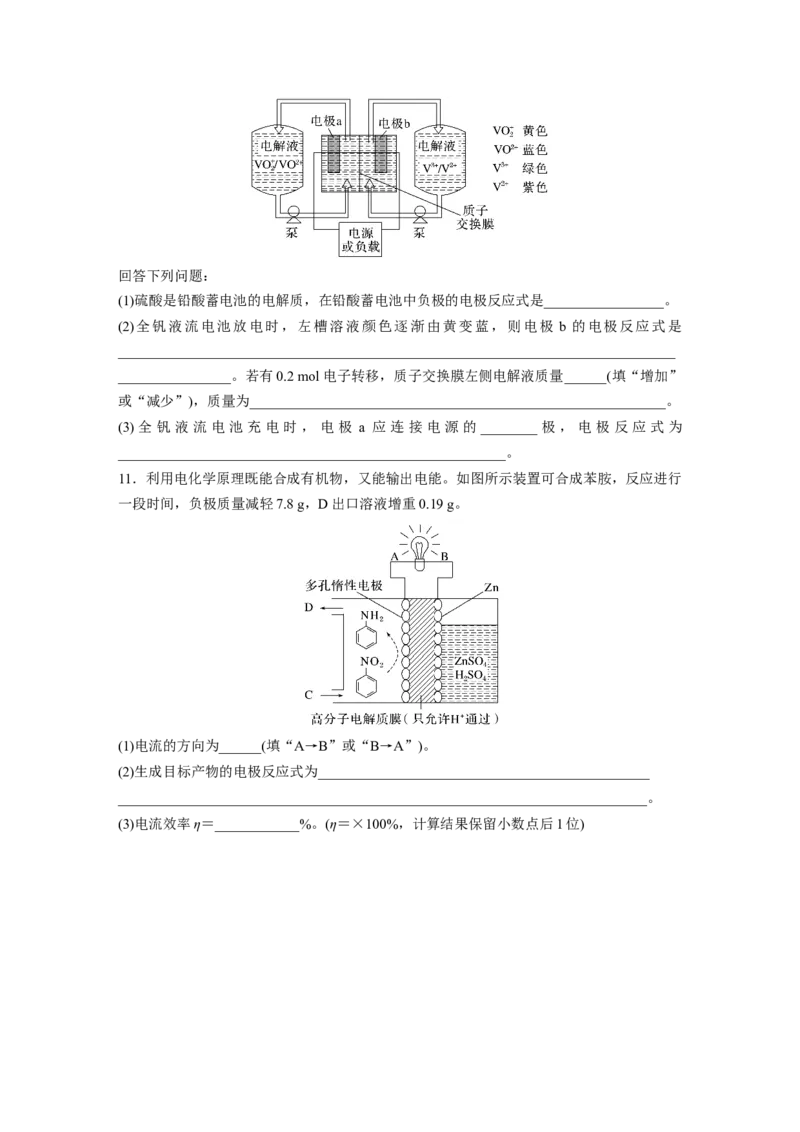
态的钒离子为电极反应的活性物质,基本工作原理示意图如下:回答下列问题:
(1)硫酸是铅酸蓄电池的电解质,在铅酸蓄电池中负极的电极反应式是_________________。
(2)全钒液流电池放电时,左槽溶液颜色逐渐由黄变蓝,则电极 b 的电极反应式是
_______________________________________________________________________________
________________。若有0.2 mol电子转移,质子交换膜左侧电解液质量______(填“增加”
或“减少”),质量为___________________________________________________________。
(3)全钒 液流电池充电时,电极 a 应连接 电源的________极,电极反应式为
_______________________________________________________。
11.利用电化学原理既能合成有机物,又能输出电能。如图所示装置可合成苯胺,反应进行
一段时间,负极质量减轻7.8 g,D出口溶液增重0.19 g。
(1)电流的方向为______(填“A→B”或“B→A”)。
(2)生成目标产物的电极反应式为_______________________________________________
___________________________________________________________________________。
(3)电流效率η=____________%。(η=×100%,计算结果保留小数点后1位)