文档内容
第 55 讲 溶液中“粒子”浓度关系
[复习目标] 1.理解电解质溶液中的电离平衡和水解平衡。2.掌握溶液中各组分之间的守恒
关系与大小比较。
(一)熟悉“两大理论”,贯通思维障碍
1.电离平衡
(1)弱电解质的电离是微弱的,电离产生的微粒都非常少,同时还要考虑水的电离,如氨水
中:NH ·H O、NH、OH-浓度的大小关系是____________________________________。
3 2
(2)多元弱酸的电离是分步进行的,其主要是第一级电离(第一级电离程度远大于第二级电
离)。如在HS溶液中:HS、HS-、S2-、H+的浓度大小关系是________________________。
2 2
2.水解平衡
(1)水解过程是微弱的。如 NH Cl溶液中:NH、Cl-、NH ·H O、H+的浓度大小关系是
4 3 2
__________________________________。
(2)多元弱酸酸根离子的水解是分步进行的,其主要是第一步水解,如在 NaCO 溶液中:
2 3
CO、HCO、HCO 的浓度大小关系应是____________________________________。
2 3
(二)巧用“三个守恒”,明确浓度关系
写出下列溶液中粒子守恒关系式
(1)Na CO 溶液
2 3
①元素质量守恒:________________________________________________________。
②电荷守恒:____________________________________________________________。
③质子守恒:____________________________________________________________。
(2)浓度均为0.1 mol·L-1 NH ·H O和NH Cl溶液等体积混合
3 2 4
①电荷守恒:____________________________________________________________。
②元素质量守恒:________________________________________________________。
(3)浓度为0.1 mol·L-1盐酸与0.1 mol·L-1 CHCOONa溶液等体积混合
3
①电荷守恒:____________________________________________________________。
②元素质量守恒:________________________________________________________。
(1)电荷守恒
电解质溶液必须保持电中性,即阴离子所带负电荷总数一定等于阳离子所带正电荷总数。
(2)元素质量守恒
变化前后某种元素的质量守恒。①单一元素守恒,如1 mol NH 通入水中形成氨水,就有n(NH )+n(NH ·H O)+n(NH)=
3 3 3 2
1 mol,即氮元素质量守恒。
②两元素守恒,如NaHCO 溶液中,c(Na+)=c(H CO)+c(HCO)+c(CO),即钠元素与碳元
3 2 3
素质量守恒。
(3)质子守恒
电解质溶液中,由于电离、水解等过程的发生,往往存在质子(H+)的转移,转移过程中质
子数量保持不变,称为质子守恒。
质子守恒的书写技巧:
①正盐溶液,用水溶液中得失质子相等比较简便。如 NaS水溶液中的质子转移情况图示如
2
下:
由图可得NaS水溶液中质子守恒式:c(H+)+2c(H S)+c(HS-)=c(OH-)
2 2
②酸式盐溶液及混合缓冲溶液,可以通过元素质量守恒和电荷守恒推出质子守恒表达式。
如NaHCO 溶液中元素质量守恒:c(Na+)=c(HCO)+c(H CO)+c(CO)①,
3 2 3
电荷守恒:c(Na+)+c(H+)=c(HCO)+c(OH-)+2c(CO)②,
将①代入②中,整理得质子守恒:c(H+)+c(H CO)=c(OH-)+c(CO)
2 3
一、单一溶液中粒子浓度的关系
1.0.1 mol·L-1的NH Cl溶液
4
(1)粒子种类:____________________________________________________________。
(2)离子浓度大小关系:____________________________________________________。
(3)元素质量守恒:________________________________________________________。
2.判断正误,错误的写出正确的关系式。
(1)0.1 mol·L-1 Na CO 溶液中:c(Na+)+c(H+)=c(HCO)+c(CO)+c(OH-)
2 3
________________________________________________________________________
(2)在NaSO 溶液中:c(Na+)=2c(SO)+c(HSO)+c(OH-)
2 3
________________________________________________________________________
(3)0.1 mol·L-1 NH HS溶液中:c(NH)<c(HS-)+c(H S)+c(S2-)
4 2
________________________________________________________________________
(4)0.2 mol·L-1 NH HCO 溶液(pH>7):c(NH)>c(H CO)>c(HCO)>c(NH ·H O)
4 3 2 3 3 2
________________________________________________________________________(5)室温下,0.1 mol·L-1 NH Fe(SO ) 溶液中存在:c(NH)+3c(Fe3+)>2c(SO)
4 4 2
________________________________________________________________________
3.(2022·广东摸底考试)次磷酸(H PO )是一种一元弱酸,与等浓度等体积的NaOH完全反
3 2
应后生成NaH PO ,下列叙述错误的是( )
2 2
A.NaH PO 的水溶液加水稀释,增大
2 2
B.HPO 溶液中存在电离平衡:HPO HPO+H+
3 2 3 2 2
C.NaH PO 溶液中:c(Na+)>c(H PO)>c(OH-)>c(H+)
2 2 2
D.NaH PO 溶液中存在:c(H PO)+c(OH-)=c(H+)+c(Na+)
2 2 2
二、混合溶液(缓冲溶液)中粒子浓度的关系判断
4.浓度均为0.1 mol·L-1的NaHCO 和NaCO 混合溶液
3 2 3
(1)电荷守恒:____________________________________________________________。
(2)元素质量守恒:________________________________________________________。
(3)离子浓度由大到小的顺序:______________________________________________
________________________________________________________________________。
5.常温下,NaOH和CHCOOH等浓度按1∶2体积比混合后pH<7
3
(1)溶液中粒子浓度的大小关系:____________________________________________
_____________________________________________________________(水分子除外)。
(2)电荷守恒:____________________________________________________________。
(3)元素质量守恒:________________________________________________________。
(4)质子守恒:____________________________________________________________。
6.判断正误,错误的写出正确的关系式。
(1)0.1 mol·L-1 NaOH 溶液和 0.1 mol·L-1 CHCOOH 溶液等体积混合后: c(Na
3
+)>c(CHCOO-)
3
>c(OH-)>c(H+)
________________________________________________________________________
(2)pH=3的盐酸和pH=11的氨水等体积混合:c(Cl-)>c(NH)>c(OH-)>c(H+)
________________________________________________________________________
(3)室温下,将浓度均为0.1 mol·L-1的氨水和NH Cl溶液等体积混合(pH=9.25):c(NH)+
4
c(H+)=c(NH ·H O)+c(OH-)
3 2
________________________________________________________________________
(4)室温下,将浓度均为 0.10 mol·L-1的HC O 和NaHC O 溶液等体积混合(pH=1.68,
2 2 4 2 4
HC O 为二元弱酸):c(H+)+c(H C O)=c(Na+)+c(C O)+c(OH-)
2 2 4 2 2 4 2
________________________________________________________________________
(5)0.1 mol·L-1NaC O 溶液与0.1 mol·L-1HCl溶液等体积混合(H C O 为二元弱酸):2c(C O)
2 2 4 2 2 4 2
+c(HC O)+c(OH-)=c(Na+)+c(H+)
2
________________________________________________________________________(6)向NH HSO 溶液中滴加NaOH溶液到恰好呈中性:c(Na+)>c(SO)>c(NH)>c(OH-)=
4 4
c(H+)
________________________________________________________________________
7.(2022·深圳七中月考)NaCONaHCO 缓冲溶液可以将溶液pH控制在9.16~10.83范围内,
2 3 3
25 ℃时,K (H CO)=4×10-7、K (H CO)=5×10-11,下列说法不正确的是( )
a1 2 3 a2 2 3
A.0.5 mol·L-1的NaCO 溶液pH约为12
2 3
B.pH=8的NaHCO 溶液中,水电离产生的c(OH-)=10-6 mol·L-1
3
C.0.1 mol·L-1的NaHCO 溶液中存在:c(HCO)>c(H CO)>c(CO)
3 2 3
D.pH=10的该缓冲溶液中存在:c(Na+)=c(CO)+c(HCO)+c(H CO)
2 3
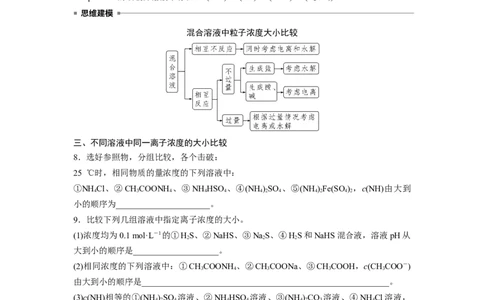
混合溶液中粒子浓度大小比较
三、不同溶液中同一离子浓度的大小比较
8.选好参照物,分组比较,各个击破:
25 ℃时,相同物质的量浓度的下列溶液中:
①NH Cl、②CHCOONH 、③NH HSO 、④(NH )SO 、⑤(NH )Fe(SO ) ,c(NH)由大到
4 3 4 4 4 4 2 4 4 2 4 2
小的顺序为______________________。
9.比较下列几组溶液中指定离子浓度的大小。
(1)浓度均为0.1 mol·L-1的①HS、②NaHS、③NaS、④HS和NaHS混合液,溶液pH从
2 2 2
大到小的顺序是____________________。
(2)相同浓度的下列溶液中:①CHCOONH 、②CHCOONa、③CHCOOH,c(CHCOO-)
3 4 3 3 3
由大到小的顺序是__________________________________________________________。
(3)c(NH)相等的①(NH )SO 溶液、②NH HSO 溶液、③(NH )CO 溶液、④NH Cl溶液,
4 2 4 4 4 4 2 3 4
其物质的量浓度由大到小的顺序为__________________________________________。
1.(2021·天津,10)常温下,下列有关电解质溶液的叙述正确的是( )
A.在0.1 mol·L-1 HPO 溶液中c(H PO )>c(H PO)>c(HPO)>c(PO)
3 4 3 4 2
B.在0.1 mol·L-1 Na C O 溶液中c(Na+)+c(H+)=c(OH-)+c(HC O)+c(C O)
2 2 4 2 2C.在0.1 mol·L-1 NaHCO 溶液中c(H CO)+c(HCO)=0.1 mol·L-1
3 2 3
D.氨水和NH Cl溶液混合,形成pH=9的溶液中c(Cl-)>c(NH)>c(OH-)>c(H+)
4
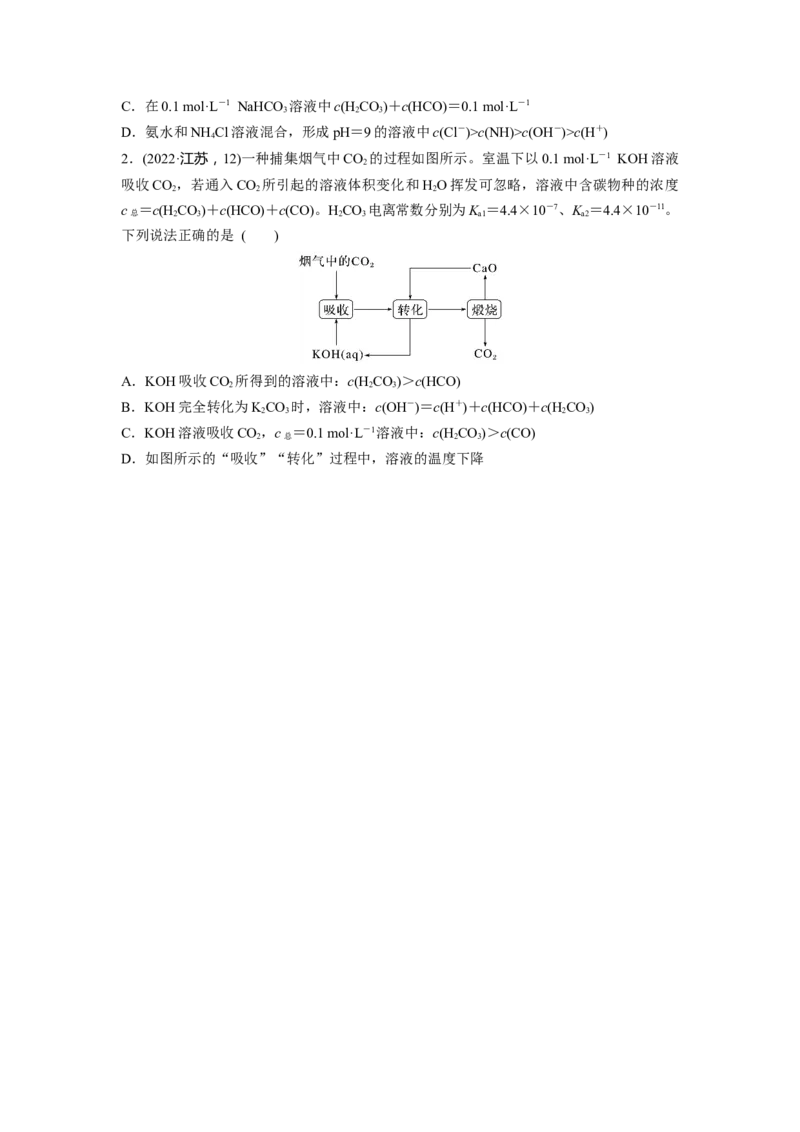
2.(2022·江苏,12)一种捕集烟气中CO 的过程如图所示。室温下以0.1 mol·L-1 KOH溶液
2
吸收CO ,若通入CO 所引起的溶液体积变化和HO挥发可忽略,溶液中含碳物种的浓度
2 2 2
c =c(H CO)+c(HCO)+c(CO)。HCO 电离常数分别为K =4.4×10-7、K =4.4×10-11。
总 2 3 2 3 a1 a2
下列说法正确的是 ( )
A.KOH吸收CO 所得到的溶液中:c(H CO)>c(HCO)
2 2 3
B.KOH完全转化为KCO 时,溶液中:c(OH-)=c(H+)+c(HCO)+c(H CO)
2 3 2 3
C.KOH溶液吸收CO,c =0.1 mol·L-1溶液中:c(H CO)>c(CO)
2 总 2 3
D.如图所示的“吸收”“转化”过程中,溶液的温度下降