文档内容
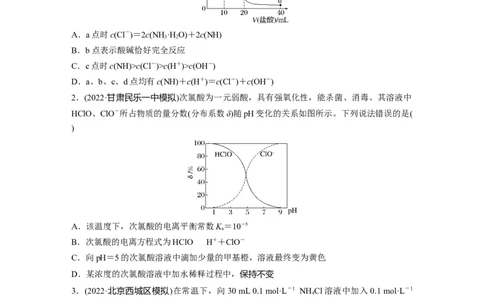
1.20 ℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1氨水的图像如图所示,下列说法正
确的是( )
A.a点时c(Cl-)=2c(NH ·H O)+2c(NH)
3 2
B.b点表示酸碱恰好完全反应
C.c点时c(NH)>c(Cl-)>c(H+)>c(OH-)
D.a、b、c、d点均有c(NH)+c(H+)=c(Cl-)+c(OH-)
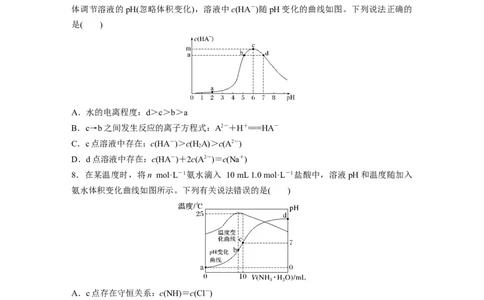
2.(2022·甘肃民乐一中模拟)次氯酸为一元弱酸,具有强氧化性,能杀菌、消毒。其溶液中
HClO、ClO-所占物质的量分数(分布系数δ)随pH变化的关系如图所示。下列说法错误的是(
)
A.该温度下,次氯酸的电离平衡常数K=10-5
a
B.次氯酸的电离方程式为HClOH++ClO-
C.向pH=5的次氯酸溶液中滴加少量的甲基橙,溶液最终变为黄色
D.某浓度的次氯酸溶液中加水稀释过程中,保持不变
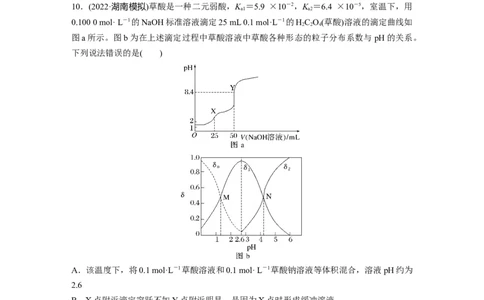
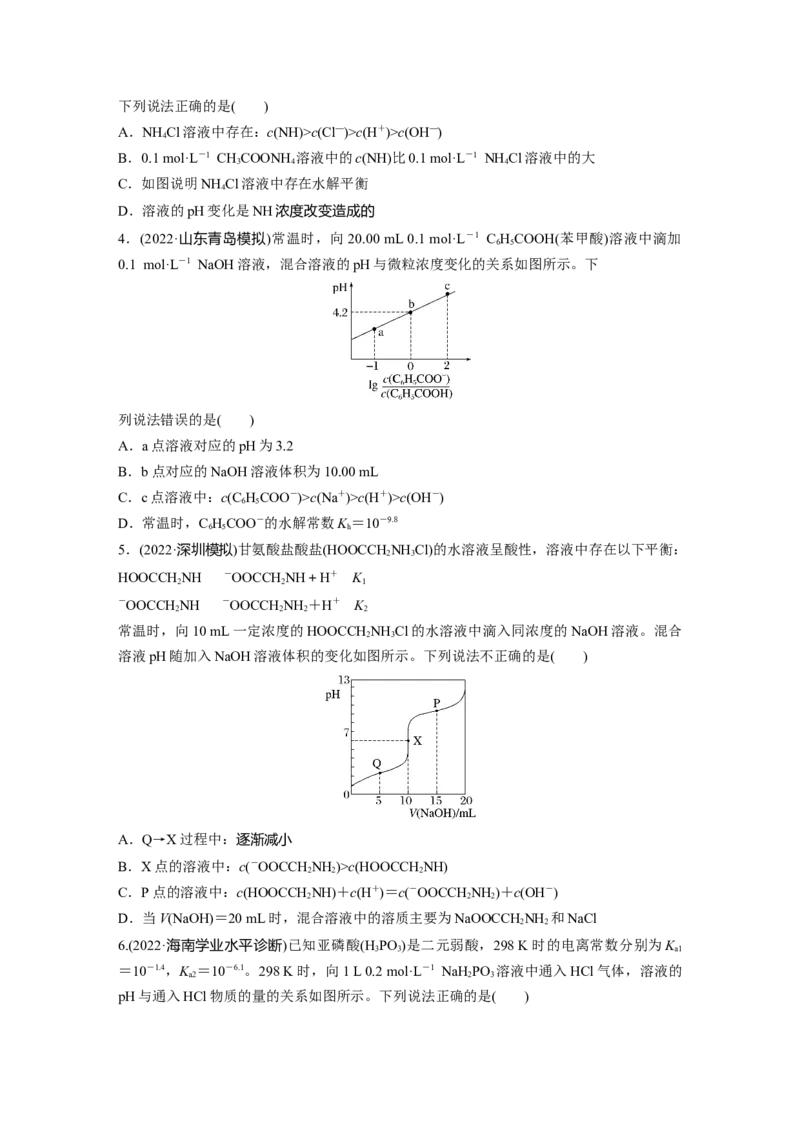
3.(2022·北京西城区模拟)在常温下,向30 mL 0.1 mol·L-1 NH Cl溶液中加入0.1 mol·L-1
4
CHCOONH 溶液,溶液的 pH 随加入 CHCOONH 溶液的体积的变化如图。已知:
3 4 3 4
CHCOONH 溶液的pH约为7。
3 4下列说法正确的是( )
A.NH Cl溶液中存在:c(NH)>c(Cl—)>c(H+)>c(OH—)
4
B.0.1 mol·L-1 CHCOONH 溶液中的c(NH)比0.1 mol·L-1 NH Cl溶液中的大
3 4 4
C.如图说明NH Cl溶液中存在水解平衡
4
D.溶液的pH变化是NH浓度改变造成的
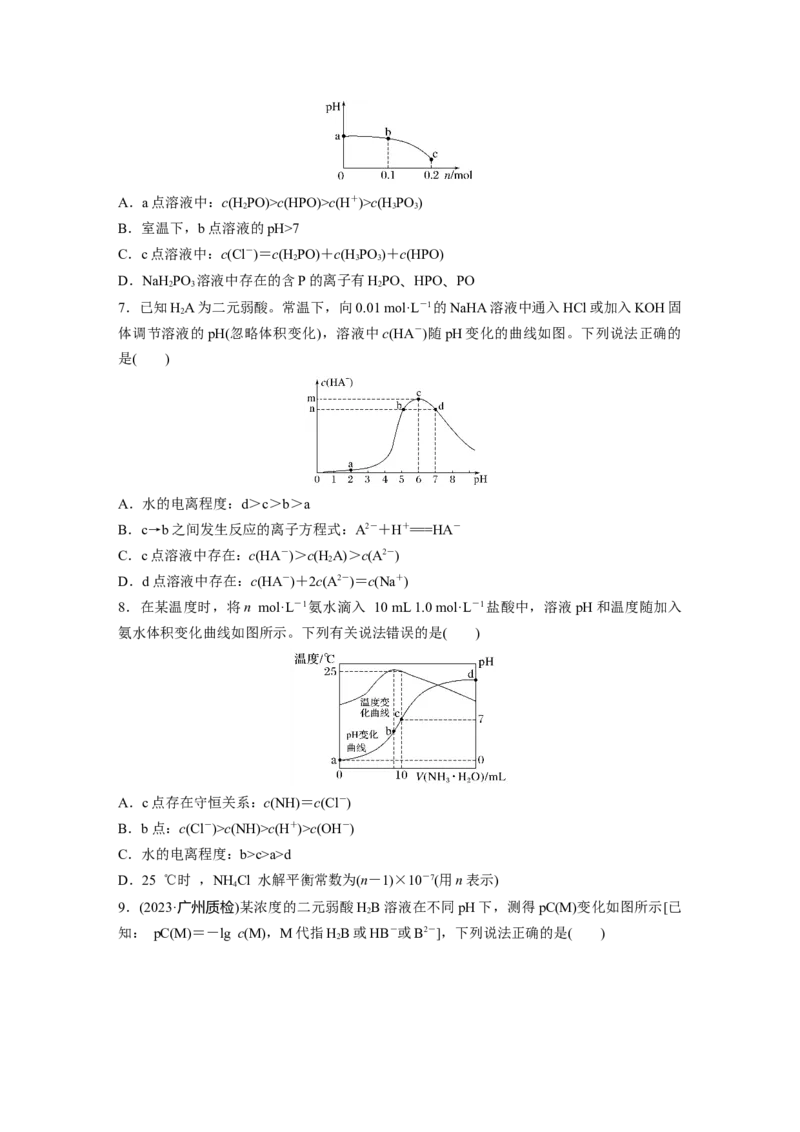
4.(2022·山东青岛模拟)常温时,向20.00 mL 0.1 mol·L-1 C H COOH(苯甲酸)溶液中滴加
6 5
0.1 mol·L-1 NaOH溶液,混合溶液的pH与微粒浓度变化的关系如图所示。下
列说法错误的是( )
A.a点溶液对应的pH为3.2
B.b点对应的NaOH溶液体积为10.00 mL
C.c点溶液中:c(C HCOO-)>c(Na+)>c(H+)>c(OH-)
6 5
D.常温时,C HCOO-的水解常数K =10-9.8
6 5 h
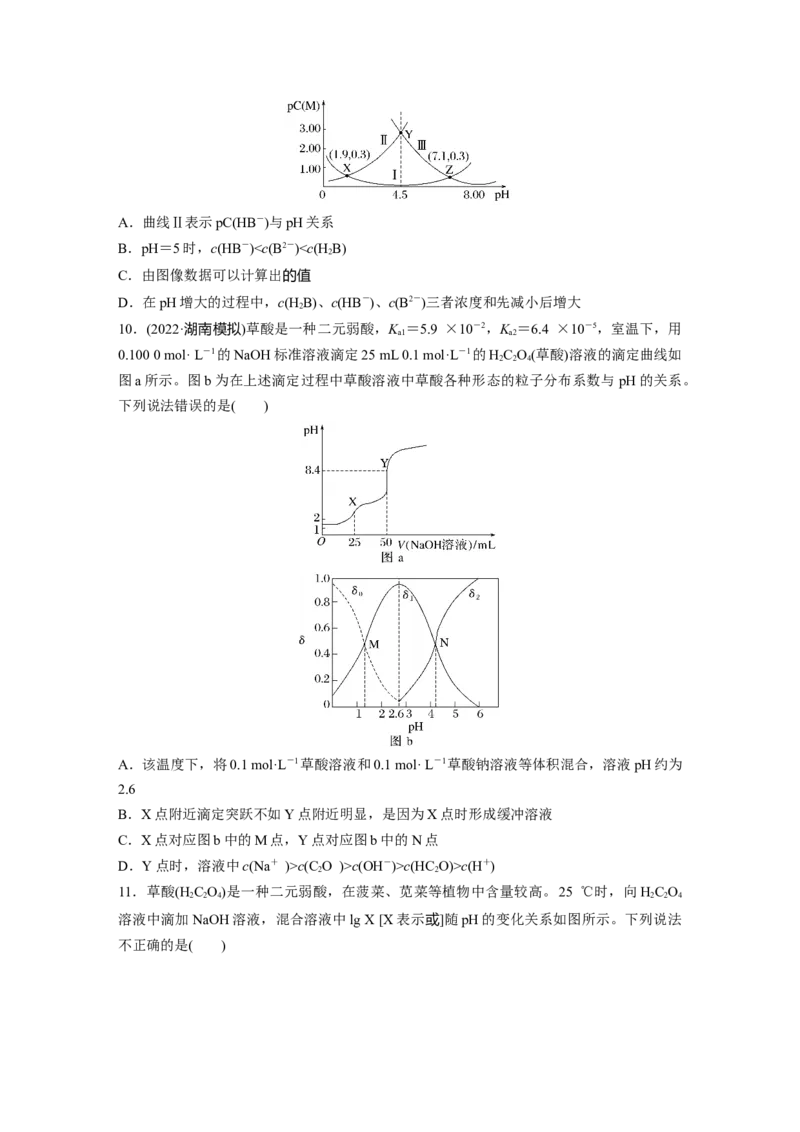
5.(2022·深圳模拟)甘氨酸盐酸盐(HOOCCH NH Cl)的水溶液呈酸性,溶液中存在以下平衡:
2 3
HOOCCH NH-OOCCH NH+H+ K
2 2 1
-OOCCH NH-OOCCH NH +H+ K
2 2 2 2
常温时,向10 mL一定浓度的HOOCCH NH Cl的水溶液中滴入同浓度的NaOH溶液。混合
2 3
溶液pH随加入NaOH溶液体积的变化如图所示。下列说法不正确的是( )
A.Q→X过程中:逐渐减小
B.X点的溶液中:c(-OOCCH NH )>c(HOOCCH NH)
2 2 2
C.P点的溶液中:c(HOOCCH NH)+c(H+)=c(-OOCCH NH )+c(OH-)
2 2 2
D.当V(NaOH)=20 mL时,混合溶液中的溶质主要为NaOOCCHNH 和NaCl
2 2
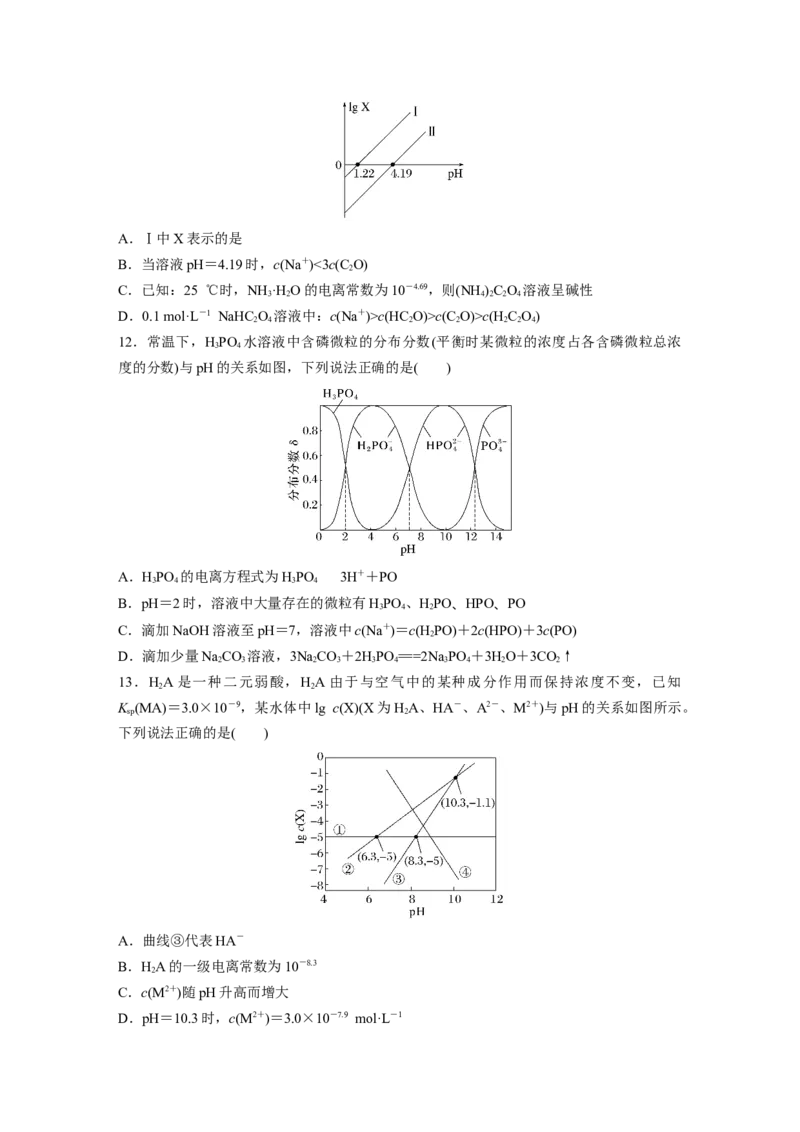
6.(2022·海南学业水平诊断)已知亚磷酸(H PO )是二元弱酸,298 K时的电离常数分别为K
3 3 a1
=10-1.4,K =10-6.1。298 K时,向1 L 0.2 mol·L-1 NaH PO 溶液中通入HCl气体,溶液的
a2 2 3
pH与通入HCl物质的量的关系如图所示。下列说法正确的是( )A.a点溶液中:c(H PO)>c(HPO)>c(H+)>c(H PO )
2 3 3
B.室温下,b点溶液的pH>7
C.c点溶液中:c(Cl-)=c(H PO)+c(H PO )+c(HPO)
2 3 3
D.NaH PO 溶液中存在的含P的离子有HPO、HPO、PO
2 3 2
7.已知HA为二元弱酸。常温下,向0.01 mol·L-1的NaHA溶液中通入HCl或加入KOH固
2
体调节溶液的pH(忽略体积变化),溶液中c(HA-)随pH变化的曲线如图。下列说法正确的
是( )
A.水的电离程度:d>c>b>a
B.c→b之间发生反应的离子方程式:A2-+H+===HA-
C.c点溶液中存在:c(HA-)>c(H A)>c(A2-)
2
D.d点溶液中存在:c(HA-)+2c(A2-)=c(Na+)
8.在某温度时,将n mol·L-1氨水滴入 10 mL 1.0 mol·L-1盐酸中,溶液pH和温度随加入
氨水体积变化曲线如图所示。下列有关说法错误的是( )
A.c点存在守恒关系:c(NH)=c(Cl-)
B.b点:c(Cl-)>c(NH)>c(H+)>c(OH-)
C.水的电离程度:b>c>a>d
D.25 ℃时 ,NH Cl 水解平衡常数为(n-1)×10-7(用n表示)
4
9.(2023·广州质检)某浓度的二元弱酸HB溶液在不同pH下,测得pC(M)变化如图所示[已
2
知: pC(M)=-lg c(M),M代指HB或HB-或B2-],下列说法正确的是( )
2A.曲线Ⅱ表示pC(HB-)与pH关系
B.pH=5时,c(HB-)c(C O )>c(OH-)>c(HC O)>c(H+)
2 2
11.草酸(H C O)是一种二元弱酸,在菠菜、苋菜等植物中含量较高。25 ℃时,向HC O
2 2 4 2 2 4
溶液中滴加NaOH溶液,混合溶液中lg X [X表示或]随pH的变化关系如图所示。下列说法
不正确的是( )A.Ⅰ中X表示的是
B.当溶液pH=4.19时,c(Na+)<3c(C O)
2
C.已知:25 ℃时,NH ·H O的电离常数为10-4.69,则(NH )C O 溶液呈碱性
3 2 4 2 2 4
D.0.1 mol·L-1 NaHC O 溶液中:c(Na+)>c(HC O)>c(C O)>c(H C O)
2 4 2 2 2 2 4
12.常温下,HPO 水溶液中含磷微粒的分布分数(平衡时某微粒的浓度占各含磷微粒总浓
3 4
度的分数)与pH的关系如图,下列说法正确的是( )
A.HPO 的电离方程式为HPO 3H++PO
3 4 3 4
B.pH=2时,溶液中大量存在的微粒有HPO 、HPO、HPO、PO
3 4 2
C.滴加NaOH溶液至pH=7,溶液中c(Na+)=c(H PO)+2c(HPO)+3c(PO)
2
D.滴加少量NaCO 溶液,3NaCO+2HPO ===2NaPO +3HO+3CO↑
2 3 2 3 3 4 3 4 2 2
13.HA 是一种二元弱酸,HA 由于与空气中的某种成分作用而保持浓度不变,已知
2 2
K (MA)=3.0×10-9,某水体中lg c(X)(X为HA、HA-、A2-、M2+)与pH的关系如图所示。
sp 2
下列说法正确的是( )
A.曲线③代表HA-
B.HA的一级电离常数为10-8.3
2
C.c(M2+)随pH升高而增大
D.pH=10.3时,c(M2+)=3.0×10-7.9 mol·L-1