文档内容
第 56 讲 反应过程中溶液粒子浓度变化的图像分析
[复习目标] 1.能正确识别图像,能从图像中找到曲线指代、趋势、关键点。2.利用溶液中
的平衡关系,学会分析不同类型图像中各粒子浓度之间的关系。
类型一 滴定过程 pH 变化曲线
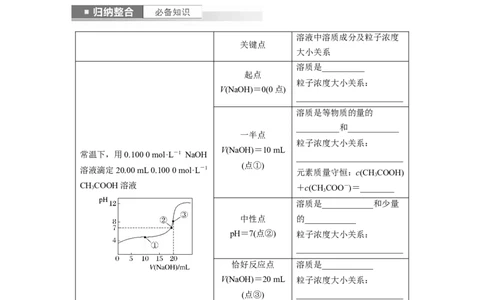
溶液中溶质成分及粒子浓度
关键点
大小关系
溶质是__________
起点
粒子浓度大小关系:
V(NaOH)=0(0点)
_________________________
溶质是等物质的量的
__________和____________
一半点
粒子浓度大小关系:
V(NaOH)=10 mL
常温下,用0.100 0 mol·L-1 NaOH
_________________________
(点①)
溶液滴定20.00 mL 0.100 0 mol·L-1 元素质量守恒:c(CHCOOH)
3
CH 3 COOH溶液 +c(CHCOO-)=________
3
溶质是____________和少量
中性点 的____________
pH=7(点②) 粒子浓度大小关系:
_________________________
恰好反应点 溶质是____________
V(NaOH)=20 mL 粒子浓度大小关系:
(点③) _________________________
溶质是等物质的量的
过量1倍点 ________和________
V(NaOH)=40 mL 粒子浓度大小关系:
_________________________一、一元弱电解质的滴定曲线
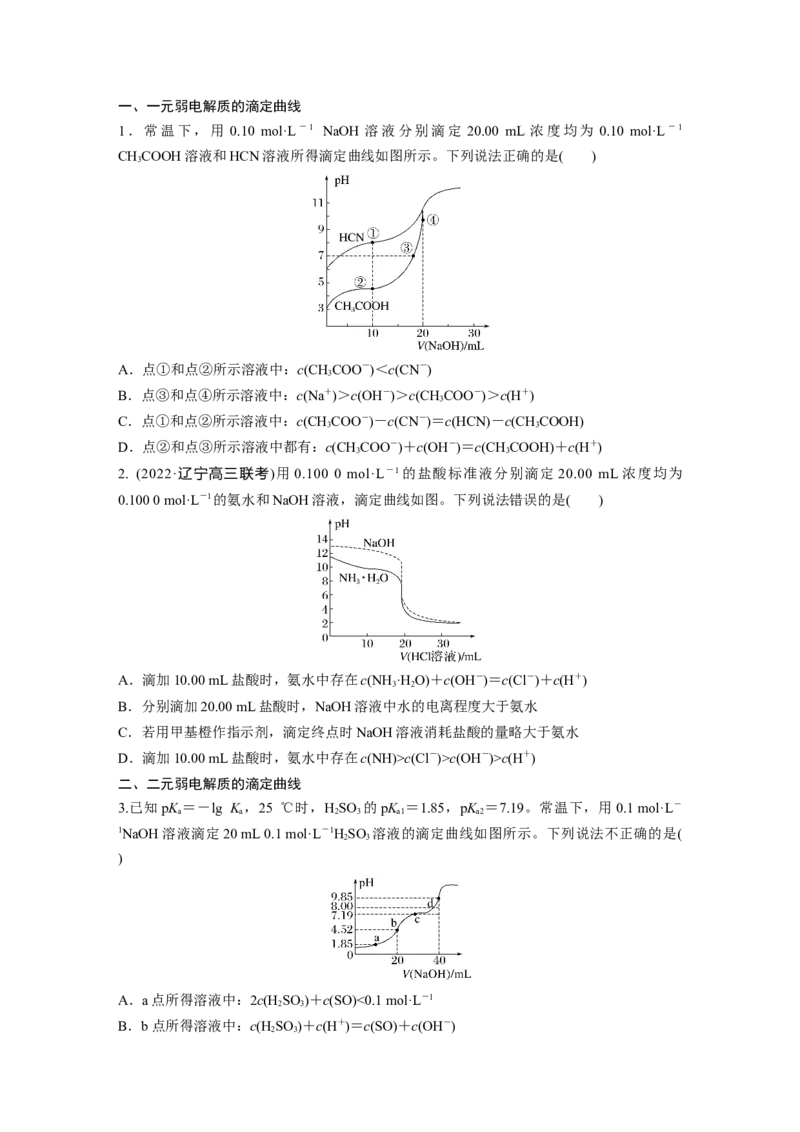
1.常温下,用 0.10 mol·L-1 NaOH 溶液分别滴定 20.00 mL 浓度均为 0.10 mol·L-1
CHCOOH溶液和HCN溶液所得滴定曲线如图所示。下列说法正确的是( )
3
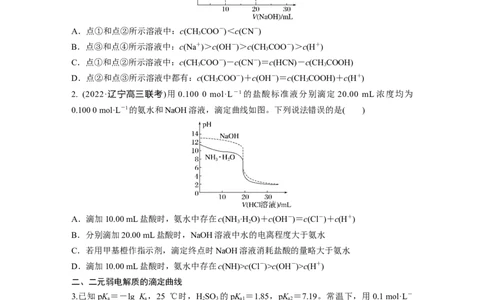
A.点①和点②所示溶液中:c(CHCOO-)<c(CN-)
3
B.点③和点④所示溶液中:c(Na+)>c(OH-)>c(CHCOO-)>c(H+)
3
C.点①和点②所示溶液中:c(CHCOO-)-c(CN-)=c(HCN)-c(CHCOOH)
3 3
D.点②和点③所示溶液中都有:c(CHCOO-)+c(OH-)=c(CHCOOH)+c(H+)
3 3
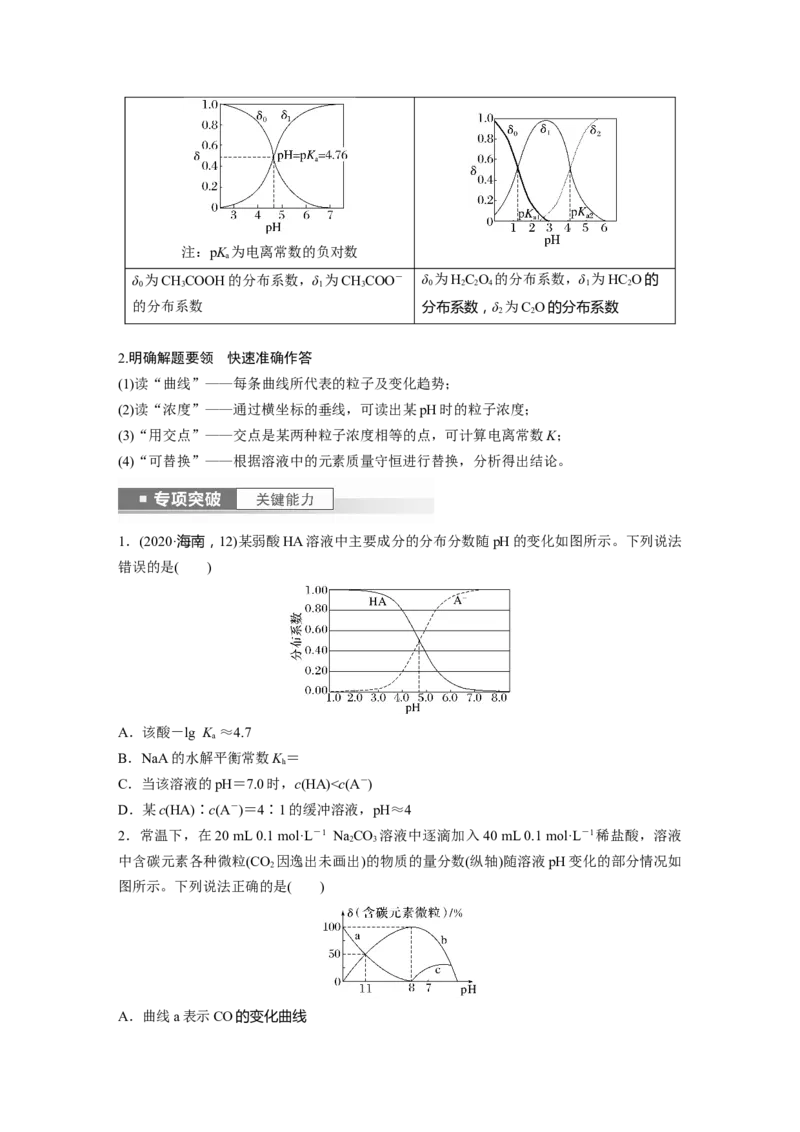
2. (2022·辽宁高三联考)用0.100 0 mol·L-1的盐酸标准液分别滴定 20.00 mL 浓度均为
0.100 0 mol·L-1的氨水和NaOH溶液,滴定曲线如图。下列说法错误的是( )
A.滴加10.00 mL盐酸时,氨水中存在c(NH ·H O)+c(OH-)=c(Cl-)+c(H+)
3 2
B.分别滴加20.00 mL盐酸时,NaOH溶液中水的电离程度大于氨水
C.若用甲基橙作指示剂,滴定终点时NaOH溶液消耗盐酸的量略大于氨水
D.滴加10.00 mL盐酸时,氨水中存在c(NH)>c(Cl-)>c(OH-)>c(H+)
二、二元弱电解质的滴定曲线
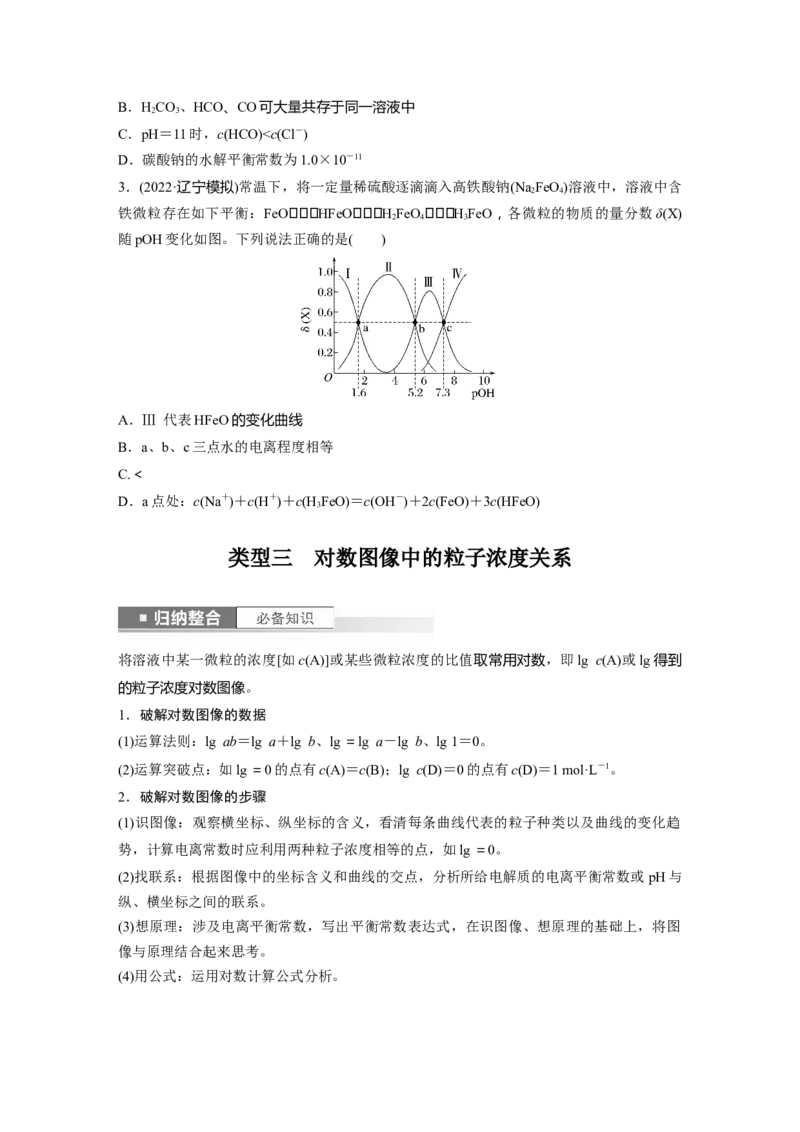
3.已知pK =-lg K ,25 ℃时,HSO 的pK =1.85,pK =7.19。常温下,用0.1 mol·L-
a a 2 3 a1 a2
1NaOH溶液滴定20 mL 0.1 mol·L-1HSO 溶液的滴定曲线如图所示。下列说法不正确的是(
2 3
)
A.a点所得溶液中:2c(H SO )+c(SO)<0.1 mol·L-1
2 3
B.b点所得溶液中:c(H SO )+c(H+)=c(SO)+c(OH-)
2 3C.c点所得溶液中:c(Na+)>3c(HSO)
D.d点所得溶液中:c(Na+)>c(HSO)>c(SO)
4.常温下向100 mL 0.1 mol·L-1 Na C O 溶液中滴加0.1 mol·L-1的盐酸,溶液中pOH与加入
2 2 4
盐酸的体积关系如图所示。已知:pOH=-lg c(OH-),K (H C O)=1×10-2,K (H C O)
a1 2 2 4 a2 2 2 4
=1×10-5。下列说法不正确的是( )
A.m的值约为5
B.若V=100,则n>7
1
C.a点:c(Na+)+c(H+)=c(HC O)+2c(C O)+c(Cl-)+c(OH-)
2 2
D.若q=10,则b点对应的溶液>100
抓两点突破二元弱电解质滴定曲线
二元弱酸(H A)与碱(NaOH)发生反应分两步进行:
2
第一滴定终点:HA+NaOH===NaHA+HO,此时,酸、碱的物质的量之比为1∶1,得到
2 2
的是NaHA的溶液,其中K =,若溶液中c(HA-)=c(H A),则K =c(H+);第二滴定终点:
a1 2 a1
NaHA+NaOH===Na A+HO,此时,酸、碱的物质的量之比为1∶2,得到的是NaA的溶
2 2 2
液,其中K =,若溶液中c(A2-)=c(HA-),则K =c(H+)。
a2 a2
类型二 分布系数曲线
1.透析分布曲线 确定思维方向
分布曲线是指以pH为横坐标、分布系数(即组分的平衡浓度占总浓度的分数)为纵坐标的关
系曲线。
一元弱酸(以CHCOOH为例) 二元弱酸(以HC O 为例)
3 2 2 4注:pK 为电离常数的负对数
a
δ 为CHCOOH的分布系数,δ 为CHCOO- δ 为HC O 的分布系数,δ 为HC O的
0 3 1 3 0 2 2 4 1 2
的分布系数 分布系数,δ 为C O的分布系数
2 2
2.明确解题要领 快速准确作答
(1)读“曲线”——每条曲线所代表的粒子及变化趋势;
(2)读“浓度”——通过横坐标的垂线,可读出某pH时的粒子浓度;
(3)“用交点”——交点是某两种粒子浓度相等的点,可计算电离常数K;
(4)“可替换”——根据溶液中的元素质量守恒进行替换,分析得出结论。
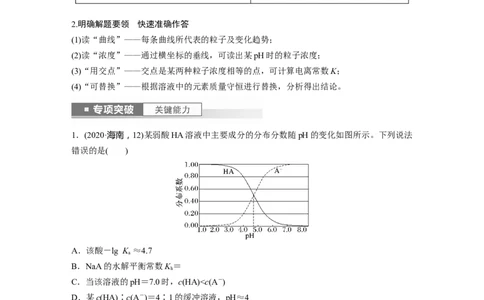
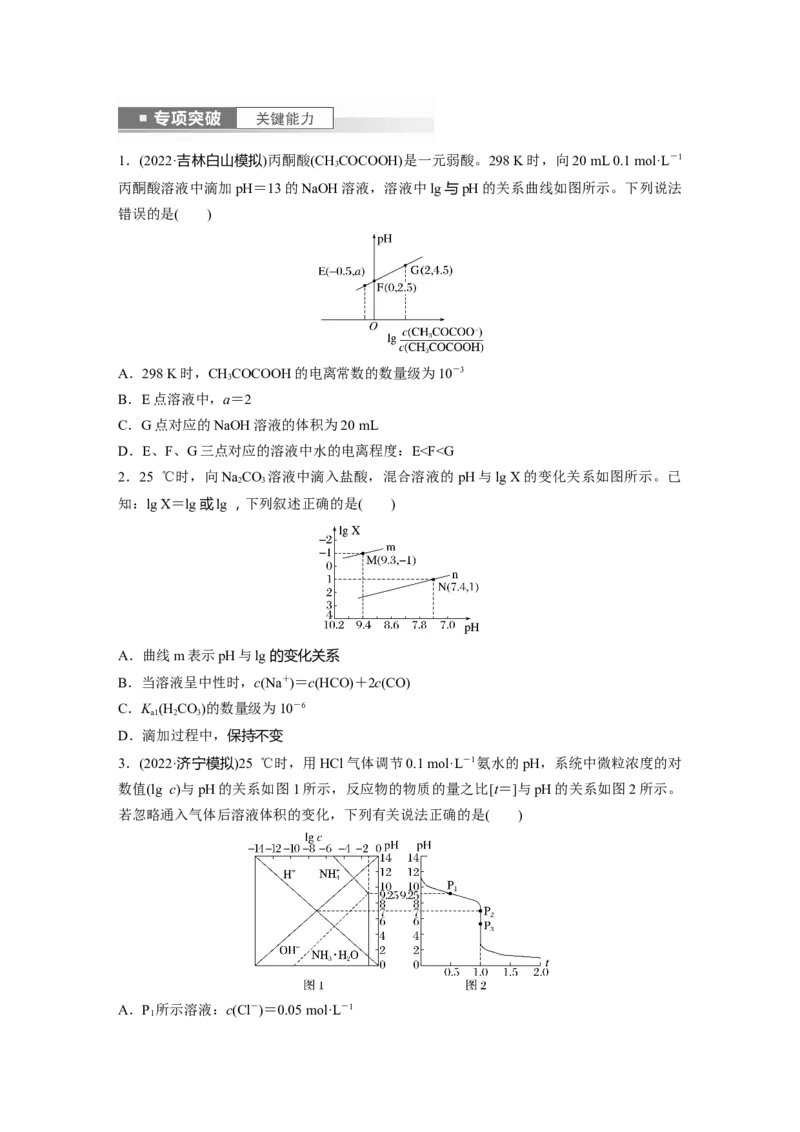
1.(2020·海南,12)某弱酸HA溶液中主要成分的分布分数随pH的变化如图所示。下列说法
错误的是( )
A.该酸-lg K ≈4.7
a
B.NaA的水解平衡常数K =
h
C.当该溶液的pH=7.0时,c(HA)y
2.(2021·湖南,9)常温下,用0.100 0 mol·L-1的盐酸分别滴定20.00 mL浓度均为0.100 0 mol·L-
1的三种一元弱酸的钠盐(NaX、NaY、NaZ)溶液,滴定曲线如图所示。下列判断错误的是(
)
A.该NaX溶液中:c(Na+)>c(X-)>c(OH-)>c(H+)
B.三种一元弱酸的电离常数:K(HX)>K(HY)>K(HZ)
a a a
C.当pH=7时,三种溶液中:c(X-)=c(Y-)=c(Z-)
D.分别滴加20.00 mL盐酸后,再将三种溶液混合:c(X-)+c(Y-)+c(Z-)=c(H+)-c(OH-)
3.(2021·海南,13改编)25 ℃时,向10.00 mL 0.100 0 mol·L-1的NaHCO 溶液中滴加
3
0.100 0 mol·L-1的盐酸,溶液的pH随加入的盐酸的体积V变化如图所示。下列有关说法正
确的是( )A.a点,溶液pH>7是由于HCO水解程度大于电离程度
B.b点,c(Na+)=c(HCO)+c(CO)+c(Cl-)
C.c点,溶液中的H+主要来自HCO的电离
D.d点,c(Na+)=c(Cl-)=0.100 0 mol·L-1
4.(2022·辽宁,15)甘氨酸(NH CHCOOH)是人体必需氨基酸之一。在 25 ℃时,
2 2
NHCHCOOH、NHCHCOO-和NH CHCOO-的分布分数[如δ(A2-)=]与溶液pH关系如图。
2 2 2 2
下列说法错误的是( )
A.甘氨酸具有两性
B.曲线c代表NH CHCOO-
2 2
C.NHCHCOO-+HONHCHCOOH+OH-的平衡常数K=10-11.65
2 2 2
D.c2(NHCHCOO-)