文档内容
1.(2022·广东模拟)对于0.1 mol·L-1 NH Cl溶液,下列说法不正确的是( )
4
A.溶液中c(Cl-)>c(NH)>c(H+)>c(OH-)
B.溶液中存在:c(H+)+c(NH)=c(Cl-)+c(OH-)
C.适当升高温度,溶液中c(H+)减小
D.工业上可用于除去铁锈
2.用物质的量都是 0.1 mol 的 CHCOOH 和 CHCOONa 配成 1 L 混合溶液,已知其中
3 3
c(CHCOO-)>c(Na+),对该溶液的下列判断正确的是( )
3
A.c(H+)>c(OH-)
B.c(CHCOO-)=0.1 mol·L-1
3
C.c(CHCOOH)>c(CHCOO-)
3 3
D.c(CHCOO-)+c(OH-)=0.1 mol·L-1
3
3.(2022·河北开滦二中模拟)氰化氢(HCN)可应用于电镀业(镀铜、镀金、镀银)、采矿业等。
常温下,浓度均为0.01 mol·L-1的HCN和NaCN的混合溶液的pH≈8,下列说法正确的是(
)
A.常温下,K(HCN)≈10-8
a
B.该混合溶液中水的电离程度大于纯水中水的电离程度
C.该混合溶液中c(HCN)c(NH)>c(OH-)>c(H+)
4
D.等物质的量浓度的NaS和NaHS混合溶液中:c(Na+)=c(S2-)+c(HS-)+c(H S)
2 2
6.(2021·河北1月选考模拟,9)醋酸为一元弱酸,25 ℃时,其电离常数K=1.75×10-5。
a
下列说法错误的是( )A.0.1 mol·L-1 CHCOOH溶液的pH在2~3范围内
3
B.CHCOONa溶液中,c(CHCOOH)+c(H+)=c(OH-)
3 3
C.将0.1 mol·L-1 CHCOOH溶液加水稀释,其电离常数和均不变
3
D.等体积的0.1 mol·L-1 NaOH溶液和0.1 mol·L-1 CHCOOH溶液混合后,溶液pH>7,
3
且c(Na+)>c(CHCOO-)>c(OH-)>c(H+)
3
7.(2021·湖北1月选考模拟,15)25 ℃时,按下表配制两份溶液。
一元弱酸溶液 加入的NaOH溶液 混合后所得溶液
HA 10.0 mL 0.20 mol·L-1 5.0 mL 0.20 mol·L-1 溶液ⅠpH=5.0
HB 10.0 mL 0.20 mol·L-1 5.0 mL 0.20 mol·L-1 溶液ⅡpH=4.0
下列说法错误的是( )
A.溶液Ⅰ中,c(A-)>c(Na+)>c(H+)>c(OH-)
B.Ⅰ和Ⅱ的pH相差1.0,说明=10
C.混合Ⅰ和Ⅱ:c(Na+)+c(H+)=c(A-)+c(B-)+c(OH-)
D.混合Ⅰ和Ⅱ:c(HA)>c(HB)
8.常温下,下列溶液中,有关微粒的物质的量浓度关系不正确的是( )
A.0.1 mol·L-1(NH )Fe(SO ) 溶液:c(SO)>c(NH)>c(Fe2+)>c(H+)
4 2 4 2
B.将10 mL 0.1 mol·L-1 Na CO 溶液逐滴滴加到10 mL 0.1 mol·L-1盐酸中:c(Na+)>c(Cl
2 3
-)> c(CO)>c(HCO)
C.0.01 mol·L-1 NaOH溶液与等体积pH=2的醋酸混合后的溶液中:c(CHCOO-)>c(Na
3
+)> c(H+)>c(OH-)
D.0.1 mol·L-1 NaHCO 溶液:c(H+)+2c(H CO)=c(OH-)+c(CO)
3 2 3
9.25 ℃时,在10 mL浓度均为0.1 mol·L-1 的NaOH和NH ·H O混合溶液中滴加0.1 mol·L-
3 2
1的盐酸,下列有关溶液中粒子浓度关系正确的是( )
A.未加盐酸时:c(OH-)>c(Na+)=c(NH ·H O)
3 2
B.加入10 mL盐酸时:c(NH)+c(H+)=c(OH-)
C.加入盐酸至溶液pH=7时:c(Cl-)=c(Na+)
D.加入20 mL盐酸时: c(Cl-)=c(NH)+c(Na+)
10.(2022·成都模拟)某二元弱酸(简写为HB)溶液,按下式发生一级和二级电离:
2
HBH++HB-
2
HB-H++B2-
已知相同浓度时的电离度:α(H B)>α(HB-),现有下列四种溶液:
2
①0.01 mol·L-1的HB溶液
2
②0.01 mol·L-1的NaHB溶液
③0.02 mol·L-1的HCl溶液与0.04 mol·L-1的NaHB溶液等体积混合后的溶液
④0.02 mol·L-1的NaOH溶液与0.02 mol·L-1的NaHB溶液等体积混合后的溶液下列说法错误的是( )
A.溶液④一定显碱性 B.c(H B)最大的是③
2
C.c(B2-)最小的是① D.c(H+)最大的是③
11.(2022·济南外国语学校质检)下列有关溶液(室温下)的说法正确的是( )
A.NaCO 和NaHCO 形成的混合溶液中:2c(Na+)=3[c(CO)+c(HCO)+c(H CO)]
2 3 3 2 3
B.0.10 mol·L-1 NaHSO 溶液中通入NH 至溶液pH=7:c(Na+)>c(NH)>c(SO)
3 3
C.物质的量浓度相等的①(NH )SO 溶液、② NH HCO 溶液、③ NH Cl 溶液、
4 2 4 4 3 4
④(NH )Fe(SO ) 溶液中,c(NH)的大小关系:④>①>②>③
4 2 4 2
D.0.10 mol·L-1 CHCOONa溶液中通入HCl至溶液pH=7:c(Na+)>c(CHCOOH)=c(Cl-)
3 3
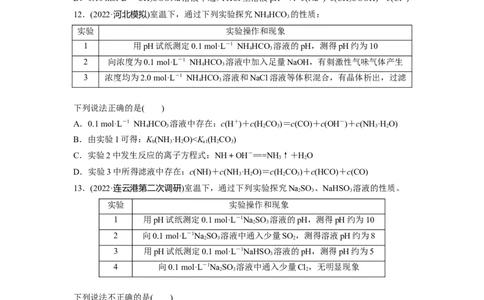
12.(2022·河北模拟)室温下,通过下列实验探究NH HCO 的性质:
4 3
实验 实验操作和现象
1 用pH试纸测定0.1 mol·L-1 NH HCO 溶液的pH,测得pH约为10
4 3
2 向浓度为0.1 mol·L-1 NH HCO 溶液中加入足量NaOH,有刺激性气味气体产生
4 3
3 浓度均为2.0 mol·L-1 NH HCO 溶液和NaCl溶液等体积混合,有晶体析出,过滤
4 3
下列说法正确的是( )
A.0.1 mol·L-1 NH HCO 溶液中存在:c(H+)+c(H CO)=c(CO)+c(OH-)+c(NH ·H O)
4 3 2 3 3 2
B.由实验1可得:K (NH ·H O)c(A-)>c(OH-)>c(H+)
B.实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)= mol·L-1
C.实验②反应后的溶液中:c(A-)+c(HA)>0.1 mol·L-1
D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-)=c(H+)
15.醋酸是日常生活中最常见的调味剂和重要的化工原料,醋酸钠是其常见的盐[已知:25
℃,K(CHCOOH)=1.69×10-5]。请回答下列问题:
a 3
(1)下列对于醋酸溶液和醋酸钠溶液的说法正确的是________(填字母,下同)。
A.加水稀释,醋酸的电离程度增大,醋酸钠的水解程度减小
B.升高温度,可以促进醋酸的电离,抑制醋酸钠的水解
C.醋酸和醋酸钠混合液中,醋酸抑制醋酸钠的水解,醋酸钠抑制醋酸的电离
(2)物质的量浓度均为0.1 mol·L-1的CHCOOH和CHCOONa溶液等体积混合(混合前后体
3 3
积变化忽略不计),混合液中的下列关系式正确的是________。
A.c(CHCOOH)+c(H+)=c(CHCOO-)+c(OH-)
3 3
B.c(H+)+c(Na+)=c(CHCOO-)+c(OH-)
3
C.c(CHCOO-)+c(CHCOOH)=0.1 mol·L-1
3 3
(3)常温时,pH=3 的醋酸溶液和 pH=11 的 NaOH 溶液等体积混合后,溶液中 c(Na
+)_____(填“>”“<”或“=”)c(CHCOO -),该溶液中电荷守恒表达式为
3
_______________。
(4)常温时,将m mol·L-1醋酸溶液和n mol·L-1 NaOH溶液等体积混合后,所得溶液的pH
=7,则m与n的大小关系是m_________________(填“>”“<”或“=”,下同)n,醋酸
溶液中c(H+)______________NaOH溶液中c(OH-)。