文档内容
1.25 ℃、1.01×105 Pa时,反应2NO(g)===4NO (g)+O(g) ΔH=+109.8 kJ·mol-1,该
2 5 2 2
反应能自发进行的原因是( )
A.该反应是吸热反应
B.该反应是放热反应
C.该反应是熵减小的反应
D.该反应的熵增大效应大于能量效应
2.下列反应在任何温度下均能自发进行的是( )
A.2N(g)+O(g)===2NO(g) ΔH=+16 kJ·mol-1
2 2 2
B.Ag(s)+Cl(g)===AgCl(s) ΔH=-127 kJ·mol-1
2
C.HgO(s)===Hg(l)+O(g) ΔH=+91 kJ·mol-1
2
D.HO(l)===O(g)+HO(l) ΔH=-98 kJ·mol-1
2 2 2 2
3.下列对化学反应的预测正确的是( )
选项 化学方程式 已知条件 预测
A A(s)===B(g)+C(s) ΔH>0 它一定是非自发反应
B A(g)+2B(g)===2C(g)+3D(g) 能自发反应 ΔH一定小于0
C M(s)+aN(g)===2Q(g) ΔH<0,自发反应 a可能等于1、2、3
D M(s)+N(g)=== 2Q(s) 常温下,自发进行 ΔH>0
4.合成氨反应达到平衡时,NH 的体积分数与温度、压强的关系如图所示。根据此图分析
3
合成氨工业最有前途的研究方向是( )
A.提高分离技术
B.研制耐高压的合成塔
C.研制低温催化剂
D.探索不用N 和H 合成氨的新途径
2 2
5.(2023·青岛一模)2007年诺贝尔化学奖颁给了德国化学家格哈德·埃特尔(GerhardErtl),以
表彰他在固体表面化学研究中取得的开拓性成就。他的成就之一是证实了氢气与氮气在固体
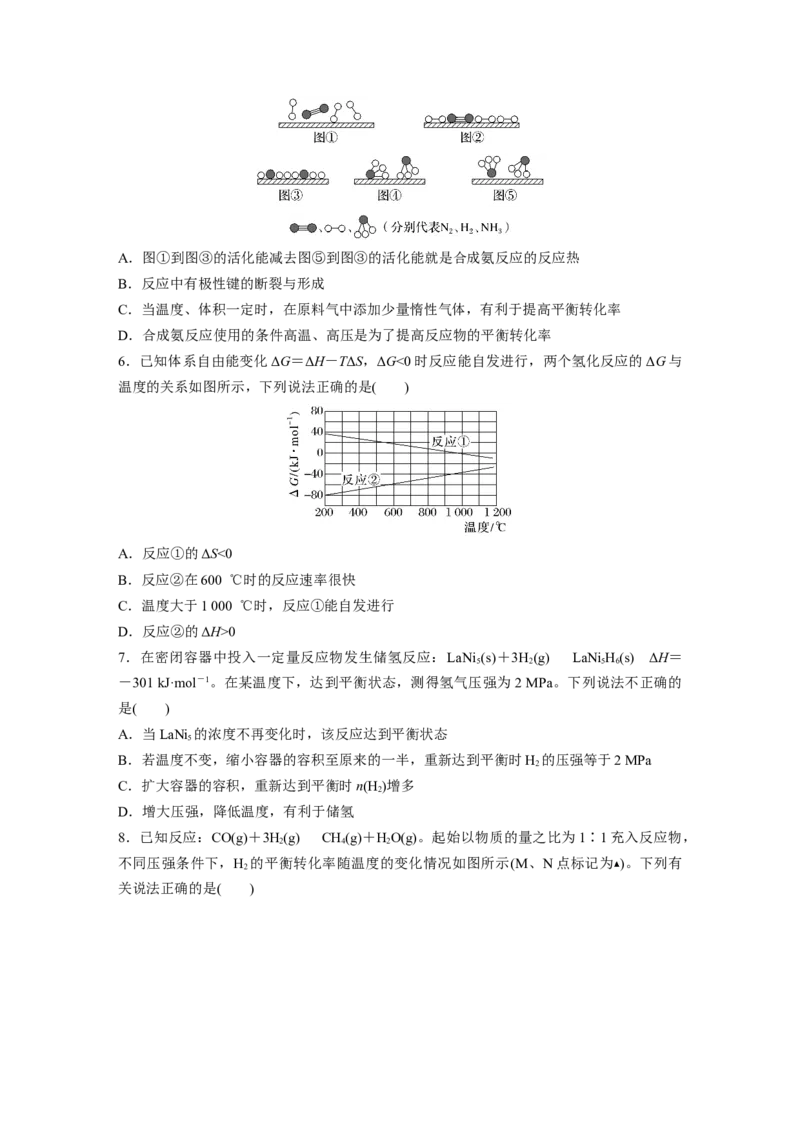
催化剂表面合成氨气的反应过程,模拟示意图如图。关于合成氨工艺,下列说法正确的是(
)A.图①到图③的活化能减去图⑤到图③的活化能就是合成氨反应的反应热
B.反应中有极性键的断裂与形成
C.当温度、体积一定时,在原料气中添加少量惰性气体,有利于提高平衡转化率
D.合成氨反应使用的条件高温、高压是为了提高反应物的平衡转化率
6.已知体系自由能变化ΔG=ΔH-TΔS,ΔG<0时反应能自发进行,两个氢化反应的ΔG与
温度的关系如图所示,下列说法正确的是( )
A.反应①的ΔS<0
B.反应②在600 ℃时的反应速率很快
C.温度大于1 000 ℃时,反应①能自发进行
D.反应②的ΔH>0
7.在密闭容器中投入一定量反应物发生储氢反应:LaNi (s)+3H (g)LaNiH(s) ΔH=
5 2 5 6
-301 kJ·mol-1。在某温度下,达到平衡状态,测得氢气压强为 2 MPa。下列说法不正确的
是( )
A.当LaNi 的浓度不再变化时,该反应达到平衡状态
5
B.若温度不变,缩小容器的容积至原来的一半,重新达到平衡时H 的压强等于2 MPa
2
C.扩大容器的容积,重新达到平衡时n(H )增多
2
D.增大压强,降低温度,有利于储氢
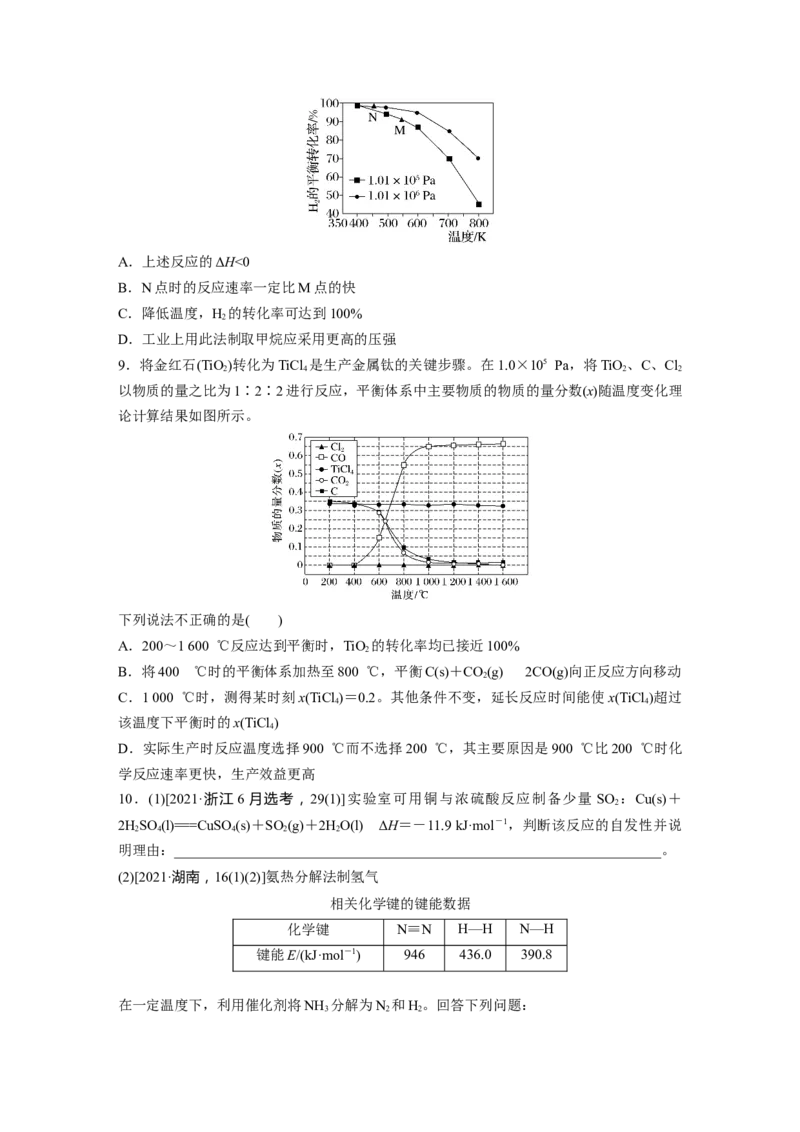
8.已知反应:CO(g)+3H(g)CH(g)+HO(g)。起始以物质的量之比为1∶1充入反应物,
2 4 2
不同压强条件下,H 的平衡转化率随温度的变化情况如图所示(M、N点标记为 )。下列有
2
关说法正确的是( )A.上述反应的ΔH<0
B.N点时的反应速率一定比M点的快
C.降低温度,H 的转化率可达到100%
2
D.工业上用此法制取甲烷应采用更高的压强
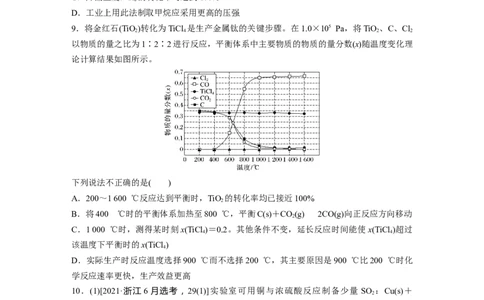
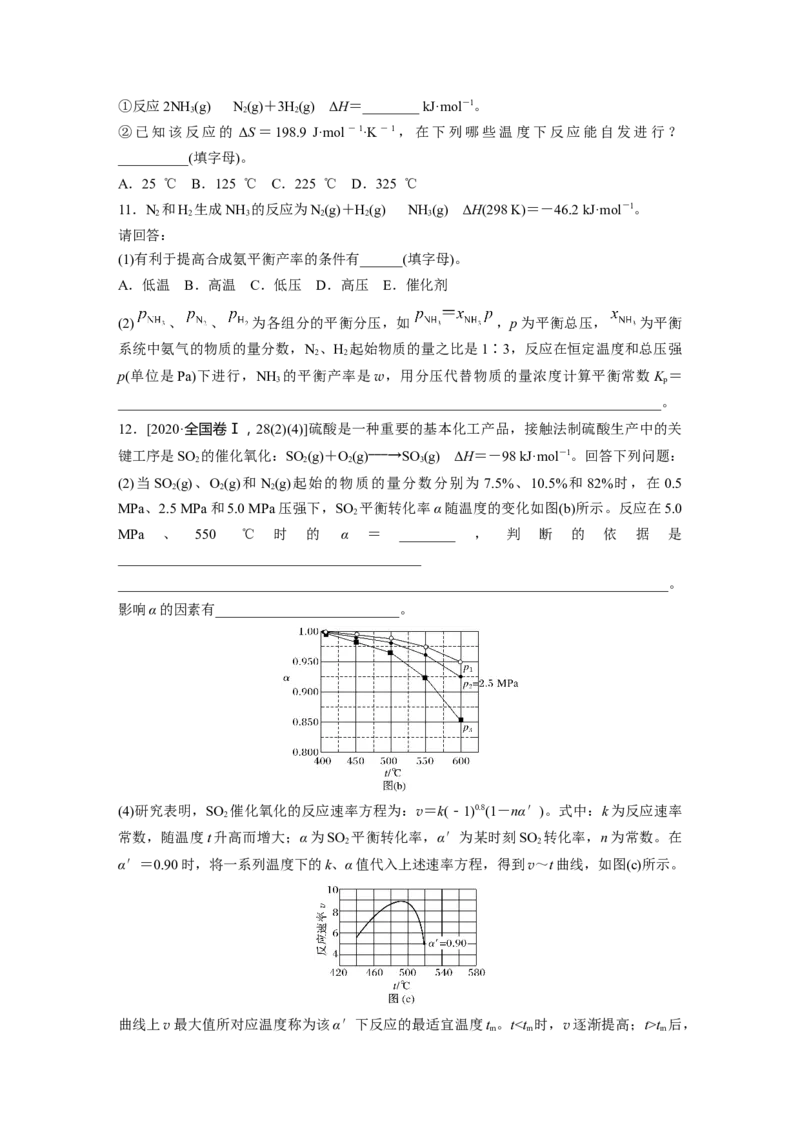
9.将金红石(TiO)转化为TiCl 是生产金属钛的关键步骤。在1.0×105 Pa,将TiO 、C、Cl
2 4 2 2
以物质的量之比为1∶2∶2进行反应,平衡体系中主要物质的物质的量分数(x)随温度变化理
论计算结果如图所示。
下列说法不正确的是( )
A.200~1 600 ℃反应达到平衡时,TiO 的转化率均已接近100%
2
B.将400 ℃时的平衡体系加热至800 ℃,平衡C(s)+CO(g)2CO(g)向正反应方向移动
2
C.1 000 ℃时,测得某时刻x(TiCl )=0.2。其他条件不变,延长反应时间能使x(TiCl )超过
4 4
该温度下平衡时的x(TiCl )
4
D.实际生产时反应温度选择900 ℃而不选择200 ℃,其主要原因是900 ℃比200 ℃时化
学反应速率更快,生产效益更高
10.(1)[2021·浙江 6 月选考,29(1)]实验室可用铜与浓硫酸反应制备少量 SO :Cu(s)+
2
2HSO (l)===CuSO (s)+SO (g)+2HO(l) ΔH=-11.9 kJ·mol-1,判断该反应的自发性并说
2 4 4 2 2
明理由:_____________________________________________________________________。
(2)[2021·湖南,16(1)(2)]氨热分解法制氢气
相关化学键的键能数据
化学键 N≡N H—H N—H
键能E/(kJ·mol-1) 946 436.0 390.8
在一定温度下,利用催化剂将NH 分解为N 和H。回答下列问题:
3 2 2①反应2NH (g)N(g)+3H(g) ΔH=________ kJ·mol-1。
3 2 2
②已知该反应的 ΔS=198.9 J·mol-1·K-1,在下列哪些温度下反应能自发进行?
__________(填字母)。
A.25 ℃ B.125 ℃ C.225 ℃ D.325 ℃
11.N 和H 生成NH 的反应为N(g)+H(g)NH (g) ΔH(298 K)=-46.2 kJ·mol-1。
2 2 3 2 2 3
请回答:
(1)有利于提高合成氨平衡产率的条件有______(填字母)。
A.低温 B.高温 C.低压 D.高压 E.催化剂
(2) 、 、 为各组分的平衡分压,如 ,p为平衡总压, 为平衡
系统中氨气的物质的量分数,N 、H 起始物质的量之比是1∶3,反应在恒定温度和总压强
2 2
p(单位是Pa)下进行,NH 的平衡产率是w,用分压代替物质的量浓度计算平衡常数K =
3 p
_____________________________________________________________________________。
12.[2020·全国卷Ⅰ,28(2)(4)]硫酸是一种重要的基本化工产品,接触法制硫酸生产中的关
键工序是SO 的催化氧化:SO (g)+O(g)―――→SO (g) ΔH=-98 kJ·mol-1。回答下列问题:
2 2 2 3
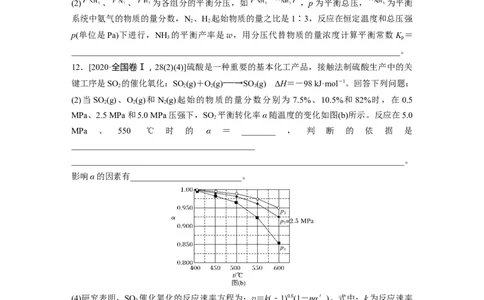
(2)当 SO (g)、O(g)和 N(g)起始的物质的量分数分别为 7.5%、10.5%和 82%时,在 0.5
2 2 2
MPa、2.5 MPa和5.0 MPa压强下,SO 平衡转化率α随温度的变化如图(b)所示。反应在5.0
2
MPa 、 550 ℃ 时 的 α = ________ , 判 断 的 依 据 是
___________________________________________
______________________________________________________________________________。
影响α的因素有__________________________。
(4)研究表明,SO 催化氧化的反应速率方程为:v=k(-1)0.8(1-nα′)。式中:k为反应速率
2
常数,随温度t升高而增大;α为SO 平衡转化率,α′为某时刻SO 转化率,n为常数。在
2 2
α′=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v~t曲线,如图(c)所示。
曲线上v最大值所对应温度称为该α′下反应的最适宜温度t 。tt 后,
m m mv逐渐下降。原因是________________________________________________________
______________________________________________________________________________。
13.丙烯是制备聚丙烯的单体,在催化剂作用下,可由丙烷直接脱氢或氧化脱氢制得。
反应Ⅰ(直接脱氢):
C H(g)C H(g)+H(g) ΔH
3 8 3 6 2 1
反应Ⅱ(氧化脱氢):
2C H(g)+O(g)2C H(g)+2HO(g) ΔH=-236 kJ·mol-1
3 8 2 3 6 2 2
已知:2H(g)+O(g)2HO(g) ΔH=-484 kJ·mol-1
2 2 2 3
(1)ΔH=________kJ·mol-1。
1
(2)向某容器中仅通入C H(g),发生反应Ⅰ,达到平衡后,下列措施能提高C H(g)的平衡产
3 8 3 6
率的有________(填字母)。
A.恒压下,充入惰性气体
B.加入高效催化剂
C.恒容下,充入C H
3 8
D.适当升高温度
(3)向某恒压密闭容器中通入C H(g)和N(g)的混合气体(N 不参与反应),发生反应Ⅰ,反应
3 8 2 2
起始时气体的总压强为100 kPa。在温度为T ℃时,C H(g)的平衡转化率与通入的混合气
1 3 8
体中C H(g)的物质的量分数的关系如图所示。
3 8
①C H 的平衡转化率随起始通入C H 的物质的量分数增大而减小,其原因是_____________
3 8 3 8
______________________________________________________________________________。
②T ℃时,反应Ⅰ的平衡常数K =________kPa(以分压表示,分压=总压×物质的量分数,
1 p
保留一位小数)。