文档内容
0,实验测得容器内压强随时间的变化关系如图
2
所示。下列说法错误的是( )
A.0~2 min内,环戊烯的平均反应速率为0.10 mol·L-1· min-1
B.环戊烯的平衡转化率为50%
C.高温低压有利于提高环戊烯的平衡转化率
D.该温度下,反应的平衡常数为K=2
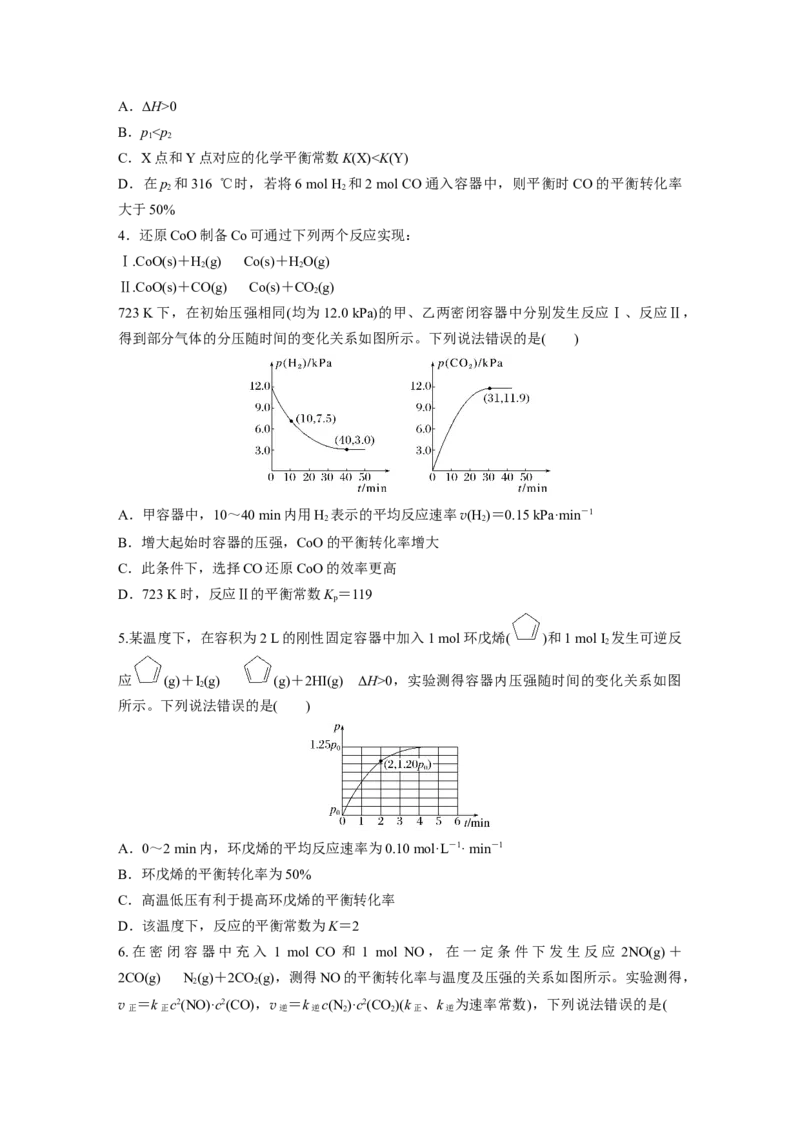
6.在密闭容器中充入 1 mol CO 和 1 mol NO,在一定条件下发生反应 2NO(g)+
2CO(g)N(g)+2CO(g),测得NO的平衡转化率与温度及压强的关系如图所示。实验测得,
2 2
v正 =k 正 c2(NO)·c2(CO),v逆 =k 逆 c(N 2 )·c2(CO 2 )(k 正 、k 逆 为速率常数),下列说法错误的是()
A.达到平衡后,仅升高温度,k 增大的倍数小于k 增大的倍数
正 逆
B.若密闭容器体积为1 L,在p 压强下,b点=160
1
C.NO的物质的量:b点>a点
D.逆反应速率:a点>c点
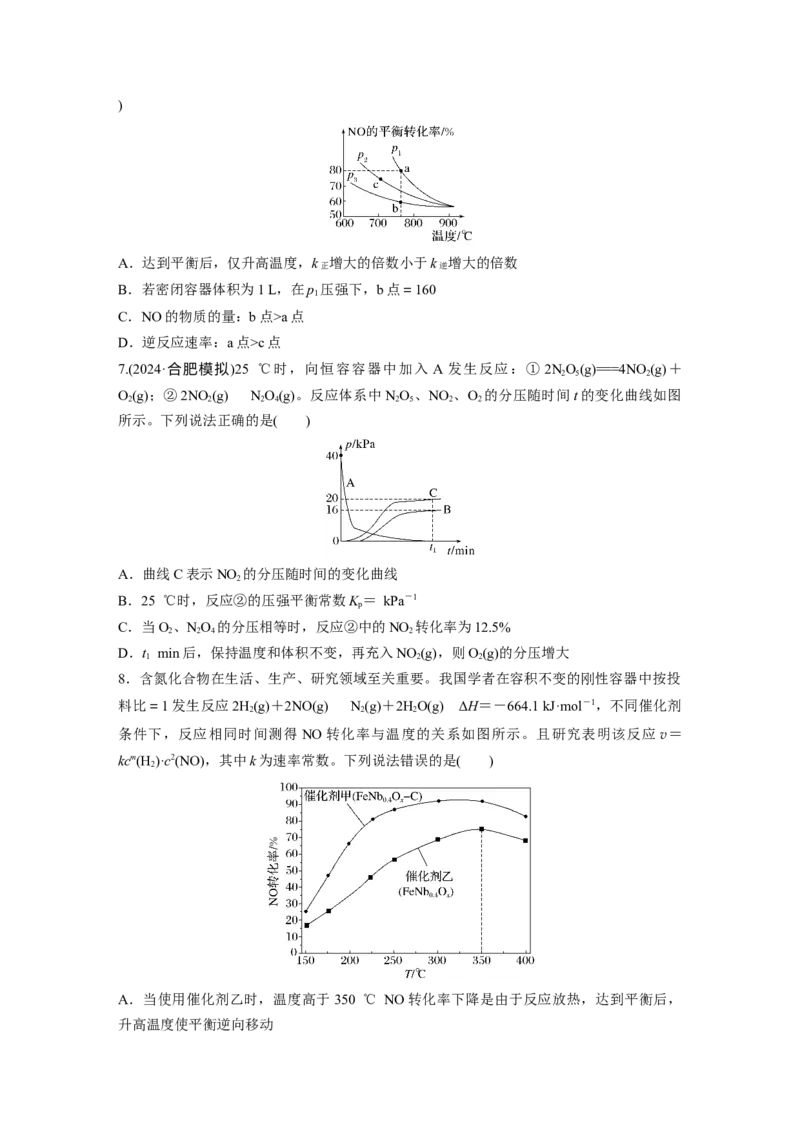
7.(2024·合肥模拟)25 ℃时,向恒容容器中加入 A 发生反应:① 2NO(g)===4NO (g)+
2 5 2
O(g);②2NO (g)NO(g)。反应体系中NO 、NO 、O 的分压随时间t的变化曲线如图
2 2 2 4 2 5 2 2
所示。下列说法正确的是( )
A.曲线C表示NO 的分压随时间的变化曲线
2
B.25 ℃时,反应②的压强平衡常数K = kPa-1
p
C.当O、NO 的分压相等时,反应②中的NO 转化率为12.5%
2 2 4 2
D.t min后,保持温度和体积不变,再充入NO (g),则O(g)的分压增大
1 2 2
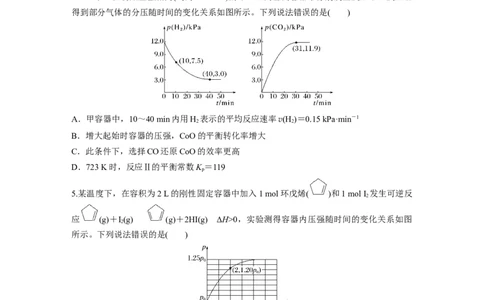
8.含氮化合物在生活、生产、研究领域至关重要。我国学者在容积不变的刚性容器中按投
料比=1发生反应2H(g)+2NO(g)N(g)+2HO(g) ΔH=-664.1 kJ·mol-1,不同催化剂
2 2 2
条件下,反应相同时间测得 NO转化率与温度的关系如图所示。且研究表明该反应 v=
kcm(H )·c2(NO),其中k为速率常数。下列说法错误的是( )
2
A.当使用催化剂乙时,温度高于350 ℃ NO转化率下降是由于反应放热,达到平衡后,
升高温度使平衡逆向移动B.使用催化剂甲比使用催化剂乙正反应的活化能更低
C.对于反应2H(g)+2NO(g)N(g)+2HO(g),其他条件不变,加压使平衡正向移动
2 2 2
D.T ℃的初始速率为v,当H 转化率为60%时,反应速率为0.064v,由此可知m=1
1 0 2 0
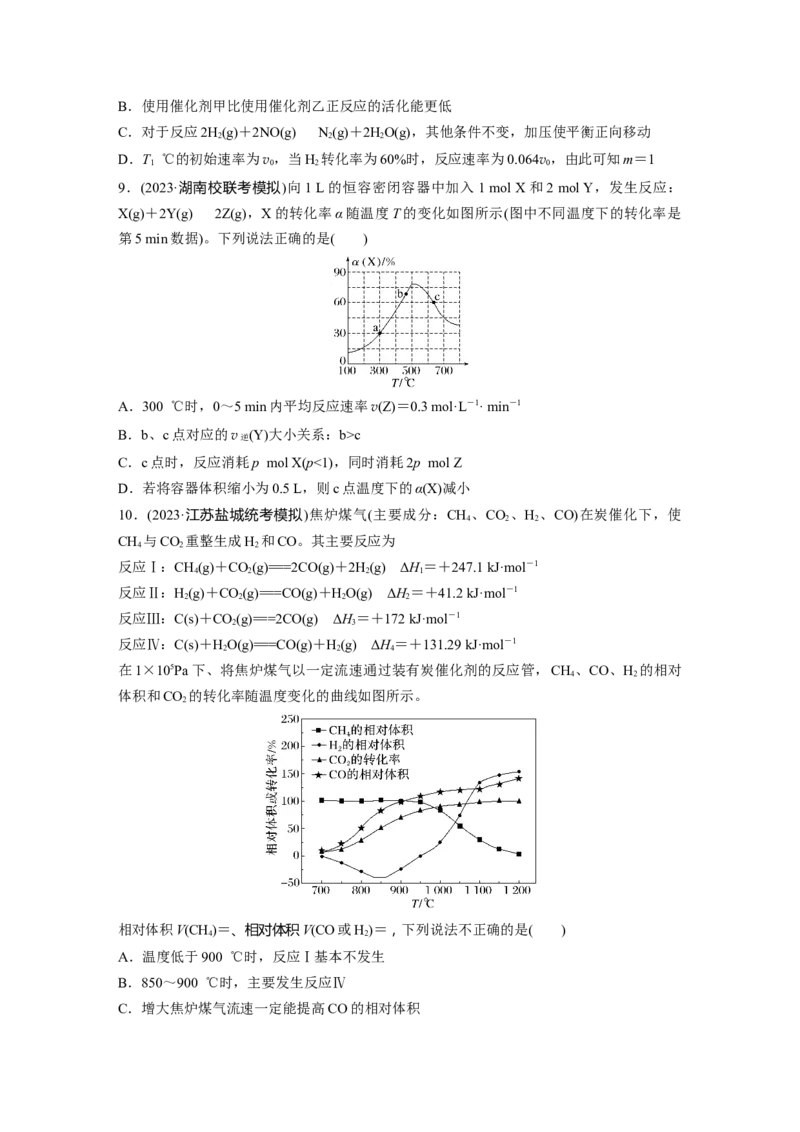
9.(2023·湖南校联考模拟)向1 L的恒容密闭容器中加入1 mol X和2 mol Y,发生反应:
X(g)+2Y(g)2Z(g),X的转化率α随温度T的变化如图所示(图中不同温度下的转化率是
第5 min数据)。下列说法正确的是( )
A.300 ℃时,0~5 min内平均反应速率v(Z)=0.3 mol·L-1· min-1
B.b、c点对应的v逆 (Y)大小关系:b>c
C.c点时,反应消耗p mol X(p<1),同时消耗2p mol Z
D.若将容器体积缩小为0.5 L,则c点温度下的α(X)减小
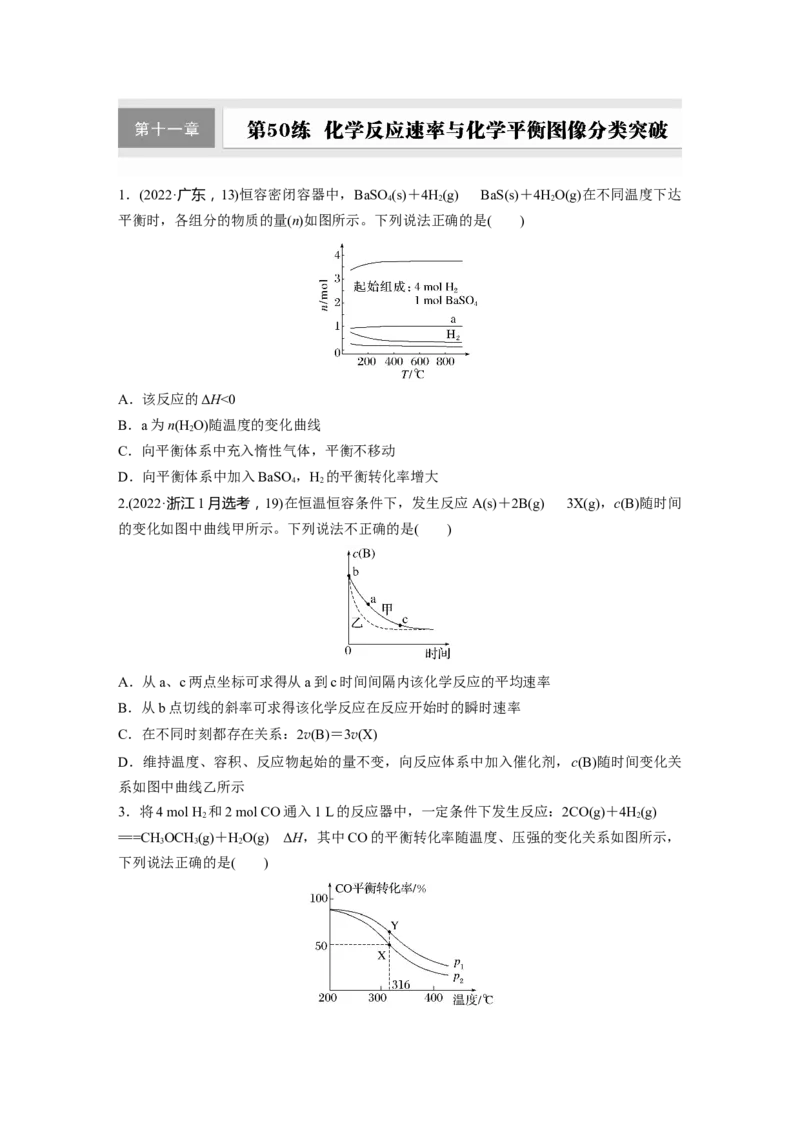
10.(2023·江苏盐城统考模拟)焦炉煤气(主要成分:CH 、CO 、H 、CO)在炭催化下,使
4 2 2
CH 与CO 重整生成H 和CO。其主要反应为
4 2 2
反应Ⅰ:CH(g)+CO(g)===2CO(g)+2H(g) ΔH=+247.1 kJ·mol-1
4 2 2 1
反应Ⅱ:H(g)+CO(g)===CO(g)+HO(g) ΔH=+41.2 kJ·mol-1
2 2 2 2
反应Ⅲ:C(s)+CO(g)===2CO(g) ΔH=+172 kJ·mol-1
2 3
反应Ⅳ:C(s)+HO(g)===CO(g)+H(g) ΔH=+131.29 kJ·mol-1
2 2 4
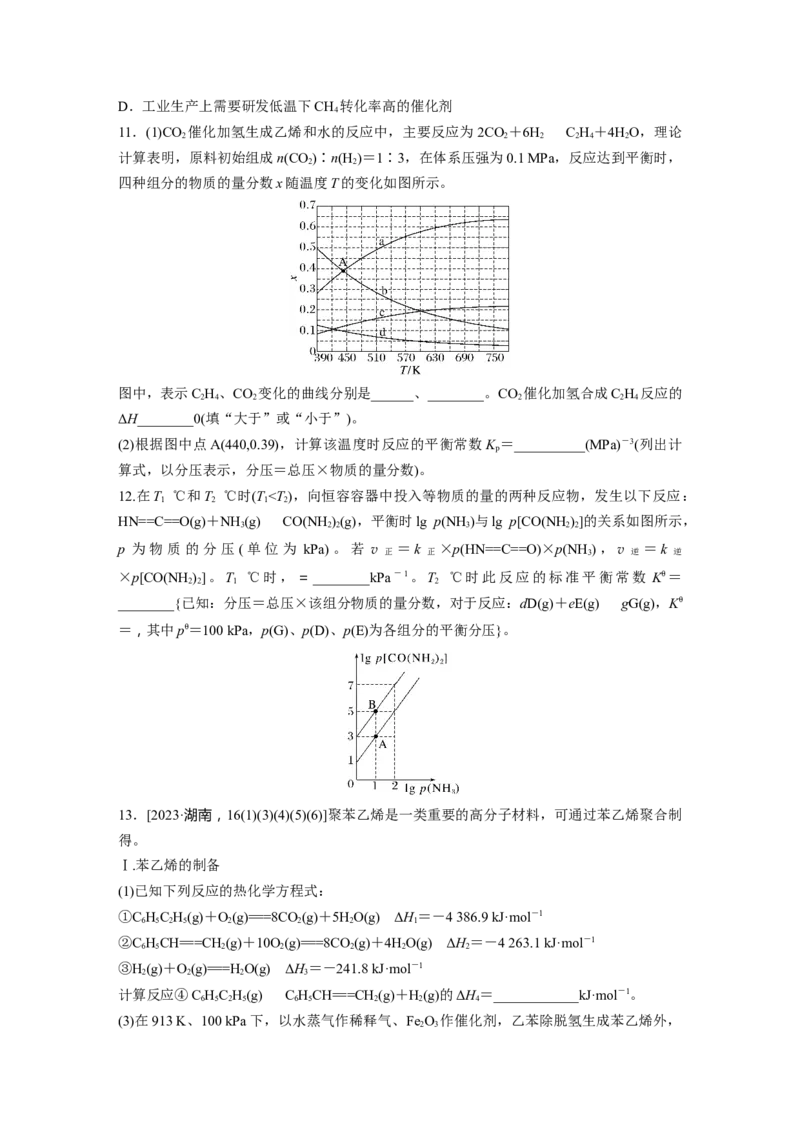
在1×105Pa下、将焦炉煤气以一定流速通过装有炭催化剂的反应管,CH 、CO、H 的相对
4 2
体积和CO 的转化率随温度变化的曲线如图所示。
2
相对体积V(CH)=、相对体积V(CO或H)=,下列说法不正确的是( )
4 2
A.温度低于900 ℃时,反应Ⅰ基本不发生
B.850~900 ℃时,主要发生反应Ⅳ
C.增大焦炉煤气流速一定能提高CO的相对体积D.工业生产上需要研发低温下CH 转化率高的催化剂
4
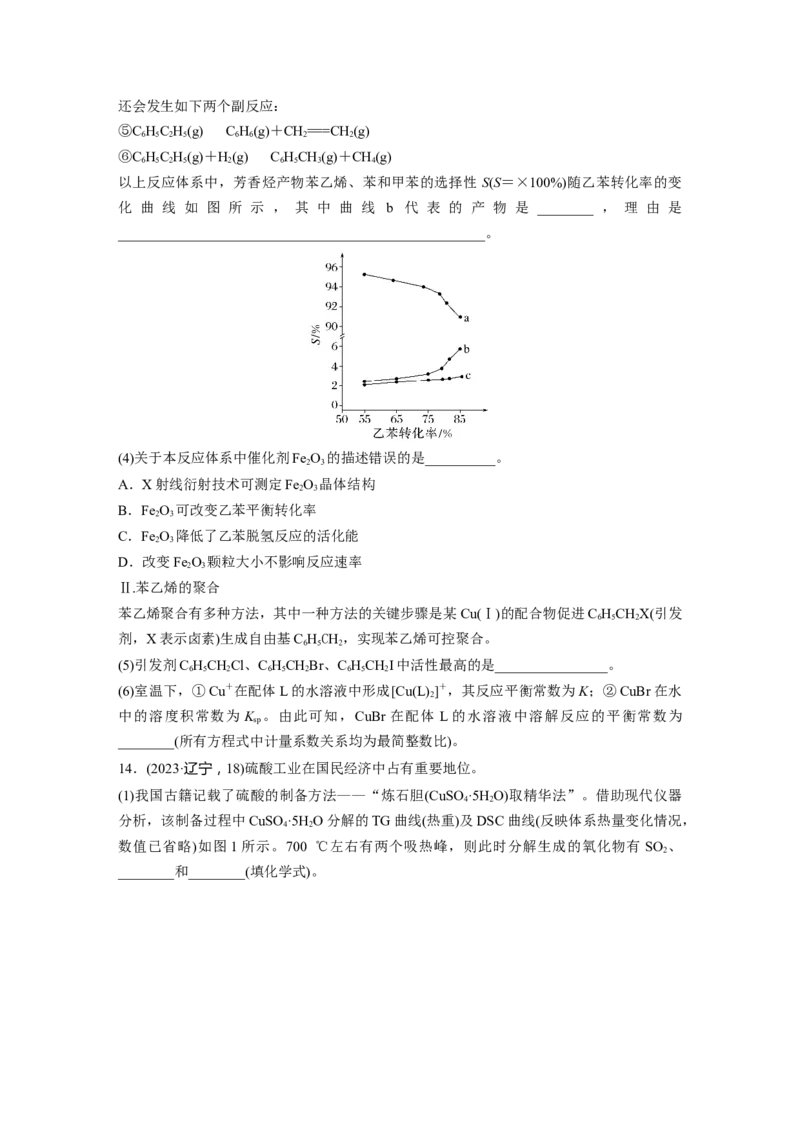
11.(1)CO 催化加氢生成乙烯和水的反应中,主要反应为2CO +6HC H +4HO,理论
2 2 2 2 4 2
计算表明,原料初始组成n(CO)∶n(H )=1∶3,在体系压强为0.1 MPa,反应达到平衡时,
2 2
四种组分的物质的量分数x随温度T的变化如图所示。
图中,表示C H、CO 变化的曲线分别是______、________。CO 催化加氢合成C H 反应的
2 4 2 2 2 4
ΔH________0(填“大于”或“小于”)。
(2)根据图中点A(440,0.39),计算该温度时反应的平衡常数K =__________(MPa)-3(列出计
p
算式,以分压表示,分压=总压×物质的量分数)。
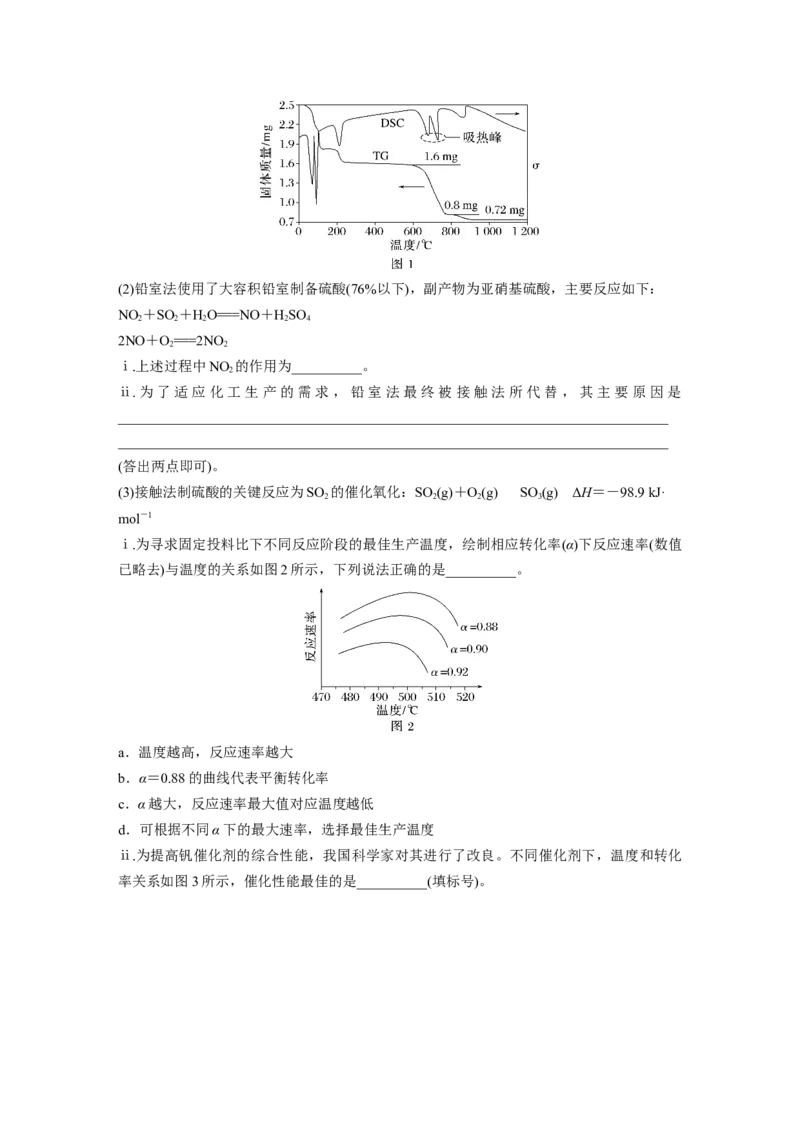
12.在T ℃和T ℃时(T