文档内容
1.下列不能用勒夏特列原理解释的事实是( )
A.红棕色的NO 加压后颜色先变深后变浅
2
B.氢气、碘蒸气、碘化氢气体组成的平衡体系加压后颜色变深
C.黄绿色的氯水光照后颜色变浅
D.向含有[Fe(SCN)]2+的红色溶液中加铁粉,振荡,溶液红色变浅或褪去
2.反应NH HS(s)NH (g)+HS(g)在某温度下达到平衡,下列各种情况不会使平衡发生移
4 3 2
动的是( )
A.温度、容积不变时,通入SO 气体
2
B.移走一部分NH HS固体
4
C.容器体积不变,充入HCl气体
D.保持压强不变,充入氮气
3.(2020·浙江7月选考,20)一定条件下:2NO (g)NO(g) ΔH<0。在测定NO 的相对
2 2 4 2
分子质量时,下列条件中,测定结果误差最小的是( )
A.温度0 ℃、压强50 kPa
B.温度130 ℃、压强300 kPa
C.温度25 ℃、压强100 kPa
D.温度130 ℃、压强50 kPa
4.在水溶液中,CrO呈黄色,Cr O呈橙色,重铬酸钾(K Cr O)在水溶液中存在以下平衡:
2 2 2 7
Cr O+HO2CrO+2H+,下列说法正确的是( )
2 2
A.向该溶液中加入过量浓NaOH溶液后,溶液呈橙色
B.该反应是氧化还原反应
C.向该溶液中滴加适量的浓硫酸,平衡向逆反应方向移动,再次达到平衡后,氢离子浓度
比原溶液大
D.向体系中加入少量水,平衡逆向移动
5.(2023·广州实验中学模拟)常压下羰基化法精炼镍的原理为Ni(s)+4CO(g)Ni(CO) (g)。
4
230 ℃时,该反应的平衡常数K=2×10-5。已知:Ni(CO) 的沸点为42.2 ℃,固体杂质不
4
参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO) ;第二阶段:将第一阶段反应后的气体分
4
离出来,加热至230 ℃制得高纯镍。
下列判断正确的是( )
A.升高温度,该反应的平衡常数减小
B.该反应达到平衡时,v生成 [Ni(CO)
4
]=4v生成 (CO)
C.第一阶段,在30 ℃和50 ℃两者之间选择反应温度应选30 ℃D.第二阶段,Ni(CO) 分解率较低
4
6.对于反应NO(g) 2NO (g) ΔH=+57 kJ·mol-1,下列有关说法正确的是( )
2 4 2
A.升高体系温度正反应速率增大,逆反应速率减小
B.若容器体积不变,密度不变时说明该反应达到化学平衡状态
C.其他条件不变,向平衡后的容器中再加入少量NO,新平衡后的值不变
2 4
D.增大体系的压强能提高NO 的反应速率和平衡转化率
2 4
7.某温度下,反应2A(g)B(g) ΔH>0,在密闭容器中达到平衡,平衡后=a,若改变某
一条件,足够时间后反应再次达到平衡状态,此时=b,下列叙述正确的是( )
A.在该温度下,保持容积固定不变,向容器内补充了B气体,则a<b
B.若a=b,则该反应中可能使用了催化剂
C.若其他条件不变,升高温度,则a<b
D.若保持温度、压强不变,充入惰性气体,则a>b
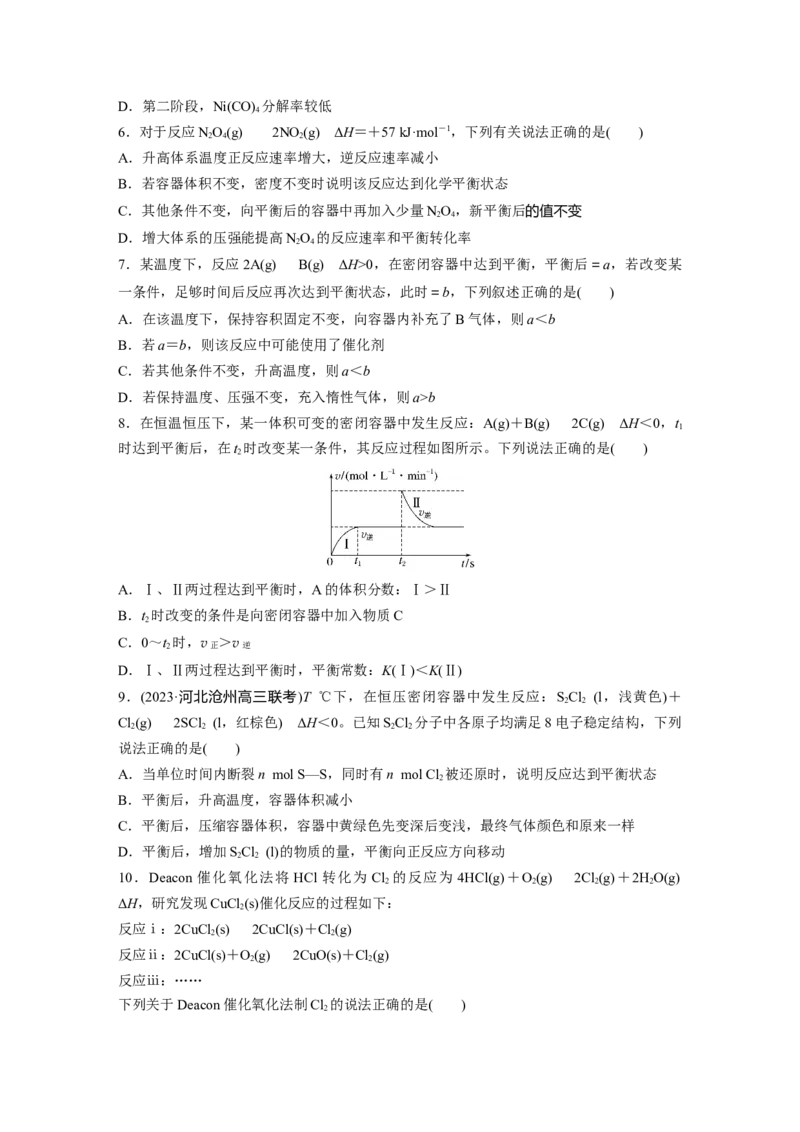
8.在恒温恒压下,某一体积可变的密闭容器中发生反应:A(g)+B(g)2C(g) ΔH<0,t
1
时达到平衡后,在t 时改变某一条件,其反应过程如图所示。下列说法正确的是( )
2
A.Ⅰ、Ⅱ两过程达到平衡时,A的体积分数:Ⅰ>Ⅱ
B.t 时改变的条件是向密闭容器中加入物质C
2
C.0~t
2
时,v正 >v逆
D.Ⅰ、Ⅱ两过程达到平衡时,平衡常数:K(Ⅰ)<K(Ⅱ)
9.(2023·河北沧州高三联考)T ℃下,在恒压密闭容器中发生反应:SCl (l,浅黄色)+
2 2
Cl(g)2SCl (l,红棕色) ΔH<0。已知SCl 分子中各原子均满足8电子稳定结构,下列
2 2 2 2
说法正确的是( )
A.当单位时间内断裂n mol S—S,同时有n mol Cl 被还原时,说明反应达到平衡状态
2
B.平衡后,升高温度,容器体积减小
C.平衡后,压缩容器体积,容器中黄绿色先变深后变浅,最终气体颜色和原来一样
D.平衡后,增加SCl (l)的物质的量,平衡向正反应方向移动
2 2
10.Deacon 催化氧化法将 HCl 转化为 Cl 的反应为 4HCl(g)+O(g)2Cl(g)+2HO(g)
2 2 2 2
ΔH,研究发现CuCl (s)催化反应的过程如下:
2
反应ⅰ:2CuCl (s)2CuCl(s)+Cl(g)
2 2
反应ⅱ:2CuCl(s)+O(g)2CuO(s)+Cl(g)
2 2
反应ⅲ:……
下列关于Deacon催化氧化法制Cl 的说法正确的是( )
2A.反应 ⅰ 增大压强,达到新平衡后Cl 浓度减小
2
B.反应4HCl(g)+O(g)2Cl(g)+2HO(g)的ΔH>0
2 2 2
C.由反应过程可知催化剂参与反应,通过改变反应路径提高平衡转化率
D.推断反应 ⅲ 应为CuO(s)+2HCl(g)CuCl (s)+HO(g)
2 2
11.如图所示,左室容积为右室的两倍,温度相同,现分别按照如图所示的量充入气体,同
时加入少量固体催化剂使两室内气体充分反应达到平衡,打开活塞,继续反应再次达到平衡。
下列说法不正确的是( )
A.第一次平衡时,SO 的物质的量左室更多
2
B.气体未反应前,左室压强和右室一样大
C.第一次平衡时,左室内压强一定小于右室
D.第二次平衡时,SO 的总物质的量比第一次平衡时左室SO 的物质的量的2倍多
2 2
12.(2023·安徽蚌埠统考模拟)能源的合理开发和利用、低碳减排是人类正在努力解决的大问
题。
(1)在固相催化剂作用下CO 加氢合成甲烷过程中发生以下两个反应:
2
主反应:CO(g)+4H(g)CH(g)+2HO(g) ΔH=-156.9 kJ·mol-1
2 2 4 2 1
副反应:CO(g)+H(g)CO(g)+HO(g) ΔH=+41.1 kJ·mol-1
2 2 2 2
工业合成甲烷通常控制温度为500 ℃左右,其主要原因为____________________________
_____________________________________________________________________________。
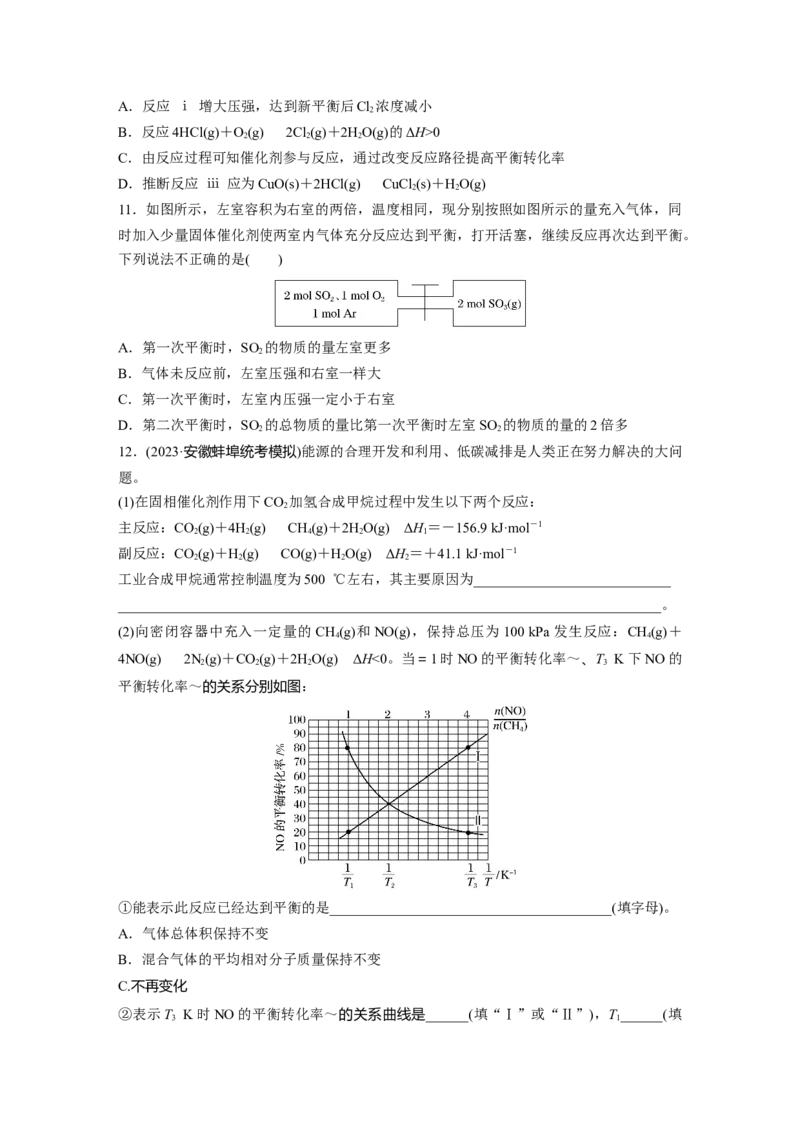
(2)向密闭容器中充入一定量的 CH(g)和NO(g),保持总压为100 kPa发生反应:CH(g)+
4 4
4NO(g)2N(g)+CO(g)+2HO(g) ΔH<0。当=1时NO的平衡转化率~、T K下NO的
2 2 2 3
平衡转化率~的关系分别如图:
①能表示此反应已经达到平衡的是________________________________________(填字母)。
A.气体总体积保持不变
B.混合气体的平均相对分子质量保持不变
C.不再变化
②表示T K时NO的平衡转化率~的关系曲线是______(填“Ⅰ”或“Ⅱ”),T______(填
3 1“>”或“<”)T。
2
③在=1、T K时,CH 的平衡分压为______________。
2 4
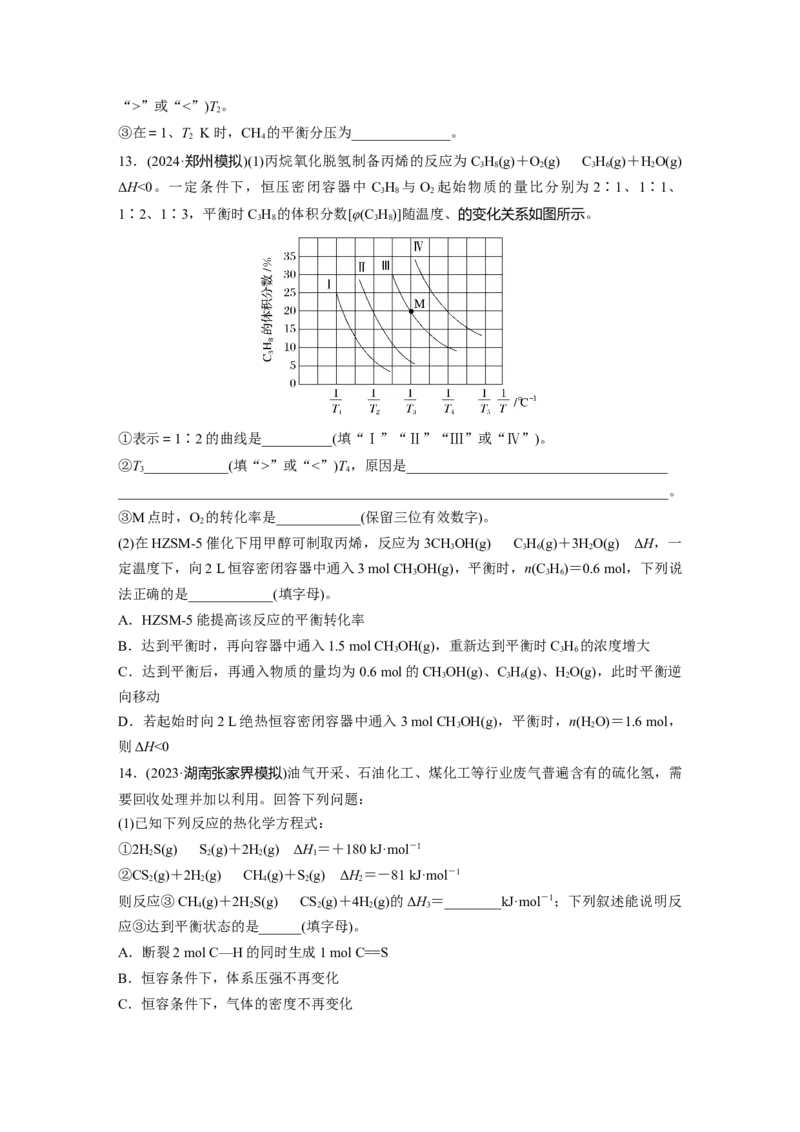
13.(2024·郑州模拟)(1)丙烷氧化脱氢制备丙烯的反应为C H(g)+O(g)C H(g)+HO(g)
3 8 2 3 6 2
ΔH<0。一定条件下,恒压密闭容器中 C H 与O 起始物质的量比分别为 2∶1、1∶1、
3 8 2
1∶2、1∶3,平衡时C H 的体积分数[φ(C H)]随温度、的变化关系如图所示。
3 8 3 8
①表示=1∶2的曲线是__________(填“Ⅰ”“Ⅱ”“Ⅲ”或“Ⅳ”)。
②T____________(填“>”或“<”)T,原因是_____________________________________
3 4
______________________________________________________________________________。
③M点时,O 的转化率是____________(保留三位有效数字)。
2
(2)在HZSM-5催化下用甲醇可制取丙烯,反应为3CHOH(g)C H(g)+3HO(g) ΔH,一
3 3 6 2
定温度下,向2 L恒容密闭容器中通入3 mol CH OH(g),平衡时,n(C H)=0.6 mol,下列说
3 3 6
法正确的是____________(填字母)。
A.HZSM-5能提高该反应的平衡转化率
B.达到平衡时,再向容器中通入1.5 mol CH OH(g),重新达到平衡时C H 的浓度增大
3 3 6
C.达到平衡后,再通入物质的量均为0.6 mol的CHOH(g)、C H(g)、HO(g),此时平衡逆
3 3 6 2
向移动
D.若起始时向2 L绝热恒容密闭容器中通入3 mol CH OH(g),平衡时,n(H O)=1.6 mol,
3 2
则ΔH<0
14.(2023·湖南张家界模拟)油气开采、石油化工、煤化工等行业废气普遍含有的硫化氢,需
要回收处理并加以利用。回答下列问题:
(1)已知下列反应的热化学方程式:
①2HS(g)S(g)+2H(g) ΔH=+180 kJ·mol-1
2 2 2 1
②CS(g)+2H(g)CH(g)+S(g) ΔH=-81 kJ·mol-1
2 2 4 2 2
则反应③CH(g)+2HS(g)CS(g)+4H(g)的ΔH =________kJ·mol-1;下列叙述能说明反
4 2 2 2 3
应③达到平衡状态的是______(填字母)。
A.断裂2 mol C—H的同时生成1 mol C==S
B.恒容条件下,体系压强不再变化
C.恒容条件下,气体的密度不再变化D.v正 (H
2
S)=2v逆 (CS
2
)
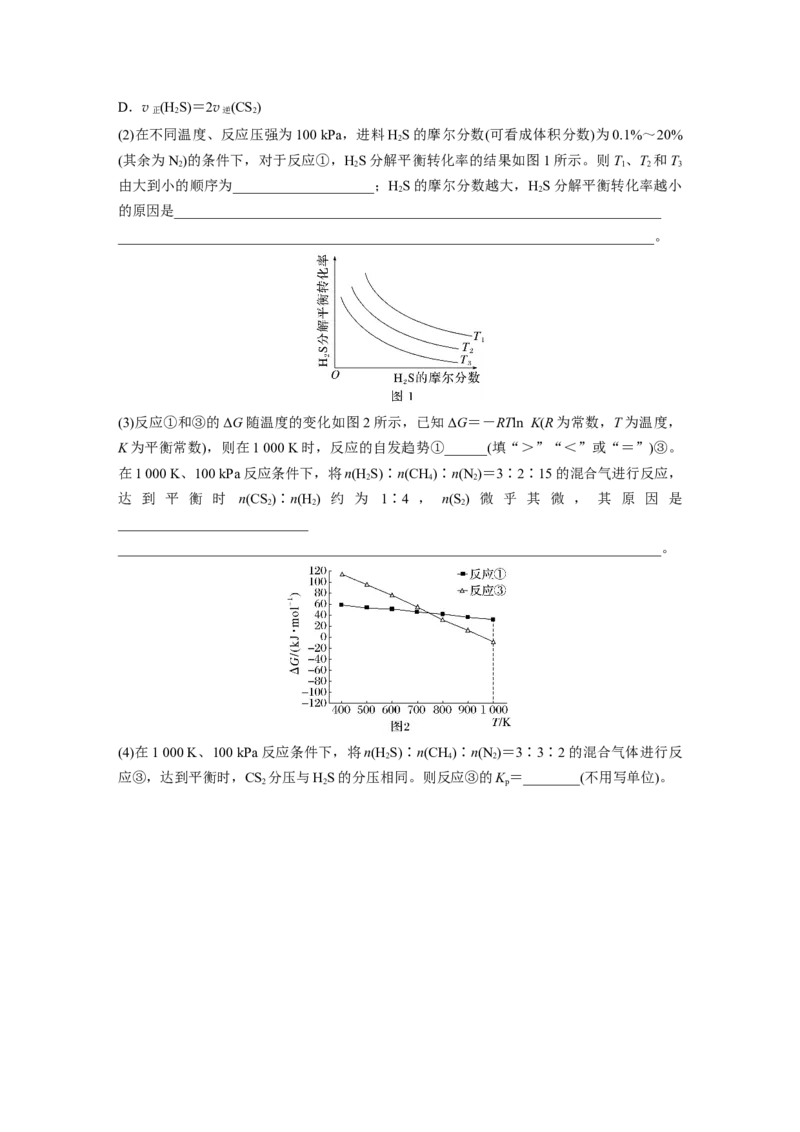
(2)在不同温度、反应压强为100 kPa,进料HS的摩尔分数(可看成体积分数)为0.1%~20%
2
(其余为N)的条件下,对于反应①,HS分解平衡转化率的结果如图1所示。则T 、T 和T
2 2 1 2 3
由大到小的顺序为____________________;HS的摩尔分数越大,HS分解平衡转化率越小
2 2
的原因是_____________________________________________________________________
____________________________________________________________________________。
(3)反应①和③的ΔG随温度的变化如图2所示,已知ΔG=-RTln K(R为常数,T为温度,
K为平衡常数),则在1 000 K时,反应的自发趋势①______(填“>”“<”或“=”)③。
在1 000 K、100 kPa反应条件下,将n(H S)∶n(CH)∶n(N )=3∶2∶15的混合气进行反应,
2 4 2
达 到 平 衡 时 n(CS)∶n(H ) 约 为 1∶4 , n(S ) 微 乎 其 微 , 其 原 因 是
2 2 2
___________________________
_____________________________________________________________________________。
(4)在1 000 K、100 kPa反应条件下,将n(H S)∶n(CH)∶n(N )=3∶3∶2的混合气体进行反
2 4 2
应③,达到平衡时,CS 分压与HS的分压相同。则反应③的K =________(不用写单位)。
2 2 p