文档内容
1.(2022·重庆,14)两种酸式碳酸盐的分解反应如下。某温度平衡时总压强分别为p 和p。
1 2
反应1:NH HCO (s)NH (g)+HO(g)+CO(g) p=3.6×104 Pa
4 3 3 2 2 1
反应2:2NaHCO (s)NaCO(s)+HO(g)+CO(g) p=4×103 Pa
3 2 3 2 2 2
该温度下,刚性密闭容器中放入NH HCO 和NaCO 固体,平衡后以上3种固体均大量存在。
4 3 2 3
下列说法错误的是( )
A.反应2的平衡常数为4×106 Pa2
B.通入NH ,再次平衡后,总压强增大
3
C.平衡后总压强为4.36×105 Pa
D.缩小体积,再次平衡后总压强不变
2.已知反应X(g)+Y(g)R(g)+Q(g)的平衡常数与温度的关系如表所示。830 ℃时,向一
个2 L的密闭容器中充入0.2 mol X和0.8 mol Y,反应初始4 s内v(X)=0.005 mol·L-1·s-1。
下列说法正确的是( )
温度/℃ 700 800 830 1 000 1 200
平衡常数 1.7 1.1 1.0 0.6 0.4
A.4 s时容器内c(Y)=0.76 mol·L-1
B.830 ℃达平衡时,X的转化率为80%
C.反应达平衡后,升高温度,平衡正向移动
D.1 200 ℃时反应R(g)+Q(g)X(g)+Y(g)的平衡常数K=0.4
3.将固体NH I置于密闭容器中,在一定温度下发生下列反应:
4
①NH I(s)NH (g)+HI(g);
4 3
②2HI(g)H(g)+I(g)。
2 2
达到平衡时,c(H )=0.5 mol·L-1,c(HI)=4 mol·L-1,下列说法错误的是( )
2
A.①的平衡常数为20
B.②的平衡常数为
C.同温时H(g)+I(g)2HI(g)和②的平衡常数互为倒数
2 2
D.温度升高,①的平衡常数增大,则①为放热反应
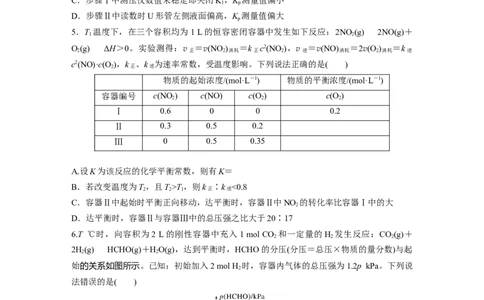
4.氨基甲酸铵发生分解的化学方程式为 NH COONH(s)2NH (g)+CO(g)。利用如下装
2 4 3 2
置测定不同温度下该反应以分压表示的化学平衡常数K 。
p
步骤Ⅰ:关闭K,打开K 和K,开启真空泵抽气至测压仪数值稳定后关闭K;
3 1 2 1
步骤Ⅱ:关闭K,缓慢开启K 至U形管两边液面相平并保持不变,读取压强数值。
2 3
记录25 ℃、30 ℃下压强分别为12.0 kPa、17.1 kPa。下列说法错误的是( )A.氨基甲酸铵分解反应的ΔH>0
B.该反应25 ℃时的化学平衡常数K =2.56×1011 Pa3
p
C.步骤Ⅰ中测压仪数值未稳定即关闭K,K 测量值偏小
1 p
D.步骤Ⅱ中读数时U形管左侧液面偏高,K 测量值偏大
p
5.T 温度下,在三个容积均为1 L的恒容密闭容器中发生如下反应:2NO (g)2NO(g)+
1 2
O
2
(g) ΔH>0。实验测得:v正 =v(NO
2
)
消耗
=k
正
c2(NO
2
),v逆 =v(NO)
消耗
=2v(O
2
)
消耗
=k
逆
c2(NO)·c(O ),k 、k 为速率常数,受温度影响。下列说法正确的是( )
2 正 逆
物质的起始浓度/(mol·L-1) 物质的平衡浓度/(mol·L-1)
容器编号 c(NO ) c(NO) c(O ) c(O )
2 2 2
Ⅰ 0.6 0 0 0.2
Ⅱ 0.3 0.5 0.2
Ⅲ 0 0.5 0.35
A.设K为该反应的化学平衡常数,则有K=
B.若改变温度为T,且T>T,则k ∶k <0.8
2 2 1 正 逆
C.容器Ⅱ中起始时平衡正向移动,达平衡时,容器Ⅱ中NO 的转化率比容器Ⅰ中的大
2
D.达平衡时,容器Ⅱ与容器Ⅲ中的总压强之比大于20∶17
6.T ℃时,向容积为2 L的刚性容器中充入1 mol CO 和一定量的H 发生反应:CO(g)+
2 2 2
2H(g)HCHO(g)+HO(g),达到平衡时,HCHO的分压(分压=总压×物质的量分数)与起
2 2
始的关系如图所示。已知:初始加入2 mol H 时,容器内气体的总压强为1.2p kPa。下列说
2
法错误的是( )
A.5 min时反应到达c点,v(H )=0.1 mol·L-1·min-1
2
B.随增大,HCHO的平衡压强不断增大
C.b点时反应的平衡常数K = kPa-1
p
D.c点时,再加入CO(g)和HO(g),使二者分压均增大0.2p kPa,平衡不移动
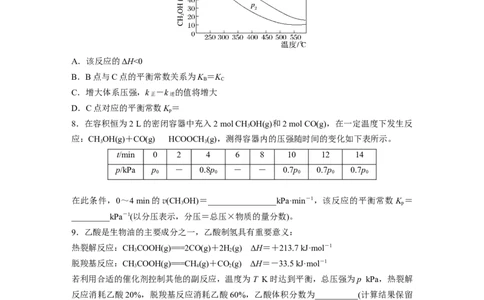
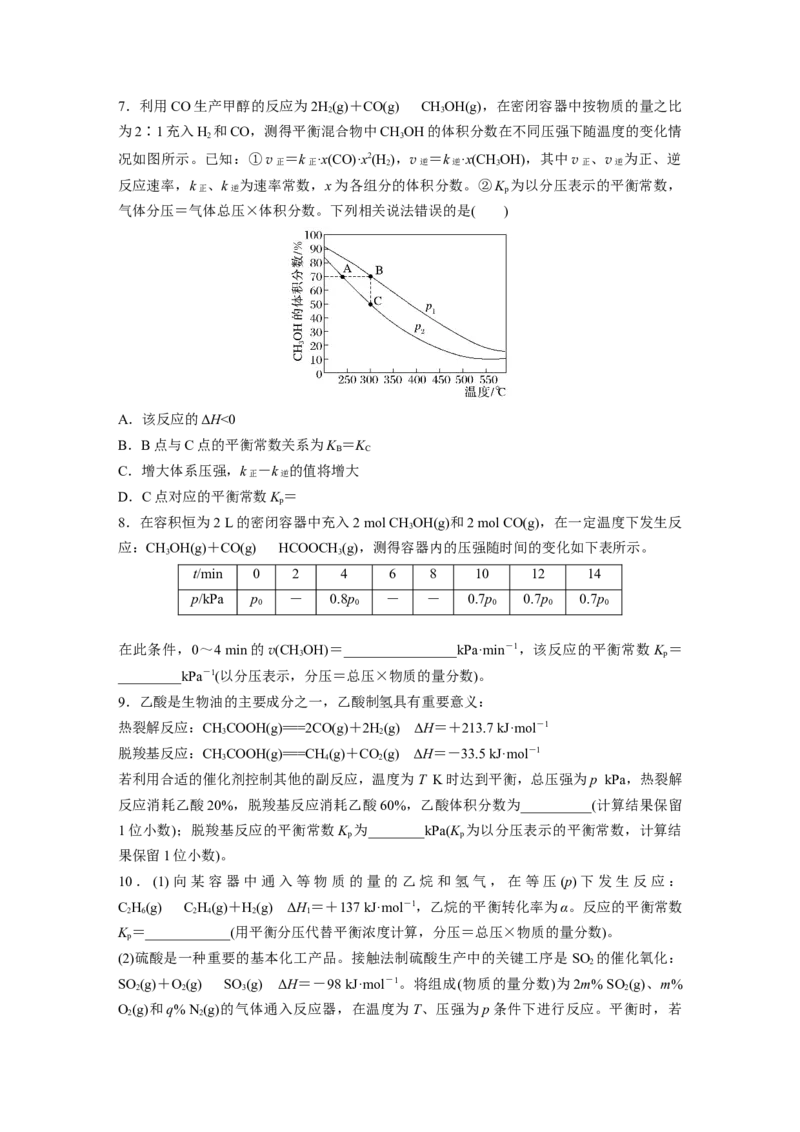
2 27.利用CO生产甲醇的反应为2H(g)+CO(g)CHOH(g),在密闭容器中按物质的量之比
2 3
为2∶1充入H 和CO,测得平衡混合物中CHOH的体积分数在不同压强下随温度的变化情
2 3
况如图所示。已知:①v正 =k
正
·x(CO)·x2(H
2
),v逆 =k
逆
·x(CH
3
OH),其中v正 、v逆 为正、逆
反应速率,k 、k 为速率常数,x为各组分的体积分数。②K 为以分压表示的平衡常数,
正 逆 p
气体分压=气体总压×体积分数。下列相关说法错误的是( )
A.该反应的ΔH<0
B.B点与C点的平衡常数关系为K =K
B C
C.增大体系压强,k -k 的值将增大
正 逆
D.C点对应的平衡常数K =
p
8.在容积恒为2 L的密闭容器中充入2 mol CH OH(g)和2 mol CO(g),在一定温度下发生反
3
应:CHOH(g)+CO(g)HCOOCH (g),测得容器内的压强随时间的变化如下表所示。
3 3
t/min 0 2 4 6 8 10 12 14
p/kPa p - 0.8p - - 0.7p 0.7p 0.7p
0 0 0 0 0
在此条件,0~4 min的v(CHOH)=________________kPa·min-1,该反应的平衡常数K =
3 p
_________kPa-1(以分压表示,分压=总压×物质的量分数)。
9.乙酸是生物油的主要成分之一,乙酸制氢具有重要意义:
热裂解反应:CHCOOH(g)===2CO(g)+2H(g) ΔH=+213.7 kJ·mol-1
3 2
脱羧基反应:CHCOOH(g)===CH(g)+CO(g) ΔH=-33.5 kJ·mol-1
3 4 2
若利用合适的催化剂控制其他的副反应,温度为T K时达到平衡,总压强为p kPa,热裂解
反应消耗乙酸20%,脱羧基反应消耗乙酸60%,乙酸体积分数为__________(计算结果保留
1位小数);脱羧基反应的平衡常数K 为________kPa(K 为以分压表示的平衡常数,计算结
p p
果保留1位小数)。
10.(1)向某容器中通入等物质的量的乙烷和氢气,在等压(p)下发生反应:
C H(g)C H(g)+H(g) ΔH =+137 kJ·mol-1,乙烷的平衡转化率为α。反应的平衡常数
2 6 2 4 2 1
K =____________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
p
(2)硫酸是一种重要的基本化工产品。接触法制硫酸生产中的关键工序是 SO 的催化氧化:
2
SO (g)+O(g)SO (g) ΔH=-98 kJ·mol-1。将组成(物质的量分数)为2m% SO (g)、m%
2 2 3 2
O(g)和q% N (g)的气体通入反应器,在温度为T、压强为p条件下进行反应。平衡时,若
2 2SO 转化率为α,则SO 压强为____________,平衡常数K =____________________(以分压
2 3 p
表示,分压=总压×物质的量分数)。
11.已知:NO(g)2NO (g) ΔH>0。298 K时,将一定量NO 气体充入恒容的密闭容器
2 4 2 2 4
中发生反应。t 时刻反应达到平衡,混合气体平衡总压强为 p,NO 气体的平衡转化率为
1 2 4
25%,则NO 的分压为________(分压=总压×物质的量分数),反应NO(g)2NO (g)的平
2 2 4 2
衡常数K =________[对于气相反应,用某组分B的物质的量分数x(B)代替物质的量浓度
x
c(B)也可表示平衡常数,记作K]。
x
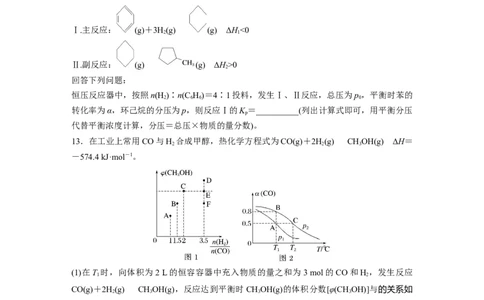
12.[2021·辽宁,17(6)]苯催化加氢制备环己烷是化工生产中的重要工艺,一定条件下,发
生如下反应:
Ⅰ.主反应: (g)+3H(g) (g) ΔH<0
2 1
Ⅱ.副反应: (g) (g) ΔH>0
2
回答下列问题:
恒压反应器中,按照n(H )∶n(C H)=4∶1投料,发生Ⅰ、Ⅱ反应,总压为p ,平衡时苯的
2 6 6 0
转化率为α,环己烷的分压为p,则反应Ⅰ的K =__________(列出计算式即可,用平衡分压
p
代替平衡浓度计算,分压=总压×物质的量分数)。
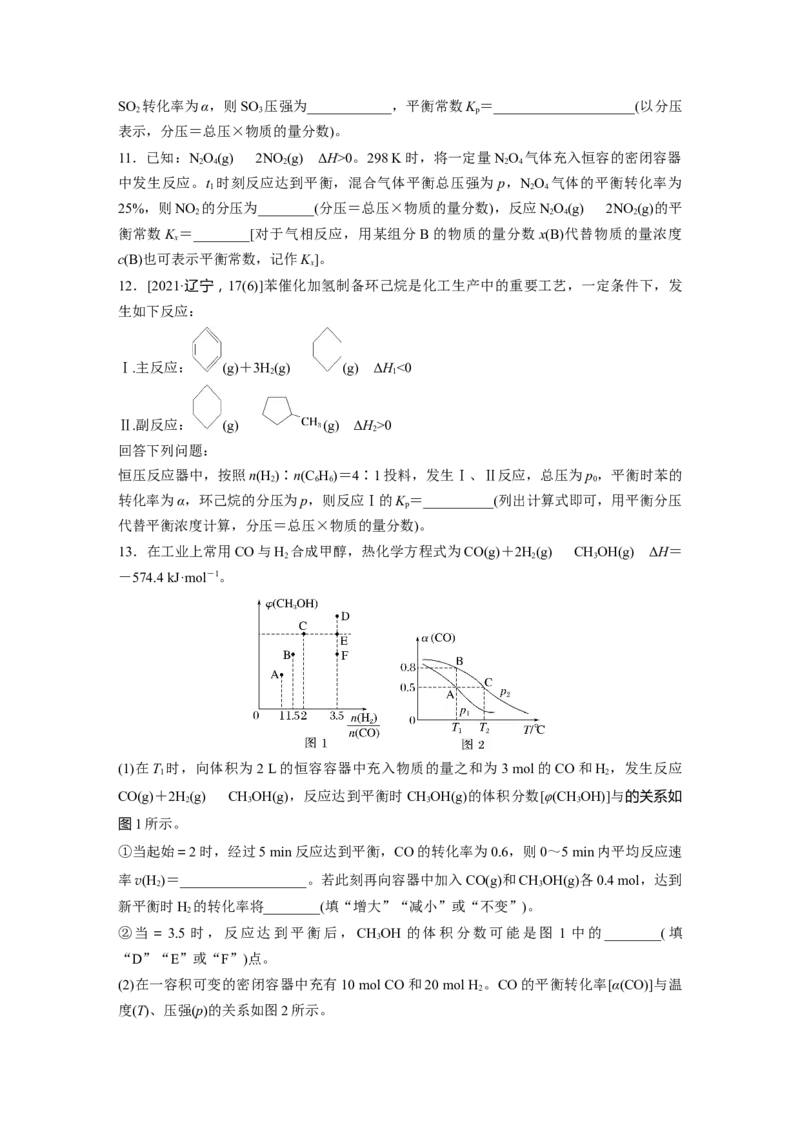
13.在工业上常用CO与H 合成甲醇,热化学方程式为CO(g)+2H(g)CHOH(g) ΔH=
2 2 3
-574.4 kJ·mol-1。
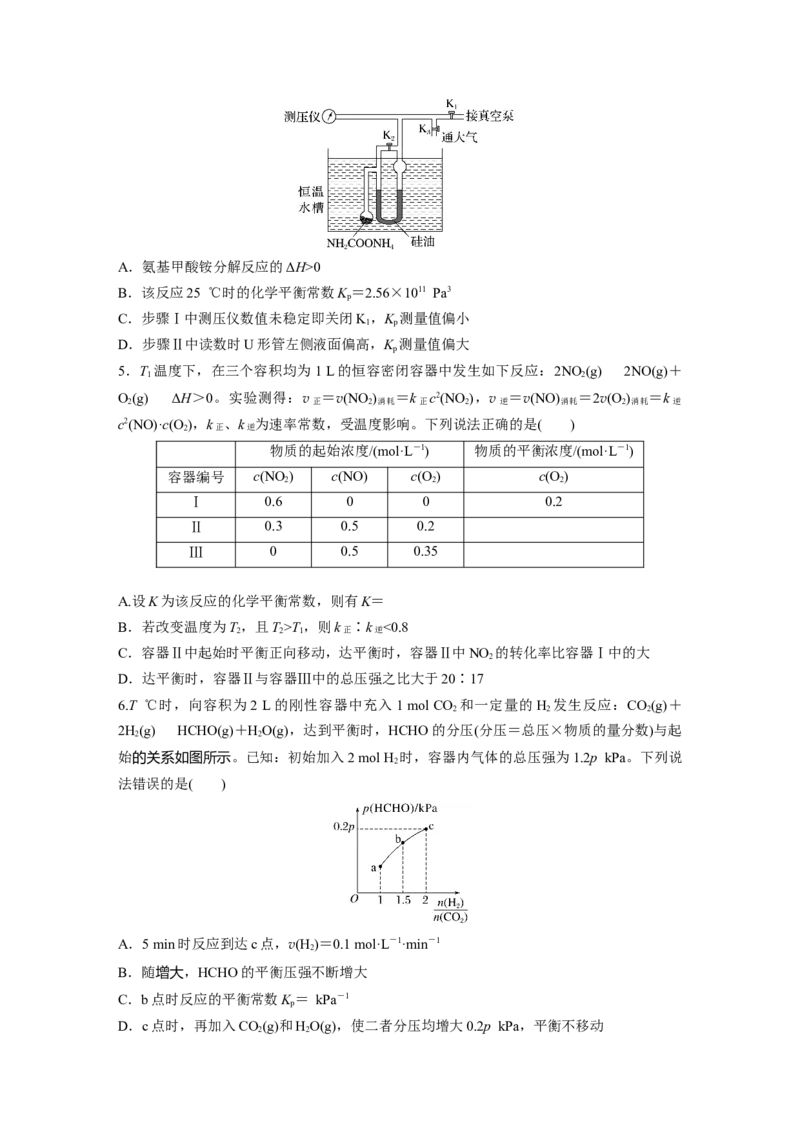
(1)在T 时,向体积为2 L的恒容容器中充入物质的量之和为3 mol的CO和H ,发生反应
1 2
CO(g)+2H(g)CHOH(g),反应达到平衡时CHOH(g)的体积分数[φ(CHOH)]与的关系如
2 3 3 3
图1所示。
①当起始=2时,经过5 min反应达到平衡,CO的转化率为0.6,则0~5 min内平均反应速
率v(H )=__________________。若此刻再向容器中加入CO(g)和CHOH(g)各0.4 mol,达到
2 3
新平衡时H 的转化率将________(填“增大”“减小”或“不变”)。
2
②当=3.5 时,反应达到平衡后,CHOH 的体积分数可能是图 1 中的________(填
3
“D”“E”或“F”)点。
(2)在一容积可变的密闭容器中充有10 mol CO和20 mol H 。CO的平衡转化率[α(CO)]与温
2
度(T)、压强(p)的关系如图2所示。①A、B、C三点对应的平衡常数K 、K 、K 的大小关系为____________。
A B C
②若达到平衡状态A时,容器的体积为10 L,则在平衡状态B时容器的体积为________L。