文档内容
1.下列依据热化学方程式得出的结论正确的是( )
A.已知Ni(CO) (s)===Ni(s)+4CO(g) ΔH=Q kJ·mol-1,则Ni(s)+4CO(g)===Ni(CO) (s)
4 4
ΔH=-Q kJ·mol-1
B.在一定温度和压强下,将 0.5 mol N 和 1.5 mol H 置于密闭容器中充分反应生成
2 2
NH (g),放出热量 19.3 kJ,则其热化学方程式为 N(g)+H(g)NH (g) ΔH=-19.3
3 2 2 3
kJ·mol-1
C.已知2H(g)+O(g)===2HO(l) ΔH,2H(g)+O(g)===2HO(g) ΔH,则ΔH>ΔH
2 2 2 1 2 2 2 2 1 2
D.已知C(s,石墨)===C(s,金刚石) ΔH>0,则金刚石比石墨稳定
2.(2023·太原模拟)分别向1 L 0.5 mol·L-1的Ba(OH) 溶液中加入①浓硫酸;②稀硫酸;③
2
稀硝酸,恰好完全反应时的热效应分别为ΔH、ΔH、ΔH,下列关系正确的是( )
1 2 3
A.ΔH>ΔH>ΔH B.ΔH<ΔH<ΔH
1 2 3 1 2 3
C.ΔH>ΔH=ΔH D.ΔH=ΔH<ΔH
1 2 3 1 2 3
3.(2023·北京市第一六六中学高三期中)以CO和H 为原料合成甲醇是工业上的成熟方法,
2
直接以CO 为原料生产甲醇是目前的研究热点。我国科学家用CO 人工合成淀粉时,第一步
2 2
就需要将CO 转化为甲醇。
2
已知:①CO(g)+2H(g)===CHOH(g) ΔH=-90.5 kJ·mol-1
2 3 1
②CO(g)+HO(g)===CO(g)+H(g) ΔH=-41.1 kJ·mol-1
2 2 2 2
③2H(g)+ O(g)===2HO(g) ΔH=-483.6 kJ·mol-1
2 2 2 3
下列说法不正确的是( )
A.若温度不变,反应①中生成1 mol CH OH(l)时,放出的热量大于90.5 kJ
3
B.CO 与H 合成甲醇的热化学方程式为CO(g)+3H(g)===CHOH(g)+HO(g)
2 2 2 2 3 2
ΔH=-49.4 kJ·mol-1
C.通过电解制H 和选用高效催化剂,可降低CO 与H 合成甲醇反应的焓变
2 2 2
D.以CO 和HO为原料合成甲醇,同时生成O,该反应需要吸收能量
2 2 2
4.根据碘与氢气反应的热化学方程式:
(ⅰ)I(?)+H(g)2HI(g) ΔH=-9.48 kJ·mol-1;
2 2
(ⅱ)I(?)+H(g)2HI(g) ΔH=+26.48 kJ·mol-1。
2 2
下列判断正确的是( )
A.反应(ⅰ)中的I 为固态,反应(ⅱ)中的I 为气态
2 2
B.1 mol固态碘与1 mol气态碘所含的能量相差35.96 kJ
C.反应(ⅰ)的生成物比反应(ⅱ)的生成物稳定
D.254 g I(g)中通入2 g H(g),反应放热9.48 kJ
2 2
5.向NaCO 溶液中滴加盐酸,反应过程中能量变化如图所示,下列说法正确的是( )
2 3A.反应HCO(aq)+H+(aq)===CO(g)+HO(l)为放热反应
2 2
B.CO(aq)+2H+(aq)===CO(g)+HO(l) ΔH=ΔH+ΔH+ΔH
2 2 1 2 3
C.ΔH>ΔH;ΔH<ΔH
1 2 2 3
D.HCO(aq)===CO(g)+HO(l),若使用催化剂,则ΔH 变小
2 3 2 2 3
6.在一定温度压强下,依据图示关系,下列说法不正确的是( )
A.C(s,石墨)+ CO(g) ===2CO(g) ΔH=ΔH-ΔH
2 1 2
B.1 mol C(s,石墨)和1 mol C(s,金刚石)分别与足量O 反应全部转化为CO(g) ,前者放
2 2
热多
C.ΔH=ΔH-ΔH
5 1 3
D.化学反应的ΔH只与反应体系的始态和终态有关,与反应途径无关
7.在25 ℃、101 kPa时,C(s)、H(g)、CHCOOH(l)的燃烧热分别为393.5 kJ·mol-1、285.8
2 3
kJ·
mol-1、870.3 kJ·mol-1,则2C(s)+2H(g)+O(g)===CHCOOH(l)的反应热为( )
2 2 3
A.-488.3 kJ·mol-1 B.+488.3 kJ·mol-1
C.-191 kJ·mol-1 D.+191 kJ·mol-1
8.黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为
S(s)+2KNO(s)+3C(s)===KS(s)+N(g)+3CO(g) ΔH=x kJ·mol-1
3 2 2 2
已知:①碳的燃烧热ΔH=a kJ·mol-1
1
②S(s)+2K(s)===KS(s) ΔH=b kJ·mol-1
2 2
③2K(s)+N(g)+3O(g)===2KNO(s) ΔH=c kJ·mol-1,则x为( )
2 2 3 3
A.3a+b-c B.c-3a-b
C.a+b-c D.c-a-b
9.室温下,将1 mol的CuSO ·5H O(s)溶于水会使溶液温度降低,热效应为ΔH ,将1 mol
4 2 1
的CuSO (s)溶于水会使溶液温度升高,热效应为ΔH ;CuSO ·5H O(s)受热分解的化学方程
4 2 4 2
式为CuSO ·5H O(s)===CuSO (s)+5HO(l),热效应为ΔH。下列判断正确的是( )
4 2 4 2 3
A.ΔH>ΔH B.ΔH<ΔH
2 3 1 3C.ΔH+ΔH=ΔH D.ΔH+ΔH>ΔH
1 3 2 1 2 3
10.已知:①2H(g)+O(g)===2HO(g) ΔH
2 2 2 1
②3H(g)+Fe O(s)===2Fe(s)+3HO(g) ΔH
2 2 3 2 2
③2Fe(s)+O(g)===Fe O(s) ΔH
2 2 3 3
④2Al(s)+O(g)===Al O(s) ΔH
2 2 3 4
⑤2Al(s)+Fe O(s)===Al O(s)+2Fe(s) ΔH
2 3 2 3 5
下列关于上述反应焓变的判断正确的是( )
A.ΔH<0,ΔH>0
1 3
B.ΔH<0,ΔH<ΔH
5 4 3
C.ΔH=ΔH+ΔH
1 2 3
D.ΔH=ΔH+ΔH
3 4 5
11.镁和氯气反应生成氯化镁的能量关系图如图所示。
已知:气态的卤素原子得电子生成气态的卤素离子是放热过程。下列说法正确的是( )
A.ΔH=ΔH+ΔH+ΔH+ΔH+ΔH
6 1 2 3 4 5
B.Ca(g)-2e-===Ca2+(g) ΔH,则ΔH>ΔH
7 7 3
C.I(g)+e-===I-(g) ΔH,则ΔH>ΔH
8 8 4
D.MgCl (s)===Mg2+(aq)+2Cl-(aq) ΔH,则ΔH>ΔH
2 9 9 5
12.(2021·浙江6月选考,21)相同温度和压强下,关于反应的ΔH,下列判断正确的是(
)
(g)+H(g)―→ (g) ΔH
2 1
(g)+2H(g)―→ (g) ΔH
2 2
(g)+3H(g)―→ (g) ΔH
2 3
(g)+H(g)―→ (g) ΔH
2 4
A.ΔH>0,ΔH>0
1 2
B.ΔH=ΔH+ΔH
3 1 2
C.ΔH>ΔH,ΔH>ΔH
1 2 3 2D.ΔH=ΔH+ΔH
2 3 4
13.(1)[2023·全国甲卷,28(1)节选]已知下列反应的热化学方程式:
①3O(g)===2O(g) ΔH=+285 kJ·mol-1
2 3 1
②2CH(g)+O(g)===2CHOH(l) ΔH=-329 kJ·mol-1
4 2 3 2
反应③CH(g)+O(g)===CHOH(l)+O(g)的ΔH=________kJ·mol-1。
4 3 3 2 3
(2)[2023·浙江6月选考,19(1)]水煤气变换反应是工业上的重要反应,可用于制氢。
水煤气变换反应:CO(g)+HO(g)CO(g)+H(g) ΔH=-41.2 kJ·mol-1
2 2 2
该反应分两步完成:
3Fe O(s)+CO(g)2Fe O(s)+CO(g) ΔH=-47.2 kJ·mol-1
2 3 3 4 2 1
2Fe O(s)+HO(g)3Fe O(s)+H(g)
3 4 2 2 3 2
ΔH
2
则ΔH=__________kJ·mol-1。
2
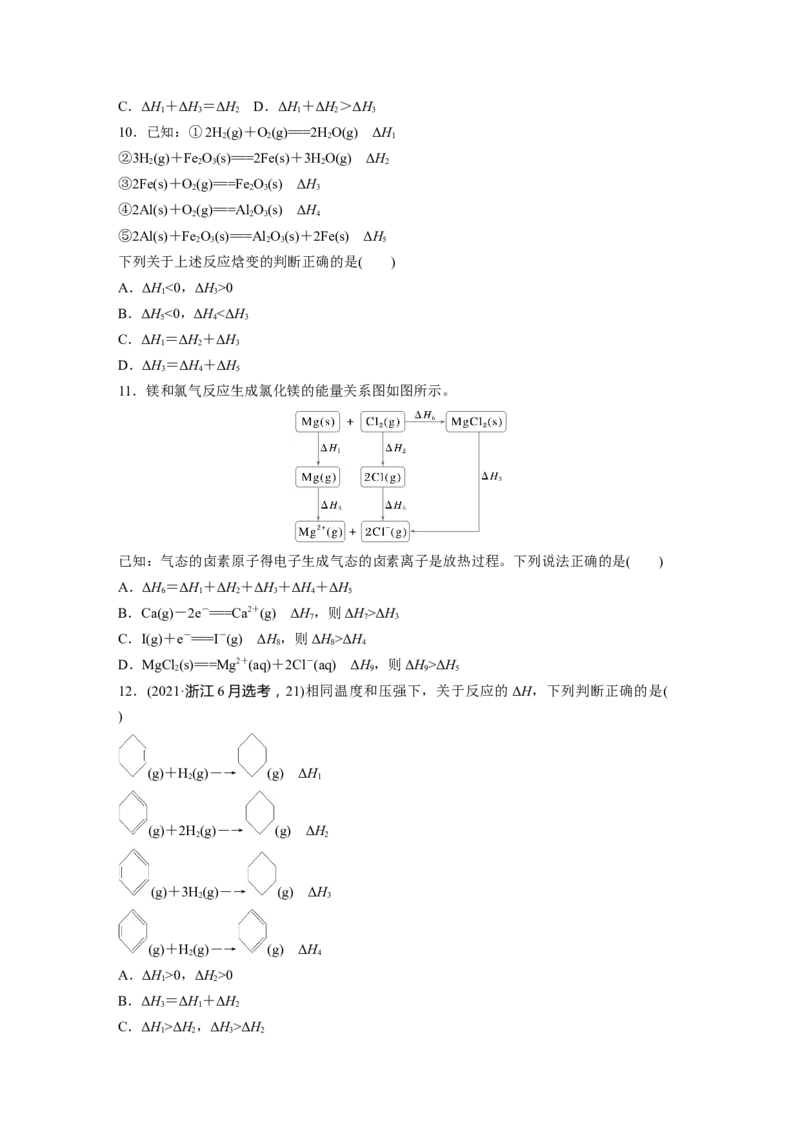
14.(1)[2022·广东,19(1)②]Cr O 催化丙烷脱氢过程中,部分反应历程如图,X(g)→Y(g)过
2 3
程的焓变为__________________________________________________________(列式表示)。
(2)[2022·湖北,19(1)]已知:
①CaO(s)+HO(l)Ca(OH) (s) ΔH=-65.17 kJ·mol-1
2 2 1
②Ca(OH) (s)Ca2+(aq)+2OH-(aq) ΔH=-16.73 kJ·mol-1
2 2
③Al(s)+OH-(aq)+3HO(l)[Al(OH) ]-(aq)+H(g) ΔH=-415.0 kJ·mol-1
2 4 2 3
则CaO(s)+2Al(s)+7HO(l)===Ca2+(aq)+2[Al(OH) ]-(aq)+3H(g)的ΔH =_______kJ·mol-
2 4 2 4
1。
15.(1)[2022·福建,13(1)]异丙醇(C HO)可由生物质转化得到,催化异丙醇脱水制取高值化
3 8
学品丙烯(C H)的工业化技术已引起人们的关注。其主要反应如下:
3 6
Ⅰ.C HO(g)C H(g)+HO(g) ΔH=+52 kJ·mol-1
3 8 3 6 2 1
Ⅱ.2C H(g)C H (g) ΔH=-97 kJ·mol-1
3 6 6 12 2
已知2C HO(g)+9O(g)===6CO(g)+8HO(g) ΔH=-3 750 kJ·mol-1,则C H(g)燃烧生成
3 8 2 2 2 3 6
CO(g)和HO(g)的热化学方程式为_______________________________________________
2 2
_____________________________________________________________________________。
(2)[2022·天津,16(1)]科研人员把铁的配合物Fe3+L(L为配体)溶于弱碱性的海水中,制成吸
收液,将气体HS转化为单质硫,改进了湿法脱硫工艺。该工艺包含两个阶段:①HS的吸
2 2收氧化;②Fe3+L的再生。反应原理如下:
①HS(g)+2Fe3+L(aq)+2OH-(aq)===S(s)+2Fe2+L(aq)+2HO(l) ΔH=-a kJ·mol-1(a>0)
2 2
②4Fe2+L(aq)+O(g)+2HO(l)===4Fe3+L(aq)+4OH-(aq) ΔH=-b kJ·mol-1(b>0)
2 2
该工艺的总反应方程式为_______________________________________________________
_____________________________________________________________________________。
1 mol H S(g)发生该反应的热量变化为________________,Fe3+L 在总反应中的作用是
2
____________。