文档内容
1.化学与人类生活、社会可持续发展密切相关,下列说法正确的是( )
A.直接燃烧煤和将煤进行深加工后再燃烧的效率相同
B.天然气、水能属于一次能源,水煤气、电能属于二次能源
C.人们可以把放热反应释放的能量转化为其他可利用的能量,而吸热反应没有利用价值
D.地热能、风能、天然气和氢能都属于新能源
2.已知2H(g)+CO(g)===CHOH(g)为放热反应,下列对该反应的说法正确的是( )
2 3
A.因该反应为放热反应,故不加热就可发生
B.相同条件下,2 mol H (g)的能量或1 mol CO(g)的能量一定高于1 mol CH OH(g)的能量
2 3
C.相同条件下,2 mol H (g)和1 mol CO(g)的总能量一定高于1 mol CH OH(g)的总能量
2 3
D.达到平衡时,CO的浓度与CHOH的浓度一定相等
3
3.某同学设计如图所示实验,探究反应中的能量变化。
下列判断正确的是( )
A.由实验可知,(a)、(b)、(c)所涉及的反应都是放热反应
B.将实验(a)中的铝片更换为等质量的铝粉后释放出的热量有所增加
C.实验(c)中将玻璃搅拌器改为铁质搅拌器对实验结果没有影响
D.若用NaOH固体测定中和反应反应热,则测定结果数值偏高
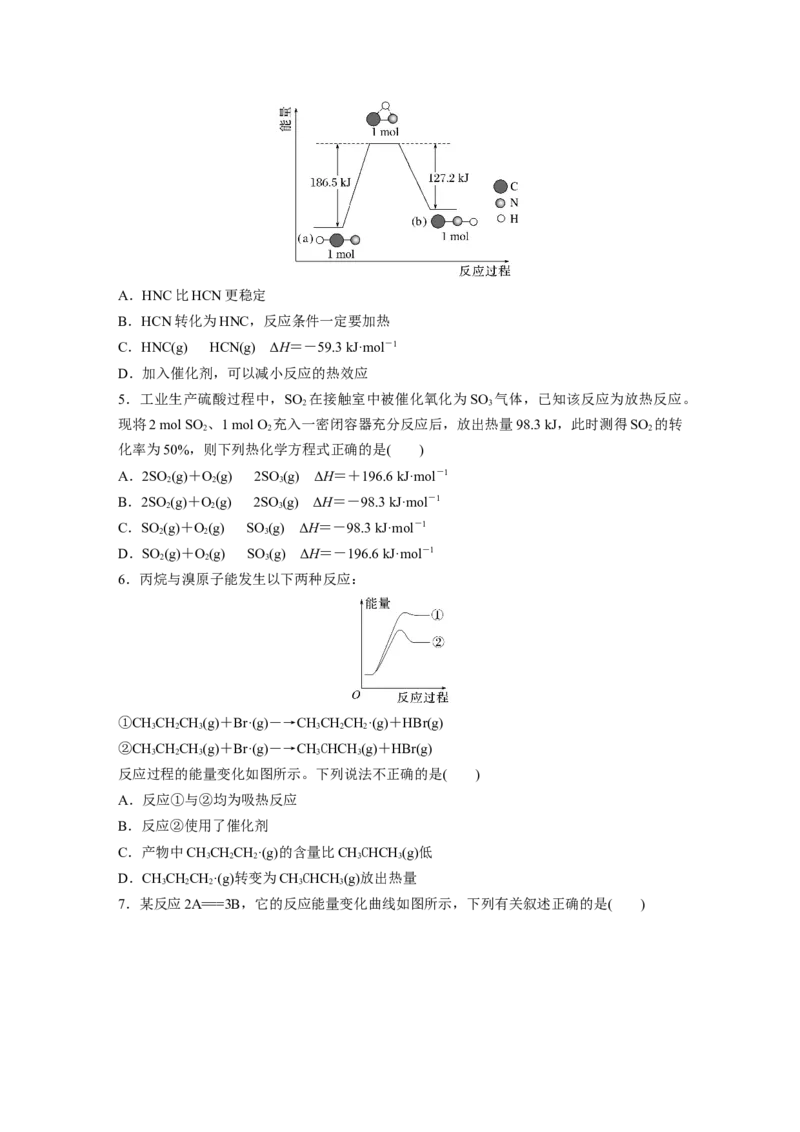
4.研究表明,在一定条件下,气态HCN(a)与HNC(b)两种分子的互变反应过程能量变化如
图所示。下列说法正确的是( )A.HNC比HCN更稳定
B.HCN转化为HNC,反应条件一定要加热
C.HNC(g)HCN(g) ΔH=-59.3 kJ·mol-1
D.加入催化剂,可以减小反应的热效应
5.工业生产硫酸过程中,SO 在接触室中被催化氧化为SO 气体,已知该反应为放热反应。
2 3
现将2 mol SO 、1 mol O 充入一密闭容器充分反应后,放出热量98.3 kJ,此时测得SO 的转
2 2 2
化率为50%,则下列热化学方程式正确的是( )
A.2SO (g)+O(g)2SO (g) ΔH=+196.6 kJ·mol-1
2 2 3
B.2SO (g)+O(g)2SO (g) ΔH=-98.3 kJ·mol-1
2 2 3
C.SO (g)+O(g)SO (g) ΔH=-98.3 kJ·mol-1
2 2 3
D.SO (g)+O(g)SO (g) ΔH=-196.6 kJ·mol-1
2 2 3
6.丙烷与溴原子能发生以下两种反应:
①CHCHCH(g)+Br·(g)―→CHCHCH·(g)+HBr(g)
3 2 3 3 2 2
②CHCHCH(g)+Br·(g)―→CHCHCH (g)+HBr(g)
3 2 3 3 3
反应过程的能量变化如图所示。下列说法不正确的是( )
A.反应①与②均为吸热反应
B.反应②使用了催化剂
C.产物中CHCHCH·(g)的含量比CHCHCH (g)低
3 2 2 3 3
D.CHCHCH·(g)转变为CHCHCH (g)放出热量
3 2 2 3 3
7.某反应2A===3B,它的反应能量变化曲线如图所示,下列有关叙述正确的是( )A.该反应为吸热反应
B.A比B更稳定
C.加入催化剂会改变反应的焓变
D.整个反应的ΔH=E-E
1 2
8.根据下列已知条件,所写热化学方程式正确的是( )
A.H 的燃烧热为a kJ·mol-1:H(g)+Cl(g)=====2HCl(g) ΔH=-a kJ·mol-1
2 2 2
B.1 mol SO 、0.5 mol O 完全反应,放出热量98.3 kJ:2SO (g)+O(g)2SO (g)
2 2 2 2 3
ΔH=-98.3 kJ·mol-1
C . H + (aq) + OH - (aq)===HO(l) ΔH = - 57.3 kJ·mol - 1 , 则 HSO (aq) +
2 2 4
Ba(OH) (aq)===BaSO(s)+2HO(l) ΔH=-114.6 kJ·mol-1
2 4 2
D.96 g O(g)能量比96 g O(g)的能量低b kJ:3O(g)2O(g) ΔH=+b kJ·mol-1
2 3 2 3
9.反应M+Z―→Q(ΔH<0)分两步进行:①M+Z―→X(ΔH>0),②X―→Q(ΔH<0)。下
列示意图中,能正确表示总反应过程中能量变化的是( )
10.(2021·浙江1月选考,20)已知共价键的键能与热化学方程式信息如下表:
共价键 H—H H—O
键能/ (kJ·mol-1) 436 463
2H(g)+O(g)===2HO(g)
2 2 2
热化学方程式
ΔH=-482 kJ·mol-1
则2O(g)===O(g)的ΔH为( )
2
A.428 kJ·mol-1 B.-428 kJ·mol-1C.498 kJ·mol-1 D.-498 kJ·mol-1
11.下列示意图表示正确的是( )
A.甲图表示Fe O(s)+3CO(g)===2Fe(s)+3CO(g) ΔH=+26.7 kJ·mo1-1反应的能量变化
2 3 2
B.乙图表示碳的燃烧热
C.丙图表示实验的环境温度为 20 ℃,将物质的量浓度相等、体积分别为 V 、V 的
1 2
HSO 、NaOH溶液混合,混合液的最高温度随V(NaOH)的变化(已知V+V=60 mL)
2 4 1 2
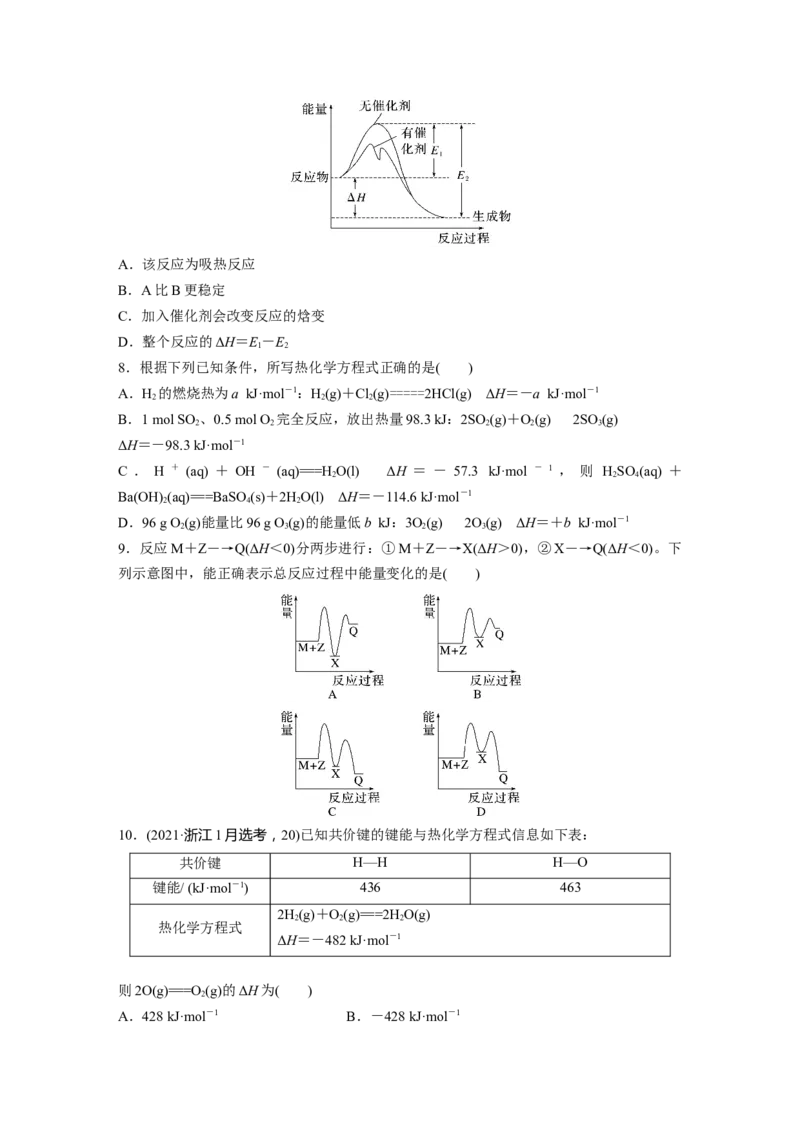
D.已知稳定性顺序:B0
B.在此反应过程中Ni的成键数目未发生变化
C.该反应过程中,最大能垒(活化能)为204.32 kJ·mol-1
D.整个过程中,Ni是该反应的催化剂
13.(1)已知CHOH(l)的燃烧热ΔH=-726.5 kJ·mol-1,CHOH(l)+O(g)===CO(g)+2H(g)
3 3 2 2 2
ΔH=-a kJ·mol-1,则a____(填“>”“<”或“=”)726.5。
(2)将Cl 和HO(g)通过灼热的炭层,生成 HCl和CO ,当有1 mol Cl 参与反应时释放出
2 2 2 2
145.0 kJ热量,写出该反应的热化学方程式:________________________。
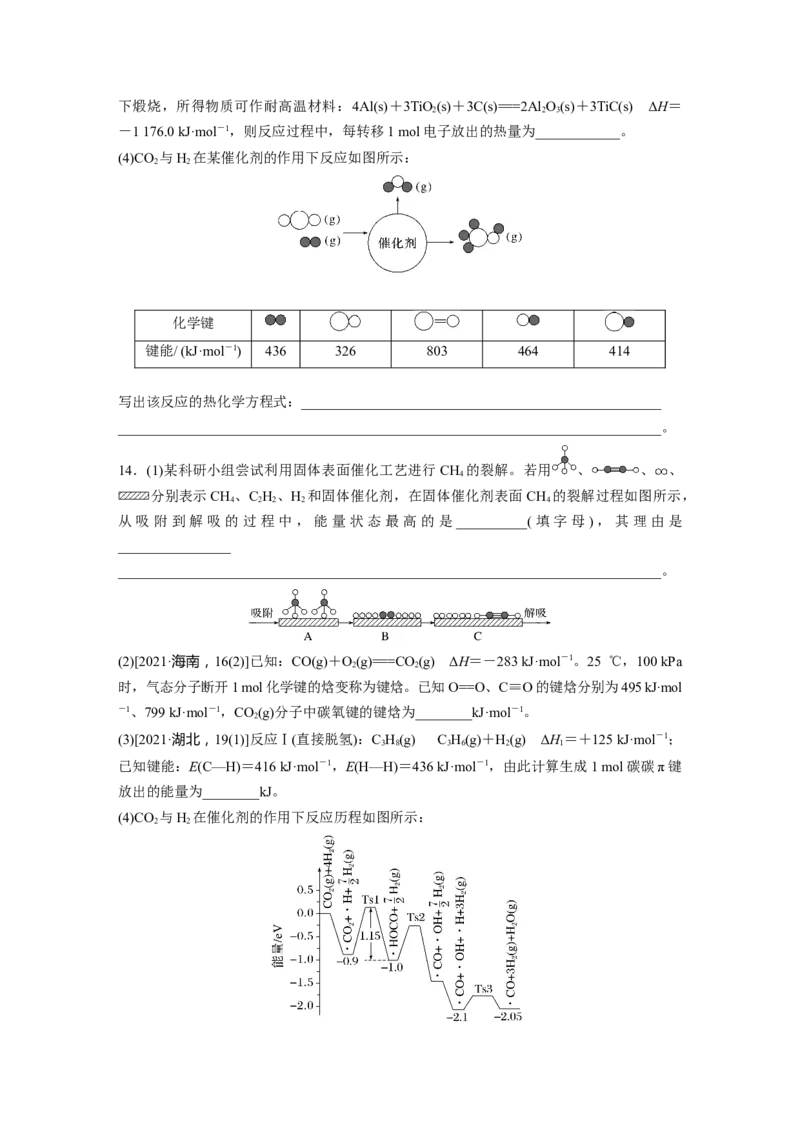
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料:4Al(s)+3TiO(s)+3C(s)===2Al O(s)+3TiC(s) ΔH=
2 2 3
-1 176.0 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为____________。
(4)CO 与H 在某催化剂的作用下反应如图所示:
2 2
化学键
键能/ (kJ·mol-1) 436 326 803 464 414
写出该反应的热化学方程式:___________________________________________________
_____________________________________________________________________________。
14.(1)某科研小组尝试利用固体表面催化工艺进行CH 的裂解。若用 、 、 、
4
分别表示CH 、C H 、H 和固体催化剂,在固体催化剂表面CH 的裂解过程如图所示,
4 2 2 2 4
从吸附到解吸的过程中,能量状态最高的是__________(填字母),其理由是
________________
_____________________________________________________________________________。
(2)[2021·海南,16(2)]已知:CO(g)+O(g)===CO(g) ΔH=-283 kJ·mol-1。25 ℃,100 kPa
2 2
时,气态分子断开1 mol化学键的焓变称为键焓。已知O==O、C≡O的键焓分别为495 kJ·mol
-1、799 kJ·mol-1,CO(g)分子中碳氧键的键焓为________kJ·mol-1。
2
(3)[2021·湖北,19(1)]反应Ⅰ(直接脱氢):C H(g)C H(g)+H(g) ΔH=+125 kJ·mol-1;
3 8 3 6 2 1
已知键能:E(C—H)=416 kJ·mol-1,E(H—H)=436 kJ·mol-1,由此计算生成1 mol碳碳π键
放出的能量为________kJ。
(4)CO 与H 在催化剂的作用下反应历程如图所示:
2 2反应历程中活化能(能垒)最大的化学方程式为_____________________________________,
CO(g)+H(g)===·CO(g)+HO(g)
2 2 2
ΔH=________eV·mol-1。