文档内容
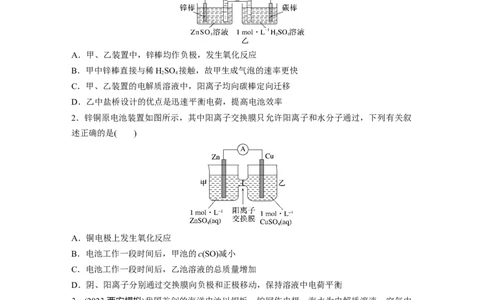
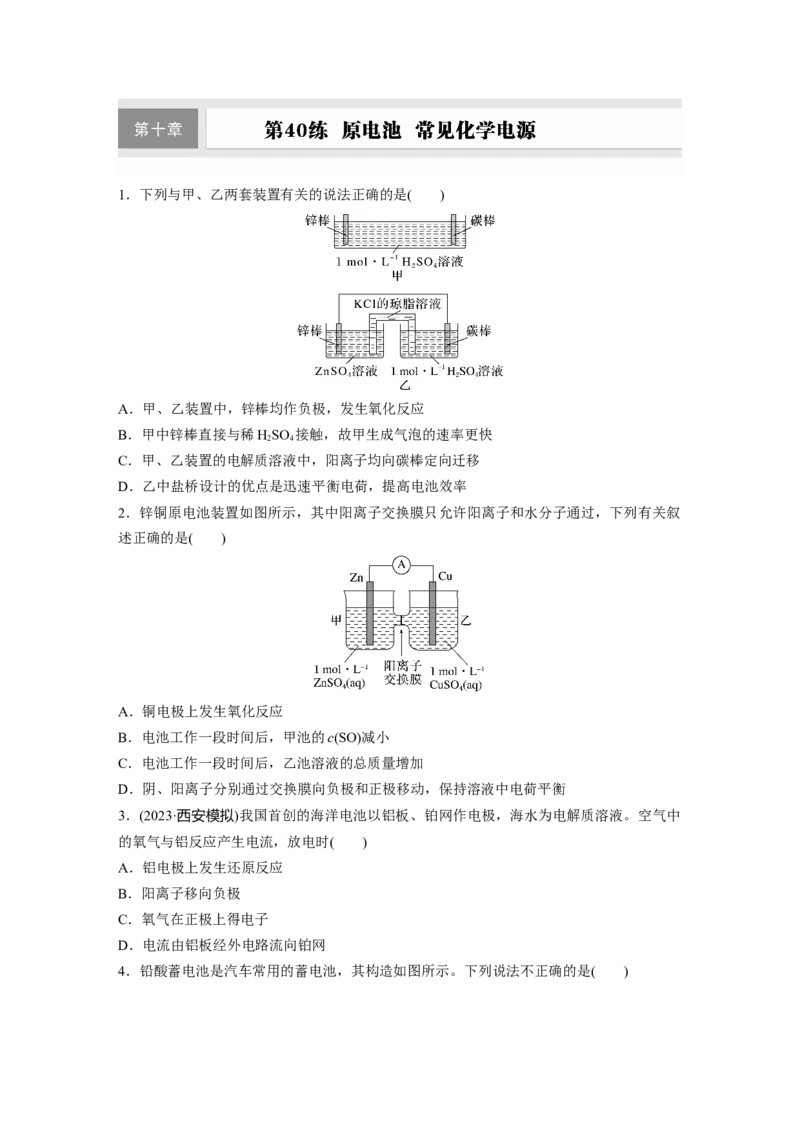
1.下列与甲、乙两套装置有关的说法正确的是( )
A.甲、乙装置中,锌棒均作负极,发生氧化反应
B.甲中锌棒直接与稀HSO 接触,故甲生成气泡的速率更快
2 4
C.甲、乙装置的电解质溶液中,阳离子均向碳棒定向迁移
D.乙中盐桥设计的优点是迅速平衡电荷,提高电池效率
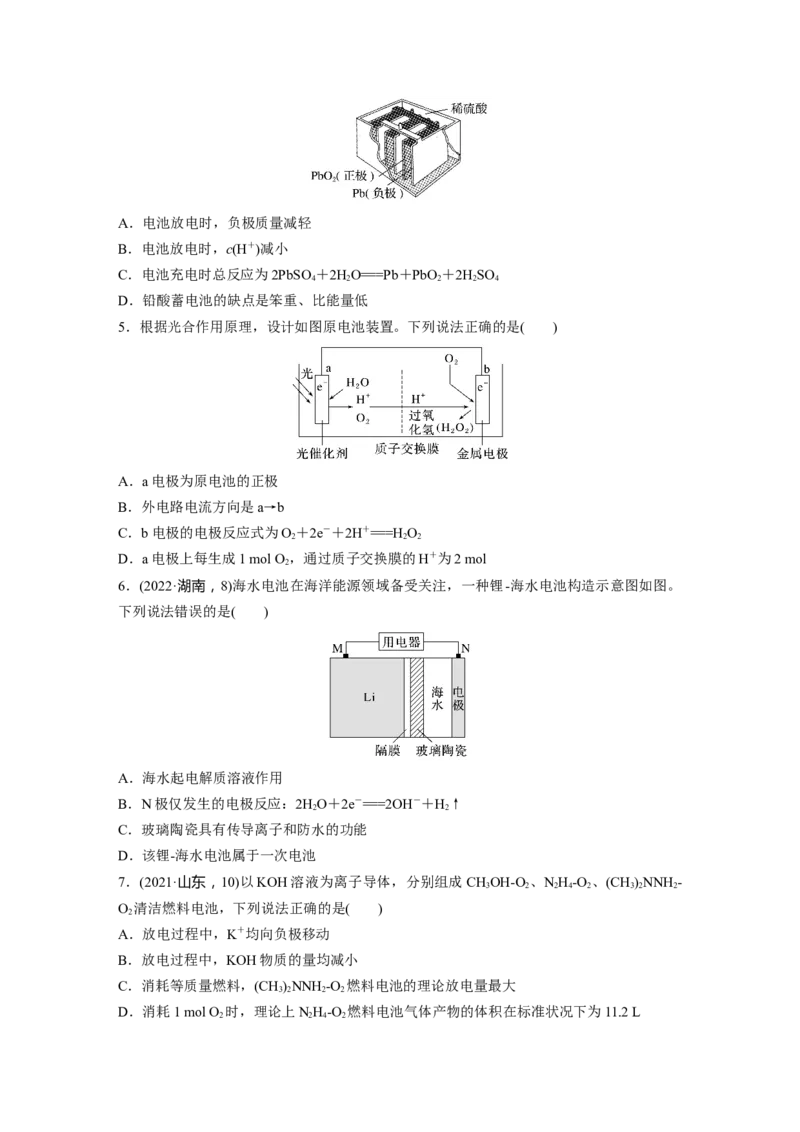
2.锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙
述正确的是( )
A.铜电极上发生氧化反应
B.电池工作一段时间后,甲池的c(SO)减小
C.电池工作一段时间后,乙池溶液的总质量增加
D.阴、阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
3.(2023·西安模拟)我国首创的海洋电池以铝板、铂网作电极,海水为电解质溶液。空气中
的氧气与铝反应产生电流,放电时( )
A.铝电极上发生还原反应
B.阳离子移向负极
C.氧气在正极上得电子
D.电流由铝板经外电路流向铂网
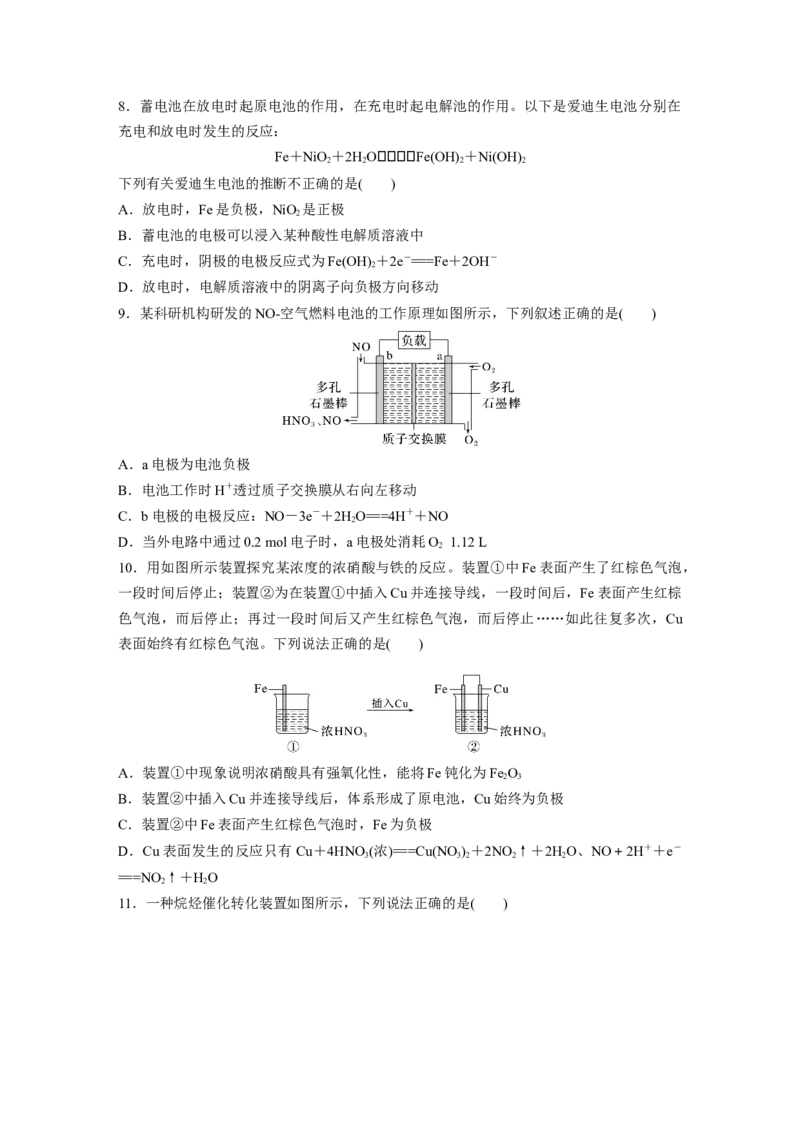
4.铅酸蓄电池是汽车常用的蓄电池,其构造如图所示。下列说法不正确的是( )A.电池放电时,负极质量减轻
B.电池放电时,c(H+)减小
C.电池充电时总反应为2PbSO +2HO===Pb+PbO +2HSO
4 2 2 2 4
D.铅酸蓄电池的缺点是笨重、比能量低
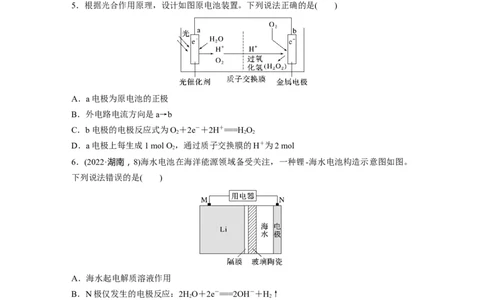
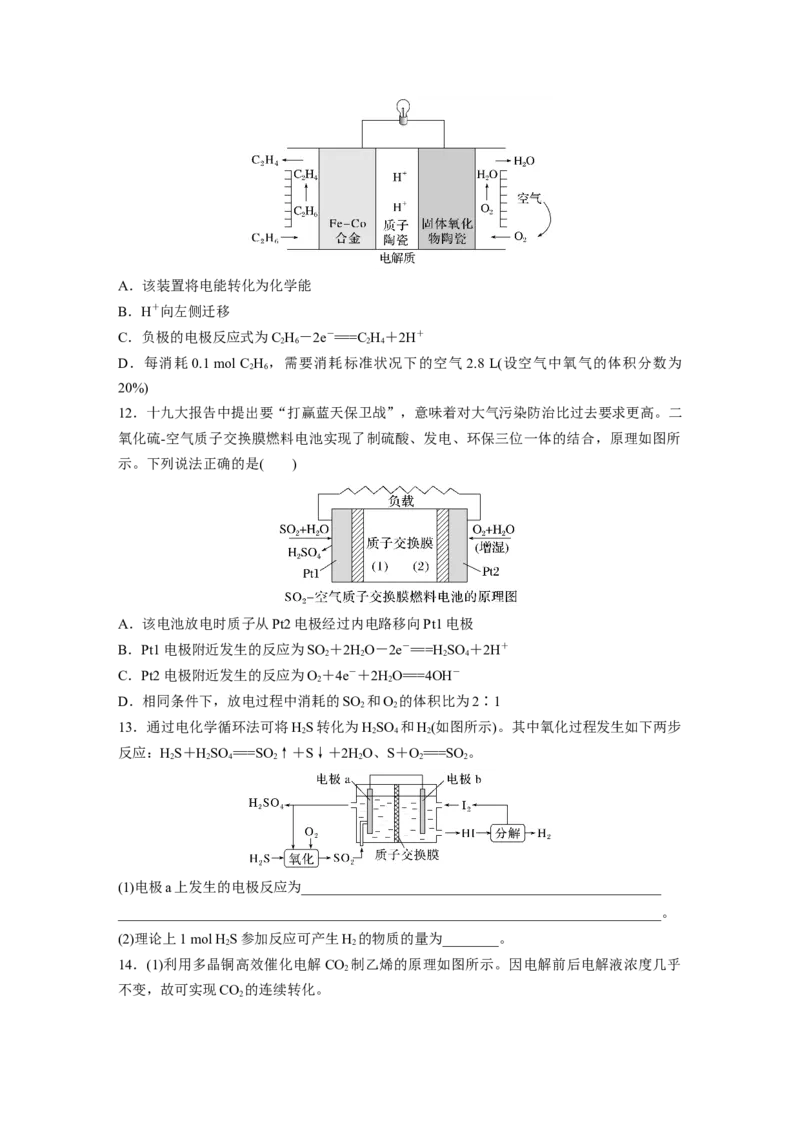
5.根据光合作用原理,设计如图原电池装置。下列说法正确的是( )
A.a电极为原电池的正极
B.外电路电流方向是a→b
C.b电极的电极反应式为O+2e-+2H+===HO
2 2 2
D.a电极上每生成1 mol O ,通过质子交换膜的H+为2 mol
2
6.(2022·湖南,8)海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如图。
下列说法错误的是( )
A.海水起电解质溶液作用
B.N极仅发生的电极反应:2HO+2e-===2OH-+H↑
2 2
C.玻璃陶瓷具有传导离子和防水的功能
D.该锂-海水电池属于一次电池
7.(2021·山东,10)以KOH溶液为离子导体,分别组成CHOH-O 、NH-O 、(CH)NNH-
3 2 2 4 2 3 2 2
O 清洁燃料电池,下列说法正确的是( )
2
A.放电过程中,K+均向负极移动
B.放电过程中,KOH物质的量均减小
C.消耗等质量燃料,(CH)NNH-O 燃料电池的理论放电量最大
3 2 2 2
D.消耗1 mol O 时,理论上NH-O 燃料电池气体产物的体积在标准状况下为11.2 L
2 2 4 28.蓄电池在放电时起原电池的作用,在充电时起电解池的作用。以下是爱迪生电池分别在
充电和放电时发生的反应:
Fe+NiO+2HOFe(OH) +Ni(OH)
2 2 2 2
下列有关爱迪生电池的推断不正确的是( )
A.放电时,Fe是负极,NiO 是正极
2
B.蓄电池的电极可以浸入某种酸性电解质溶液中
C.充电时,阴极的电极反应式为Fe(OH) +2e-===Fe+2OH-
2
D.放电时,电解质溶液中的阴离子向负极方向移动
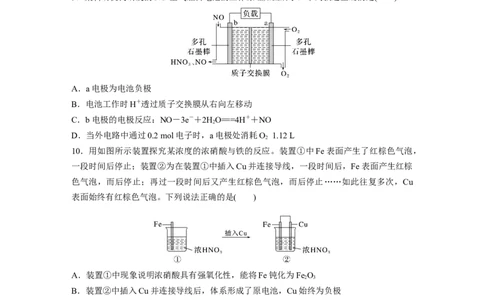
9.某科研机构研发的NO-空气燃料电池的工作原理如图所示,下列叙述正确的是( )
A.a电极为电池负极
B.电池工作时H+透过质子交换膜从右向左移动
C.b电极的电极反应:NO-3e-+2HO===4H++NO
2
D.当外电路中通过0.2 mol电子时,a电极处消耗O 1.12 L
2
10.用如图所示装置探究某浓度的浓硝酸与铁的反应。装置①中Fe表面产生了红棕色气泡,
一段时间后停止;装置②为在装置①中插入Cu并连接导线,一段时间后,Fe表面产生红棕
色气泡,而后停止;再过一段时间后又产生红棕色气泡,而后停止……如此往复多次,Cu
表面始终有红棕色气泡。下列说法正确的是( )
A.装置①中现象说明浓硝酸具有强氧化性,能将Fe钝化为Fe O
2 3
B.装置②中插入Cu并连接导线后,体系形成了原电池,Cu始终为负极
C.装置②中Fe表面产生红棕色气泡时,Fe为负极
D.Cu表面发生的反应只有Cu+4HNO(浓)===Cu(NO ) +2NO ↑+2HO、NO+2H++e-
3 3 2 2 2
===NO ↑+HO
2 2
11.一种烷烃催化转化装置如图所示,下列说法正确的是( )A.该装置将电能转化为化学能
B.H+向左侧迁移
C.负极的电极反应式为C H-2e-===C H+2H+
2 6 2 4
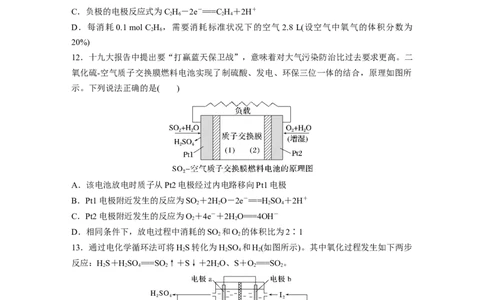
D.每消耗0.1 mol C H ,需要消耗标准状况下的空气 2.8 L(设空气中氧气的体积分数为
2 6
20%)
12.十九大报告中提出要“打赢蓝天保卫战”,意味着对大气污染防治比过去要求更高。二
氧化硫-空气质子交换膜燃料电池实现了制硫酸、发电、环保三位一体的结合,原理如图所
示。下列说法正确的是( )
A.该电池放电时质子从Pt2电极经过内电路移向Pt1电极
B.Pt1电极附近发生的反应为SO +2HO-2e-===HSO +2H+
2 2 2 4
C.Pt2电极附近发生的反应为O+4e-+2HO===4OH-
2 2
D.相同条件下,放电过程中消耗的SO 和O 的体积比为2∶1
2 2
13.通过电化学循环法可将HS转化为HSO 和H(如图所示)。其中氧化过程发生如下两步
2 2 4 2
反应:HS+HSO ===SO ↑+S↓+2HO、S+O===SO 。
2 2 4 2 2 2 2
(1)电极a上发生的电极反应为___________________________________________________
_____________________________________________________________________________。
(2)理论上1 mol H S参加反应可产生H 的物质的量为________。
2 2
14.(1)利用多晶铜高效催化电解CO 制乙烯的原理如图所示。因电解前后电解液浓度几乎
2
不变,故可实现CO 的连续转化。
2①电解过程中HCO向________(填“铂”或“多晶铜”)电极方向移动。
②多晶铜电极的电极反应式为___________________________________________________
_____________________________________________________________________________。
③理论上当生成0.05 mol乙烯时,铂电极产生的气体在标准状况下体积为__________(不考
虑气体的溶解)。
(2)某钠离子电池结构如图所示,电极A为含钠过渡金属氧化物(NaTMO),电极B为硬碳,
x 2
充电时Na+得电子成为Na嵌入硬碳中,NaTMO 失去电子生成Na TMO ,充电时B极的
2 1-x 2
电极反应式:_________________________________________________________________,
放电时A极的电极反应式:_____________________________________________________
_____________________________________________________________________________。