文档内容
考向 07 铁及其化合物
【2022湖南卷】为探究 的性质,进行了如下实验( 和 溶液浓度均为 )。
实
操作与现象
验
① 在 水中滴加2滴 溶液,呈棕黄色;煮沸,溶液变红褐色。
在 溶液中滴加2滴 溶液,变红褐色;
②
再滴加 溶液,产生蓝色沉淀。
在 溶液中滴加2滴 溶液,变红褐色;
③
将上述混合液分成两份,一份滴加 溶液,无蓝色沉淀生;
另一份煮沸,产生红褐色沉淀。
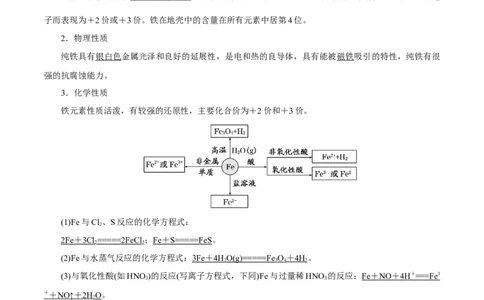
依据上述实验现象,结论不合理的是A.实验①说明加热促进 水解反应
B.实验②说明 既发生了水解反应,又发生了还原反应
C.实验③说明 发生了水解反应,但没有发生还原反应
D.整个实验说明 对 的水解反应无影响,但对还原反应有影响
【答案】D
【解析】铁离子水解显酸性,亚硫酸根离子水解显碱性,两者之间存在相互促进的水解反应,同时铁离子
具有氧化性,亚硫酸根离子具有还原性,两者还会发生氧化还原反应,在同一反应体系中,铁离子的水解
反应与还原反应共存并相互竞争,结合实验分析如下:实验①为对照实验,说明铁离子在水溶液中显棕黄
色,存在水解反应Fe3++3H O Fe(OH) +3H+,煮沸,促进水解平衡正向移动,得到红褐色的氢氧化铁
2 3
胶体;实验②说明少量亚硫酸根离子加入铁离子后,两者发生水解反应得到红褐色的氢氧化铁胶体;根据铁氰化钾检测结果可知,同时发生氧化还原反应,使铁离子被还原为亚铁离子,而出现特征蓝色沉淀;实
验③通过反滴操作,根据现象描述可知,溶液仍存在铁离子的水解反应,但由于铁离子少量,没检测出亚
铁离子的存在,说明铁离子的水解反应速率快,铁离子的还原反应未来得及发生。
A.铁离子的水解反应为吸热反应,加热煮沸可促进水解平衡正向移动,使水解程度加深,生成较多的氢
氧化铁,从而使溶液显红褐色,故A正确;
B.在5mLFeCl 溶液中滴加2滴同浓度的NaSO 溶液,根据现象和分析可知,Fe3+既发生了水解反应,生
3 2 3
成红褐色的氢氧化铁,又被亚硫酸根离子还原,得到亚铁离子,加入铁氰化钾溶液后,出现特征蓝色沉淀,
故B正确;
C.实验③中在5mL Na SO 溶液中滴加2滴同浓度少量FeCl 溶液,根据现象和分析可知,仍发生铁离子
2 3 3
的水解反应,但未来得及发生铁离子的还原反应,即水解反应比氧化还原反应速率快,故C正确;
D.结合三组实验,说明铁离子与亚硫酸根离子混合时,铁离子的水解反应占主导作用,比氧化还原反应
的速率快,因证据不足,不能说明亚硫酸离子对铁离子的水解作用无影响,事实上,亚硫酸根离子水解显
碱性,可促进铁离子的水解反应,故D错误。
综上所述,答案为D。知识点一 铁的主要性质及应用
1.原子结构
铁位于元素周期表第四周期第Ⅷ族,原子结构示意图为 ,在化学反应中易失去2个或3个电
子而表现为+2价或+3价。铁在地壳中的含量在所有元素中居第4位。
2.物理性质
纯铁具有银白色金属光泽和良好的延展性,是电和热的良导体,具有能被磁铁吸引的特性,纯铁有很
强的抗腐蚀能力。
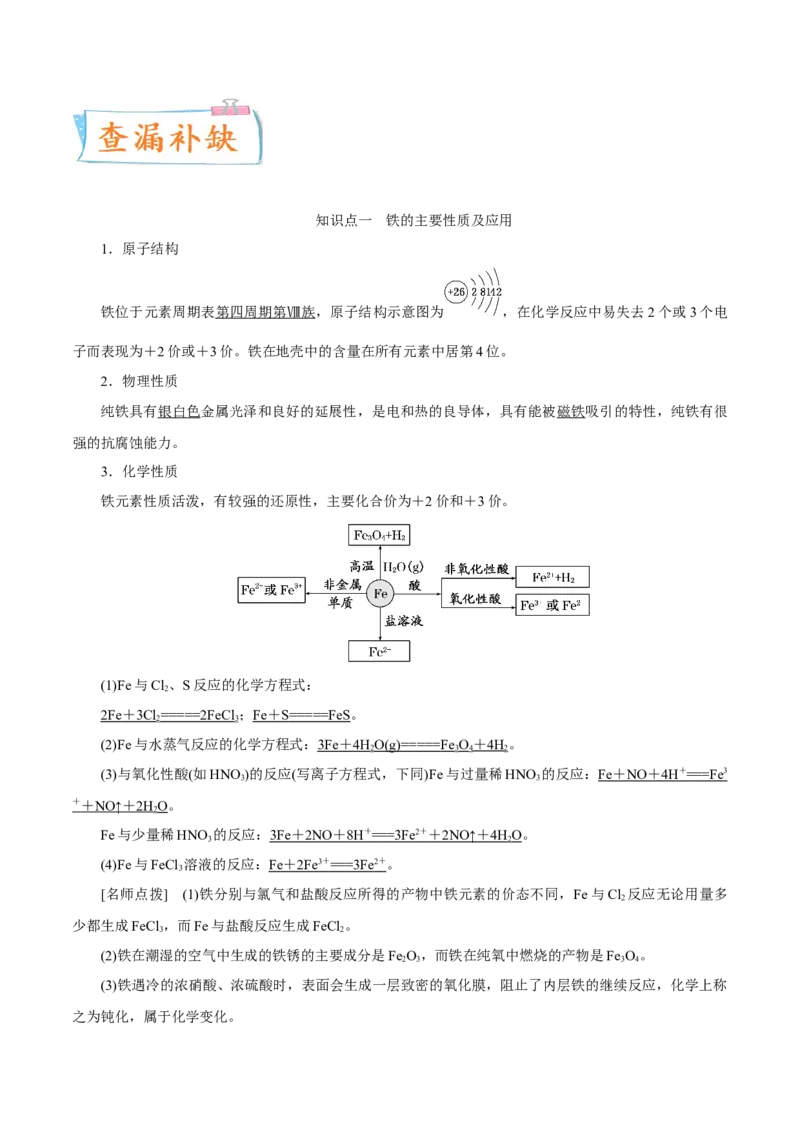
3.化学性质
铁元素性质活泼,有较强的还原性,主要化合价为+2价和+3价。
(1)Fe与Cl、S反应的化学方程式:
2
2Fe + 3Cl ===== 2FeCl ; Fe + S ===== FeS 。
2 3
(2)Fe与水蒸气反应的化学方程式: 3Fe + 4H O(g) ===== Fe O + 4H 。
2 3 4 2
(3)与氧化性酸(如HNO)的反应(写离子方程式,下同)Fe与过量稀HNO 的反应: Fe + NO + 4H + == =Fe 3
3 3
+ + NO ↑ + 2H O。
2
Fe与少量稀HNO 的反应: 3Fe + 2NO + 8H + == =3Fe 2 + + 2NO↑ + 4H O。
3 2
(4)Fe与FeCl 溶液的反应: Fe + 2Fe 3 + == =3Fe 2 + 。
3
[名师点拨] (1)铁分别与氯气和盐酸反应所得的产物中铁元素的价态不同,Fe与Cl 反应无论用量多
2
少都生成FeCl ,而Fe与盐酸反应生成FeCl 。
3 2
(2)铁在潮湿的空气中生成的铁锈的主要成分是Fe O,而铁在纯氧中燃烧的产物是Fe O。
2 3 3 4
(3)铁遇冷的浓硝酸、浓硫酸时,表面会生成一层致密的氧化膜,阻止了内层铁的继续反应,化学上称
之为钝化,属于化学变化。知识点二 铁的氧化物和氢氧化物
1.铁的氧化物
(1)物理性质
化学式 FeO Fe O Fe O
2 3 3 4
俗称 — 铁红 磁性氧化铁
颜色状态 黑色粉末 红棕色粉末 黑色晶体
铁的价态 + 2 价 + 3 价 + 2 价、+ 3 价
(2)化学性质
①FeO、Fe O 分别与盐酸反应的离子方程式:
2 3
FeO + 2H + == =Fe 2 + + H O、Fe O + 6H + == =2F e 3 + + 3H O。
2 2 3 2
②FeO与稀硝酸反应的化学方程式:
3FeO + 10HNO == =3Fe(NO ) + NO ↑ + 5H O。
3 3 3 2
③FeO、Fe O 分别与HI溶液反应的化学方程式:
2 3
FeO + 2HI == =FeI + H O、Fe O + 6H I == =2Fe I + I + 3H O。
2 2 2 3 2 2 2
2.铁的氢氧化物(是离子反应的写离子方程式)
化学式 Fe(OH) Fe(OH)
2 3
颜色状态 白色固体 红褐色固体
与盐酸反应 Fe(OH) + 2H + == =F e 2 + + 2H O Fe(OH) + 3H + == =F e 3 + + 3H O
2 2 3 2
受热分解 — 2Fe(OH) =====Fe O+3HO
3 2 3 2
可溶性亚铁盐与碱溶液反应: Fe 2 可溶性铁盐与碱溶液反应: Fe 3 +
制法
+ + 2OH - == =Fe(OH ) ↓ + 3OH - == =Fe(OH ) ↓
2 3
在空气中,Fe(OH) 能够非常迅速地被氧气氧化成Fe(OH) ,现象是色
2 3
二者的关系 絮状沉淀迅速变成灰绿色,最后变成红褐色,反应方程式为4Fe(OH)
2
+ O + 2H O == =4Fe(OH)
2 2 3
[名师点拨] (1)FeO、Fe O 、Fe(OH) 与足量HNO 反应时,发生氧化还原反应,Fe2+被HNO 氧化生
3 4 2 3 3
成Fe3+。
(2)Fe O、Fe O、Fe(OH) 与足量HI反应时,发生氧化还原反应,Fe3+被I-还原生成Fe2+。
2 3 3 4 3
3.Fe(OH) 的制备方法
2
(1)制备原理
①制备原理:Fe2++2OH-===Fe(OH) ↓。
2
②成功关键:溶液中不含O 等氧化性物质;制备过程中,保证生成的Fe(OH) 在密闭的、隔绝空气的
2 2
体系中。(2)常用方法
①有机层隔离法
a.反应在试管底部进行(这是唯一一种把胶头滴管插入反应溶液的实验)。
b.加隔氧剂,如加入汽油、苯等比水轻的有机溶剂[如图,由于苯的液封作用,可防止生
成的Fe(OH) 被氧化,因而可较长时间观察到白色的Fe(OH) 沉淀]。
2 2
②还原性气体保护法
该方法是先在装置Ⅰ中产生FeSO 溶液,并利用产生的H 排尽整个装置中的空气,待检验H 的纯度
4 2 2
后,再关闭止水夹K,利用产生的H 把FeSO 溶液压入装置Ⅱ中与NaOH溶液进行反应。
2 4
③电解法
该方法中铁作电解池的阳极,电极反应为 Fe-2e-===Fe2+,阴极反应为 2H++2e-
===H ↑,生成的氢气可以赶走溶液中的氧气,溶液中 c(OH-)增大,与Fe2+结合生成Fe(OH)
2 2
沉淀,汽油起液封作用。
电解时,在两极间最先观察到白色沉淀。
知识点三 铁盐、亚铁盐的性质
1.亚铁盐
(1)Fe2+的氧化性和还原性
含有Fe2+的溶液呈浅绿色,Fe2+处于铁的中间价态,既有氧化性,又有还原性,其中以还原性为主,
如遇Br 、Cl、HO、NO(H+)等均表现为还原性。
2 2 2 2
Fe2+的酸性溶液与HO 反应的离子方程式:
2 2
2Fe 2 + + H O + 2H + == =2F e 3 + + 2H O。
2 2 2
FeCl 溶液与HNO 溶液反应的离子方程式:
2 3
3Fe 2 + + NO + 4H + == =3Fe 3 + + NO↑ + 2H O。
2
(2)Fe2+可发生水解反应
Fe(OH) 是弱碱,含Fe2+的盐(如硫酸亚铁)溶液呈酸性。配制硫酸亚铁溶液时常加少量硫酸抑制Fe2+的
2
水解,加少量铁屑防止Fe2+被氧化。2.铁盐
(1)氧化性:含有Fe3+的溶液呈棕黄色,Fe3+处于铁的高价态,遇Fe、Cu、HI、HS等均表现为氧化性。
2
Fe3+可腐蚀印刷电路板上的铜箔,反应的离子方程式为 2Fe 3 + + Cu == =Cu 2 + + 2Fe 2 + 。
FeCl 溶液滴入淀粉KI溶液,溶液变蓝,离子方程式为 2I - + 2Fe 3 + == =I + 2F e 2 + 。
3 2
(2)易水解:Fe(OH) 是很弱的碱,且溶度积很小,因而Fe3+极易水解,只能存在于酸性较强的溶液中。
3
①利用Fe3+易水解的性质,实验室可将饱和FeCl 溶液滴入沸水中制取氢氧化铁胶体,反应的化学方
3
程式为FeCl + 3H O ===== Fe(OH) ( 胶体 ) + 3HCl 。
3 2 3
②利用Fe3+易水解的性质,工业上常用调节pH的方法除去溶液中的铁离子。
③利用Fe3+易水解的性质,实验室配制氯化铁溶液,通常将氯化铁固体先溶于较浓的盐酸中,然后再
稀释至所需浓度。
④Fe3+与HCO、AlO、CO等水解呈碱性的离子不能大量共存。
知识点四 铁的转化和检验
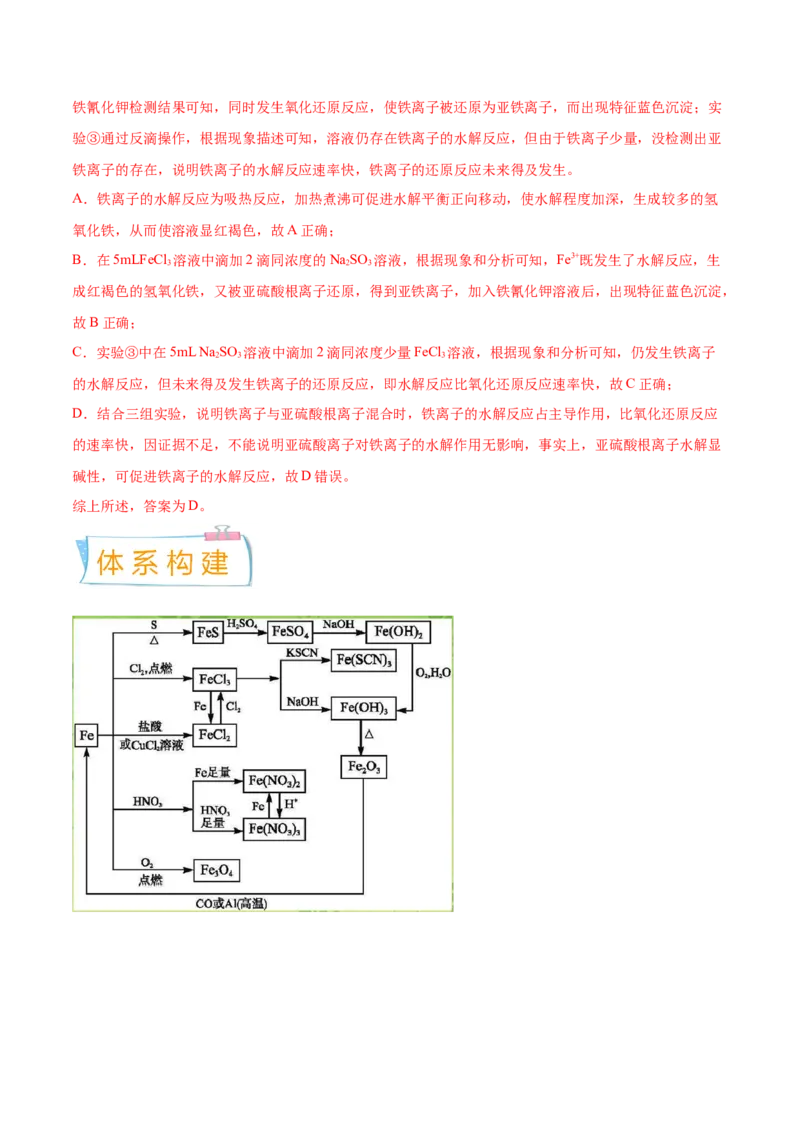
1.铁及其化合物的相互转化
完成下列变化的离子方程式,体会Fe2+与Fe3+转化条件。
(1)将HS气体通入FeCl 溶液中产生淡黄色沉淀:
2 3
H S + 2Fe 3 + == =S↓ + 2Fe 2 + + 2H + 。
2
(2)将FeCl 溶液滴入淀粉KI溶液,溶液变蓝:
3
2I - + 2Fe 3 + == =I + 2F e 2 + 。
2
(3)FeCl 可溶解铁片: 2Fe 3 + + Fe == =3Fe 2 + 。
3
(4)FeSO 可使酸性KMnO 溶液褪色:
4 4
5Fe 2 + + MnO + 8H + == =5Fe 3 + + Mn 2 + + 4H O。
2
(5)将FeCl 溶液滴入HNO 溶液中,有无色气体放出: 3Fe 2 + + NO + 4H + == =3Fe 3 + + NO↑ + 2H O。
2 3 2
2.Fe2+、Fe3+的检验
(1)Fe2+的检验①――――――――――――→现象――→溶液变 色,证明含有 F e2+。
②―――――――――→产生白色絮状沉淀,迅速变成灰绿色,最终变为红褐色,证明含有Fe2+。
③―――――――――→生成 色沉淀,证明含有 F e2+。
(2)Fe3+的检验
①―――――――――→溶液变红色,证明含有Fe3+。
②―――――――――→产生红褐色沉淀,证明有Fe3+存在。
(3)含Fe2+、Fe3+的混合溶液中Fe3+、Fe2+的检验
①Fe3+的检验
ⅰ.―――――――――→溶液变红色,说明含有Fe3+。
ⅱ.―――――――――→试纸变 色,说明含有 F e3+。
②Fe2+的检验
ⅰ.―――――――――→酸性KMnO 溶液紫红色褪去,说明含有Fe2+。
4
ⅱ.―――――――――→溴水褪色,说明含有Fe2+。
[名师点拨] Fe3+、Fe2+、Cl-同时存在时不能用酸性KMnO 溶液检验Fe2+(Cl-能还原酸性KMnO ,
4 4
有干扰)。
3.含Fe2+、Fe3+的除杂问题
主要成分 杂质 除杂方法
FeCl (aq) FeCl (aq) 加入氯水或HO
3 2 2 2
FeCl (aq) FeCl (aq) 加过量铁粉后过滤
2 3
FeCl (aq) CuCl (aq) 加过量铁粉后过滤
2 2
[名师点拨] 除去混合溶液中Fe3+、Fe2+的常用方法
(1)除去Mg2+中混有的Fe3+的方法
向混合溶液中加入MgO、MgCO 、Mg(OH) 中之一,与Fe3+水解产生的H+反应,促进Fe3+的水解,
3 2
将Fe3+转化为Fe(OH) 沉淀而除去。
3
(2)除去Cu2+中混有的Fe3+的方法
向混合溶液中加入CuO、CuCO 、Cu(OH) 、Cu (OH) CO 中之一,与Fe3+水解产生的H+反应,促进
3 2 2 2 3
Fe3+的水解,将Fe3+转化为Fe(OH) 沉淀而除去。
3
(3)除去Mg2+中混有的Fe2+的方法
先加入氧化剂(如HO)将溶液中的Fe2+氧化成Fe3+,然后再按(1)的方法除去溶液中的Fe3+。
2 2
(4)除去Cu2+中混有的Fe2+的方法
先加入氧化剂(如HO)将溶液中的Fe2+氧化成Fe3+,然后再按(2)的方法除去溶液中的Fe3+。
2 21.春秋初年,我国已掌握了冶铁技术。下列有关铁的化学反应的叙述正确的是( )
A. 室温下,过量Fe与浓硫酸反应生成FeSO
4
B. 加热时,过量Fe与氯气反应生成FeCl
2
C. 高温下,铁与水蒸气反应有磁性四氧化三铁生成
D. 高温下,铁粉与氧化铝粉末反应生成单质铝
2.用废铁屑制备磁性胶体粒子,制取过程如下。下列说法不正确的是( )
A. 用NaCO 溶液浸泡是为了除去废铁屑表面的油污
2 3
B. 通入N 是防止空气中的O 氧化二价铁元素
2 2
C. 加适量的HO 是为了将部分Fe2+氧化为Fe3+,涉及反应:HO+2Fe2++2H+===2Fe3++2HO
2 2 2 2 2
D. 溶液A中Fe2+和Fe3+的浓度比为2∶1
3. 某同学欲利用图示装置制取能较长时间存在的Fe(OH) ,其中实验所用溶液现配现用且蒸馏水先加
2
热煮沸。下列分析正确的是( )
A. X可以是稀硫酸或稀硝酸或稀盐酸
B. 实验开始时应先关闭止水夹a、打开b,再向烧瓶中加入X
C. 反应一段时间后可在烧瓶中观察到白色沉淀
D. 反应结束后若关闭b及分液漏斗活塞,则Fe(OH) 可较长时间存在
2
4. 已知:2FeSO ·7H O=====Fe O +SO ↑+SO ↑+14HO↑,用如图所示装置检验FeSO ·7H O的所有
4 2 2 3 2 3 2 4 2
分解产物,下列说法不正确的是( )
A. 乙、丙、丁中可依次盛装无水CuSO 、Ba(NO ) 溶液、品红溶液
4 3 2B. 实验时应先打开K,缓缓通入N,再点燃酒精喷灯
2
C. 甲中残留固体加稀硫酸溶解,再滴加KSCN溶液变红
D. 还应在丁装置后面连接盛有NaOH溶液的洗气瓶
5.硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如图所示)。下列说法错误的是( )
A. 碱式硫酸铁水解能产生Fe(OH) 胶体,可用作净水剂
3
B. 为防止NH HCO 分解,生产FeCO 需在较低温度下进行
4 3 3
C. 可用KSCN溶液检验(NH )Fe(SO ) 是否被氧化
4 2 4 2
D. 常温下,(NH )Fe(SO ) 在水中的溶解度比FeSO 的大
4 2 4 2 4
1.我国清代《本草纲目拾遗》中叙述了“铁线粉”:“粤中洋行有舶上铁丝,……日久起销,用刀
刮其销,……,所刮下之销末,名铁线粉”。这里的“铁线粉”是指( )
A.Fe B.FeCl
3
C.FeO D.Fe O
2 3
2.(2021·南京模拟)下列有关物质性质与用途具有对应关系的是( )
A.FeCl 易发生水解,可用于蚀刻铜制的印制线路板
3
B.漂白粉具有氧化性,可用于脱除烟气中SO 和NO
2
C.CaCO 高温下能分解,可用于修复被酸雨侵蚀的土壤
3
D.活性炭具有还原性,可用于除去水体中Pb2+等重金属
3.将铁屑溶于过量的稀盐酸后,再加入下列物质,会有Fe3+生成的是( )
A.硫酸 B.氯水
C.硫酸锌 D.氯化铜
4.(2021·银川模拟)下列关于物质或离子检验的叙述正确的是( )
A.在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+B.气体通过无水硫酸铜,粉末变蓝,证明原气体中含有水蒸气
C.灼烧白色粉末,火焰呈黄色,证明原粉末中有Na+,无K+
D.将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO
2
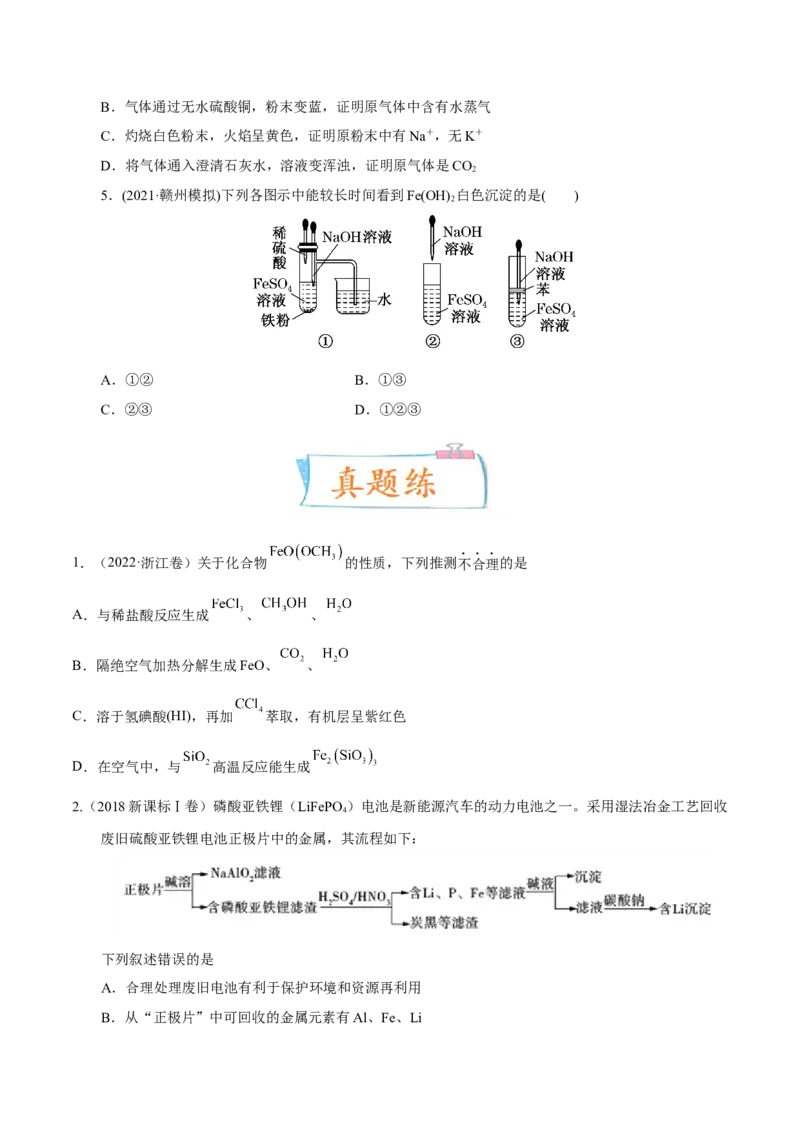
5.(2021·赣州模拟)下列各图示中能较长时间看到Fe(OH) 白色沉淀的是( )
2
A.①② B.①③
C.②③ D.①②③
1.(2022·浙江卷)关于化合物 的性质,下列推测不合理的是
A.与稀盐酸反应生成 、 、
B.隔绝空气加热分解生成FeO、 、
C.溶于氢碘酸(HI),再加 萃取,有机层呈紫红色
D.在空气中,与 高温反应能生成
2.(2018新课标Ⅰ卷)磷酸亚铁锂(LiFePO )电池是新能源汽车的动力电池之一。采用湿法冶金工艺回收
4
废旧硫酸亚铁锂电池正极片中的金属,其流程如下:
下列叙述错误的是
A.合理处理废旧电池有利于保护环境和资源再利用
B.从“正极片”中可回收的金属元素有Al、Fe、LiC.“沉淀”反应的金属离子为Fe3+
D.上述流程中可用硫酸钠代替碳酸钠
3.(2020山东新高考)以菱镁矿(主要成分为MgCO ,含少量SiO,Fe O 和A1 O)为原料制备高纯镁砂的
3 2 2 3 2 3
工艺流程如下:
已知浸出时产生的废渣中有SiO,Fe(OH) 和Al(OH) 。下列说法错误的是
2 3 3
A.浸出镁的反应为
B.浸出和沉镁的操作均应在较高温度下进行
C.流程中可循环使用的物质有NH 、NH Cl
3 4
D.分离Mg2+与Al3+、Fe3+是利用了它们氢氧化物K 的不同
sp
4.(2019天津)下列有关金属及其化合物的应用不合理的是
A.将废铁屑加入 溶液中,可用于除去工业废气中的
B.铝中添加适量锂,制得低密度、高强度的铝合金,可用于航空工业
C.盐碱地(含较多 等)不利于作物生长,可施加熟石灰进行改良
D.无水 呈蓝色,吸水会变为粉红色,可用于判断变色硅胶是否吸水
5.(2018江苏卷)在给定条件下,下列选项所示的物质间转化均能实现的是
A.
B.
C.
D.1. 【答案】C
【解析】
室温下,Fe在浓硫酸中钝化,A错误;Fe在Cl 中燃烧得到FeCl ,B错误;Fe在高温下与水蒸气反应生成
2 3
Fe O 和H,C正确;铝的活泼性强于铁,故铁粉不能与氧化铝反应,D错误。
3 4 2
2. 【答案】D
【解析】
碳酸钠溶液浸泡可以除去废铁屑表面的油污,A正确;Fe2+容易被氧气氧化,因此通入N 的目的是防止空
2
气中的氧气氧化Fe2+,B正确;利用HO 的氧化性,把Fe2+氧化成Fe3+,涉及反应:2Fe2++HO +2H+
2 2 2 2
===2Fe3++2HO,C正确;Fe O 中Fe2+和Fe3+物质的量之比为1∶2,D错误。
2 3 4
3. 【答案】 D
【解析】
硝酸可氧化Fe生成硝酸铁,A错误;实验开始时应先打开止水夹a、b,利用生成的氢气将装置内的空气
排出,然后关闭a,B错误;利用氢气的压强将亚铁盐排入锥形瓶中,NaOH与亚铁盐反应生成Fe(OH) ,
2
可在锥形瓶中观察到白色沉淀,C错误;反应后装置内空气及溶液中氧气已除去,则Fe(OH) 可较长时间
2
存在,D正确。
4. 【答案】A
【解析】
丙装置验证的是SO ,因为NO在酸性条件下具有强氧化性,能把SO 氧化成SO,对SO 的检验产生干扰,
3 2 3
丙装置应换成BaCl 溶液,A错误;先通N ,排除装置中空气,防止Fe2+被氧化,B正确;残留固体加稀
2 2
硫酸溶解,再滴加KSCN溶液,溶液变红说明溶液中含有Fe3+,反之不含有,C正确;SO 有毒,为防止
2
污染空气,因此在丁装置后面再加一尾气处理装置,即添加盛有NaOH溶液的洗气瓶,D正确。
5. 【答案】D
【解析】
碱式硫酸铁电离产生Fe3+,Fe3+能发生水解生成Fe(OH) 胶体,Fe(OH) 胶体具有吸附性,可用作净水剂,
3 3
A正确;NH HCO 不稳定,受热易分解,B正确;(NH )Fe(SO ) 若被氧化则生成Fe3+,KSCN溶液遇Fe3+
4 3 4 2 4 2
变红,C 正确;(NH )Fe(SO ) 在水中的溶解度比 FeSO 的小,所以 FeSO 才能与(NH )SO 反应生成
4 2 4 2 4 4 4 2 4
(NH )Fe(SO ),D错误。
4 2 4 21.【答案】D
【解析】
铁在空气中容易发生吸氧腐蚀,根据题意“舶上铁丝,……日久起销”,说明销是铁锈,铁锈的主要成分
为Fe O,D项正确。
2 3
2.【答案】B
【解析】
FeCl 具有强氧化性,能与Cu等金属反应,可用于蚀刻铜制的印制线路板,与FeCl 易发生水解无关,A错
3 3
误; 漂白粉的主要成分是次氯酸钙,次氯酸钙具有强氧化性,能氧化SO 和NO生成硫酸盐和硝酸盐,所
2
以漂白粉可用于脱除烟气中的SO 和NO,B正确;CaCO 能与酸反应,能改良、修复被酸雨侵蚀的土壤,
2 3
与CaCO 高温下能分解无关,C错误;活性炭与Pb2+等金属离子不反应,不能用于除去水体中的Pb2+等重
3
金属,D错误。
3.【答案】B
【解析】
Fe+2HCl===FeCl +H↑,选项中,HSO 、ZnSO、CuCl 均不能与FeCl 反应,但氯水中的Cl 能氧化Fe2+
2 2 2 4 4 2 2 2
生成Fe3+,离子方程式为2Fe2++Cl===2Fe3++2Cl-。
2
4.【答案】B
【解析】
Fe3+遇KSCN会使溶液呈红色,Fe2+遇KSCN不反应,无现象,滴加KSCN溶液,溶液呈红色,则证明存
在Fe3+,并不能证明无 Fe2+,故 A错误;气体通过无水硫酸铜,粉末变蓝,则发生反应:CuSO +
4
5HO===CuSO·5H O,可证明原气体中含有水蒸气,故B正确;灼烧白色粉末,火焰呈黄色,证明原粉末
2 4 2
中有Na+,并不能证明无K+,Na+的焰色反应为黄色,可遮住紫光,K+的焰色反应需透过蓝色的钴玻璃
滤去黄光后观察,故C错误;能使澄清石灰水变浑浊的气体有CO 、SO 等,故将气体通入澄清石灰水,
2 2
溶液变浑浊,则原气体不一定是CO,故D错误。
2
5.【答案】B
【解析】
因为Fe(OH) 在空气中易被氧化成Fe(OH) ,故要长时间观察到Fe(OH) 白色沉淀,就要排除装置中的空气
2 3 2
或氧气。装置①是先用Fe粉与稀硫酸反应产生的H 将装置中的空气排尽,然后滴入NaOH溶液,与
2
FeSO 发生复分解反应生成Fe(OH) ,并使生成的Fe(OH) 处在氢气的保护中,可以达到目的,①正确;②
4 2 2
滴入的NaOH溶液会吸收空气中的氧气,与试管中的FeSO 发生复分解反应生成Fe(OH) 和NaSO ,溶液
4 2 2 4
中有氧气,会氧化Fe(OH) 变为Fe(OH) ,因此会看到沉淀由白色迅速变为灰绿色,最后变为红褐色,不能
2 3
达到实验目的,②错误;③中液面上加苯阻止了空气进入,在隔绝空气的环境中 NaOH、FeSO 发生复分
4解反应生成Fe(OH) 和NaSO ,由于没有空气,Fe(OH) 不能被氧化,能较长时间观察到白色沉淀,③正确;
2 2 4 2
故合理选项是B。
1.【答案】B
【解析】
已知化合物 中Fe的化合价为+3价,CHO-带一个单位负电荷,据此分析解题。
3
A.由分析可知,化合物 中Fe的化合价为+3价,故其与稀盐酸反应生成 、 、
,反应原理为:FeO(OCH)+3HCl=FeCl +H O+CHOH,A不合题意;
3 3 2 3
B.由分析可知,化合物 中Fe的化合价为+3价,C为-1,若隔绝空气加热分解生成FeO、
、 则得失电子总数不相等,不符合氧化还原反应规律,即不可能生成FeO、 、 ,B符合题意;
C.由分析可知,化合物 中Fe的化合价为+3价,故其溶于氢碘酸(HI)生成的Fe3+能将I-氧化为
I,反应原理为:2FeO(OCH)+6HI=2FeI +I +2H O+2CHOH,再加 萃取,有机层呈紫红色,C不合题
2 3 2 2 2 3
意;
D.化合物 在空气中高温将生成Fe O、CO 和HO,然后Fe O 为碱性氧化物,SiO 为酸性氧
2 3 2 2 2 3 2
化物,故化合物 与 高温反应能生成 ,D不合题意;
故答案为:B。
2.【答案】D
【解析】
分析:正极片碱溶时铝转化为偏铝酸钠,滤渣中含有磷酸亚铁锂,加入硫酸和硝酸酸溶,过滤后滤渣是炭
黑,得到含Li、P、Fe的滤液,加入碱液生成氢氧化铁沉淀,滤液中加入碳酸钠生成含锂的沉淀,据此解
答。
详解:A、废旧电池中含有重金属,随意排放容易污染环境,因此合理处理废旧电池有利于保护环境和资源再利用,A正确;
B、根据流程的转化可知从正极片中可回收的金属元素有Al、Fe、Li,B正确;
C、得到含Li、P、Fe的滤液,加入碱液生成氢氧化铁沉淀,因此“沉淀”反应的金属离子是Fe3+,C正确;
D、硫酸锂能溶于水,因此上述流程中不能用硫酸钠代替碳酸钠,D错误。答案选D。
点睛:本题以废旧电池的回收为载体考查金属元素的回收,明确流程中元素的转化关系是解答的关键,题
目难度不大。
3.【答案】B
【分析】
菱镁矿煅烧后得到轻烧粉,MgCO 转化为MgO,加入氯化铵溶液浸取,浸出的废渣有SiO、Fe(OH) 、
3 2 3
Al(OH) ,同时产生氨气,则此时浸出液中主要含有Mg2+,加入氨水得到Mg(OH) 沉淀,煅烧得到高纯镁
3 2
砂。
【详解】
A.高温煅烧后Mg元素主要以MgO的形式存在,MgO可以与铵根水解产生的氢离子反应,促进铵根的水
解,所以得到氯化镁、氨气和水,化学方程式为MgO+2NH Cl=MgCl +2NH↑+H O,故A正确;
4 2 3 2
B.一水合氨受热易分解,沉镁时在较高温度下进行会造成一水合氨大量分解,挥发出氨气,降低利用率,
故B错误;
C.浸出过程产生的氨气可以回收制备氨水,沉镁时氯化镁与氨水反应生成的氯化铵又可以利用到浸出过
程中,故C正确;
D.Fe(OH) 、Al(OH) 的K 远小于Mg(OH) 的K ,所以当pH达到一定值时Fe3+、Al3+产生沉淀,而
3 3 sp 2 sp
Mg2+不沉淀,从而将其分离,故D正确;
故答案为B。
4.【答案】C
【解析】
【分析】A、氯气能将铁和亚铁氧化;
B、根据合金的性质判断;
C、Na CO +Ca(OH) =CaCO ↓+2NaOH,产物仍然呈碱性;
2 3 2 3
D、利用无水氯化钴和氯化钴晶体的颜色不同。
【详解】A、铁和亚铁能将氯气还原为氯离子,从而除去工业废气中的氯气,故A不选;
B、根据铝合金的性质,铝合金具有密度低、强度高,故可应用于航空航天等工业,故B不选;
C、Na CO +Ca(OH) =CaCO ↓+2NaOH,产物仍然呈碱性,不能改变土壤的碱性,反而使土壤更板结,
2 3 2 3
故C选;D、利用无水氯化钴和氯化钴晶体的颜色不同,故可根据颜色判断硅胶中是否能吸水,故D不选。
故选C。
5.【答案】A
【解析】
A项,NaHCO 受热分解成NaCO 、CO 和HO,NaCO 与饱和石灰水反应生成CaCO 和NaOH,两步反
3 2 3 2 2 2 3 3
应均能实现;B项,Al与NaOH溶液反应生成NaAlO 和H ,NaAlO 与过量盐酸反应生成NaCl、AlCl 和
2 2 2 3
HO,第二步反应不能实现;C项,AgNO 中加入氨水可获得银氨溶液,蔗糖中不含醛基,蔗糖不能发生
2 3
银镜反应,第二步反应不能实现;D项,Al与Fe O 高温发生铝热反应生成Al O 和Fe,Fe与HCl反应生
2 3 2 3
成FeCl 和H,第二步反应不能实现;物质间转化均能实现的是A项,答案选A。
2 2
点睛:本题考查元素及其化合物之间的相互转化和反应条件,解题的关键是熟悉常见物质的化学性质和转
化的条件。注意量的多少对生成物的影响,如NaAlO 与少量HCl反应生成NaCl和Al(OH),NaAlO 与
2 3 2
过量HCl反应生成NaCl、AlCl 和HO。
3 2