文档内容
考向 06 钠及其化合物
【2022浙江1月】下列实验对应的离子方程式不正确的是
A.将碳酸氢钙溶液与过量的澄清石灰水混合: +Ca2++OH-=CaCO ↓+H O
3 2
B.将少量NO 通入NaOH溶液:2NO +2OH-= + +H O
2 2 2
C.将少量SO 通入NaClO溶液:SO +H O+2ClO-= +2HClO
2 2 2
D.向氨水中滴入少量硝酸银溶液:Ag++2NH·H O= +2H O
3 2 2
【答案】C
【详解】A. 将碳酸氢钙溶液与过量的澄清石灰水混合,反应生成碳酸钙和水,反应的离子方程式为:
+Ca2++OH-=CaCO ↓+H O,选项A正确;B. 将少量NO 通入NaOH溶液,反应生成硝酸钠、亚硝酸
3 2 2
钠和水,反应的离子方程式为:2NO +2OH-= + +H O,选项B正确;C. 将少量SO 通入NaClO
2 2 2
溶液,反应生成硫酸钠和盐酸,反应的离子方程式为:SO +H O+2ClO-= +HClO+H++Cl-,选项C不正
2 2
确;D. 向氨水中滴入少量硝酸银溶液,反应生成氢氧化二氨合银,反应的离子方程式为:Ag++2NH·H O=
3 2
+2H O,选项D正确;答案选C。
2知识点一 钠的性质及应用
1.钠的物理性质
(1)颜色:银白色,具有金属光泽。
(2)密度:ρ(H O)>ρ(Na)>ρ(煤油)
2
(3)熔点:低于 100 ℃。
(4)硬度:质地柔软,可以用小刀切割。
(5)传导性:可导电导热。
2.从钠的原子结构认识钠的化学性质——强还原性
Na ―――――――――→Na+
(1)与非金属单质(如O、Cl)反应
2 2
与O 反应
2
(2)与水反应
①化学方程式: 2Na + 2H O == =2NaOH + H ↑。
2 2
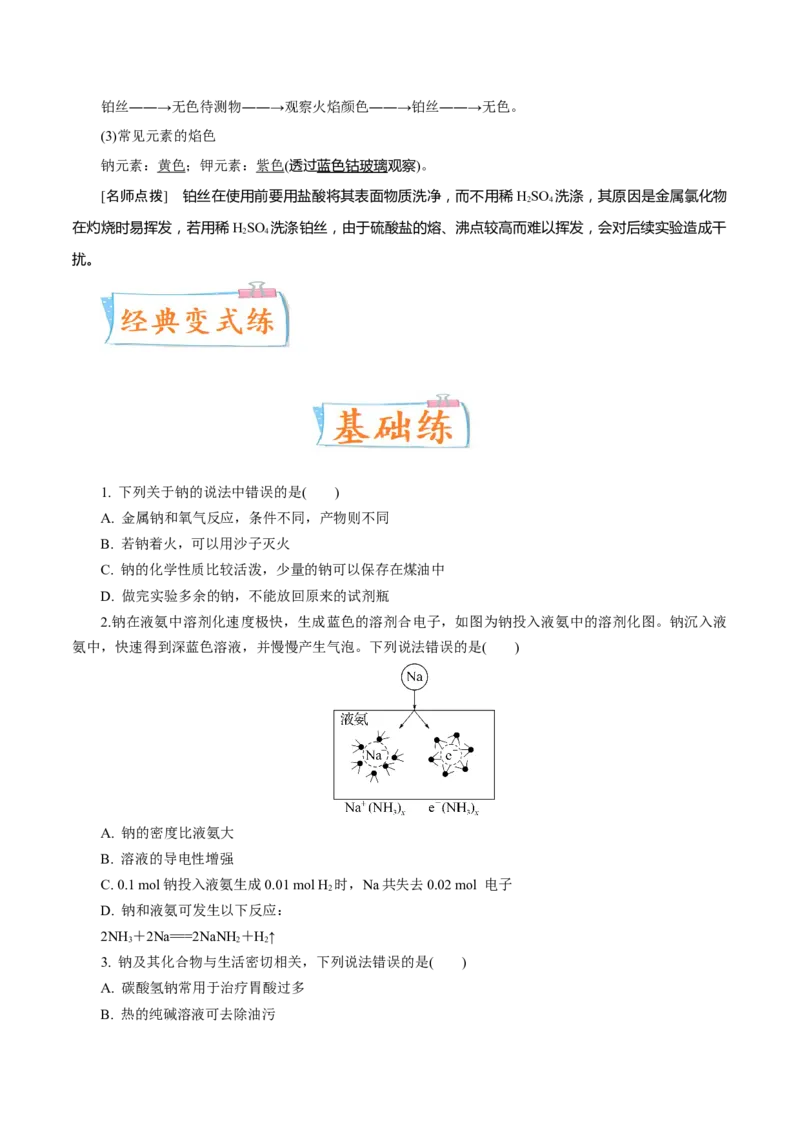
②与滴加酚酞的水反应的现象与解释
(3)与酸(如盐酸)反应离子方程式: 2Na + 2H + == =2Na + + H ↑,钠与酸的反应比钠与水的反应更剧烈。
2
(4)与盐(如CuSO )溶液的反应
4
离子方程式: 2Na + 2H O == =2Na + + 2OH - + H ↑,
2 2
Cu 2 + + 2OH - == = _Cu(OH) ↓_。
2
总反应的离子方程式:2Na+Cu2++2HO===Cu(OH) ↓+H↑+2Na+。
2 2 2
(5)与乙醇反应:2Na+2C HOH―→2C HONa+H↑。
2 5 2 5 2
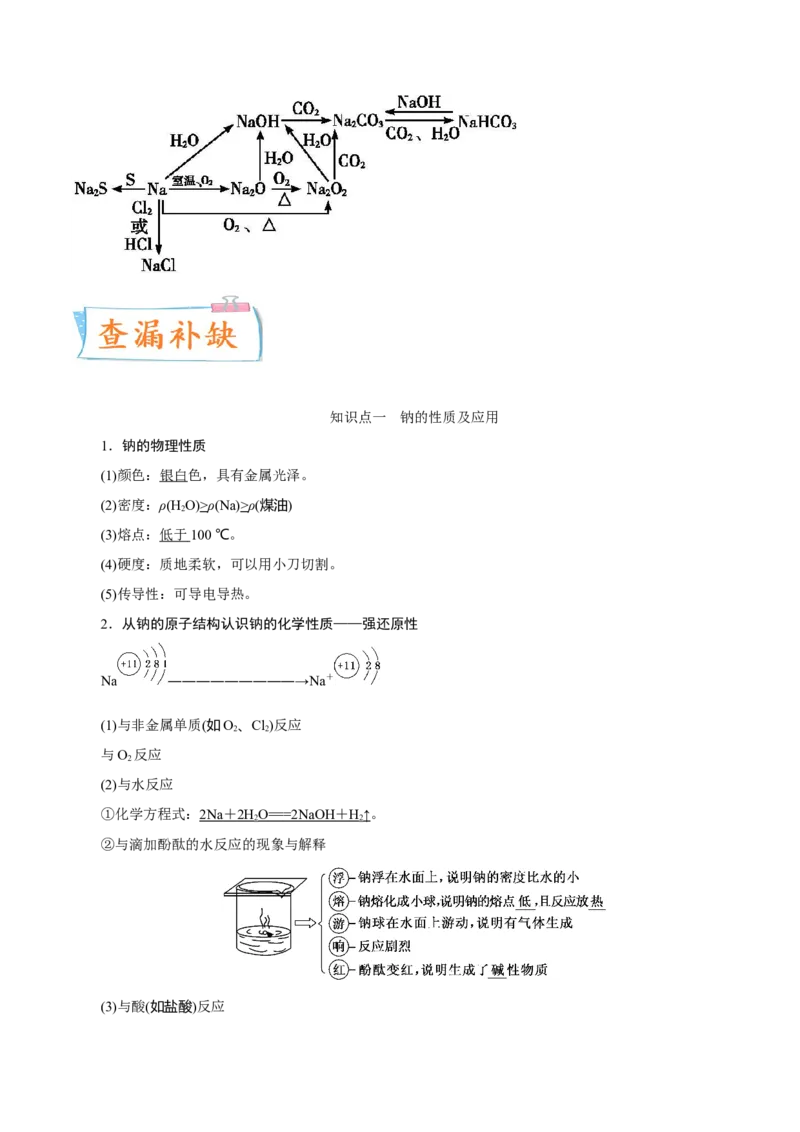
[名师点拨] (1)钠在空气中的变化过程:Na→NaO→NaOH→NaCO·10H O→NaCO ,最终变成
2 2 3 2 2 3
NaCO 粉末。
2 3
(2)钠与盐溶液反应时并非发生金属之间的置换反应,而是钠先与水反应生成 NaOH和H ,生成的
2
NaOH再与盐发生复分解反应,即分两步进行反应。
3.钠的制取、保存与用途
制取 化学方程式为 2NaCl( 熔融 ) ===== 2Na + Cl ↑
2
保存 通常保存在石蜡油或煤油中
(1)钠、钾合金(液态)用于原子反应堆,作导热剂。
用途 (2)作强还原剂,熔融状态冶炼某些金属(如钛)。
(3)作电光源,制作高压钠灯
知识点二 钠的重要化合物
一、氧化钠与过氧化钠
名称 氧化钠 过氧化钠
电子式
氧元素
- 2 - 1
化合价
色、态 白色固体 淡黄色固体
阴、阳离
1 ∶ 2 1 ∶ 2
子个数比
是否为碱
是 不是
性氧化物与水反
2NaO + 2H O == =4NaOH
应的化 Na O + H O == =2NaOH 2 2 2
2 2 + O ↑
2
学方程式
与CO 反
2
2NaO + 2CO == =2Na CO
应的化学 Na O + CO == =Na CO 2 2 2 2 3
2 2 2 3 + O
2
方程式
与盐酸反
Na O + 2HCl == =2NaCl + 2NaO + 4HC l == =4NaC l +
应的化学 2 2 2
HO 2H O + O ↑
2 2 2
方程式
[名师点拨] (1)氧化钠、过氧化钠都属于氧化物,氧化钠是碱性氧化物,而过氧化钠不是。
(2)Na O 具有强氧化性,但NaO 与水、CO 反应时,水中的氢与CO 中的碳都处于最高价态,不能被
2 2 2 2 2 2
氧化,故反应为NaO 自身的氧化还原反应。
2 2
二、碳酸钠和碳酸氢钠
1.碳酸钠和碳酸氢钠的重要性质
2.碳酸钠和碳酸氢钠的转化关系
NaCONaHCO 。
2 3 3
3.碳酸钠和碳酸氢钠的鉴别与除杂
(1)Na CO、NaHCO 的鉴别方法
2 3 3(2)Na CO、NaHCO 的除杂
2 3 3
混合物(括号内为杂质) 除杂方法
NaCO(s)(NaHCO ) 加热法
2 3 3
NaHCO (aq)(Na CO) 通入足量CO
3 2 3 2
NaCO(aq)(NaHCO ) 滴加适量NaOH溶液
2 3 3
知识点三 碱金属 焰色反应
1.碱金属的一般性与特殊性
(1)一般性
相似性 递变性(由Li→Cs)
电子层数逐渐增多
原子结构 最外层均为1个电子 核电荷数逐渐增大
原子半径逐渐增大
都具有较强的金属性,最高正价均为
元素性质 金属性逐渐增强
+1价
单
物理 (除Cs外)都呈银白色,密度较小, 密度逐渐增大(钾反常),熔、沸点逐
质 性质 熔、沸点较低 渐降低
性 化学 还原性逐渐增强;与O 反应越来越
质 都具有较强的还原性 2
性质 剧烈,产物越来越复杂
(2)特殊性
①碱金属的密度一般随核电荷数的增大而增大,但钾的密度比钠的小。
②碱金属一般都保存在煤油中,但由于锂的密度小于煤油的密度而将锂保存在石蜡中。
③碱金属跟氢气反应生成的碱金属氢化物都是离子化合物,其中氢以H-形式存在,显-1价,碱金属
氢化物是强还原剂。
2.焰色反应
(1)概念:很多金属或它们的化合物在灼烧时火焰呈现特殊颜色的现象。
(2)操作步骤铂丝――→无色待测物――→观察火焰颜色――→铂丝――→无色。
(3)常见元素的焰色
钠元素:黄色;钾元素:紫色(透过蓝色钴玻璃观察)。
[名师点拨] 铂丝在使用前要用盐酸将其表面物质洗净,而不用稀 HSO 洗涤,其原因是金属氯化物
2 4
在灼烧时易挥发,若用稀HSO 洗涤铂丝,由于硫酸盐的熔、沸点较高而难以挥发,会对后续实验造成干
2 4
扰。
1. 下列关于钠的说法中错误的是( )
A. 金属钠和氧气反应,条件不同,产物则不同
B. 若钠着火,可以用沙子灭火
C. 钠的化学性质比较活泼,少量的钠可以保存在煤油中
D. 做完实验多余的钠,不能放回原来的试剂瓶
2.钠在液氨中溶剂化速度极快,生成蓝色的溶剂合电子,如图为钠投入液氨中的溶剂化图。钠沉入液
氨中,快速得到深蓝色溶液,并慢慢产生气泡。下列说法错误的是( )
A. 钠的密度比液氨大
B. 溶液的导电性增强
C. 0.1 mol钠投入液氨生成0.01 mol H 时,Na共失去0.02 mol 电子
2
D. 钠和液氨可发生以下反应:
2NH +2Na===2NaNH +H↑
3 2 2
3. 钠及其化合物与生活密切相关,下列说法错误的是( )
A. 碳酸氢钠常用于治疗胃酸过多
B. 热的纯碱溶液可去除油污C. 发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔
D. 相同温度下NaHCO 的溶解度大于NaCO 的溶解度
3 2 3
4. 为除去括号内的杂质,下列各选项中所选用的试剂或方法错误的是( )
A. Na CO 溶液(NaHCO ),选用适量的NaOH溶液
2 3 3
B. NaHCO 溶液(Na CO),应通入过量的CO 气体
3 2 3 2
C. Na O 粉末(Na O),将混合物在空气中加热
2 2 2
D. Na CO 溶液(Na SO ),加入适量的Ba(OH) 溶液,过滤
2 3 2 4 2
5. 下列装置能达到实验目的的是( )
A B C D
加热分解NaHCO 固
3
熔化NaCO 加热比较热稳定性 制备干燥氨气
2 3
体
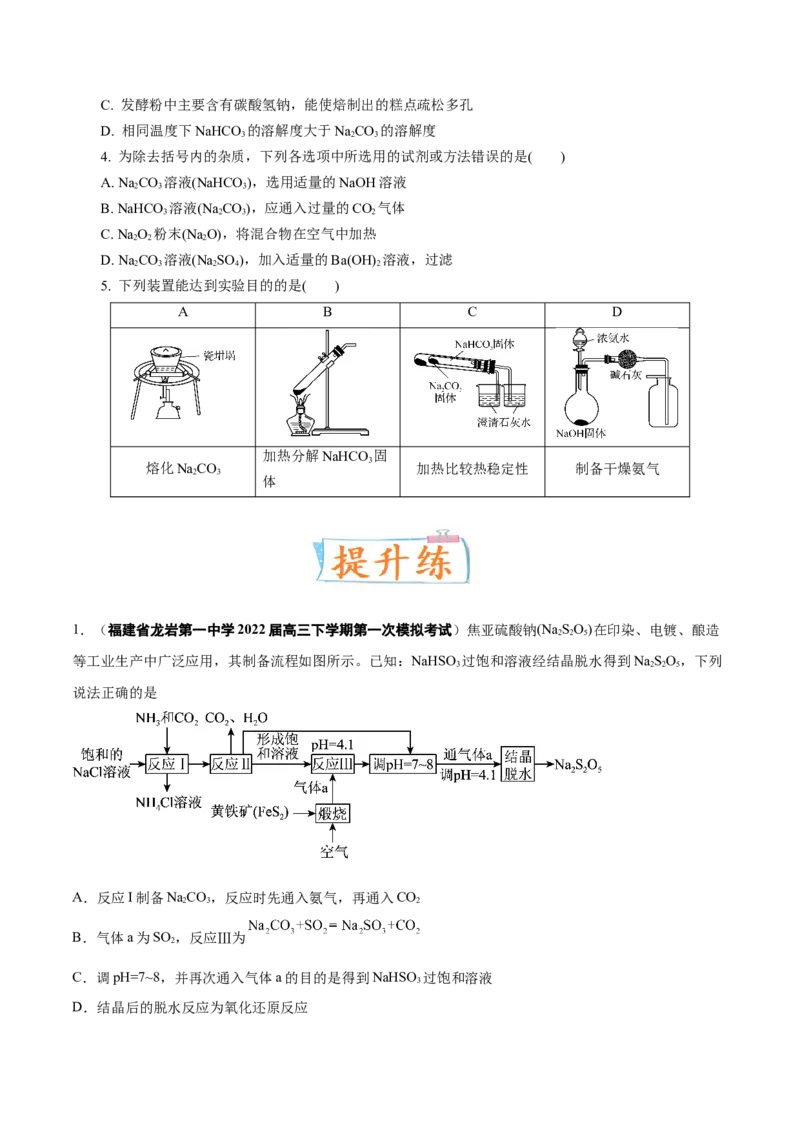
1.(福建省龙岩第一中学2022届高三下学期第一次模拟考试)焦亚硫酸钠(Na SO)在印染、电镀、酿造
2 2 5
等工业生产中广泛应用,其制备流程如图所示。已知:NaHSO 过饱和溶液经结晶脱水得到NaSO,下列
3 2 2 5
说法正确的是
A.反应I制备NaCO,反应时先通入氨气,再通入CO
2 3 2
B.气体a为SO ,反应Ⅲ为
2
C.调pH=7~8,并再次通入气体a的目的是得到NaHSO 过饱和溶液
3
D.结晶后的脱水反应为氧化还原反应2.(甘肃省2022届高三第二次高考诊断考试(二模))下列过程中的化学反应,相应的离子方程式书写
不正确的是
A.向稀盐酸中加入少量钠粒:2Na+2HO=Na++2OH-+H ↑
2 2
B.硫酸酸化的淀粉溶液久置后变蓝:4I-+O +4H+=2I +2H O
2 2 2
C.用稀硫酸除去硫酸钠溶液中少量的硫代硫酸钠: +2H+=2SO↑+S↓+H O
2 2
D.向含氯化铁的氧化镁溶液中加入氧化镁:2Fe3++3MgO+3HO=2Fe(OH) ↓+3Mg2+
2 3
3.(2021·长春模拟)下列有关物质的实验操作、现象及结论描述正确的是( )
选项 实验操作及现象 结论
用铂丝蘸取某待测液在酒精灯外焰上灼 待测试液中一定含有钾元素,可能含钠
A
烧,火焰呈紫色(透过蓝色钴玻璃) 元素
向某无色溶液中通入过量的 CO 气体,
B 2 该溶液中一定含有SiO
有白色沉淀产生
C 向品红溶液中通入某气体后,溶液褪色 该气体一定是SO
2
向NaOH溶液中滴加MgCl 溶液,产生
2 Fe(OH) 的溶解度小于Mg(OH) 的溶解
D 白色沉淀,继续滴加FeCl 溶液,产生红 3 2
3 度
褐色沉淀
4.如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发现 U形管内液体慢慢
右移,恢复到原温度后液面左边与右边基本相平,则烧杯内的物质是( )
A.过氧化钠 B.钠
C.氧化钠 D.钾
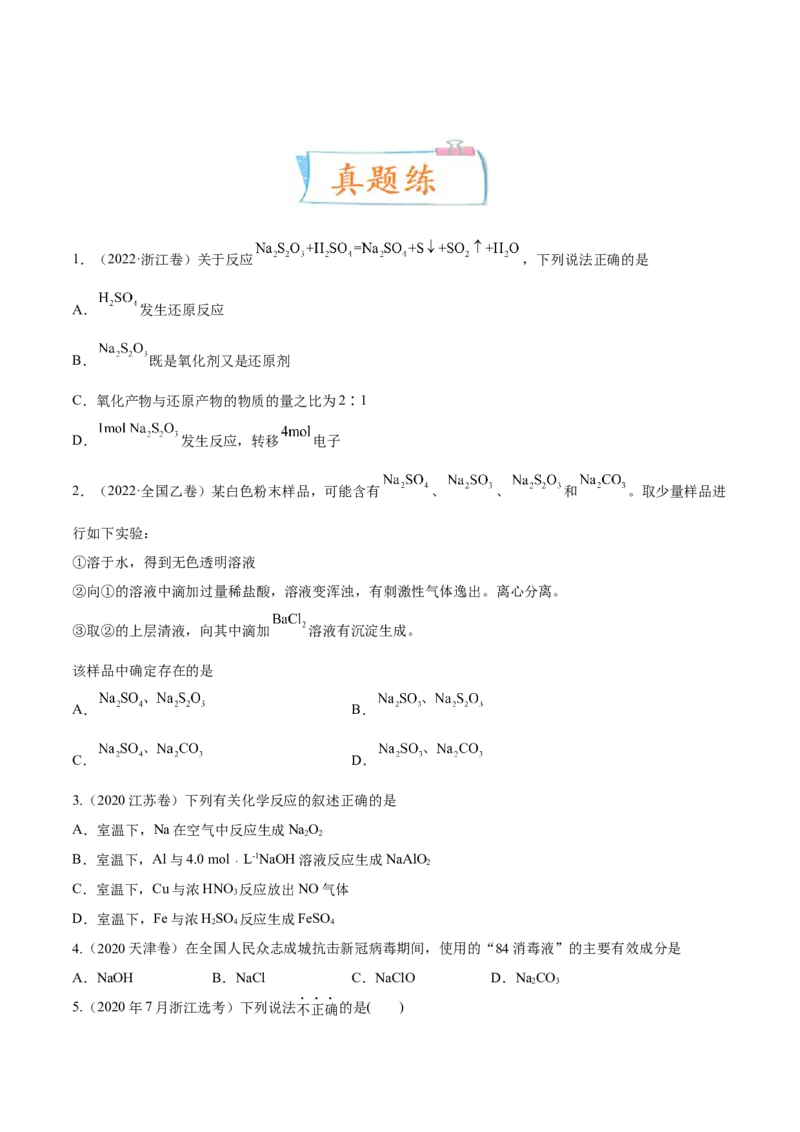
5.(2021·佳木斯模拟)以CO 和NaO 为原料,制取纯净干燥的O,实验装置如下:
2 2 2 2
下列说法不正确的是( )
A.装置②中试剂可以是NaOH溶液
B.装置③的作用是干燥O
2
C.收集氧气应选择装置a
D.装置②、③之间应增加盛澄清石灰水的洗气瓶1.(2022·浙江卷)关于反应 ,下列说法正确的是
A. 发生还原反应
B. 既是氧化剂又是还原剂
C.氧化产物与还原产物的物质的量之比为2∶1
D. 发生反应,转移 电子
2.(2022·全国乙卷)某白色粉末样品,可能含有 、 、 和 。取少量样品进
行如下实验:
①溶于水,得到无色透明溶液
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
③取②的上层清液,向其中滴加 溶液有沉淀生成。
该样品中确定存在的是
A. B.
C. D.
3.(2020江苏卷)下列有关化学反应的叙述正确的是
A.室温下,Na在空气中反应生成NaO
2 2
B.室温下,Al与4.0 mol﹒L-1NaOH溶液反应生成NaAlO
2
C.室温下,Cu与浓HNO 反应放出NO气体
3
D.室温下,Fe与浓HSO 反应生成FeSO
2 4 4
4.(2020天津卷)在全国人民众志成城抗击新冠病毒期间,使用的“84消毒液”的主要有效成分是
A.NaOH B.NaCl C.NaClO D.NaCO
2 3
5.(2020年7月浙江选考)下列说法不正确的是( )A. 会破坏铝表面的氧化膜
B. 的热稳定性比 强
C. 具有氧化性,其稀溶液可用于消毒
D.钢铁在潮湿空气中生锈主要是发生了电化学腐蚀
1. 【答案】D
【解析】 常温下钠与氧气反应:4Na+O===2Na O,加热条件下与氧气反应2Na+O=====NaO ,条件
2 2 2 2 2
不同,产物不同,A正确;钠性质活泼,与水能够剧烈反应生成氢氧化钠和氢气,所以钠着火时可用沙土
盖灭,不能用水灭火,B正确;钠的密度比煤油大,且与煤油不反应,少量的钠可保存在煤油中,C正确;
因钠活泼,易与水、氧气反应,如在实验室随意丢弃,可引起火灾,因此剩余的钠粒需要放回原试剂瓶中,
D错误。
2. 【答案】C
【解析】 钠沉入液氨说明钠的密度比液氨大,A正确;液氨中没有能导电的离子,而钠投入液氨中生成蓝
色的溶剂合电子,能导电,说明溶液的导电性增强,B正确;0.1 mol钠反应失去0.1 mol电子,C错误;反
应中钠失去电子,只能是氢元素得到电子,所以钠和液氨可发生以下反应:2NH +2Na===2NaNH +H↑,
3 2 2
D正确。
3. 【答案】D
【解析】 相同温度下碳酸氢钠的溶解度小于碳酸钠的溶解度,D错误。
4. 【答案】 D
【解析】 NaCO 溶液中含NaSO ,加Ba(OH) 溶液,NaCO、NaSO 都产生沉淀,无法分离。
2 3 2 4 2 2 3 2 4
5. 【答案】 C
【解析】 瓷坩埚中含SiO ,高温下SiO 可与NaCO 发生反应,A错误;加热固体时试管口应略朝下,B
2 2 2 3
错误;NH 的密度小于空气,应该用向下排空气法收集,D错误。
31. 【答案】C
【分析】
饱和NaCl溶液中通入NH 和CO,生成NaHCO 沉淀和NH Cl溶液;过滤出沉淀,加热,溶于水得到
3 2 3 4
NaCO 饱和溶液;通入气体a(SO ),调节pH=4.1,得到NaSO 溶液,加入NaCO 调节pH=7~8,此时
2 3 2 2 3 2 3
NaHSO 转化为NaSO ,再通入SO ,并使pH=4.1,则生成NaHSO 过饱和溶液,结晶脱水得NaSO。
3 2 3 2 3 2 2 5
【详解】
A.反应I、Ⅱ是通过侯氏制碱法制备碳酸钠,反应I制备NaHCO 的化学方程式为
3
,反应时先通入氨气,再通入CO,反应Ⅱ为NaHCO 加热分
2 3
解生成NaCO,选项A错误;
2 3
B.根据已知信息可知,反应Ⅲ是为了制备NaHSO,发生反应: ,
3
选项B错误;
C.由于得到的NaHSO 不是过饱和溶液,后加碳酸钠固体、并再次充入SO 的目的,得到NaHSO 过饱和
3 2 3
溶液,结晶得NaHSO 晶体,选项C正确;
3
D.由流程图可知,NaHSO 失水得到NaSO,反应的化学方程式为 ,该反应中
3 2 2 5
各元素化合价不变,为非氧化还原反应,选项D正确;
答案选C。
2.【答案】A
【详解】
A.向稀盐酸中加入少量钠粒,钠和HCl电离的氢离子反应,2Na+2H+=2Na++H ↑,A错误;
2
B.硫酸酸化的碘化钾淀粉溶液久置后变蓝是因为碘离子被空气中的氧气氧化为碘单质,B正确;
C.硫代硫酸钠在酸性条件下发生反应生成二氧化硫、硫单质和水,该离子方程式正确,C正确;
D.向含氯化铁的氯化镁溶液中加入氧化镁,氧化镁消耗Fe3+水解产生的氢离子,使Fe3+的水解平衡正向移
动生成Fe(OH) 沉淀,该离子方程式正确,D正确;
3
答案选A。
3.【答案】A
【解析】
火焰呈紫色(透过蓝色钴玻璃),说明待测试液中一定含有钾元素,由于蓝色钴玻璃能滤去黄色光,所以可
能含钠元素,故A正确;白色沉淀可能是硅酸、氢氧化铝等,该溶液中可能含有 SiO、AlO,故B错误;
使品红溶液褪色的气体可能是臭氧、氯气、二氧化硫等,故 C错误;NaOH溶液过量,可与氯化镁、氯化铁反应,均有沉淀生成,而不是沉淀的转化,则不能说明 Fe(OH) 的溶解度小于Mg(OH) 的溶解度,故D
3 2
错误。
4. 【答案】C
【解析】
过氧化钠溶于水放出热量并生成氧气,使容器内温度升高,压强增大,U形管内液体慢慢右移,但恢复到
原温度后液面左边仍然比右边低,故A错误;钠加入水中放热并生成氢气,使容器内温度升高,压强增大,
U形管内液体慢慢右移,但恢复到原温度后液面左边仍然比右边低,故B错误;氧化钠与水反应放出热量,
使容器内温度升高,压强增大,U形管内液体慢慢右移,恢复到原温度后液面左边与右边基本相平,故C
正确;钾加入水中放热并生成氢气,使容器内温度升高,压强增大,U形管内液体慢慢右移,但恢复到原
温度后液面左边仍然比右边低,故D错误。
5. 【答案】C
【解析】
装置②中试剂可以是NaOH溶液,用来除掉二氧化碳气体,故A正确;装置③中盛有浓硫酸,作用是干燥
O ,故B正确;由于氧气密度大于空气,应选择装置b,故C错误;装置②、③之间应增加盛澄清石灰水
2
的洗气瓶,验证二氧化碳是否除尽,故D正确。
1. 【答案】B
【解析】NaSO+H SO =Na SO +S ↓+SO ↑ +H O,该反应的本质是硫代硫酸根离子在酸性条件下发上歧化
2 2 3 2 4 2 4 2 2
反应生成硫和二氧化硫,化合价发生变化的只有S元素一种,硫酸的作用是提供酸性环境。
A.HSO 转化为硫酸钠和水,其中所含元素的化合价均未发生变化,故其没有发生还原反应,A说法不正
2 4
确;
B.NaSO 中的S的化合价为+2,其发生歧化反应生成S(0价)和SO (+4价),故其既是氧化剂又是还原剂,
2 2 3 2
B说法正确;
C.该反应的氧化产物是SO ,还原产物为S,氧化产物与还原产物的物质的量之比为1:1,C说法不正确;
2
D.根据其中S元素的化合价变化情况可知,1mol Na SO 发生反应,要转移2 mol电子,D说法不正确。
2 2 3
综上所述,本题选B。
2. 【答案】A
【解析】由题意可知,①取少量样品溶于水得到无色透明溶液,说明固体溶于水且相互之间能共存,②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体放出,说明固体中存在NaSO,发生反应SO
2 2 3 2
+2H+=S↓+H O+SO ↑,离心分离,③取②的上层清液,向其中滴加BaCl 溶液,有沉淀生成,则沉淀为
2 2 2
BaSO,说明固体中存在NaSO ,不能确定是否有NaSO 和NaCO,NaSO 与过量盐酸反应生成二氧化
4 2 4 2 3 2 3 2 3
硫,NaCO 与过量盐酸反应生成二氧化碳,而这些现象可以被NaSO 与过量盐酸反应的现象覆盖掉,综
2 3 2 2 3
上分析,该样品中确定存在的是:NaSO 、NaSO,
2 4 2 2 3
答案选A。
3.【答案】B
【解析】A.室温下,钠与空气中氧气反应生成氧化钠,故A错误;
B.室温下,铝与NaOH溶液反应生成偏铝酸钠和氢气,故B正确;
C.室温下,铜与浓硝酸反应生成二氧化氮气体,故C错误;
D.室温下,铁在浓硫酸中发生钝化,故D错误。
综上所述,答案为B。
4.【答案】C
【解析】工业上用Cl 与NaOH溶液反应制取“84消毒液”,反应原理为Cl+2NaOH=NaCl+NaClO+H O,
2 2 2
NaClO具有强氧化性,能用于杀菌消毒,故“84消毒液”的主要有效成分是NaClO,答案选C。
5.【答案】B
【解析】A.Cl-很容易被吸附在铝表面的氧化膜上,将氧化膜中的氧离子取代出来,从而破坏氧化膜,A
选项正确;
B.碳酸氢钠受热分解可产生碳酸钠、水和二氧化碳,则稳定性:NaHCO <NaCO,B选项错误;
3 2 3
C.KMnO 具有强氧化性,可使病毒表面的蛋白质外壳变形,其稀溶液可用于消毒,C选项正确;
4
D.钢铁在潮湿的空气中,铁和碳、水膜形成原电池,发生电化学腐蚀,腐蚀速率更快,D选项正确;
答案选B。