文档内容
考向 12 氮及其化合物
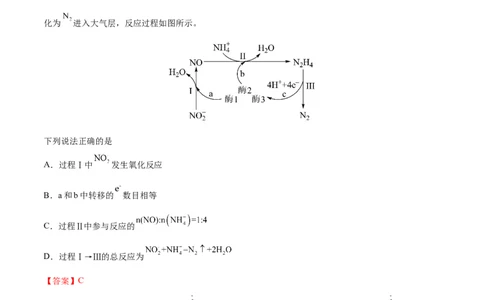
【2022湖南卷】科学家发现某些生物酶体系可以促进 和 的转移(如a、b和c),能将海洋中的 转
化为 进入大气层,反应过程如图所示。
下列说法正确的是
A.过程Ⅰ中 发生氧化反应
B.a和b中转移的 数目相等
C.过程Ⅱ中参与反应的
D.过程Ⅰ→Ⅲ的总反应为
【答案】C
【解析】A.由图示可知,过程I中NO 转化为NO,氮元素化合价由+3价降低到+2价,NO 作氧化剂,
被还原,发生还原反应,A错误;
B.由图示可知,过程I为NO 在酶1的作用下转化为NO和HO,依据得失电子守恒、电荷守恒和原子守
2
恒可知,反应的离子方程式为:NO +2H++e- NO+H O,生成1molNO,a过程转移1mole-,过程II为NO
2和NH 在酶2的作用下发生氧化还原反应生成HO和NH,依据得失电子守恒、电荷守恒和原子守恒可
2 2 4
知,反应的离子方程式为:2NO+8NH 2HO+5NH+8H+,消耗1molNO,b过程转移4mol e-,转移电子
2 2 4
数目不相等,B错误;
C.由图示可知,过程II发生反应的参与反应的离子方程式为:2NO+8NH 2HO+5NH+8H+,
2 2 4
n(NO):n(NH )=1:4,C正确;
D.由图示可知,过程III为NH 转化为N 和4H+、4e-,反应的离子方程式为:NH= N +4H++4e-,过程I-
2 4 2 2 4 2
III的总反应为:2NO +8NH =5N ↑+4H O+24H++18e-,D错误;
2 2
答案选C。
知识点一 氮气及氮的氧化物
1.氮的存在和氮的固定2.氮气
(1)物理性质:色味气体,密度比空气略小,溶于水。
(2)化学性质
写出有关化学方程式:
① 3Mg + N ===== Mg N;
2 3 2
②N + 3H 2NH ;
2 2 3
③N + O ===== 2NO 。
2 2
[名师点拨] (1)N 到NO 不能一步转化完成。
2 2
(2)Mg N 只能干态制取,遇水强烈反应,生成氢氧化镁沉淀,放出氨气。
3 2
3.氮的氧化物
(1)氮有多种价态的氧化物:NO、NO、NO、NO 、NO、NO 等,其中属于酸性氧化物的是NO、
2 2 3 2 2 4 2 5 2 3
NO。
2 5
(2)NO和NO 性质的比较
2
NO NO
2
颜色 无色 红棕色
物理
毒性 有毒 有毒
性质
溶解性 不溶于水 易溶于水
与O 反应 2NO + O == =2NO —
2 2 2
化学
能与HO
2
性质 — 3NO + H O == =2HNO + NO
2 2 3
反应
[名师点拨] (1)氮的氧化物都有毒,其中NO 与NO 存在下列平衡:2NO NO ,因此实
2 2 4 2 2 4
验测得NO 的相对分子质量总大于46。
2
(2)验证某无色气体为NO的方法是向无色气体中通入O(或空气),无色气体变为红棕色。
2(3)NO与血红蛋白结合使人中毒。
4.氮氧化物对环境的污染及防治
(1)常见的污染类型
NO 在紫外线作用下,与碳氢化合物发生一系列光化学反应,产生一种有毒
光化学烟雾 x
的烟雾
酸雨 NO 排入大气中后,与水反应生成HNO 和HNO,随雨雪降到地面
x 3 2
破坏臭氧层 NO 可使平流层中的臭氧减少,导致地面紫外线辐射量增加
2
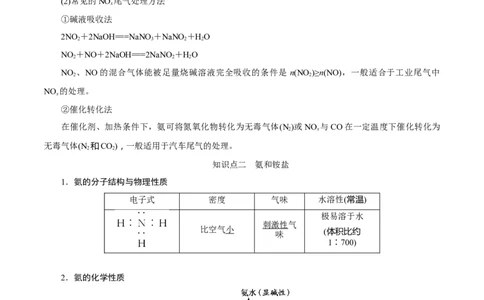
(2)常见的NO 尾气处理方法
x
①碱液吸收法
2NO +2NaOH===NaNO +NaNO +HO
2 3 2 2
NO +NO+2NaOH===2NaNO +HO
2 2 2
NO 、NO的混合气体能被足量烧碱溶液完全吸收的条件是 n(NO )≥n(NO),一般适合于工业尾气中
2 2
NO 的处理。
x
②催化转化法
在催化剂、加热条件下,氨可将氮氧化物转化为无毒气体(N )或NO 与CO在一定温度下催化转化为
2 x
无毒气体(N 和CO),一般适用于汽车尾气的处理。
2 2
知识点二 氨和铵盐
1.氨的分子结构与物理性质
电子式 密度 气味 水溶性(常温)
极易溶于水
刺激性气
比空气小
味
(体积比约
1∶700)
2.氨的化学性质
(1)氨气与水的反应
NH +HONH ·H ONH+OH-,氨气溶于水得氨水。
3 2 3 2
①氨水中含有的微粒:NH ·H O 、 NH 、 H O 、 NH 、 OH - 、 H + 。
3 2 3 2
②NH ·H O为可溶性一元弱碱,易挥发,不稳定,易分解:NH ·H O=====NH ↑+HO。
3 2 3 2 3 2
(2)氨气与酸的反应蘸有浓盐酸的玻璃棒与蘸有浓氨水的玻璃棒靠近,其现象有白烟生成,将浓盐酸改为浓硝酸,也会出
现相同的现象。化学方程式: HCl + NH == =NH Cl、NH + HNO == =NH NO 。
3 4 3 3 4 3
(3)氨气与盐溶液的反应
如过量氨气与AlCl 溶液反应的离子方程式: Al 3 + + 3NH + 3H O == =Al(OH) ↓ + 3NH 。
3 3 2 3
(4)氨气的还原性
性质 化学方程式
催化氧化 4NH +5O4NO+6HO
3 2 2
被CuO氧化 2NH +3CuO=====3Cu+N+3HO
3 2 2
2NH +3Cl===N +6HCl
3 2 2
被氯气氧化
或8NH +3Cl===N +6NH Cl
3 2 2 4
6NO+4NH =====5N+6HO
被氮氧化物氧 3 2 2
化
6NO +8NH =====7N+12HO
2 3 2 2
3.氨气的实验室制法
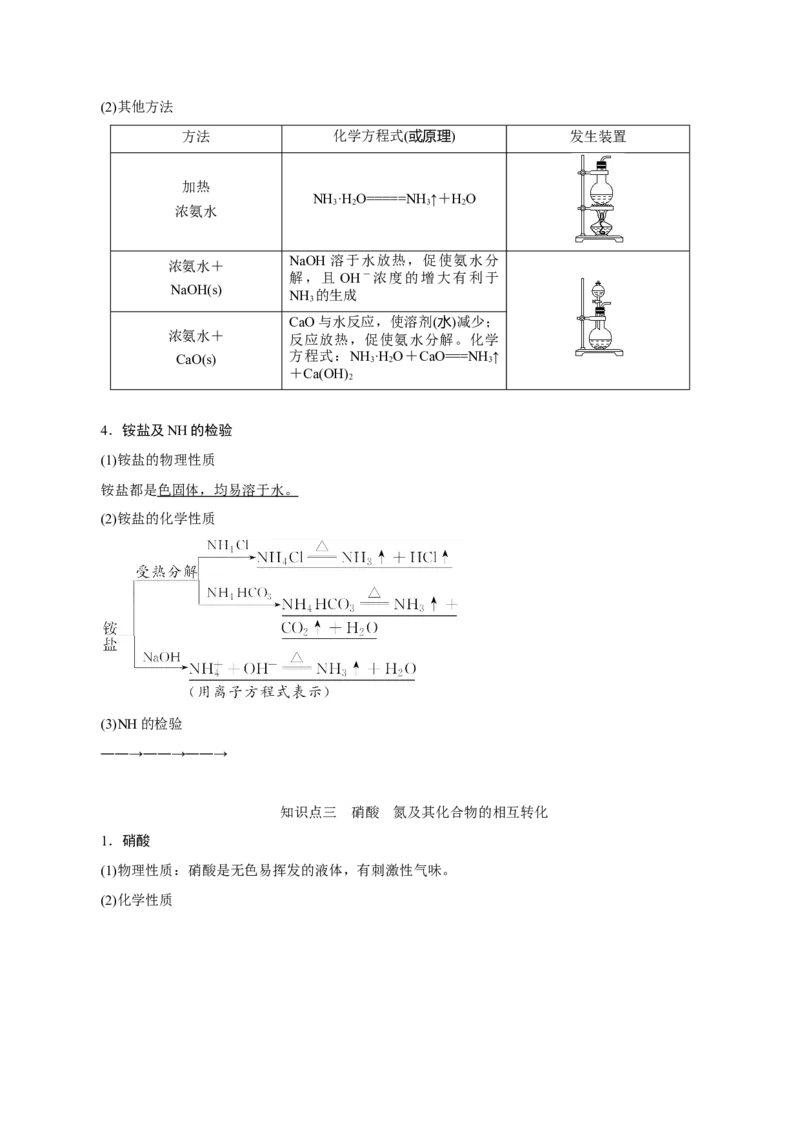
(1)常规方法:固+固――→氨气(2)其他方法
方法 化学方程式(或原理) 发生装置
加热
NH ·H O=====NH ↑+HO
3 2 3 2
浓氨水
NaOH 溶于水放热,促使氨水分
浓氨水+
解,且 OH-浓度的增大有利于
NaOH(s)
NH 的生成
3
CaO与水反应,使溶剂(水)减少;
浓氨水+
反应放热,促使氨水分解。化学
CaO(s) 方程式:NH 3 ·H 2 O+CaO===NH 3 ↑
+Ca(OH)
2
4.铵盐及NH的检验
(1)铵盐的物理性质
铵盐都是色固体,均易溶于水。
(2)铵盐的化学性质
(3)NH的检验
――→――→――→
知识点三 硝酸 氮及其化合物的相互转化
1.硝酸
(1)物理性质:硝酸是无色易挥发的液体,有刺激性气味。
(2)化学性质①不稳定性
反应:4HNO ( 浓 ) ===== 2H O + 4NO ↑ + O ↑。
3 2 2 2
[名师点拨] (1)市售浓硝酸呈黄色的原因是:硝酸分解生成的NO 溶解在硝酸里。
2
(2)硝酸要保存在棕色试剂瓶中,置于冷暗处,不能用橡胶塞。
②强氧化性
浓、稀硝酸均具有强氧化性,浓度越大,氧化性越强,其还原产物的价态越高。还原产物一般为
HNO(浓)―→NO ,HNO(稀)―→NO。
3 2 3
稀硝酸与铜反应的化学方程式:
能与金 3Cu + 8HNO ( 稀 ) == =3Cu(NO ) + 2NO ↑ + 4H O
3 3 2 2
属反应 浓硝酸与铜反应的化学方程式:
Cu + 4HNO ( 浓 ) == =Cu(NO ) + 2NO ↑ + 2H O
3 3 2 2 2
能与非
浓硝酸与C反应的化学方程式:
金属
C + 4HNO ( 浓 ) ===== CO ↑ + 4NO ↑ + 2H O
3 2 2 2
反应
能与还原
可氧化Fe2+、HS、SO 、NaSO 、HI等还原性物质。如与
性化合 2 2 2 3
FeSO 溶液反应:3Fe2++4H++NO===3Fe3++NO↑+2HO
4 2
物反应
[名师点拨] 常温下,铁、铝遇浓硝酸能发生“钝化”,并非不反应,故浓硝酸可以用铁桶盛放。
(3)工业制法
①NH 在催化剂作用下与O 反应生成NO:4NH + 5O ===== 4NO + 6H O。
3 2 3 2 2
②NO进一步氧化生成NO : 2NO + O == =2NO 。
2 2 2
③用水吸收NO 生成HNO:3NO + H O == =2HNO + NO 。
2 3 2 2 3
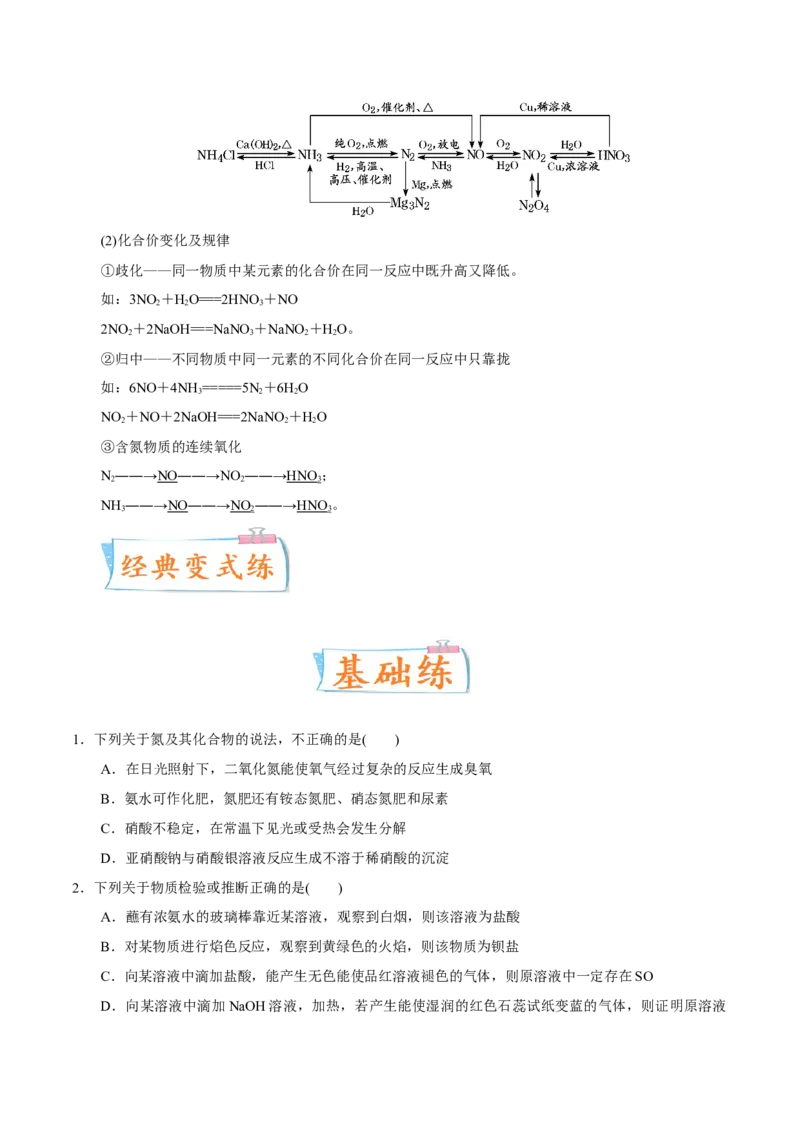
2.氮及其化合物的转化
(1)转化关系(2)化合价变化及规律
①歧化——同一物质中某元素的化合价在同一反应中既升高又降低。
如:3NO +HO===2HNO +NO
2 2 3
2NO +2NaOH===NaNO +NaNO +HO。
2 3 2 2
②归中——不同物质中同一元素的不同化合价在同一反应中只靠拢
如:6NO+4NH =====5N+6HO
3 2 2
NO +NO+2NaOH===2NaNO +HO
2 2 2
③含氮物质的连续氧化
N――→NO――→NO ――→HNO;
2 2 3
NH ――→NO――→NO ――→HNO。
3 2 3
1.下列关于氮及其化合物的说法,不正确的是( )
A.在日光照射下,二氧化氮能使氧气经过复杂的反应生成臭氧
B.氨水可作化肥,氮肥还有铵态氮肥、硝态氮肥和尿素
C.硝酸不稳定,在常温下见光或受热会发生分解
D.亚硝酸钠与硝酸银溶液反应生成不溶于稀硝酸的沉淀
2.下列关于物质检验或推断正确的是( )
A.蘸有浓氨水的玻璃棒靠近某溶液,观察到白烟,则该溶液为盐酸
B.对某物质进行焰色反应,观察到黄绿色的火焰,则该物质为钡盐
C.向某溶液中滴加盐酸,能产生无色能使品红溶液褪色的气体,则原溶液中一定存在SO
D.向某溶液中滴加NaOH溶液,加热,若产生能使湿润的红色石蕊试纸变蓝的气体,则证明原溶液中存在NH
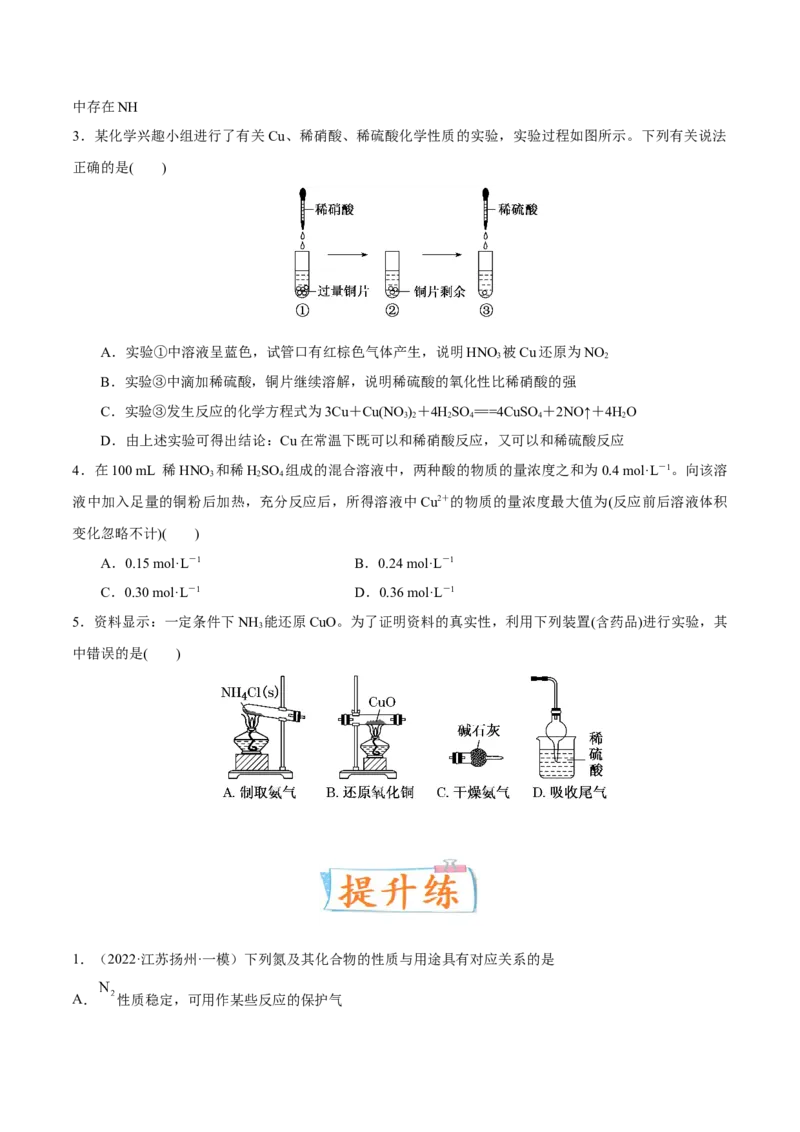
3.某化学兴趣小组进行了有关Cu、稀硝酸、稀硫酸化学性质的实验,实验过程如图所示。下列有关说法
正确的是( )
A.实验①中溶液呈蓝色,试管口有红棕色气体产生,说明HNO 被Cu还原为NO
3 2
B.实验③中滴加稀硫酸,铜片继续溶解,说明稀硫酸的氧化性比稀硝酸的强
C.实验③发生反应的化学方程式为3Cu+Cu(NO )+4HSO ===4CuSO+2NO↑+4HO
3 2 2 4 4 2
D.由上述实验可得出结论:Cu在常温下既可以和稀硝酸反应,又可以和稀硫酸反应
4.在100 mL 稀HNO 和稀HSO 组成的混合溶液中,两种酸的物质的量浓度之和为0.4 mol·L-1。向该溶
3 2 4
液中加入足量的铜粉后加热,充分反应后,所得溶液中Cu2+的物质的量浓度最大值为(反应前后溶液体积
变化忽略不计)( )
A.0.15 mol·L-1 B.0.24 mol·L-1
C.0.30 mol·L-1 D.0.36 mol·L-1
5.资料显示:一定条件下NH 能还原CuO。为了证明资料的真实性,利用下列装置(含药品)进行实验,其
3
中错误的是( )
1.(2022·江苏扬州·一模)下列氮及其化合物的性质与用途具有对应关系的是
A. 性质稳定,可用作某些反应的保护气B. 易溶于水,可用作制冷剂
C. 受热易分解,可用作氮肥
D. 呈红棕色,可用于制备硝酸
2.(2022·江苏省如皋中学三模)氮及其化合物在生产生活中具有广泛的应用。氨气可用于生产氮肥和处
理NO 等气体,氨水可用于吸收SO ,NO 可用于制取硝酸,硝酸可洗涤试管上的银镜。NO 能与悬浮在
x 2 x 2
大气中海盐粒子相互作用,反应为2NO +NaCl=NaNO +ClNO(ClNO中N为中心原子,各原子均达到8电
2 3
子稳定结构)。NO能被FeSO 溶液吸收生成[Fe(NO)HO) ]SO 。在给定条件下,下列选项所示的物质间转
4 2 5 4
化均能实现的是
A.NH ·H O(aq) NH HSO (aq) B.NH NO
3 2 4 3 3 2
C.NO HNO D.Ag H
3 2
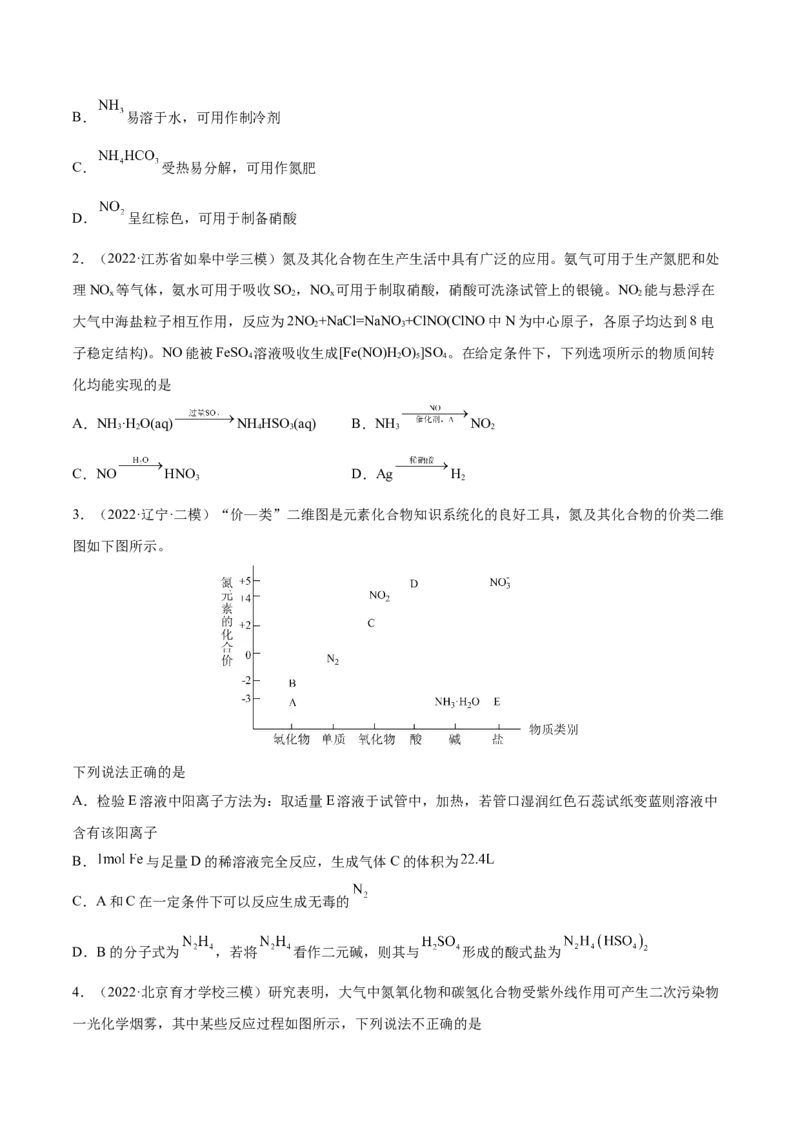
3.(2022·辽宁·二模)“价—类”二维图是元素化合物知识系统化的良好工具,氮及其化合物的价类二维
图如下图所示。
下列说法正确的是
A.检验E溶液中阳离子方法为:取适量E溶液于试管中,加热,若管口湿润红色石蕊试纸变蓝则溶液中
含有该阳离子
B. 与足量D的稀溶液完全反应,生成气体C的体积为
C.A和C在一定条件下可以反应生成无毒的
D.B的分子式为 ,若将 看作二元碱,则其与 形成的酸式盐为
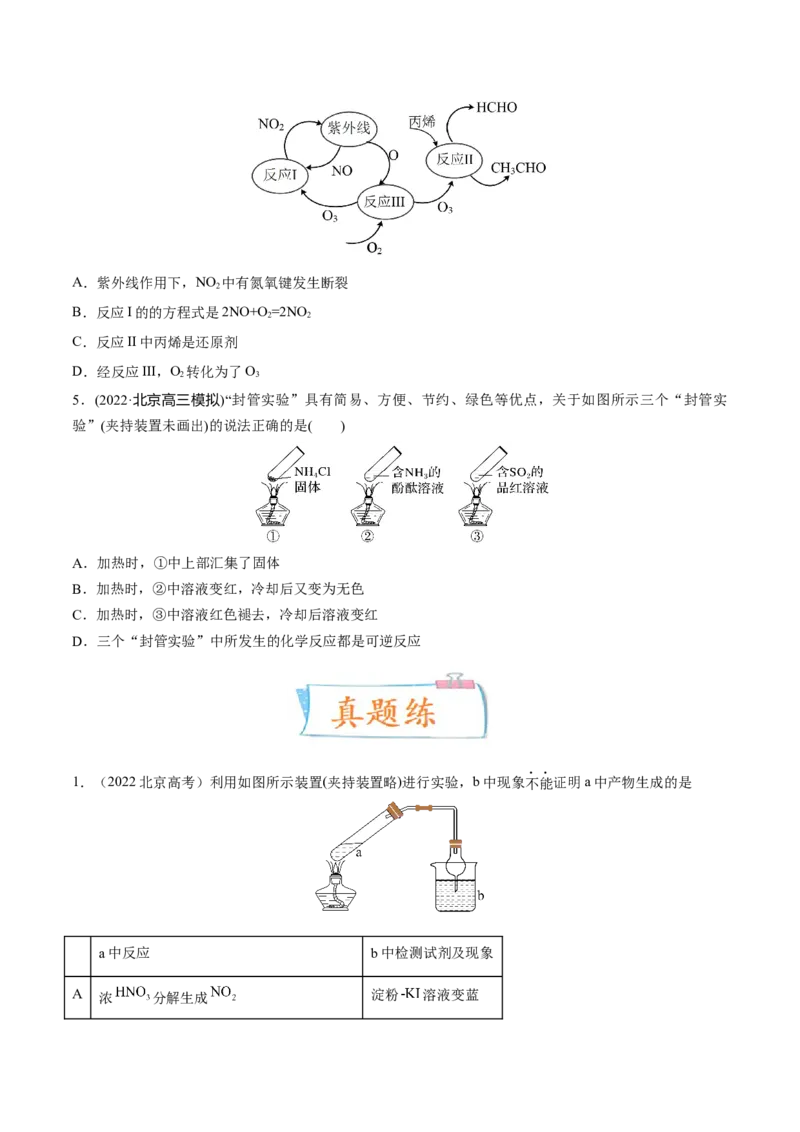
4.(2022·北京育才学校三模)研究表明,大气中氮氧化物和碳氢化合物受紫外线作用可产生二次污染物
一光化学烟雾,其中某些反应过程如图所示,下列说法不正确的是A.紫外线作用下,NO 中有氮氧键发生断裂
2
B.反应I的的方程式是2NO+O =2NO
2 2
C.反应II中丙烯是还原剂
D.经反应III,O 转化为了O
2 3
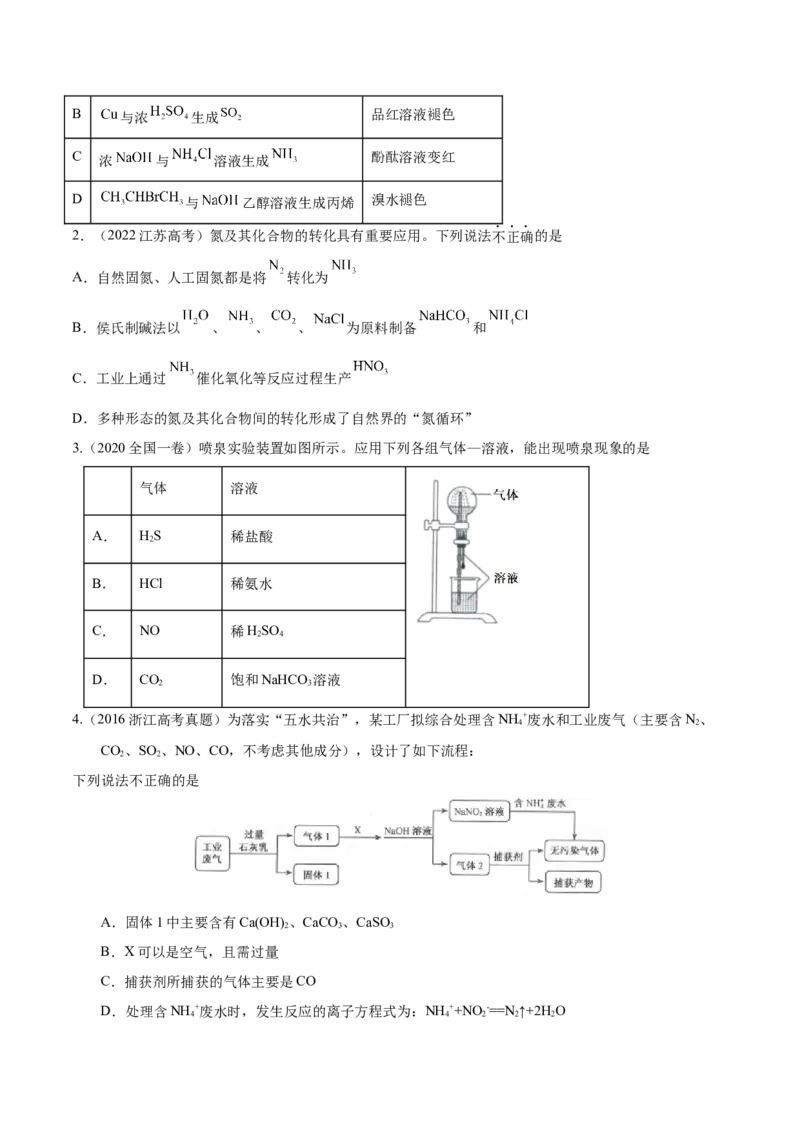
5.(2022·北京高三模拟)“封管实验”具有简易、方便、节约、绿色等优点,关于如图所示三个“封管实
验”(夹持装置未画出)的说法正确的是( )
A.加热时,①中上部汇集了固体
B.加热时,②中溶液变红,冷却后又变为无色
C.加热时,③中溶液红色褪去,冷却后溶液变红
D.三个“封管实验”中所发生的化学反应都是可逆反应
1.(2022北京高考)利用如图所示装置(夹持装置略)进行实验,b中现象不能证明a中产物生成的是
a中反应 b中检测试剂及现象
A 浓 分解生成 淀粉 溶液变蓝B 与浓 生成 品红溶液褪色
C 浓 与 溶液生成 酚酞溶液变红
D 与 乙醇溶液生成丙烯 溴水褪色
2.(2022江苏高考)氮及其化合物的转化具有重要应用。下列说法不正确的是
A.自然固氮、人工固氮都是将 转化为
B.侯氏制碱法以 、 、 、 为原料制备 和
C.工业上通过 催化氧化等反应过程生产
D.多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
3.(2020全国一卷)喷泉实验装置如图所示。应用下列各组气体—溶液,能出现喷泉现象的是
气体 溶液
A. HS 稀盐酸
2
B. HCl 稀氨水
C. NO 稀HSO
2 4
D. CO 饱和NaHCO 溶液
2 3
4.(2016浙江高考真题)为落实“五水共治”,某工厂拟综合处理含NH +废水和工业废气(主要含N、
4 2
CO、SO 、NO、CO,不考虑其他成分),设计了如下流程:
2 2
下列说法不正确的是
A.固体1中主要含有Ca(OH) 、CaCO 、CaSO
2 3 3
B.X可以是空气,且需过量
C.捕获剂所捕获的气体主要是CO
D.处理含NH +废水时,发生反应的离子方程式为:NH ++NO-==N ↑+2H O
4 4 2 2 25.(2015全国高考真题)我国清代《本草纲目拾遗》中记叙无机药物335种,其中“强水”条目下写道:
“性最烈,能蚀五金……其水甚强,五金八石皆能穿第,惟玻璃可盛。”这里的“强水”是指
A.氨水 B.硝酸 C.醋 D.卤水
1.【答案】D
【解析】光化学烟雾形成的过程中,在日光照射下,二氧化氮能使氧气经过复杂的反应生成臭氧,臭氧与
空气中的一些碳氢化合物发生作用,生成一种有毒的烟雾,叫作光化学烟雾,据此可知,A正确;氮肥是
指以氮(N)为主要成分,施于土壤可提供植物氮素营养的肥料,氮肥按含氮基团可分为氨态氮肥、铵态氮肥、
硝态氮肥、硝铵态氮肥、氰氨态氮肥和酰胺态氮肥(尿素),B正确;硝酸不稳定,在常温下见光或受热会
发生分解:4HNO=====4NO ↑+2HO+O↑,C 正确;亚硝酸钠与硝酸银溶液反应:NaNO +
3 2 2 2 2
AgNO===AgNO ↓+NaNO ,生成淡黄色的AgNO,AgNO 可以与稀硝酸反应,D错误。
3 2 3 2 2
2.【答案】D
【解析】浓硝酸也具有挥发性,可以和氨气反应生成硝酸铵固体,也可以观察到白烟,故 A错误;对某物
质进行焰色反应,观察到黄绿色的火焰,说明含有钡元素,但不一定是钡盐,也可能是氢氧化钡,故 B错
误;含有HSO的溶液也可以和盐酸反应生成二氧化硫,故 C错误;向某溶液中滴加NaOH溶液,加热,
产生能使湿润的红色石蕊试纸变蓝的气体,说明产生了氨气,则原溶液含有NH,故D正确。
3.【答案】C
【解析】稀硝酸被Cu还原为NO,故A错误;Cu与稀硫酸不反应,但硝酸铜在酸性条件下具有硝酸的强
氧化性,继续与Cu反应,稀硫酸的氧化性比稀硝酸弱,故B错误;实验③发生反应的化学方程式为3Cu
+Cu(NO ) +4HSO ===4CuSO +2NO↑+4HO,故C正确;由上述实验可得出结论:Cu在常温下可以和
3 2 2 4 4 2
稀硝酸反应,故D错误。
4.【答案】B
【解析】反应的离子方程式为3Cu+2NO+8H+===3Cu2++2NO↑+4HO,铜足量,由上述反应方程式可知,
2
NO和H+的物质的量之比为1∶4时,反应生成的铜离子物质的量最大,设HNO 、HSO 各为x mol、y
3 2 4
mol,则n(NO)∶n(H+)=x∶(x+2y)=1∶4,x+y=0.4 mol·L-1×0.1 L,解得x=0.016 mol、y=0.024 mol,由方程式可知,生成铜离子的物质的量为0.016 mol×=0.024 mol,故铜离子的最大浓度为=0.24 mol·L-1。
5.【答案】A
【解析】氯化铵分解生成氨和氯化氢,在试管口附近氨和氯化氢相遇又生成了白色固体氯化铵,故不能用
于制备氨,选项A错误;可以在硬质玻璃管中进行氨还原氧化铜的反应,选项B正确;碱石灰可以干燥氨,
选项C正确;氨极易溶于稀硫酸,该装置吸收尾气中的氨可以防止倒吸,选项D正确。
1.【答案】A
【详解】A.氮气具有稳定性,可用作某些反应的保护气,故A正确;
B.液氨汽化吸收大量的热,具有制冷作用,所以可用作制冷剂,故B错误;
C.碳酸氢铵含有氮元素,所以可用作氮肥,与其受热分解的性质无关,故C错误;
D.二氧化氮可以和水反应生成硝酸,可用于制备硝酸,故D错误;
故选A。
2.【答案】A
【详解】A.一水合氨溶液显碱性,与过量二氧化硫溶液反应生成NH4HSO3,A正确;
B.NH3与NO反应,可能发生归中反应生成N2,不可能生成生成NO2,B错误;
C.NO不溶于水,不能和水反应生成硝酸 ,C错误;
D.稀硝酸为氧化性酸,与Ag反应生成NO,不会生成氢气,D错误;
故选A。
3.【答案】C
【分析】根据示意图可判断A是氨气,B是N2H4,C是NO,D是硝酸,E是铵盐,据此解答。
【详解】A.E为铵盐,铵盐在溶液中不一定都易分解,且产物也不一定产生氨气,所以该实验方法不能
检验铵根离子,A错误;
B.铁与稀硝酸反应生成NO,但气体所处温度和压强未知,不能计算其体积,B错误;
C.氨气和NO在一定条件下发生氧化还原反应,生成氮气和水,C正确;
D.若将 看作二元碱,则其与 形成的酸式盐为 ,D错误;
答案选C。
4.【答案】B
【详解】A.由分析知,紫外线作用下,NO2 反应生成 ,NO2中有氮氧键发生断裂,故A正确;B.根据图示可知,反应Ⅰ的化学方程式为 ,故B错误;
C.由图示可知,反应Ⅱ发生氧化还原反应,其中 是氧化剂, 为还原剂,故C正确;
D.反应 中 与氧气结合生成 ,则反应 的方程式为 ,O2转化为了O3 ,故D正确;
故答案为B。
5.【答案】 A
【解析】加热氯化铵分解,在①中上方HCl与氨气化合生成氯化铵,A正确;氨气的水溶液显碱性,加热
时氨气逸出,酚酞溶液褪色,冷却时氨气溶于酚酞溶液,溶液显红色,B错误;二氧化硫可使品红褪色,
化合生成无色物质,加热可分解,则加热时,③中溶液变红,冷却后红色褪去,C错误;可逆反应应在同
一条件下进行,题中实验分别在加热条件下和冷却后进行,不是可逆反应,D错误。
1.【答案】A
【详解】
A.浓硝酸具有挥发性,挥发出的硝酸也能与碘化钾溶液反应生成遇淀粉溶液变蓝色的碘,则淀粉碘化钾
溶液变蓝色不能说明浓硝酸分解生成二氧化氮,故A符合题意;
B.铜与浓硫酸共热反应生成的二氧化硫具有漂白性,能使品红溶液褪色,则品红溶液褪色能说明铜与浓
硝酸共热反应生成二氧化硫,故B不符合题意;
C.浓氢氧化钠溶液与氯化铵溶液共热反应生成能使酚酞溶液变红的氨气,则酚酞溶液变红能说明浓氢氧
化钠溶液与氯化铵溶液共热反应生成氨气,故C不符合题意;
D.乙醇具有挥发性,挥发出的乙醇不能与溴水反应,则2—溴丙烷与氢氧化钠乙醇溶液共热发生消去反应
生成能使溴水褪色的丙烯气体,则溴水褪色能说明2—溴丙烷与氢氧化钠乙醇溶液共热发生消去反应生成
丙烯,故D不符合题意;
故选A。
2.【答案】A
【详解】
A.自然固氮是将N 转化为含氮化合物,不一定是转化为NH ,比如大气固氮是将N 会转化为NO,A错
2 3 2
误;
B.侯氏制碱法以HO、NH 、CO、NaCl为原料制备NaHCO 和NH Cl,反应的化学方程式为
2 3 2 3 4HO+NH +CO +NaCl=NaHCO ↓+NHCl,B正确;
2 3 2 3 4
C.工业上通过NH 催化氧化等反应过程生产HNO,相关的化学反应方程式为4NH +5O
3 3 3 2
4NO+6H O、2NO+O =2NO、3NO +H O=2HNO +NO、4NO +O +2H O=4HNO ,C正确;
2 2 2 2 2 3 2 2 2 3
D.氮元素在自然界中既有游离态又有化合态,多种形态的氮及其化合物间的转化形成了自然界的“氮循
环”,D正确;
故选A。
3.【答案】B
【解析】能够发生喷泉实验,需要烧瓶内外产生明显的压强差;产生压强差可以通过气体溶于水的方法,
也可以通过发生反应消耗气体产生压强差,据此分析。A.由于硫化氢气体和盐酸不发生反应且硫化
氢在水中的溶解度较小,烧瓶内外压强差变化不大,不会出现喷泉现象,A错误;B.氯化氢可以和
稀氨水中的一水合氨发生反应,使烧瓶内外产生较大压强差,能够出现喷泉实验,B正确;C.一氧
化氮不与硫酸发生反应且不溶于水,烧瓶内外不会产生压强差,不能发生喷泉现象,C错误;D.二
氧化碳不会溶于饱和碳酸氢钠溶液中,烧瓶内外不会产生压强差,不能发生喷泉实验,D错误;故选
B。
4.【答案】B
【解析】工业废气中CO、SO 可被石灰水吸收,生成固体1为CaCO 、CaSO,气体1是不能被过量石灰
2 2 3 3
水吸收的N、NO、CO,气体1通入气体X,用氢氧化钠溶液处理后到的NaNO ,X可为空气,但不
2 2
能过量,否则得到硝酸钠,NaNO 与含有NH +的溶液反应生成无污染气体,应生成氮气,则气体2含
2 4
有CO、N,捕获剂所捕获的气体主要是CO。A.工业废气中CO、SO 可被石灰水吸收,生成
2 2 2
CaCO 、CaSO,因氢氧化钙过量,则固体1为主要含有Ca(OH) 、CaCO 、CaSO,正确;B.由分析
3 3 2 3 3
可知,气体1是不能被过量石灰水吸收的N、NO、CO,气体1通入气体X,用氢氧化钠溶液处理后
2
到的NaNO ,X可为空气,但不能过量,否则得到硝酸钠,错误;C.气体2含有CO、N,经捕获剂
2 2
得到氮气和CO,所捕获的气体主要是CO,防止污染空气,正确;D.NaNO 与含有NH +的溶液反应
2 4
生成无污染气体,应生成氮气,发生氧化还原反应,离子方程式为NH ++NO-=N ↑+2H O,正确;故
4 2 2 2
选B。
5.【答案】B
【解析】根据题意该物质能够与很多金属反应,根据选项B最符合,该强水为硝酸,硝酸具有强氧化性,
可溶解大部分金属;答案选B。