文档内容
考向 11 硫及其化合物
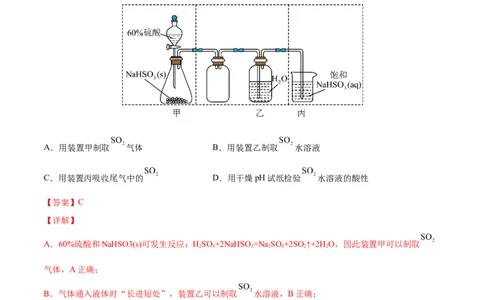
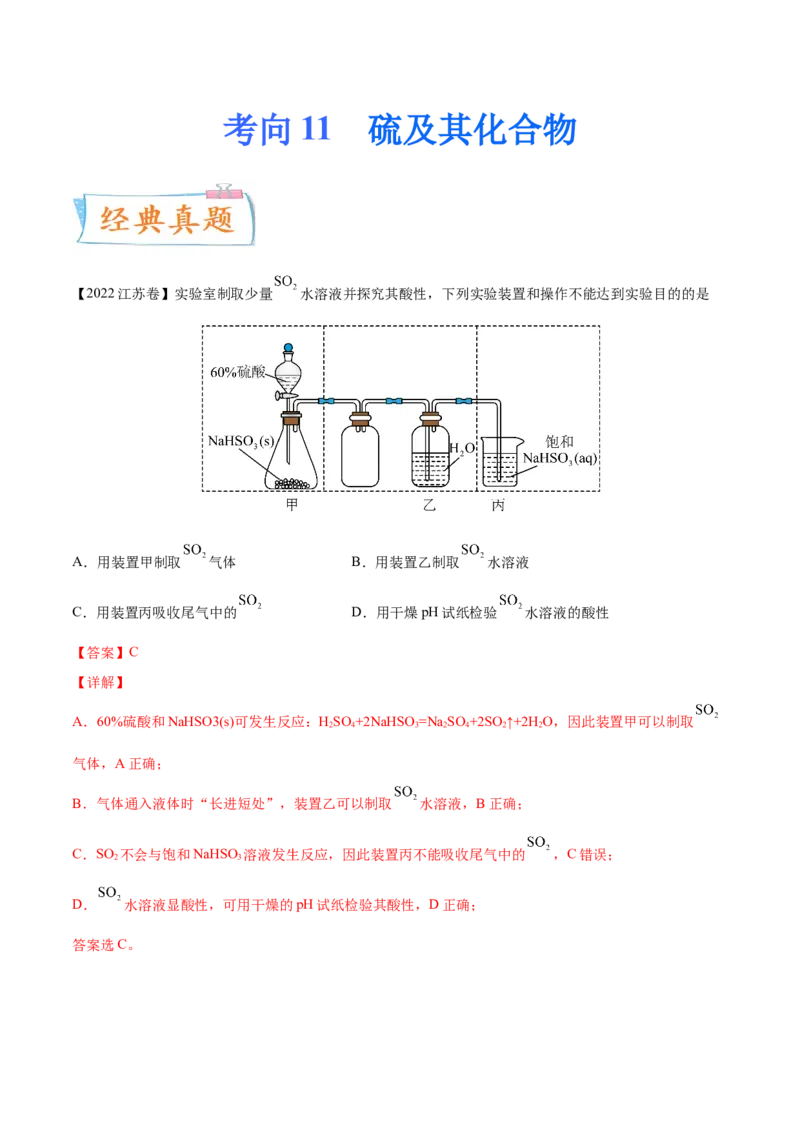
【2022江苏卷】实验室制取少量 水溶液并探究其酸性,下列实验装置和操作不能达到实验目的的是
A.用装置甲制取 气体 B.用装置乙制取 水溶液
C.用装置丙吸收尾气中的 D.用干燥pH试纸检验 水溶液的酸性
【答案】C
【详解】
A.60%硫酸和NaHSO3(s)可发生反应:HSO +2NaHSO =Na SO +2SO↑+2H O,因此装置甲可以制取
2 4 3 2 4 2 2
气体,A正确;
B.气体通入液体时“长进短处”,装置乙可以制取 水溶液,B正确;
C.SO 不会与饱和NaHSO 溶液发生反应,因此装置丙不能吸收尾气中的 ,C错误;
2 3
D. 水溶液显酸性,可用干燥的pH试纸检验其酸性,D正确;
答案选C。知识点一 硫及其氧化物
1.硫单质
(1)硫元素存在形态
①游离态:硫单质俗称硫黄,主要存在于火山喷口附近或地壳的岩层里。
②化合态:主要以硫化物和硫酸盐的形式存在,有关化学式如下:
硫铁矿 黄铜矿 石膏 芒硝
FeS CuFeS CaSO·2H O NaSO ·10H O
2 2 4 2 2 4 2
(2)物理性质
颜色状态 溶解性
黄色晶体 不溶于水,微溶于酒精,易溶于CS
2
(3)化学性质
①能与金属反应表现氧化性②能与非金属反应
③能与强氧化剂反应(如浓硫酸): S + 2H SO ( 浓 ) ===== 3SO ↑ + 2H O,表现还原性。
2 4 2 2
④能与NaOH溶液反应:3S+6NaOH=====2NaS+NaSO +3HO,表现氧化性和还原性。
2 2 3 2
[名师点拨] (1)硫与变价金属反应时,生成低价态金属硫化物(如Cu S、FeS)。
2
(2)汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理。
2.二氧化硫(SO )
2
(1)物理性质
颜色 气味 毒性 密度 溶解性
无色 有刺激性气味 毒 比空气 易溶于水
(2)化学性质
[名师点拨] 三类漂白剂的区别
类型 原理 举例 特点 备注
HClO、NaClO、
氧化型 将有机色质内部“生 Ca(ClO) 2 、 不可逆、 无选
色团”破坏掉 持久 择性
NaO、HO、O 等
2 2 2 2 3
与有机色质内部“生 可逆、 有选
加合型 色团”“化合”成无 SO
2
色物质 不持久 择性
将有色物质吸附而褪 物理 吸附
吸附型 活性炭
色 变化 色素
(3)实验室制备与探究流程[名师点拨] 用70%左右的浓硫酸而不用98.3%的浓硫酸或稀硫酸的原因:若用98.3%的浓硫酸,因其
含水少,硫酸主要以分子形式存在,H+浓度很小,难以反应。若用稀硫酸,则含水量多,因SO 易溶于水,
2
不利于SO 的逸出。
2
3.硫的氧化物的污染与治理
(1)硫的氧化物的来源、危害及治理
(2)硫酸型酸雨的形成过程:
知识点二 硫酸 硫酸根离子的检验
1.硫酸的物理性质
(1)纯硫酸是一种无色油状液体,沸点高,难挥发。(2)溶解性:浓HSO 与水以任意比互溶,溶解时可放出大量的热。
2 4
(3)浓硫酸的稀释方法:将浓硫酸沿器壁慢慢注入水中,并用玻璃棒不断搅拌。
2.稀HSO 具有酸的通性
2 4
硫酸是强电解质,在水溶液中的电离方程式为,能与指示剂、金属、碱性氧化物、碱、盐等物质发生
反应。
3.浓HSO 的特性
2 4
[名师点拨] (1)H SO 是高沸点、难挥发性的强酸,利用这一性质可以制取HCl和HF:HSO (浓)+
2 4 2 4
NaCl=====NaHSO+HCl↑,CaF +HSO ===CaSO +2HF↑。
4 2 2 4 4
(2)由“量变”引起的“质变”:金属(如Cu、Zn等)与浓HSO 反应时,开始阶段产生SO 气体,随着
2 4 2
反应的进行,HSO 的浓度变小,最后变为稀HSO ,Cu与稀HSO 不反应,Zn与稀HSO 反应生成H 而
2 4 2 4 2 4 2 4 2
不是SO 。
2
4.硫酸的工业制备
(1)工艺流程[名师点拨] 工业上用98%的硫酸吸收SO ,可以避免用水吸收SO 产生的酸雾腐蚀设备,并且可以提
3 3
高吸收率。
(2)反应原理
①燃烧硫铁矿(FeS )或硫制备SO :
2 2
4FeS + 11O ===== 2Fe O + 8SO 或S+O=====SO 。
2 2 2 3 2 2 2
②SO 转化为SO :2SO + O 2SO 。
2 3 2 2 3
③SO 被吸收生成HSO :SO + H O == =H SO 。
3 2 4 3 2 2 4
5.SO的检验
(1)检验方法
检验SO的正确操作方法:被检液加足量盐酸酸化,取清液滴加BaCl 溶液有无白色沉淀产生(判断有
2
无SO)
(2)检验误区
只加可溶性钡盐、而 导致将CO、SO等干扰离子判断成SO。因上述离子会产
误区1
不先加盐酸酸化 生BaCO 、BaSO 白色沉淀
3 3
如向待测液中滴加BaCl 溶液,再加稀盐酸有白色沉淀
2
误区2 误将Ag+判断成SO 便断定含SO。其错误是未注意溶液中不含SO,而含Ag
+时也会产生同样的现象:Ag++Cl-===AgCl↓(白色)
如先用稀硝酸酸化,再加入 BaCl 溶液或向待测液中滴
2
误将SO
加用稀盐酸酸化的Ba(NO ) 溶液生成白色沉淀,便误以
误区3 3 2
判断成SO
为有SO。该错误是未注意NO在酸性环境中具有强氧化
性,将SO氧化成SO而产生干扰
6.重要的硫酸盐
化学式 俗名 颜色 主要性质 用途
2CaSO·H O+ 塑像、模型、
4 2
2CaSO·H O 熟石膏 白色 3HO===2(CaSO ·2H O 粉笔、医疗绷
4 2 2 4 2
) 带等
2(CaSO·2H O)
4 2
CaSO·2H O 生石膏 白色 =====3HO+ 水泥添加剂
4 2 2
2CaSO·H O
4 2
FeSO ·7H O 绿矾 浅绿色 暴露在空气中被氧化 用于配制蓝黑
4 2为三价铁盐 墨水,补血剂
CuSO ·5H O=====5H 配制波尔多
CuSO ·5H O 胆矾、蓝矾 蓝色 4 2 2
4 2 O+CuSO (白) 液,镀铜液
4
造纸,制缓泻
NaSO ·10H O 芒硝 白色 — 剂、合成洗涤
2 4 2
剂
KAl(SO )·12H O 明矾 白色 — 净水剂
4 2 2
知识点三 硫及其化合物的相互转化及应用
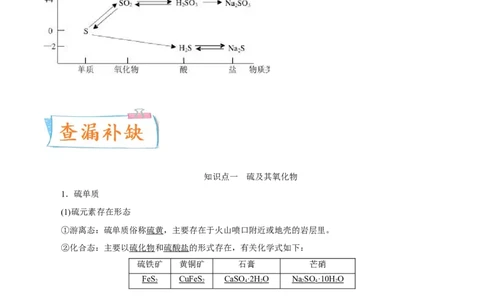
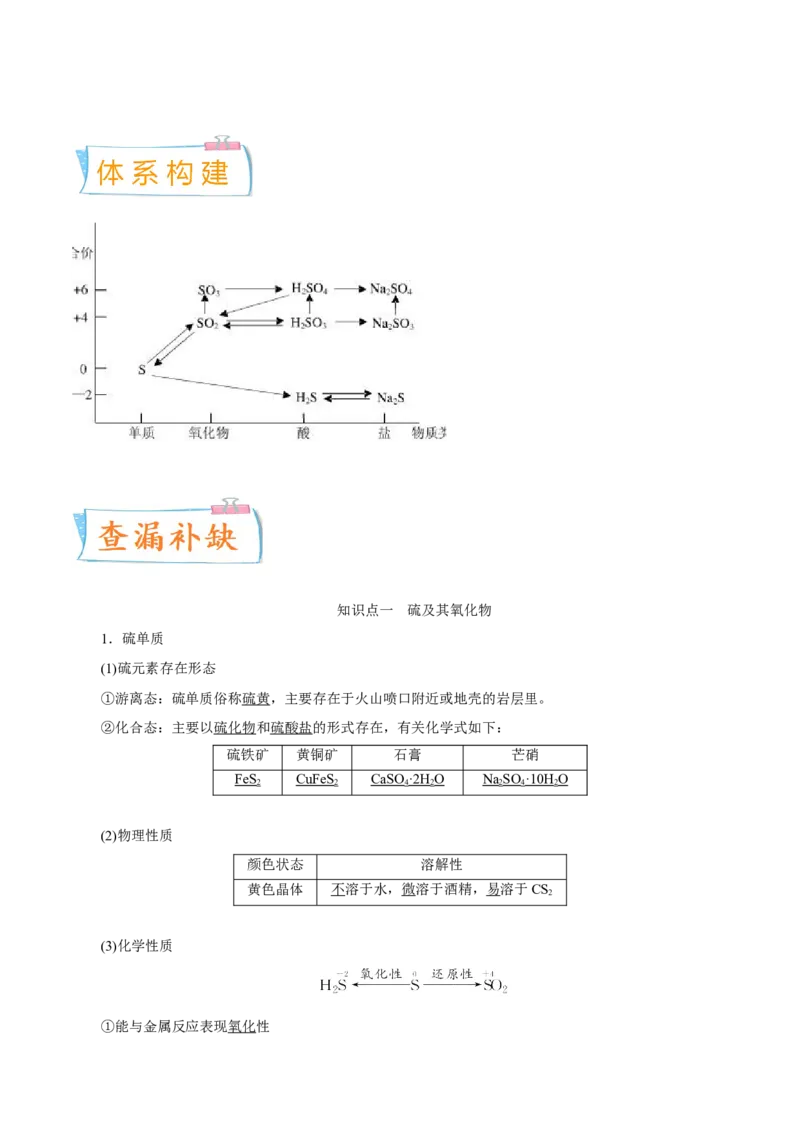
1.理清硫元素的化合价与氧化性、还原性之间的关系
2.掌握硫及其化合物之间的转化规律
(1)相同价态硫的转化是通过与酸、碱反应实现的
如:
②、③、④反应的化学方程式分别为
②HSO +2NaOH===Na SO +2HO;
2 3 2 3 2
③NaSO +HSO ===Na SO +HO+SO ↑;
2 3 2 4 2 4 2 2
④SO +NaSO +HO===2NaHSO 。
2 2 3 2 3
(2)不同价态硫的转化是通过氧化还原反应实现的
当硫元素的化合价升高或降低时,一般升高或降低到其相邻的价态,即台阶式升降,可用下图表示
如:HSSSO ――――――→SO
2 2 3
③、④、⑤反应的化学方程式分别为
③2SO +O2SO ;
2 2 3④S+H=====HS;
2 2
⑤SO +2HS===3S↓+2HO。
2 2 2
[名师点拨] (1)同种元素相邻价态的微粒间不发生氧化还原反应,如 S和HS、S和SO 、SO 和浓硫
2 2 2
酸之间不发生氧化还原反应。
(2)当硫元素的高价态微粒与低价态微粒反应时,一般生成中间价态,如 2NaS+NaSO +
2 2 3
3HSO ===3Na SO +3S↓+3HO。
2 4 2 4 2
1.硫是生物必需的营养元素之一,下列关于自然界中硫循环(如图所示)的说法正确的是( )
A.含硫杆菌及好氧/厌氧菌促进了硫的循环
B.硫循环中硫的化合物均为无机物
C.上述硫循环中硫元素均被氧化
D.烧煤时加石灰石,可减少酸雨和温室气体
2.下列能够确定溶液中一定含有SO的事实是( )
A.取少量试液,加入用盐酸酸化的氯化钡溶液,有白色沉淀生成
B.取少量试液,加入氯化钡溶液,有白色沉淀生成,再加稀硝酸沉淀不消失
C.取少量试液,加入硝酸钡溶液,有白色沉淀生成
D.取少量试液,加入盐酸无明显现象产生,再加入氯化钡溶液,有白色沉淀生成
3.天然气因含有少量HS等气体开采应用受限。T.F菌在酸性溶液中可实现天然气的催化脱硫,其原理如
2
图所示。下列说法不正确的是( )A.该脱硫过程需要不断添加Fe (SO ) 溶液
2 4 3
B.脱硫过程O 间接氧化HS
2 2
C.亚铁是血红蛋白的重要组成成分,FeSO 可用于治疗缺铁性贫血
4
D.《华阳国志》记载“取井火煮之,一斛水得五斗盐”,说明我国古代已利用天然气煮盐
4.已知2FeSO =====Fe O+SO ↑+SO ↑。下列有关操作、装置、原理及对现象的表述正确的是( )
4 2 3 2 3
A.用装置甲高温分解FeSO ,点燃酒精喷灯前应先向装置内通一段时间N
4 2
B.用装置乙可检验分解产生的SO ,现象是石蕊溶液先变红后褪色
2
C.用装置丙可检验分解产生的SO ,现象是产生白色沉淀
3
D.用装置丁可吸收尾气,避免污染环境
5.下列实验操作、现象与结论均正确的是( )
编号 实验操作 实验现象 实验结论
向酸性KMnO 溶液中通入
A 4 紫红色褪去 SO 具有漂白性
SO 2
2
酸性:HS>
2
B 向CuSO 溶液中通入HS 出现黑色沉淀
4 2
HSO
2 4
向碘水溶液中加入CCl ,振 碘在CCl 中的溶解度大于
C 4 上层褪色,下层变紫 4
荡 它在水中的溶解度
向装有蔗糖的烧杯中加入浓
D 出现“黑面包”现象 浓HSO 具有吸水性
HSO 2 4
2 4
1.(江西省九江市2022届第二次高考模拟统一考试)实验室制取下列气体方法可行的是
选项 气体 方法A 氢气 向铁粉中滴加稀硝酸
B 二氧化硫 向亚硫酸钠固体中滴加70%硫酸
C 硫化氢 向硫化铜中滴加稀硫酸
D 二氧化碳 向块状碳酸钙固体中滴加稀硫酸
2.(浙江省绍兴市2022届高三选考科目适应性考试)下列推理合理的是
A.NaCl固体与浓HSO 加热可制HCl, 则NaI固体与浓HSO 加热制HI
2 4 2 4
B.NaO 与CO 反应生成NaCO 和O,则NaO 与SO 反应生成NaSO 和O
2 2 2 2 3 2 2 2 2 2 3 2
C.实验室可利用AlCl 与足量氨水反应来制备Al(OH) ,则也可利用CuCl 与足量氨水反应生成Cu(OH)
3 3 2 2
D.Fe与S反应生成FeS,则Cu与S反应生成Cu S
2
3.(重庆市天星桥中学2021-2022学年高三下学期学业质量调研)实验室中为研究不同物质之间的反应进
行如下实验。下列说法正确的是
A.丙为还原产物,丁为氧化产物
B.上述有4个氧化还原反应
C.每生成标准状况下 气体丙,消耗
D.若 完全反应,转移 个电子( 为阿伏加德罗常数的值)
4.下图是一种综合处理SO 废气的工艺流程。下列说法正确的是( )
2
A.向溶液B中滴加KSCN溶液,溶液可能变为红色
B.溶液B转化为溶液C发生反应的离子方程式为4H++2Fe2++O===2Fe3++2HO
2 2
C.溶液酸性:A>B>C
D.加氧化亚铁可以使溶液C转化为溶液A5.已知2FeSO =====Fe O+SO ↑+SO ↑。下列有关操作、装置、原理及对现象的表述正确的是( )
4 2 3 2 3
A.用装置甲高温分解FeSO ,点燃酒精喷灯前应先向装置内通一段时间N
4 2
B.用装置乙可检验分解产生的SO ,现象是石蕊溶液先变红后褪色
2
C.用装置丙可检验分解产生的SO ,现象是产生白色沉淀
3
D.用装置丁可吸收尾气,避免污染环境
1.(2022·全国乙卷)某白色粉末样品,可能含有 、 、 和 。取少量样品进
行如下实验:
①溶于水,得到无色透明溶液
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
③取②的上层清液,向其中滴加 溶液有沉淀生成。
该样品中确定存在的是
A. B.
C. D.
2.(2022·广东卷)若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实验,下
列分析正确的是A. 与浓硫酸反应,只体现 的酸性
B.a处变红,说明 是酸性氧化物
C.b或c处褪色,均说明 具有漂白性
D.试管底部出现白色固体,说明反应中无 生成
3.【2018浙江高考真题】下列反应中能产生二氧化硫的是
A.氧化铜和稀硫酸反应 B.亚硫酸钠和氧气反应
C.三氧化硫和水反应 D.铜和热的浓硫酸反应
4.【2020天津高考真题】检验下列物所选用的试剂正确的是
待检验物质 所用试剂
A 海水中的碘元素 淀粉溶液
B SO 气体 澄清石灰水
2
C 溶液中的Cu2+ 氨水
D 溶液中的 NaOH溶液,湿润的蓝色石蕊试纸
5.【2020浙江高考真题】100%硫酸吸收 可生成焦硫酸(分子式为 或 )。下列说
法不正确的是( )
A.焦硫酸具有强氧化性
B. 水溶液呈中性
C. 可与碱性氧化物反应生成新盐
D.100%硫酸吸收 生成焦硫酸的变化是化学变化1.【答案】A
【解析】由题图可知,硫酸盐和亚硫酸盐等在含硫杆菌及好氧/厌氧菌作用下缓慢转化为植物中的R SR ,
1 2
促进了硫的循环,故A说法正确;硫循环中硫的化合物存在含硫有机物,故B说法错误;硫循环中硫元素
既存在被氧化的过程,也存在被还原的过程,如含硫杆菌及好氧/厌氧菌将硫酸盐还原为R SR ,故C说法
1 2
错误;烧煤时加石灰石,分解产生的CaO可以吸收SO ,但分解的同时会产生温室气体CO ,故D说法错
2 2
误。
2.【答案】D
【解析】SO的检验,先用稀盐酸酸化,直到没有现象为止,排除 Ag+、CO等的干扰,再加入氯化钡溶液,
看是否生成白色沉淀。直接加入稀盐酸酸化的氯化钡溶液,不能排除Ag+的干扰,A错误;先加氯化钡不
能排除Ag+的干扰,B错误;加入硝酸钡,不能排除碳酸根、亚硫酸根等的干扰,C错误;加入盐酸无明
显现象,排除Ag+等的干扰,再加入氯化钡有白色沉淀,说明有SO,D正确。
3.【答案】A
【解析】T.F菌在酸性溶液中可实现天然气的催化脱硫,Fe (SO ) 氧化硫化氢,自身被还原成硫酸亚铁,
2 4 3
硫酸亚铁被氧气氧化成硫酸铁,Fe (SO ) 可视为催化剂,该脱硫过程不需要不断添加Fe (SO ) 溶液,A错
2 4 3 2 4 3
误;脱硫过程:Fe (SO ) 氧化硫化氢,自身被还原成硫酸亚铁,硫酸亚铁被氧气氧化成硫酸铁,脱硫过程
2 4 3
O 间接氧化HS,B正确;亚铁是血红蛋白的重要组成成分,起着向人体组织传送 O 的作用,若缺铁就可
2 2 2
能出现缺铁性贫血,需补充一定量的亚铁离子,C正确;天然气的主要成分为甲烷,甲烷燃烧放出热量,
井火为天然气燃烧出现的火焰,故说明我国古代已利用天然气煮盐,D正确。
4.【答案】A
【解析】A项,点燃酒精喷灯前应先向装置内通一段时间N ,排除装置中的空气,避免空气中氧气的干扰,
2
正确;B项,装置乙不能检验分解产生的SO ,产物中有SO 会对SO 的检验造成干扰,并且SO 只能使石
2 3 2 2
蕊溶液变红,错误;C项,SO 易溶于水,当混合气体经过乙时,SO 会被吸收,所以要想检验SO ,应该
3 3 3
把乙和丙的位置互换,错误;D项,装置丁中应该用饱和NaSO 溶液,错误。
2 3
5.【答案】C
【解析】向酸性 KMnO 溶液中通入 SO ,紫红色褪去,体现 SO 的还原性,故 A 错误;酸性:
4 2 2
HS