文档内容
考向 10 氯及其化合物
【2022浙江卷1月】下列说法不正确的是
A.镁合金密度较小、强度较大,可用于制造飞机部件
B.还原铁粉可用作食品干燥剂
C.氯气、臭氧、二氧化氯都可用于饮用水的消毒
D.油脂是热值最高的营养物质
【答案】B
【详解】
A.金属镁的密度较小,镁合金的强度高、机械性能好,是制造汽车、飞机、火箭的重要材料,故A正确;
B.还原铁粉能吸收氧气,可用作食品脱氧剂,故B错误;
C.氯气、臭氧、二氧化氯都具有强氧化性,能杀菌消毒,都可用于饮用水的消毒,故C正确;
D.油脂在代谢中可以提供的能量比糖类和蛋白质约高一倍,油脂是热值最高的营养物质,故D正确 ;
选B。知识点一 氯及其化合物的性质及应用
1.氯气的性质
(1)物理性质
颜色状态 气味 密度 毒性 溶解性(25 ℃) 特性
黄绿色 强烈刺激 比空 1体积水溶解
有毒 易液化
气体 性气味 气大 约2体积氯气
[名师点拨] 实验室里闻有毒气体及未知气体气味的方法是用手在瓶口轻轻扇动,使极少量的气体飘进鼻
孔即可。
(2)化学性质
①能与金属反应:与变价金属反应生成高价金属氯化物。
与铁反应: 2Fe + 3Cl ===== 2FeCl 。
2 3
与铜反应: Cu + Cl ===== CuCl 。
2 2
②能与非金属反应
与H 反应:H + C l ===== 2HCl 。
2 2 2
③能与水或碱反应(填写化学方程式)
与水反应 Cl + H OHCl + HClO
2 2
与烧碱溶液反应 Cl + 2NaOH == =NaC l + NaClO + H O
2 2
④能与某些还原性物质反应(书写离子方程式)
与碘化钾溶液 2I - + Cl == =I + 2C l -
2 2
与SO 水溶液 Cl + SO + 2H O == =4H + + 2Cl - + SO
2 2 2 2
与FeCl 溶液 2Fe 2 + + Cl == =2Fe 3 + + 2Cl -
2 2
2.氯水的成分及性质
氯气能溶于水,氯气的水溶液称为氯水,溶于水的氯气只有少量与水反应。(1)氯水中存在三种平衡关系:
①Cl+HOHCl+HClO;
2 2
②HClOH++ClO-;
③HOH++OH-。
2
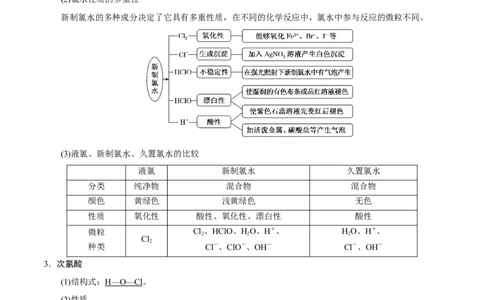
(2)氯水性质的多重性
新制氯水的多种成分决定了它具有多重性质,在不同的化学反应中,氯水中参与反应的微粒不同。
(3)液氯、新制氯水、久置氯水的比较
液氯 新制氯水 久置氯水
分类 纯净物 混合物 混合物
颜色 黄绿色 浅黄绿色 无色
性质 氧化性 酸性、氧化性、漂白性 酸性
微粒 Cl、HClO、HO、H+、 HO、H+、
2 2 2
Cl
2
种类 Cl-、ClO-、OH- Cl-、OH-
3.次氯酸
(1)结构式:H—O—Cl。
(2)性质
①弱酸性:一元弱酸,酸性比HCO 还弱。
2 3
②不稳定性:见光易分解, 2HClO ===== 2HCl + O ↑,因此次氯酸要现用现配,保存在棕色试剂瓶中。
2
③强氧化性:具有漂白、杀菌能力,用作消毒剂、漂白剂,可以使有色布条、品红溶液等褪色。
[名师点拨] (1)HClO和ClO-都具有强氧化性,无论酸性、碱性条件下都可以和亚铁盐、碘化物、硫
化物等发生氧化还原反应。
(2)向NaClO溶液中通入CO(不论是少量还是过量),均生成HCO和HClO。原因是酸性:HCO >
2 2 3
HClO>HCO。4.次氯酸盐
(1)84消毒液
有效成分为NaClO,它与洁厕灵(主要成分为盐酸)混合会立即产生氯气,其离子方程式是 ClO - + Cl -
+ 2H + == =C l ↑ + H O。
2 2
(2)漂白粉
知识点二 氯气的实验室制法
1.制取原理
实验室通常用强氧化剂(如KMnO 、KCr O 、KClO 、MnO 等)氧化浓盐酸制取氯气。用 MnO 制取
4 2 2 7 3 2 2
Cl 的化学方程式:MnO + 4HCl ( 浓 ) ===== MnC l + C l ↑ + 2H O。
2 2 2 2 2
2.制取过程
3.实验装置[名师点拨] 氯气制备的“四注意”
(1)反应物的选择:必须用浓盐酸,稀盐酸与 MnO 不反应,且随着反应的进行,浓盐酸变为稀盐酸时,
2
反应停止,故盐酸中的HCl不可能全部参加反应。
(2)加热温度:不宜过高,以减少HCl挥发。
(3)实验结束后,先使反应停止并排出残留的Cl 后,再拆卸装置,避免污染空气。
2
(4)尾气吸收时,用NaOH溶液吸收Cl,不能用澄清石灰水吸收,因为澄清石灰水中含Ca(OH) 的量少,
2 2
吸收不完全。
4.工业制法
电解饱和食盐水:2NaCl+2HO=====H↑+2NaOH+Cl↑。
2 2 2
电解熔融NaCl:2NaCl(熔融)=====2Na+Cl↑。
2
知识点三 卤素的性质 卤素离子的检验
一、卤素单质的提取
1.氯的提取——氯碱工业
海水―→粗盐――→饱和食盐水――→
化学方程式为 2NaCl + 2H O ===== H ↑ + 2NaOH + Cl ↑。
2 2 2
2.海水提取溴
(1)流程
(2)发生反应的化学方程式
① 2NaBr + Cl == =Br + 2NaC l;
2 2
②Br + SO + 2H O == =2HBr + H SO ;
2 2 2 2 4
③ 2HBr + Cl == =Br + 2HC l。
2 2
3.海带中提取碘(1)流程
(2)发生反应的离子方程式Cl + 2 I - == =2C l - + I。
2 2
二、卤素单质的性质
1.溴、碘单质物理性质的比较
物质
Br I
2 2
性质
颜色 深红棕色 紫黑色
状态 液体 固体
溶 水中 溶解度不大 溶解度不大
解
性 有机溶剂中 易溶 易溶
特性 易挥发、有毒 易升华
2.氯、溴、碘单质化学性质的比较
(1)能与碱溶液反应:如与NaOH溶液反应的化学方程式为
2NaOH + X == =NaX + NaXO + H O(X=Cl、Br、I)。
2 2
(2)氧化性
①都能与金属反应生成金属卤化物,如与钠反应的化学方程式为 2Na + X ===== 2NaX (X=Cl、Br、
2
I)。
②氯、溴、碘单质的氧化性强弱顺序是Cl>Br >I ,阴离子的还原性强弱顺序是Cl-