文档内容
第四单元 物质构成的奥秘
课题 1 原子的构成
(第一、二板块你应尽力完成,第三板块则由你决定取舍)
第一板块 本课题你学到多少基础知识?不妨检测一下。
1.下列关于原子的叙述,错误的是( )
A.原子是化学变化中最小的粒子 B.原子是构成物质的一种粒子
C.原子一定由质子、中子和电子构成 D.原子的质量主要集中在原子核上
2.原子显电中性的原因是( )
A.构成原子的各种粒子均不带电 B.原子核外电子数大于核内质子数
C.核内质子数等于中子数 D.原子核所带电量和核外电子的电量相等,但电性相反
3.铁的相对原子质量为56,表示的意义是( )
A.表示铁原子的相对原子质量为56g B.表示一个铁原子的质量为56g
C.表示铁原子的原子核内有56个质子 D.表示一个铁原子质量是一个碳原子质量的1/12的56倍。
4. 在原子中,不带电荷的粒子是( )
A.质子 B.中子 C.电子 D.原子核
5.下列物质不是由原子直接构成的是( )
A.氧气 B.氩气 C.黄金 D.硫磺
6.⑴已知在原子中“相对原子质量≈质子数 + 中子数”。请填写下面表格
原子种类 质子数 中子数 核外电子数 相对原子质量
氢(H) 1 0 1
氧(O) 8 8
钠(Na) 11 23
⑵根据上表的信息,计算一个水分子所含总质子数为 。
7. 某些花岗石材中含有对人体有害的放射性元素——氡,氡原子质子数为86,中子数为 136,这种氡原
子核外电子数为 ,核电荷数为 ,相对原子质量为 。已知一个碳-12原子
的质量为1.993×10-27kg,则氡原子的质量为 。
第二板块 你能把所学的知识用来解决下面的问题吗?祝你成功!
8.1993年8月,我国科学家利用超高真空扫描隧道显微镜,在一块晶体硅(Si)的表面上通过探针的作用
搬走原子,写下了“中国”两个字。下列说法中不正确的是( )
A .上述操作中发生了化学变化 B.上述操作发生了物理变化
C.这两个汉字是目前世界上最小的汉字 D.这标志着我国科学家进入操纵原子的阶段
9.化学上称“原子是化学变化中的最小粒子”的根据是( )
A.原子质量小 B.原子是构成物质的最小粒子
C.原子体积小 D.原子在化学变化前后的种类、数目不变
10.下列各种原子的质量各1g,所含原子个数最多的是( )
A.氧原子 B.铁原子 C.氢原子 D.碳原子
11. 在分子、原子、质子、中子、电子、原子核这些粒子中:
(1)能直接构成物质的粒子有 ;(2)能保持物质的化学性质的有 ;
(3)显示电中性的粒子有 ;(4)带正电荷的有 ;
(5)带负电荷的有 ;(6)质量最小的粒子是 ;
(7)参加化学反应时,一定发生变化的是 ;(8)在同一原子里数目相等的是 ;
(9)质量与原子质量相近的是 ;(10)原子中可以不含 。九年级化学练习册(上册) 2(3)
12. 人们揭示原子的结构的奥秘,经历了漫长的探究过程。自 1897年汤姆生发现电子并提出类似“西
瓜”的原子模型,1911年著名物理学家卢瑟福等人为探索原子的内部结构又进行了下面的实验。他们在用
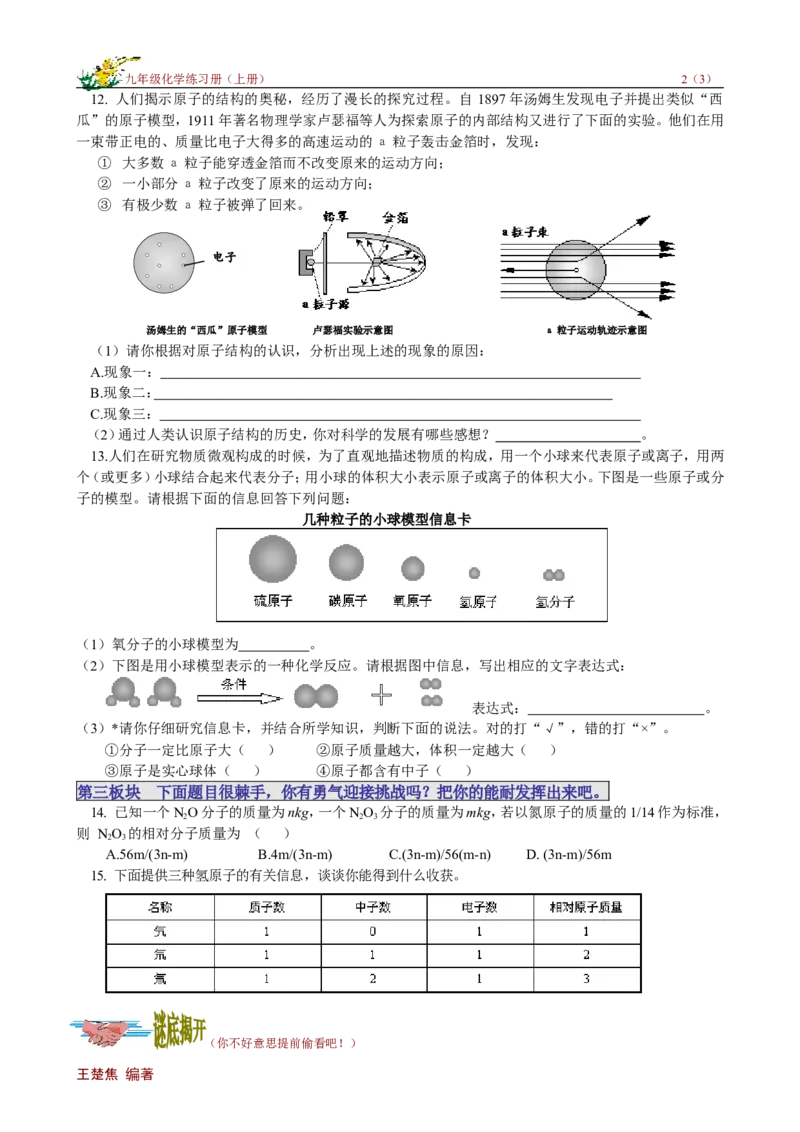
一束带正电的、质量比电子大得多的高速运动的а粒子轰击金箔时,发现:
① 大多数а粒子能穿透金箔而不改变原来的运动方向;
② 一小部分а粒子改变了原来的运动方向;
③ 有极少数а粒子被弹了回来。
电子
汤姆生的“西瓜”原子模型 卢瑟福实验示意图 а粒子运动轨迹示意图
(1)请你根据对原子结构的认识,分析出现上述的现象的原因:
A.现象一:
B.现象二:
C.现象三:
(2)通过人类认识原子结构的历史,你对科学的发展有哪些感想? 。
13.人们在研究物质微观构成的时候,为了直观地描述物质的构成,用一个小球来代表原子或离子,用两
个(或更多)小球结合起来代表分子;用小球的体积大小表示原子或离子的体积大小。下图是一些原子或分
子的模型。请根据下面的信息回答下列问题:
几种粒子的小球模型信息卡
(1)氧分子的小球模型为 。
(2)下图是用小球模型表示的一种化学反应。请根据图中信息,写出相应的文字表达式:
表达式: 。
(3)*请你仔细研究信息卡,并结合所学知识,判断下面的说法。对的打“√”,错的打“×”。
①分子一定比原子大( ) ②原子质量越大,体积一定越大( )
③原子是实心球体( ) ④原子都含有中子( )
第三板块 下面题目很棘手,你有勇气迎接挑战吗?把你的能耐发挥出来吧。
14. 已知一个NO分子的质量为nkg,一个NO 分子的质量为mkg,若以氮原子的质量的1/14作为标准,
2 2 3
则 NO 的相对分子质量为 ( )
2 3
A.56m/(3n-m) B.4m/(3n-m) C.(3n-m)/56(m-n) D. (3n-m)/56m
15. 下面提供三种氢原子的有关信息,谈谈你能得到什么收获。
(你不好意思提前偷看吧!)
王楚焦 编著第一板块
1.C 2.D 3.D 4.B 5.A 6.⑴H:1;O:8、16;Na:11、12 ⑵18个 7. 86、86、3.687×10-26㎏
第二板块
8.A 9.D 10.C 11(. 1)分子、原子;(2)分子、原子;(3)分子、原子、中子;(4)质子、原子核;(5)电子;(6)电子;(7)
分子;(8)质子和电子;(9)原子核;(10)中子
12.(1)现象一:大多数а粒子没有受到金原子的原子核的排斥力的作用;
现象二:少数а粒子受到金原子的原子核的排斥力的作用;
现象三:金原子核的体积相对原子的体积小得多,故此只有极少数а粒子与金原子核正面碰撞而被弹回。
(2)科学是不断发展的;科学发展的道路是曲折而漫长的;任何一种科学理论都有它的局限性。
13.(1) (2)水Com氧气+ 氢气 ; (3)①× ②× ③× ④×
bin
第三板块
14.A 15.参考收获:(1)不是所有的原子都含中子;(2)相对原子质量 = 质子数 + 中子数; (3)在原子中,质子数等于电子
数;(4)“同种原子”和“同类原子”的意义不同。“同类原子”要求原子的质子数相等,而“同种原子”不但要求质子数相等,
还要求中子数也相等。
(下面文字不列入考试内容,能让你在放松片刻 的过程中,不知不觉开阔视野)
原子结构的发现
原子“绝对不可再分”的观点在9世纪末受到了新的科学发现的冲击。1879年,英国著名的物理学家
和化学家克鲁克斯(William Crookes,1832—1919)在高真空放电管中发现了一种带负电荷的粒子流——
“阴极射线”。1879年,英国的剑桥大学物理学家汤姆生利用阴极射线能被电场和磁场联合偏转的作用,
测定了这种粒子的荷质比(即电荷和质量之比)。实验表明,不论电极用什么材料制成和在阴极射线管中充
以什么样的气体,生成带负电的粒子其荷质比都是相同的,说明它是原子的共同组成部分,称之为“电子”。
1903年,电子的发现者汤姆生提出了一个原子的“葡萄干面包”模型,认为电子嵌在原子中,如同葡萄干
铅在面包中一样。1909年,英国物理学家卢瑟福(E.Rutherford,1871-1939)用一束高能的α粒子(带正电
荷的氦离子)留轰击金箔时发现,绝大多α粒子几乎不受阻碍而直接通过金箔,说明原子的内部空旷;但也
有极少数(约万分之几)α粒子穿过金箔后发生偏转,个别α粒子的偏转程度较大,甚至被反弹回来,卢瑟
福设想,这是由于原子中存在一个几乎集中了原子全部质量并带正电荷的极小的核,是它对α粒子产生了
静电排斥作用。1911年,卢瑟福提出了原子的结构的“核式模型”:每个原子中心有一个极小的原子核,几
乎集中了原子的全部质量并带有Z个单位的正电荷,核外有Z个电子绕核旋转,电子绕核旋转如同行星绕
日运行,因此这一模型也称为“行星式模型”。后来对原子光谱的深入研究和量子力学的出现,才逐步形成
了现代的结构理论。