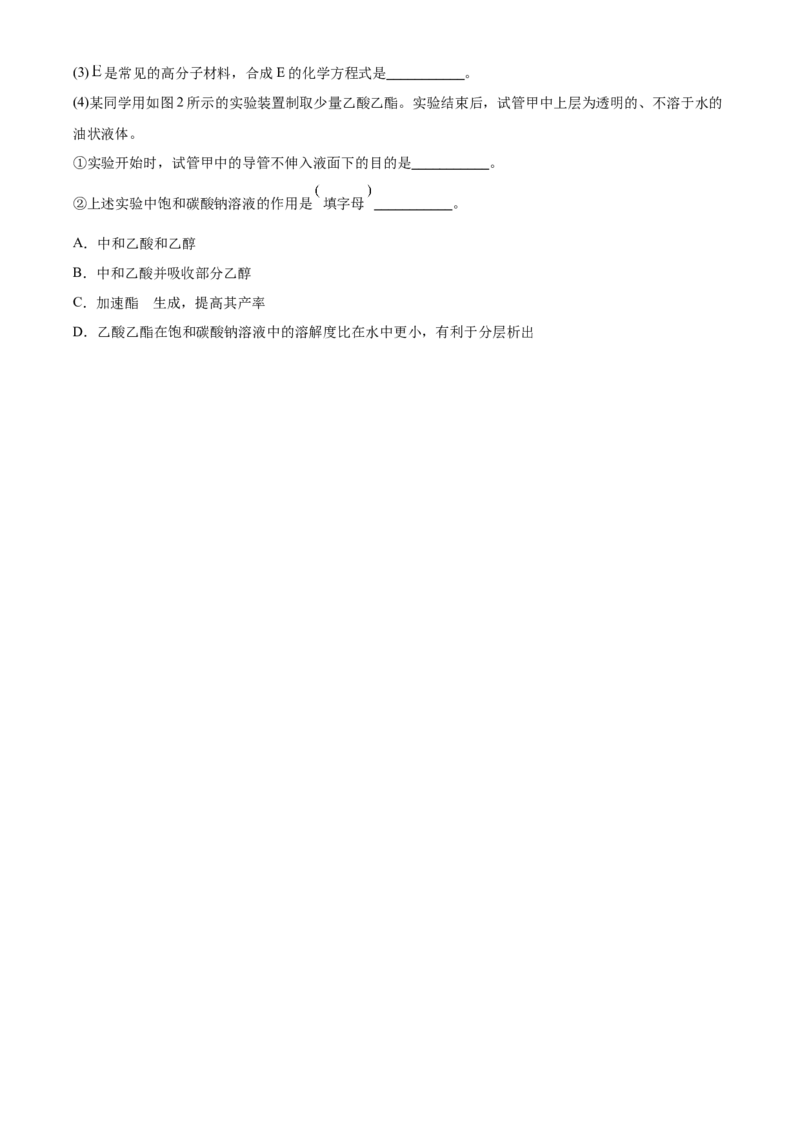文档内容
河婆中学 2020 2021 学年度第二学期期末考试
~
高一化学试题
注意事项:1、本试卷分为选择题和非选择题两部分,满分100分,考试时间75分钟。
2、题目在规定时间内完成,答案必须答在答题卷上,否则不给分;
3、可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Fe 56 Cl 35.5 Al 27
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题
4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 古诗词是古人为我们留下的宝贵精神财富,下列诗句不涉及氧化还原反应的是
A. 野火烧不尽,春风吹又生 B. 春蚕到死丝方尽,蜡炬成灰泪始干
C. 粉身碎骨浑不怕,要留清白在人间 D. 爆竹声中一岁除,春风送暖入屠苏
2. 周杰伦在歌曲《青花瓷》中唱到“帘外芭蕉惹骤雨,门环惹铜绿”,其中的“铜绿”即是铜锈,它的化
学成分是Cu (OH) CO(碱式碳酸铜)。铜在潮湿的空气中生锈的化学反应为:2Cu+O+CO+
2 2 3 2 2
HO=Cu (OH) CO。下列有关该反应的说法正确的是
2 2 2 3
A. 该反应不是氧化还原反应
B. 该反应中氧元素和碳元素化合价发生变化,所以是氧化还原反应
C. 该反应中1mol铜参加反应失去2mol电子,同时消耗1mol O
2
D. 该反应是氧化还原反应,变价的只有两种元素
3. 下列变化中,气体被还原的是
A. 二氧化碳使NaO 固体变白 B. 氯气使KBr溶液变黄
2 2
C. 乙烯使Br 的四氯化碳溶液褪色 D. 氨气使AlCl 溶液产生白色沉淀
2 3
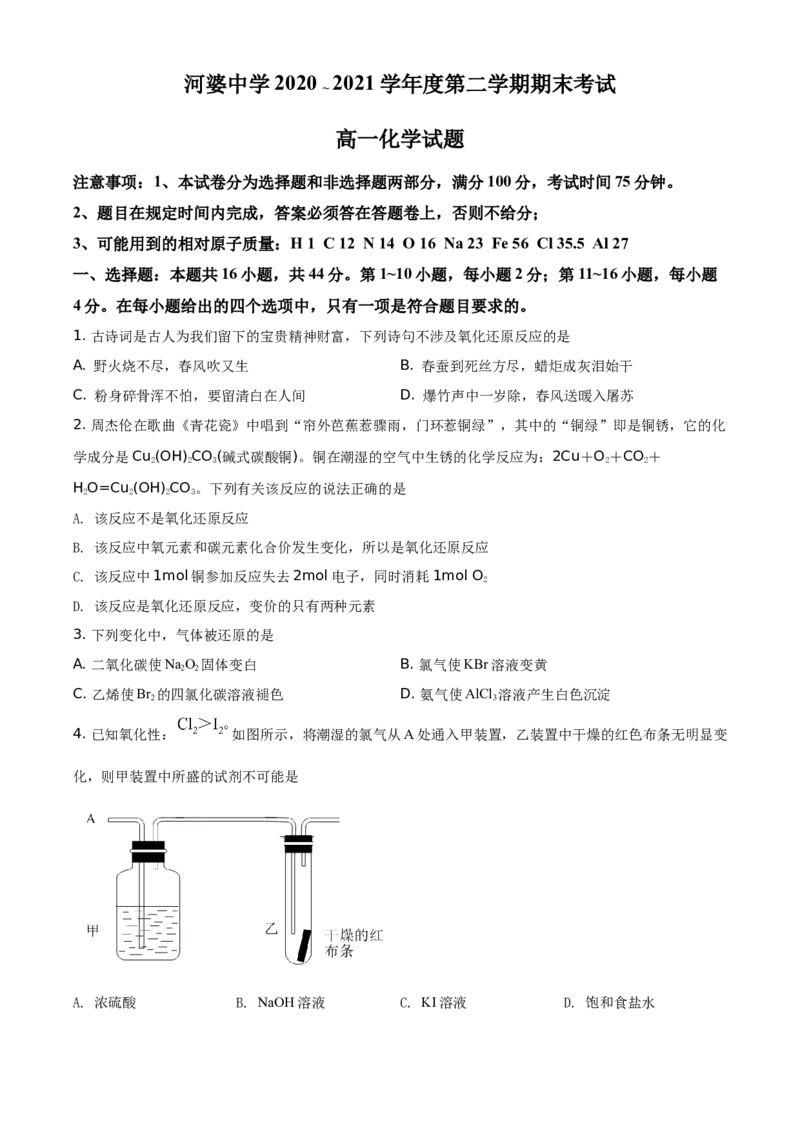
4. 已知氧化性: 如图所示,将潮湿的氯气从A处通入甲装置,乙装置中干燥的红色布条无明显变
化,则甲装置中所盛的试剂不可能是
A. 浓硫酸 B. NaOH溶液 C. KI溶液 D. 饱和食盐水5. 设N 为阿伏伽德罗常数的值,下列说法正确的是( )
A
A. 32克18O,中含有的中子数为10N
8 2 A
B. 25℃时,1L pH=12的Ba(OH) 溶液中OH-数目为0.02N
2 A
C. 标况下,224L Cl 与足量HO反应转移的电子数为0.1N
2 2 A
D. 4.6gNa与足量O 充分反应后的产物中含离子数目为0.3N
2 A
6. 下列反应的离子方程式书写正确的是
A. 向NaSiO 溶液中滴加稀盐酸:NaSiO+2H+=H SiO↓+2Na+
2 3 2 3 2 3
B. NO 通入水中制硝酸:2NO +H O=2H++ +NO
2 2 2
C. HNO 溶液与氨水反应:H++OH-=H O
3 2
D. 铜与浓硝酸的反应:Cu+4H++2 =Cu2++2NO↑+2H O
2 2
7. 下列能量转化过程与氧化还原反应无关的是
A. 硅太阳能电池工作时,光能转化成电能
B. 锂离子电池放电时,化学能转化成电能
C. 熔融电解质通电时,电能转化成化学能
D. 葡萄糖为人类生命活动提供能量时,化学能转化成热能
8. 不能用组成元素的单质直接反应得到的物质是
A. NO B. FeCl C. SO D. NH
2 2 3
9. 短周期金属元素甲~戊在元素周期表中的相对位置如右表所示,下面判断正确的是
A. 原子半径:丙<丁<戊 B. 金属性:甲>丙
C. 氢氧化物碱性:丙>丁>戊 D. 最外层电子数:甲>乙
10. 下列反应既属于放热反应,又属于非氧化还原反应的是
A. 锌与稀盐酸反应制取氢气 B. 灼热的炭与二氧化碳反应
C. 与盐酸的中和反应 D. 铝热反应
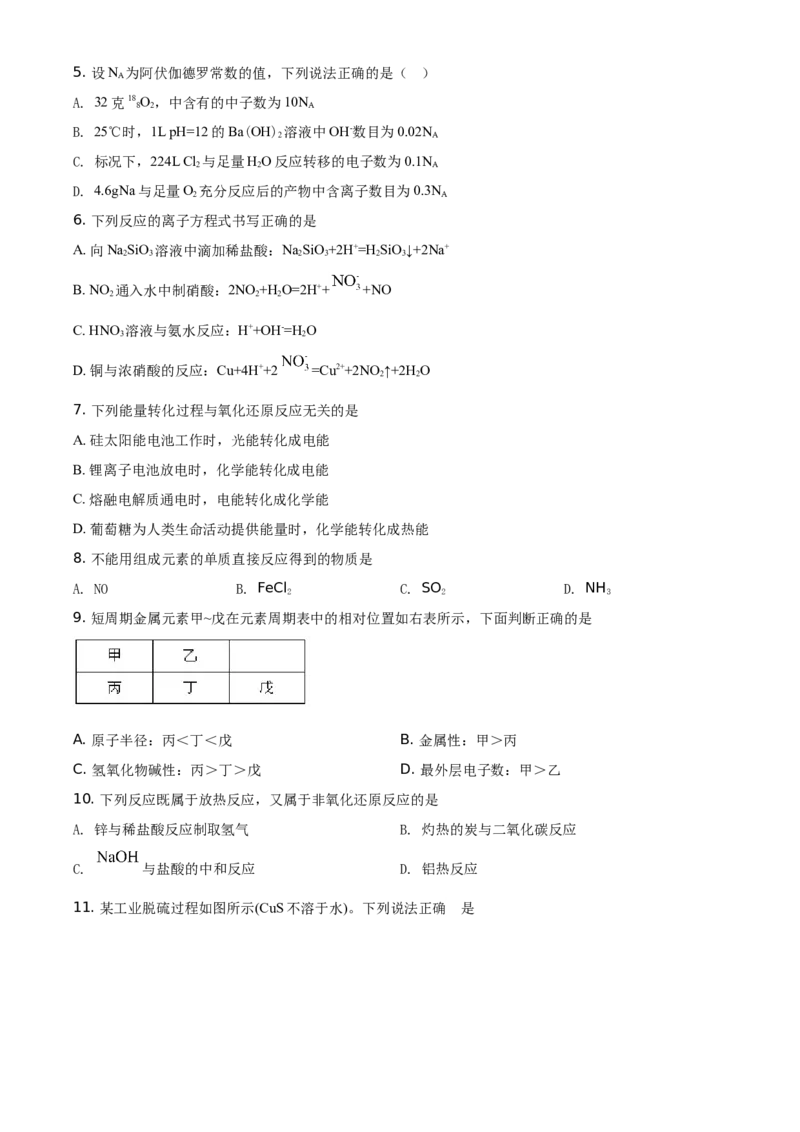
11. 某工业脱硫过程如图所示(CuS不溶于水)。下列说法正确 的是.
A 过程①发生复分解反应,由强酸反应得到弱酸
B. 过程②中,发生反应的离子方程式为:
C. 过程③中,每有11.2L 参加反应转移电子数2
D. 脱硫过程总反应为
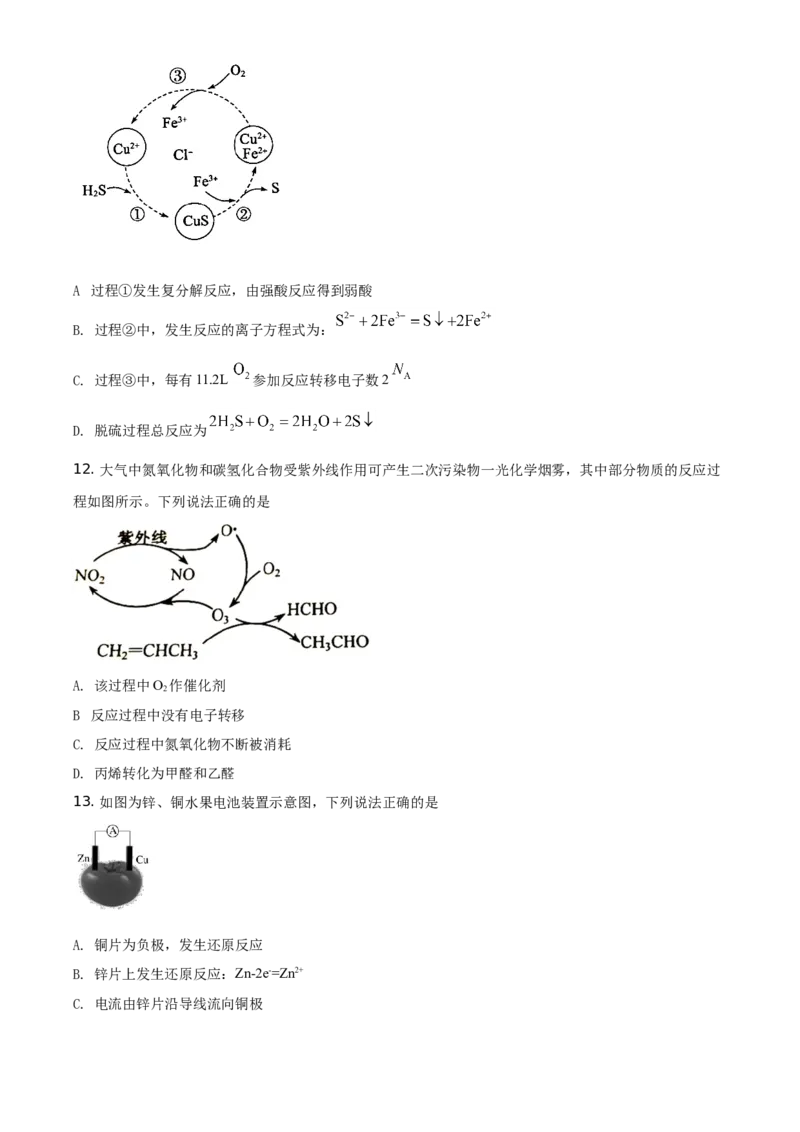
12. 大气中氮氧化物和碳氢化合物受紫外线作用可产生二次污染物一光化学烟雾,其中部分物质的反应过
程如图所示。下列说法正确的是
A. 该过程中O 作催化剂
2
.
B 反应过程中没有电子转移
C. 反应过程中氮氧化物不断被消耗
D. 丙烯转化为甲醛和乙醛
13. 如图为锌、铜水果电池装置示意图,下列说法正确的是
A. 铜片为负极,发生还原反应
B. 锌片上发生还原反应:Zn-2e-=Zn2+
C. 电流由锌片沿导线流向铜极D. 电子由锌片沿导线流向铜极
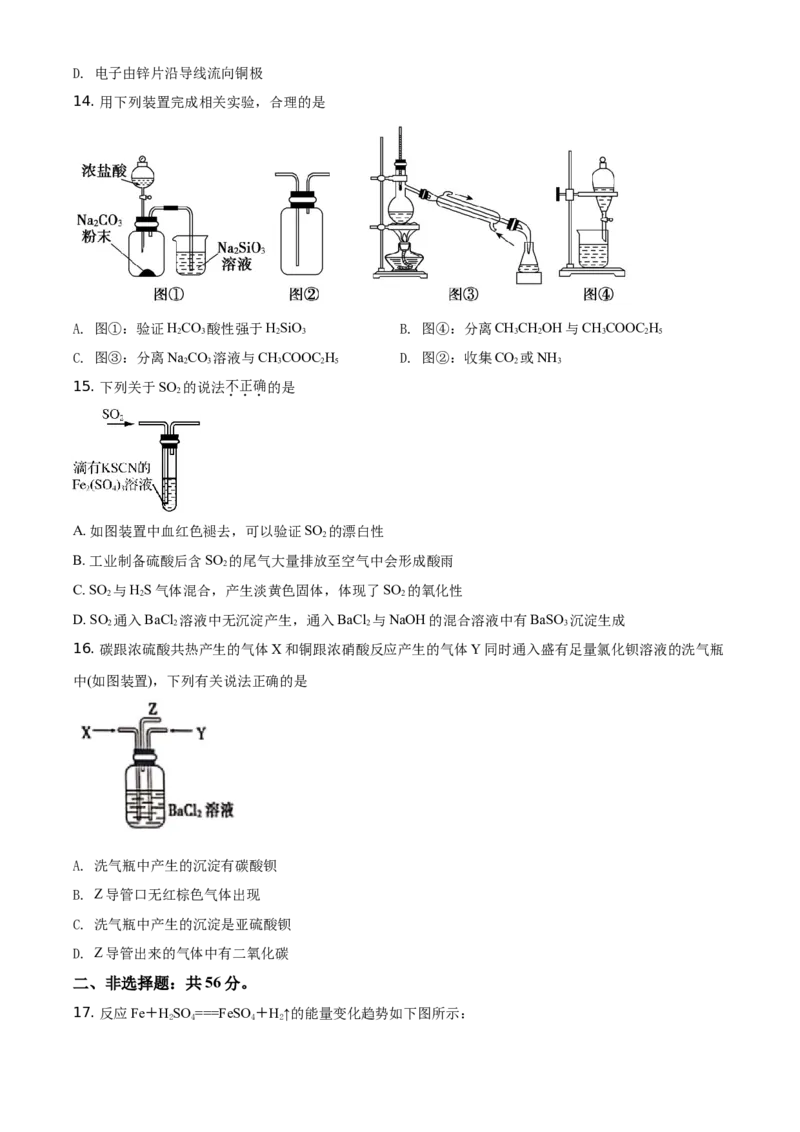
14. 用下列装置完成相关实验,合理的是
A. 图①:验证HCO 酸性强于HSiO B. 图④:分离CHCHOH与CHCOOC H
2 3 2 3 3 2 3 2 5
C. 图③:分离NaCO 溶液与CHCOOC H D. 图②:收集CO 或NH
2 3 3 2 5 2 3
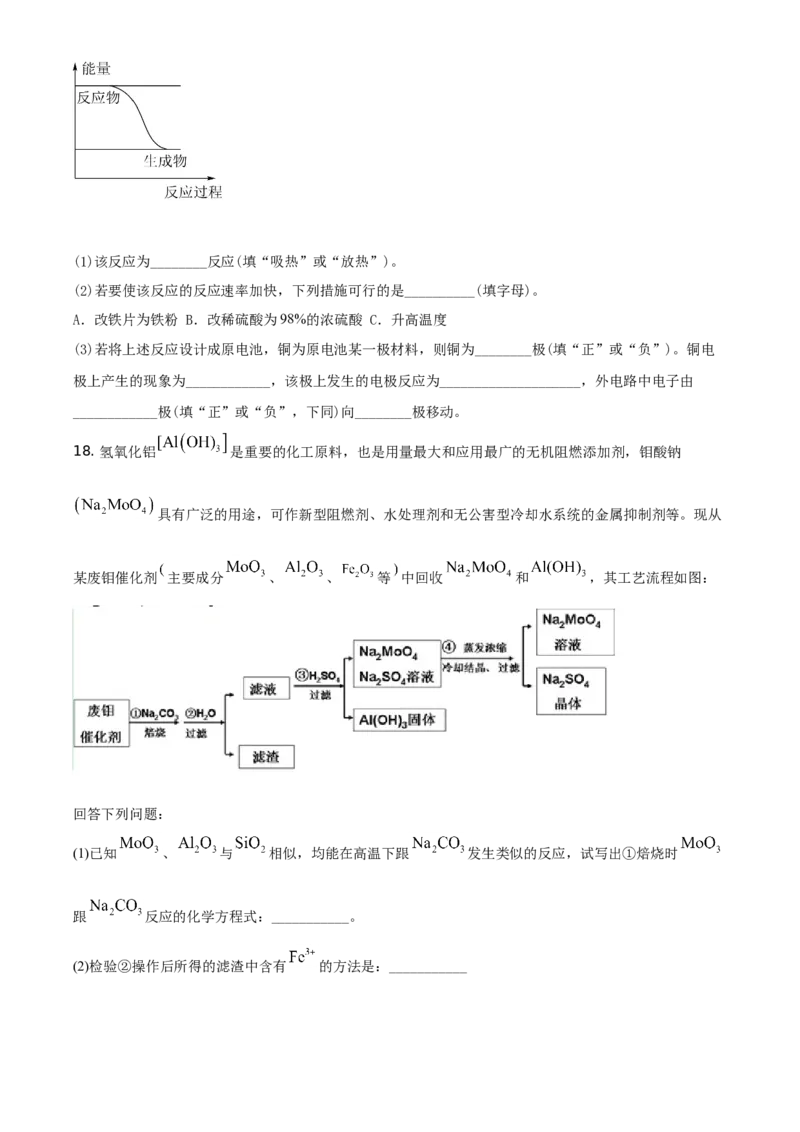
15. 下列关于SO 的说法不正确的是
2
A. 如图装置中血红色褪去,可以验证SO 的漂白性
2
B. 工业制备硫酸后含SO 的尾气大量排放至空气中会形成酸雨
2
C. SO 与HS气体混合,产生淡黄色固体,体现了SO 的氧化性
2 2 2
D. SO 通入BaCl 溶液中无沉淀产生,通入BaCl 与NaOH的混合溶液中有BaSO 沉淀生成
2 2 2 3
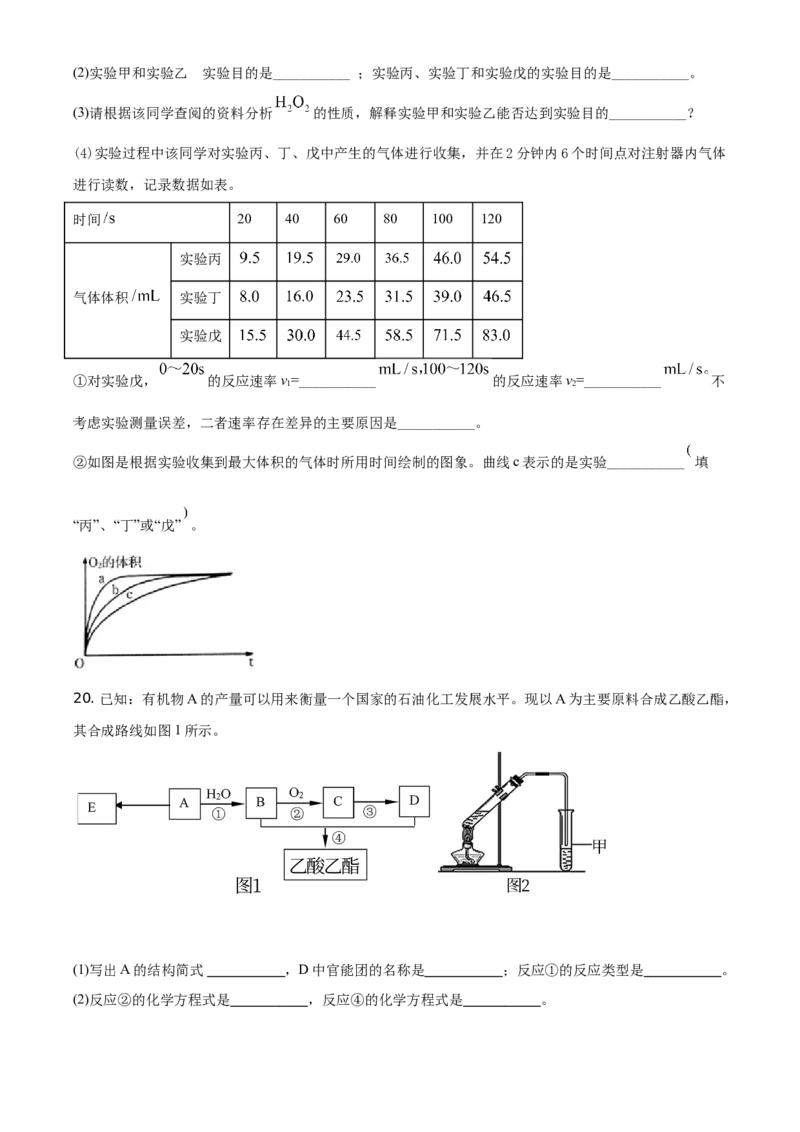
16. 碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶
中(如图装置),下列有关说法正确的是
A. 洗气瓶中产生的沉淀有碳酸钡
B. Z导管口无红棕色气体出现
C. 洗气瓶中产生的沉淀是亚硫酸钡
D. Z导管出来的气体中有二氧化碳
二、非选择题:共56分。
17. 反应Fe+HSO ===FeSO+H↑的能量变化趋势如下图所示:
2 4 4 2(1)该反应为________反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是__________(填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为________极(填“正”或“负”)。铜电
极上产生的现象为____________,该极上发生的电极反应为____________________,外电路中电子由
____________极(填“正”或“负”,下同)向________极移动。
18. 氢氧化铝 是重要的化工原料,也是用量最大和应用最广的无机阻燃添加剂,钼酸钠
具有广泛的用途,可作新型阻燃剂、水处理剂和无公害型冷却水系统的金属抑制剂等。现从
某废钼催化剂 主要成分 、 、 等 中回收 和 ,其工艺流程如图:
回答下列问题:
(1)已知 、 与 相似,均能在高温下跟 发生类似的反应,试写出①焙烧时
跟 反应的化学方程式:___________。
(2)检验②操作后所得的滤渣中含有 的方法是:___________(3)第③步操作中加入 需要适量,可以通过测定溶液___________来控制 的用量。该步操作
中制备 的离子方程式为___________
(4)从题目信息可知,下图曲线 ___________ 填序号 为 的溶解度曲线。
(5)利用铝热反应可以回收金属钼。将所得钼酸钠溶液用酸处理得到沉淀,再加热可得 。写出
发生铝热反应的化学方程式:___________
19. 某同学学习了化学反应速率后,联想到曾用 制备氧气,于是设计了下面的实验方案并进行实验
探究。
实验编号 反应物 催化剂
甲 试管中加入3mL 溶液和3滴蒸馏水 无
乙 试管中加入3mL 溶液和3滴蒸馏水 无
丙 试管中加入3mL 溶液和3滴蒸馏水 1mL 溶液
丁 试管中加入3mL 溶液和3滴稀盐酸溶液 1mL 溶液
戊 试管中加入3mL 溶液和3滴NaOH溶液 1mL 溶液
【查阅资料】过氧化氢 ,其水溶液俗称双氧水,常温下是一种无色液体,性质比较稳定。在加热
的条件下,它能分解生成氧气。研究表明,将新制的 的 溶液加热到 时就有氧气放出,加热
到 时就有较多氧气产生。
(1)上述实验发生反应的化学方程式为___________。(2)实验甲和实验乙 的实验目的是___________ ;实验丙、实验丁和实验戊的实验目的是___________。
(3)请根据该同学查阅的资料分析 的性质,解释实验甲和实验乙能否达到实验目的___________?
(4)实验过程中该同学对实验丙、丁、戊中产生的气体进行收集,并在2分钟内6个时间点对注射器内气体
进行读数,记录数据如表。
时间 20 40 60 80 100 120
实验丙
气体体积 实验丁
实验戊
①对实验戊, 的反应速率v=___________ 的反应速率v=___________ 不
1 2
考虑实验测量误差,二者速率存在差异的主要原因是___________。
②如图是根据实验收集到最大体积的气体时所用时间绘制的图象。曲线c表示的是实验___________ 填
“丙”、“丁”或“戊” 。
20. 已知:有机物A的产量可以用来衡量一个国家的石油化工发展水平。现以A为主要原料合成乙酸乙酯,
其合成路线如图1所示。
(1)写出A的结构简式 ___________,D中官能团的名称是___________;反应①的反应类型是___________。
(2)反应②的化学方程式是___________,反应④的化学方程式是___________。(3) 是常见的高分子材料,合成E的化学方程式是___________。
(4)某同学用如图2所示的实验装置制取少量乙酸乙酯。实验结束后,试管甲中上层为透明的、不溶于水的
油状液体。
①实验开始时,试管甲中的导管不伸入液面下的目的是___________。
②上述实验中饱和碳酸钠溶液的作用是 填字母 ___________。
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.加速酯 的生成,提高其产率
D.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出