文档内容
考向 13 碳及其化合物 无机非金属材料
【2022浙江卷1月】关于反应4CO+SiH 4CO+2HO+SiO,下列说法正确的是
2 4 2 2
A.CO是氧化产物 B.SiH 发生还原反应
4
C.氧化剂与还原剂的物质的量之比为1∶4 D.生成1molSiO 时,转移8mol电子
2
【答案】D
【详解】
A.根据反应方程式,碳元素的化合价由+4价降为+2价,故CO为还原产物,A错误;
B.硅元素化合价由-4价升为+4价,故SiH 发生氧化反应,B错误;
4
C.反应中氧化剂为二氧化碳,还原剂为SiH,,则氧化剂与还原剂的物质的量之比为4:1,C错误;
4
D.根据反应方程式可知,Si元素的化合价由-4价升高至+4价,因此生成1molSiO 时,转移8mol电子,D
2
正确;
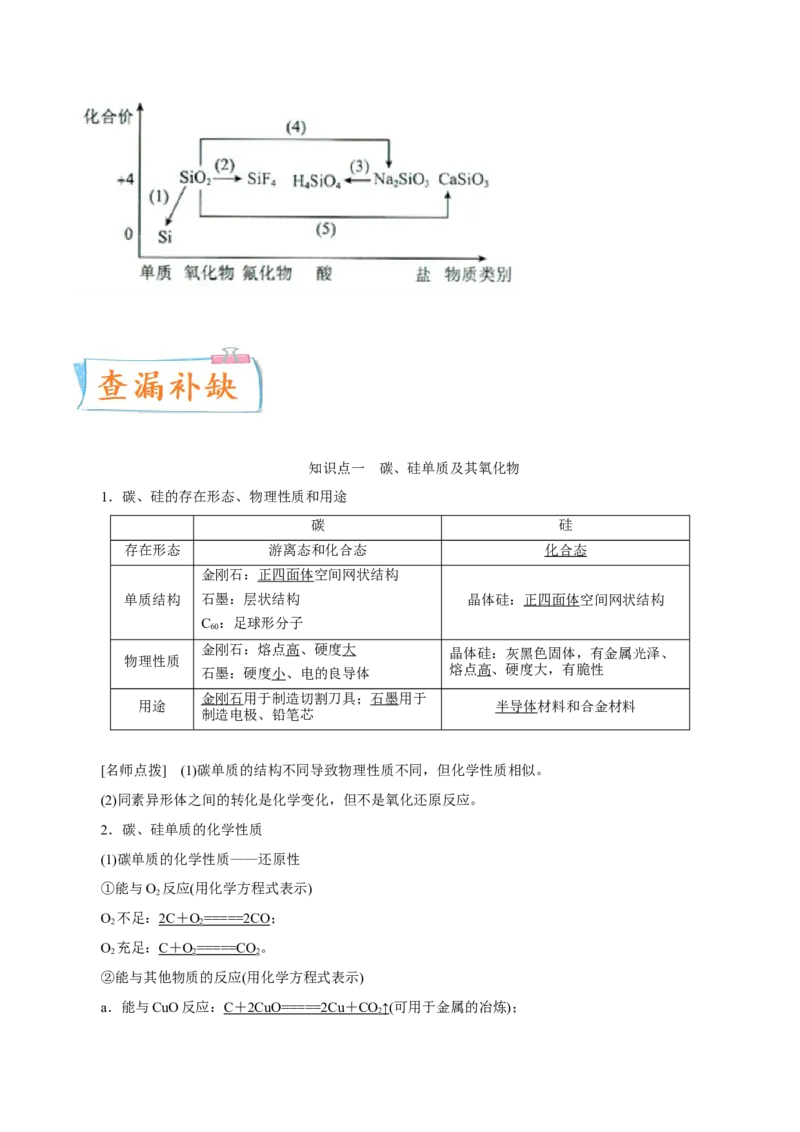
答案选D。知识点一 碳、硅单质及其氧化物
1.碳、硅的存在形态、物理性质和用途
碳 硅
存在形态 游离态和化合态 化合态
金刚石:正四面体空间网状结构
单质结构 石墨:层状结构 晶体硅:正四面体空间网状结构
C :足球形分子
60
金刚石:熔点高、硬度大 晶体硅:灰黑色固体,有金属光泽、
物理性质
石墨:硬度小、电的良导体 熔点高、硬度大,有脆性
金刚石用于制造切割刀具;石墨用于
用途 半导体材料和合金材料
制造电极、铅笔芯
[名师点拨] (1)碳单质的结构不同导致物理性质不同,但化学性质相似。
(2)同素异形体之间的转化是化学变化,但不是氧化还原反应。
2.碳、硅单质的化学性质
(1)碳单质的化学性质——还原性
①能与O 反应(用化学方程式表示)
2
O 不足: 2C + O ===== 2CO ;
2 2
O 充足: C + O ===== CO 。
2 2 2
②能与其他物质的反应(用化学方程式表示)
a.能与CuO反应: C + 2CuO ===== 2Cu + CO ↑(可用于金属的冶炼);
2b.能与CO 反应: C + CO ===== 2CO ;
2 2
c.能与水蒸气反应: C + H O(g) ===== CO + H (制水煤气);
2 2
d.能与浓硫酸反应: C + 2H SO ( 浓 ) ===== CO ↑ + 2SO ↑ + 2H O。
2 4 2 2 2
(2)硅单质的化学性质——还原性
①能与O 反应: Si + O ===== SiO ;
2 2 2
②能与氢氟酸反应(用化学方程式表示,下同): Si + 4HF == =SiF ↑ + 2H ↑;
4 2
③能与NaOH溶液反应: Si + 2NaOH + H O == =Na SiO + 2H ↑。
2 2 3 2
3.硅的制备
(1)原料:二氧化硅、焦炭。
(2)原理:SiO + 2C ===== Si ( 粗 ) + 2CO ↑。
2
(3)提纯: Si( 粗 ) + 2Cl ===== SiCl ,SiCl + 2H ===== Si( 纯 ) + 4HCl 。
2 4 4 2
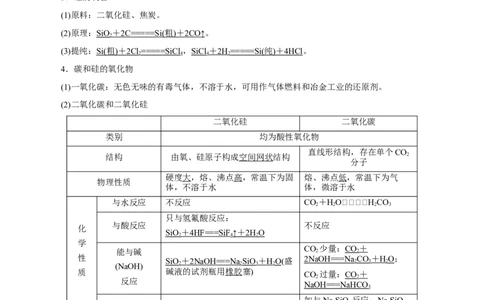
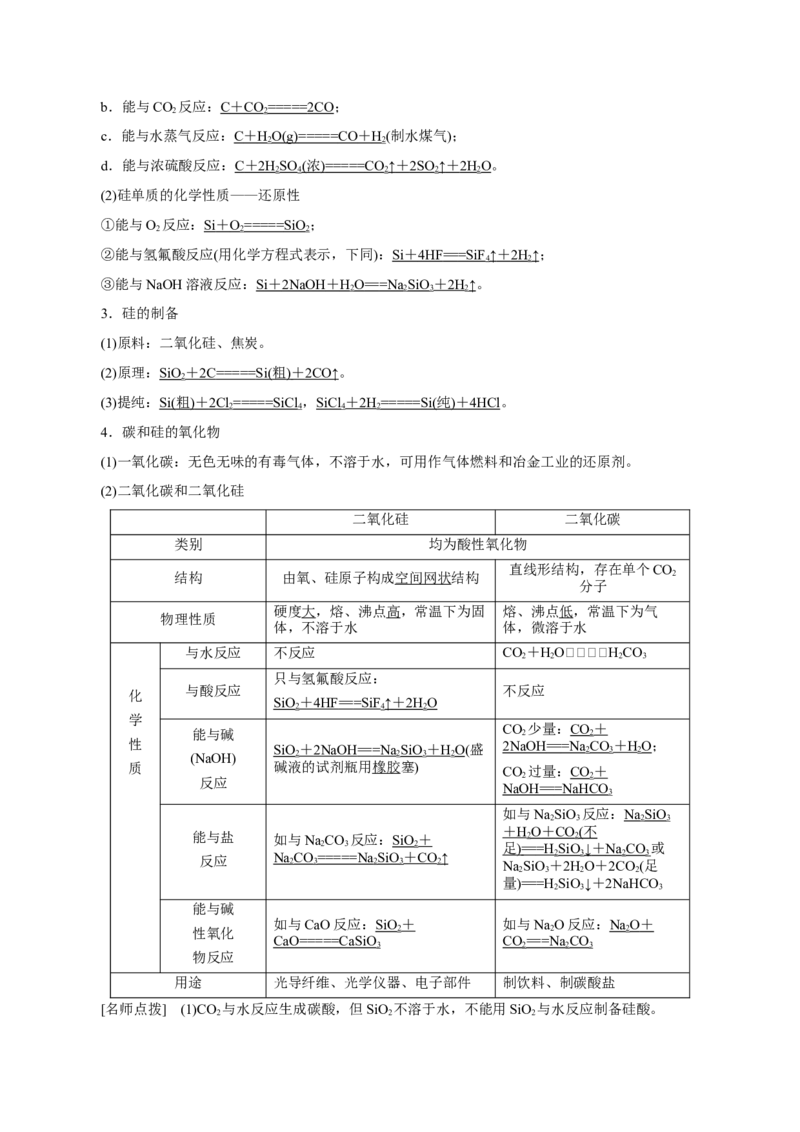
4.碳和硅的氧化物
(1)一氧化碳:无色无味的有毒气体,不溶于水,可用作气体燃料和冶金工业的还原剂。
(2)二氧化碳和二氧化硅
二氧化硅 二氧化碳
类别 均为酸性氧化物
直线形结构,存在单个CO
结构 由氧、硅原子构成空间网状结构 2
分子
硬度大,熔、沸点高,常温下为固 熔、沸点低,常温下为气
物理性质
体,不溶于水 体,微溶于水
与水反应 不反应 CO+HOHCO
2 2 2 3
只与氢氟酸反应:
与酸反应 不反应
化
SiO + 4HF == =SiF ↑ + 2H O
2 4 2
学
CO 少量:CO+
能与碱 2 2
性 (NaOH) SiO 2 + 2NaOH == =N a 2 SiO 3 + H 2 O(盛 2NaOH == =Na 2 CO 3 + H 2 O;
质 碱液的试剂瓶用橡胶塞) CO 过量:CO+
2 2
反应
NaOH == =NaHCO
3
如与NaSiO 反应:NaSiO
2 3 2 3
+ H O + CO ( 不
能与盐 如与NaCO 反应:SiO+ 2 2
2 3 2 足 ) == =H SiO ↓ + Na CO 或
反应 Na 2 CO 3 ===== Na 2 SiO 3 + CO 2 ↑ NaSiO+ 2 2H 3 O+2C 2 O(足 3
2 3 2 2
量)===H SiO↓+2NaHCO
2 3 3
能与碱
如与CaO反应:SiO+ 如与NaO反应:Na O +
性氧化 2 2 2
CaO ===== CaSiO CO == =Na CO
3 2 2 3
物反应
用途 光导纤维、光学仪器、电子部件 制饮料、制碳酸盐
[名师点拨] (1)CO 与水反应生成碳酸,但SiO 不溶于水,不能用SiO 与水反应制备硅酸。
2 2 2(2)SiO 既能与HF反应,又能与NaOH溶液反应,但SiO 不是两性氧化物。
2 2
知识点二 硅酸、硅酸盐和无机非金属材料
1.硅酸
(1)弱酸性:HSiO 难溶于水,其酸性比碳酸弱,不能使指示剂变色,能与强碱(如NaOH)反应,化学
2 3
方程式为HSiO + 2NaOH == =N a SiO + 2H O。
2 3 2 3 2
(2)不稳定性:HSiO 不稳定,受热易分解,化学方程式为HSiO ===== SiO + H O。
2 3 2 3 2 2
(3)硅酸的制备及硅胶
①制备原理:可溶性硅酸盐(如NaSiO)与较强的酸(如盐酸)反应,化学方程式为NaSiO+
2 3 2 3
2HCl == =H SiO ↓ + 2NaCl 。
2 3
②硅胶:硅酸在水中易聚合形成硅酸凝胶,经干燥脱水后即得硅胶,常用作干燥剂和催化剂的载体。
2.硅酸盐
(1)硅酸盐是由硅、氧和金属元素组成的化合物的总称,是构成地壳岩石的重要成分。
(2)硅酸盐组成的表示方法
通常用二氧化硅和金属氧化物的组合形式表示硅酸盐的组成:
①氧化物的书写顺序:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水,不同氧化物间以“·”隔
开。
②各元素的化合价保持不变,且满足化合价代数和为零,各元素原子个数比符合原来的组成。
如硅酸钠(Na SiO)可表示为NaO·SiO ,长石(KAlSi O)可表示为KO·Al O·6SiO。
2 3 2 2 3 8 2 2 3 2
(3)硅酸钠
①物理性质:白色、可溶于水的粉末状固体,其水溶液俗称水玻璃,有黏性,水溶液显性。
②化学性质:能与酸性较硅酸强的酸反应
a.与盐酸反应的化学方程式:
NaSiO + 2HC l == =2NaC l + H SiO↓。
2 3 2 3
b.与少量CO 水溶液反应的化学方程式:
2
NaSiO + H O + CO == =Na CO + H SiO↓。
2 3 2 2 2 3 2 3
③用途:黏合剂(矿物胶),耐火阻燃材料。
3.无机非金属材料
(1)传统无机非金属材料(如水泥、玻璃、陶瓷等硅酸盐材料)
水泥 玻璃 陶瓷
生产原料 石灰石、黏土 纯碱、石灰石、石英砂 黏土
主要设备 水泥回转窑 玻璃窑 陶瓷窑玻璃生产中的两个重要反应:
NaCO + SiO ===== Na SiO + CO ↑;CaCO + SiO ===== CaSiO + CO ↑。
2 3 2 2 3 2 3 2 3 2
(2)新型无机非金属材料:如高温结构陶瓷、生物陶瓷、压电陶瓷等。
[名师点拨] (1)玻璃中含有二氧化硅,因此氢氟酸可用于雕刻玻璃,盛放氢氟酸不用玻璃瓶而用塑料
瓶。
(2)NaOH溶液可以用玻璃瓶盛放,但不能用玻璃塞而使用橡胶塞。
1.能证明硅酸的酸性弱于碳酸酸性的实验事实是( )
A.CO 溶于水形成碳酸,SiO 难溶于水
2 2
B.CO 通入可溶性硅酸盐中析出硅酸沉淀
2
C.高温下SiO 与碳酸盐反应生成CO
2 2
D.氯化氢通入可溶性碳酸盐溶液中放出气体,其气体通入可溶性硅酸盐溶液中生成沉淀
2.下列关于SiO 和CO 的叙述不正确的是( )
2 2
A.都是共价化合物
B.都是酸性氧化物,都能与强碱溶液反应
C.都能溶于水且与水反应生成相应的酸
D.SiO 可用于制光导纤维,干冰可用于人工降雨
2
3.由二氧化硅制高纯硅的流程如图,下列判断中错误的是( )
A.①②③均属于氧化还原反应
B.氢气和氯化氢均可循环利用
C.二氧化硅是一种坚硬难熔的固体
D.三氯甲硅烷(SiHCl )摩尔质量为135.5 g
34.《青花瓷》中所描述的“瓶身描述的牡丹一如你初妆”“色白花青的锦鲤跃然于碗底”等图案让人赏
心悦目,但古瓷中所用颜料成分一直是个谜,近年来科学家才得知大多为硅酸盐,如蓝紫色的硅酸铜钡
(BaCuSi O,铜为+2价),下列有关硅酸铜钡的说法不正确的是( )
2 x
A.可用氧化物形式表示为BaO·CuO·2SiO
2
B.易溶解于强酸和强碱
C.性质稳定,不易脱色
D.x=6
5.工业上利用无机矿物资源生产部分材料的流程示意图如下。下列说法正确的是( )
(注:铝土矿中含有Al O、SiO、Fe O)
2 3 2 2 3
A.在铝土矿制备较高纯度Al的过程中只用到NaOH溶液、CO 气体
2
B.石灰石、纯碱、石英、玻璃都属于盐,都能与盐酸反应
C.在制粗硅时,氧化剂与还原剂的物质的量之比为1∶2
D.黄铜矿(CuFeS)与O 反应产生的Cu S、SO 均只是还原产物
2 2 2 2
1.(2022·河南焦作·一模)2020年12月17日,嫦娥五号带回了近2公斤的月壤样品。将月壤进行20倍
放大后能明显看到褐色的玻璃状物质。下列有关玻璃的说法中正确的是
A.普通玻璃的原料是烧碱、石英、石灰石
B.普通玻璃和石英玻璃都属于硅酸盐产品
C.制备普通玻璃时的反应有NaCO + SiO CO↑+ Na SiO
2 3 2 2 2 3
D.普通玻璃用于镶嵌建筑物的门窗、墙面,但其不具有保温和防辐射等特征
2.(2022·江西·模拟预测)我国有着五千年文明历史,下列有关说法正确的是
A.《本草图经》有“白矾多入药用”,其白矾是[KAl(SO)·12H O],具有杀菌、消毒之功效
4 2 2B.诗句“月落乌啼霜满天,江枫渔火对愁眠”。其中不包含有化学变化过程
C.“凡石灰,经火焚炼为用……火力用后,烧酥石性,置于风中,久自吹成粉”中的“粉”为CaO
D.古代烧制的“明如镜,声如磬”的瓷器,其主要成分为硅酸盐
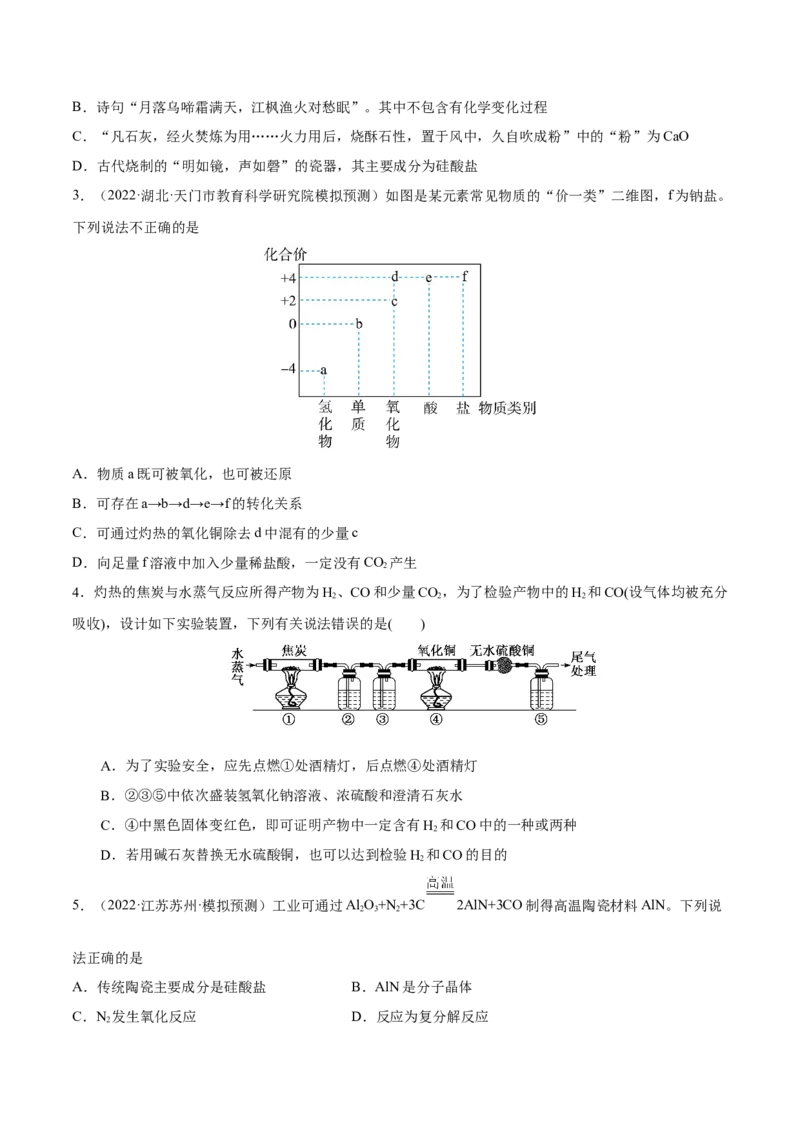
3.(2022·湖北·天门市教育科学研究院模拟预测)如图是某元素常见物质的“价一类”二维图,f为钠盐。
下列说法不正确的是
A.物质a既可被氧化,也可被还原
B.可存在a→b→d→e→f的转化关系
C.可通过灼热的氧化铜除去d中混有的少量c
D.向足量f溶液中加入少量稀盐酸,一定没有CO 产生
2
4.灼热的焦炭与水蒸气反应所得产物为H、CO和少量CO,为了检验产物中的H 和CO(设气体均被充分
2 2 2
吸收),设计如下实验装置,下列有关说法错误的是( )
A.为了实验安全,应先点燃①处酒精灯,后点燃④处酒精灯
B.②③⑤中依次盛装氢氧化钠溶液、浓硫酸和澄清石灰水
C.④中黑色固体变红色,即可证明产物中一定含有H 和CO中的一种或两种
2
D.若用碱石灰替换无水硫酸铜,也可以达到检验H 和CO的目的
2
5.(2022·江苏苏州·模拟预测)工业可通过Al O+N +3C 2AlN+3CO制得高温陶瓷材料AlN。下列说
2 3 2
法正确的是
A.传统陶瓷主要成分是硅酸盐 B.AlN是分子晶体
C.N 发生氧化反应 D.反应为复分解反应
21.(2022·辽宁·高考真题)北京冬奥会备受世界瞩目。下列说法错误的是
A.冰壶主材料花岗岩属于无机非金属材料
B.火炬“飞扬”使用的碳纤维属于有机高分子材料
C.冬奥会“同心”金属奖牌属于合金材料
D.短道速滑服使用的超高分子量聚乙烯属于有机高分子材料
2.(2022·河北·高考真题)定窑是宋代五大名窑之一,其生产的白瓷闻名于世。下列说法正确的是
A.传统陶瓷是典型的绝缘材料 B.陶瓷主要成分为 和
C.陶瓷烧制的过程为物理变化 D.白瓷的白色是因铁含量较高
3.(2022·广东·高考真题)陈述Ⅰ和Ⅱ均正确但不具有因果关系的是
选项 陈述Ⅰ 陈述Ⅱ
A 用焦炭和石英砂制取粗硅 可制作光导纤维
B 利用海水制取溴和镁单质 可被氧化, 可被还原
C 石油裂解气能使溴的 溶液褪色 石油裂解可得到乙烯等不饱和烃
D 水解可生成 胶体 可用作净水剂
4.(2019·浙江高考真题)下列说法不正确的是
A.液氯可以储存在钢瓶中
B.天然气的主要成分是甲烷的水合物
C.天然石英和水晶的主要成分都是二氧化硅
D.硫元素在自然界的存在形式有硫单质、硫化物和硫酸盐等
5.(2020·浙江高考真题) 是硅酸盐水泥的重要成分之一,其相关性质的说法不正确的是( )
A.可发生反应:
B.具有吸水性,需要密封保存
C.能与 ,反应生成新盐D.与足量盐酸作用,所得固体产物主要为
1. 【答案】B
【解析】酸性强弱与水溶性没有关系,则无法据此比较酸性强弱,故A错误;CO 通入可溶性硅酸盐中析
2
出硅酸沉淀,反应方程式是NaSiO+HO+CO===Na CO+HSiO↓,反应原理是强酸制弱酸,说明碳酸
2 3 2 2 2 3 2 3
比硅酸酸性强,故B正确;比较强酸制取弱酸是在溶液中进行的反应,则在高温下固体之间的反应不能比
较酸性强弱,故C错误;HCl通入可溶性碳酸盐溶液中放出气体,其气体通入可溶性硅酸盐溶液中生成沉
淀,根据强酸制弱酸,只能说明盐酸的酸性比碳酸强,可溶性硅酸盐溶液中生成沉淀,可能为盐酸与硅酸
盐的反应,无法确定碳酸与硅酸酸性的强弱,故D错误。
2. 【答案】C
【解析】SiO 和CO 都是共价化合物,A正确;都是酸性氧化物,都能与强碱溶液反应产生盐和水,B正
2 2
确;SiO 不能溶于水且不能与水反应生成相应的酸,C错误;光在SiO 中可以全反射,因此SiO 可用于制
2 2 2
光导纤维,固态CO 容易升华,升华时吸收大量的热,因此干冰可用于人工降雨,D正确。
2
3.【答案】D
【解析】 ①②③反应前后元素化合价发生改变,故①②③发生的反应均是氧化还原反应,A正确;由二
氧化硅制高纯硅的流程图中反应过程中生成氢气和氯化氢,同时氯化氢和氢气也作为反应物参与化学反应,
故氢气和氯化氢均可循环利用,B正确;二氧化硅熔点比较高,硬度比较大,C正确;三氯甲硅烷(SiHCl )
3
摩尔质量为135.5 g·mol-1,D错误。
4.【答案】B
【解析】硅酸盐用氧化物形式表示时,书写顺序为:活泼金属氧化物、不活泼金属氧化物、二氧化硅、水,
所以硅酸铜钡用氧化物形式表示BaO·CuO·2SiO ,故A正确;硅酸铜钡能稳定存在,说明不易溶解于强酸
2
和强碱,故B错误;青花瓷能长期不褪色,说明硅酸铜钡性质稳定不易脱色,故C正确;硅酸铜钡中Ba
为+2价、Cu为+2价、Si为+4价、O为-2价,根据化合价代数和等于0,可知x=6,故D正确。
5. 【答案】C【解析】由铝土矿制备较高纯度Al,可用氧化铝与氢氧化钠反应生成偏铝酸钠溶液,过滤后通入CO 气体
2
生成氢氧化铝,氢氧化铝分解生成氧化铝,电解氧化铝可生成铝,电解时为降低熔点,可加入冰晶石,A
错误;石英主要成分为二氧化硅,不是盐,与盐酸不反应,且玻璃也与盐酸不反应,B错误;粗硅的反应:
SiO+2C=====Si+2CO↑,反应中SiO 为氧化剂,C为还原剂,则氧化剂与还原剂的物质的量之比为
2 2
1∶2,C正确;黄铜矿(CuFeS)与O 反应产生的Cu S、SO 、FeO中CuO元素化合价降低,则Cu S、FeO
2 2 2 2 2
均是还原产物,SO 既是还原产物又是氧化产物,D错误。
2
1. 【答案】C
【详解】A.制造普通玻璃的主要原料是:纯碱、石灰石和石英,A项错误;
B.石英玻璃的主要成分是二氧化硅,B项错误;
C.制造普通玻璃的主要原料是:纯碱、石灰石和石英,则反应有Na2CO3 + SiO2 CO2↑+ Na2SiO3,C
项正确;
D.普通玻璃具有透光、隔热、隔声、耐磨、耐气候变化的性能,有的还有保温、吸热、防辐射等特征,D
项错误;
答案选C。
2. 【答案】D
【详解】A.明矾只能作净水剂,不具有杀菌、消毒的作用,A项错误;
B.火是物质燃烧时所表现出来的发热、发光的现象,是包含了化学变化过程,B项错误;
C.CaCO3煅烧后生成CaO,经久置于空气中最终变为CaCO3,C项错误;
D.陶瓷为传统的硅酸盐材料,D项正确;
故答案选D。
3. 【答案】D
【分析】结合图示可知,a为CH4、b为C、c为CO、d为CO2、e为H2CO3,f为CO 或HCO 。
【详解】A.a为CH4,碳元素化合价可升高,氢元素化合价可降低,物质a既可被氧化,也可被还原,故
A正确;B. 可存在a→b→d→e→f的转化关系:甲烷高温分解生成碳,碳燃烧生成二氧化碳,二氧化碳溶于水生
成碳酸,与适量的碱生成盐,故B正确;
C. CO能被灼热的氧化铜氧化生成二氧化碳,可通过灼热的氧化铜除去d中混有的少量c,故C正确;
D. f可能为正盐或酸式盐,向足量f溶液中加入少量稀盐酸,正盐转化成酸式盐,可能没有CO2产生,
酸式盐和盐酸,一定有二氧化碳产生,故D错误;
故选D。
4. 【答案】D
【解析】由图可知,①中C与水蒸气反应生成H、CO和少量CO,实验目的为检验产物中的H 和CO,
2 2 2
则②中NaOH溶液可除去CO,③中浓硫酸干燥气体,④中H 和CO均还原CuO,若无水硫酸铜变蓝,则
2 2
检验出含有氢气,⑤中澄清石灰水变浑浊可检验出含有CO,最后处理尾气。A项,H、CO不纯时加热易
2
发生爆炸,则为了实验安全性,应先点燃①处酒精灯,排出装置中空气后点燃④处酒精灯,正确;B项,
由上述分析可知,②、③、⑤中依次盛装氢氧化钠溶液、浓硫酸和澄清石灰水,正确;C项,H 和CO均
2
还原CuO,当黑色氧化铜变红色,只能说明产物中一定含有H 和CO中的一种或两种,无法确定具体是哪
2
种气体,正确;D项,若用碱石灰替换无水硫酸铜,碱石灰可吸收水、二氧化碳,不能检验氢气,故D错
误。
5. 【答案】A
【详解】A.玻璃、水泥和陶瓷均属于无机硅酸盐产品,则传统陶瓷主要成分是硅酸盐,A正确;
B.AlN具有很高的熔点,故不是分子晶体,而是共价晶体(或者称为原子晶体),B错误;
C.Al O+N +3C 2AlN+3CO反应中N的化合价由0价降低到-3价,故N2发生还原反应,C错误;
2 3 2
D.复分解反应是指两种化合物互相交换成分生成两种新的化合物的反应,故该反应不属于复分解反应,
属于氧化还原反应,D错误;
故答案为:A。
1. 【答案】B
【详解】A.花岗岩的主要成分是石英、云母、长石等矿物,属于无机非金属材料,A正确;
B.碳纤维指的是含碳量在90%以上的高强度高模量纤维,属于无机非金属材料,B错误;
C.金属奖牌属于合金材料,C正确;D.聚乙烯属于有机高分子材料,D正确;
故答案选B。
2. 【答案】A
【详解】A.陶瓷是良好的绝缘体,传统陶瓷是典型的绝缘材料,常用于高压变压器的开关外包装和器件,
A正确;
B.陶瓷的主要成分为硅酸盐,而不是SiO2和MgO,C错误;
C.陶瓷烧制过程发生复杂的化学反应,由新物质生成,属于化学变化,C错误;
D.由于Fe2+、Fe3+和铁的氧化物均有颜色,故陶瓷中含铁量越多,陶瓷的颜色越深,白瓷的白色是因为
铁含量较低甚至几乎不含,D错误;
故答案为:A。
3.【答案】A
【详解】A.焦炭具有还原性,工业上常利用焦炭与石英砂(SiO2)在高温条件下制备粗硅,这与SiO2是
否做光导纤维无因果关系,故A符合题意;
B.海水中存在溴离子,可向其中通入氯气等氧化剂将其氧化为溴单质,再经过萃取蒸馏物理操作分离提
纯溴单质,另外,通过富集海水中的镁离子,经过沉淀、溶解等操作得到无水氯化镁,随后电解熔融氯化
镁可制备得到镁单质,陈述I和陈述II均正确,且具有因果关系,B不符合题意;
C.石油在催化剂加热条件下进行裂解可得到乙烯等不饱和烃,从而使溴的CCl4溶液褪色,陈述I和陈述
II均正确,且具有因果关系,C不符合题意;
D.FeCl3溶液中铁离子可发生水解,生成具有吸附性的氢氧化铁胶体,从而可用作净水剂,陈述I和陈述
II均正确,且具有因果关系,D不符合题意;
综上所述,答案为A。
4.【答案】B
【解析】A.液氯就是液态的氯气,与钢瓶不反应,可以储存在钢瓶中,正确;B.天然气的主要成分是甲
烷,可燃冰的主要成分是甲烷的水合物,错误;C.石英、水晶、硅石、沙子的主要成分均为二氧化
硅,正确;D.硫在地壳中主要以硫化物、硫酸盐等形式存在,火山口处有硫单质,正确。故答案选
B。
5.【答案】D
【解析】将Ca SiO 改写为氧化物形式后的化学式为:3CaO·SiO ,性质也可与NaSiO 相比较,据此解答。
3 5 2 2 3
A.Ca SiO 与NH Cl反应的方程式为:Ca SiO+4NHCl CaSiO +2CaCl +4NH↑+2H O,A正确;
3 5 4 3 5 4 3 2 3 2B.CaO能与水反应,所以需要密封保存,B正确;C.亚硫酸的酸性比硅酸强,当二氧化硫通入到
Ca SiO 溶液时,发生反应:3SO +H O+ Ca SiO=3 CaSO+H SiO,C正确;D.盐酸的酸性比硅酸强,
3 5 2 2 3 5 3 2 3
当盐酸与Ca SiO 反应时,发生反应:6HCl+ Ca SiO=3CaCl +H SiO+2H O,D不正确;故选D。
3 5 3 5 2 2 3 2