文档内容
考向 14 原子结构 核外电子排布
【2022浙江卷1月】下列表示不正确的是
A.乙炔的结构简式HC≡CH B.KOH的电子式
C.乙烷的球棍模型: D.氯离子的结构示意图:
【答案】C
【详解】
A.乙炔中碳碳之间为三键,故结构简式HC≡CH,选项A正确;
B.KOH为离子化合物,故电子式为 ,选项B正确;
C. 为乙烷的比例模型,不是球棍模型,选项C错误;
D.氯离子的核电荷数是17,电子数为18,氯离子的结构示意图为 ,选项D正确;
故答案是C。知识点一 原子结构
1.原子的构成
(1)构成原子的微粒及作用
(2)微粒之间的关系
①原子中:质子数(Z)=核电荷数=核外电子数;
②质量数(A)=质子数(Z)+中子数(N);
③阳离子的核外电子数=质子数-所带电荷数;
④阴离子的核外电子数=质子数+所带电荷数。
(3)微粒符号周围数字的含义
[名师点拨] (1)原子中不一定都含有中子,如H中没有中子。
(2)电子排布完全相同的原子不一定是同一种原子,如互为同位素的各原子。
(3)破坏原子结构的核裂变不属于化学变化。
(4)质子数相同的微粒不一定属于同一种元素,如F和OH-。
知识点二 原子核外电子排布
1.核外电子排布(1)核外电子排布规律
(2)核外电子排布与元素性质的关系
①金属元素原子的最外层电子数一般小于4,较易失去电子,形成阳离子,表现出还原性,在化合物
中显正化合价。
②非金属元素原子的最外层电子数一般大于或等于4,较易得到电子,活泼非金属原子易形成阴离子,
在化合物中主要显负化合价。
③稀有气体元素的原子最外层为8电子(氦为2电子)稳定结构,不易失去或得到电子,它们的化合价
通常表现为0价。
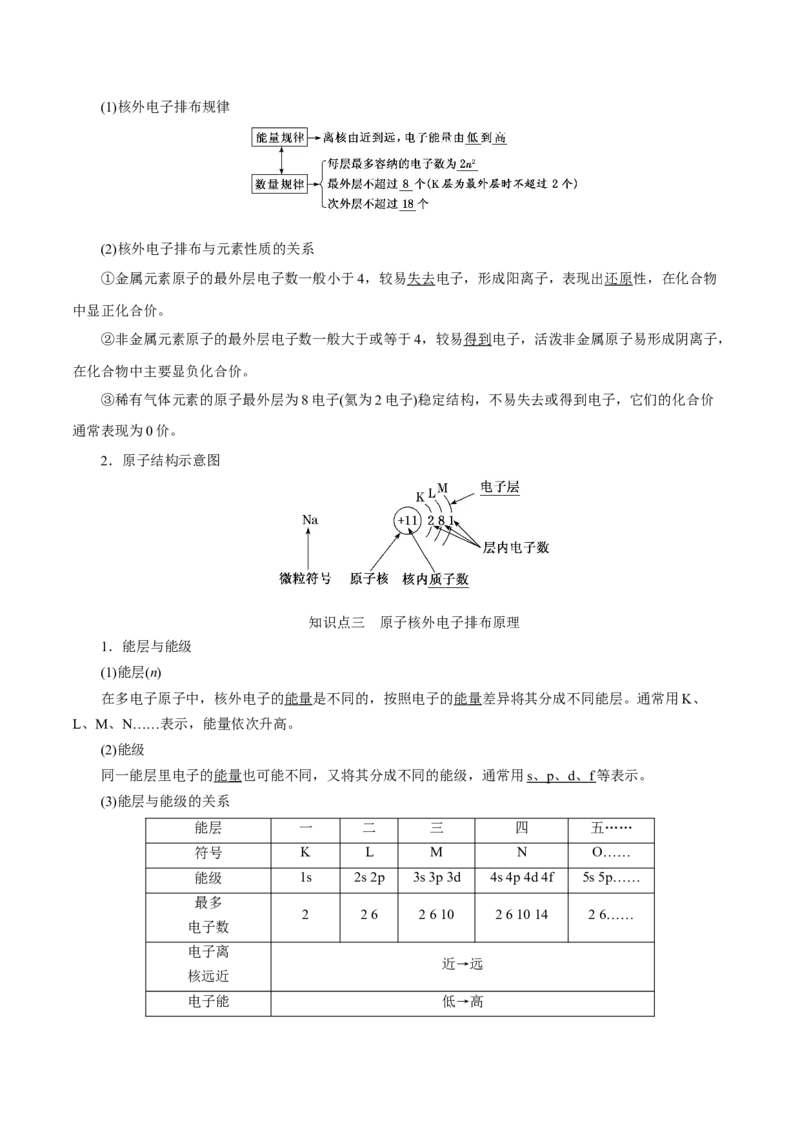
2.原子结构示意图
知识点三 原子核外电子排布原理
1.能层与能级
(1)能层(n)
在多电子原子中,核外电子的能量是不同的,按照电子的能量差异将其分成不同能层。通常用K、
L、M、N……表示,能量依次升高。
(2)能级
同一能层里电子的能量也可能不同,又将其分成不同的能级,通常用 s 、 p 、 d 、 f 等表示。
(3)能层与能级的关系
能层 一 二 三 四 五……
符号 K L M N O……
能级 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p……
最多
2 2 6 2 6 10 2 6 10 14 2 6……
电子数
电子离
近→远
核远近
电子能 低→高量高低
[名师点拨] (1)能层数=电子层数。
(2)第一能层(K),只有s能级;第二能层(L),有s、p两种能级,p能级上有三个原子轨道p、p、p,
x y z
它们具有相同的能量;第三能层(M),有s、p、d三种能级。
2.电子云与原子轨道
(1)电子云
①由于核外电子的概率密度分布看起来像一片云雾,因而被形象地称为电子云。
②电子云轮廓图称为原子轨道。
(2)原子轨道
原子轨道
3.基态原子的核外电子排布
(1)能量最低原理:即电子尽可能地先占有能量低的轨道,然后进入能量高的轨道,使整个原子的能量
处于最低状态。如图为构造原理示意图,即基态原子核外电子在原子轨道上的排布顺序图:
[注意] 所有电子排布规则都需要满足能量最低原理。
(2)泡利原理
每个原子轨道里最多只能容纳个电子,且自旋状态相反。
如2s轨道上的电子排布为 ,不能表示为 。
(3)洪特规则
当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个轨道,且自旋状态相
同。 如2p3的电子排布为 ,不能表示为
或 。
[名师点拨] 当能量相同的原子轨道在全满(p6、d10、f14)、半满(p3、d5、f7)、全空(p0、d0、f0)时原子的
能量最低,如 Cr的电子排布式为[Ar]3d54s1, Cu的电子排布式为[Ar]3d104s1。
24 29
(4)基态原子核外电子排布的表示方法表示方法 以硫原子为例
电子排布式 1s 2 2s 2 2p 6 3s 2 3p 4
简化电子
[Ne]3s 2 3p 4
排布式
电子排布图
(或轨道表示式)
价电子排布式 3s 2 3p 4
价电子排布图
4.电子的跃迁与原子光谱
(1)电子的跃迁
(2)不同元素的原子发生跃迁时会吸收或释放不同的光,可以用光谱仪摄取各种元素的电子的吸收光谱
或发射光谱,总称原子光谱。
附:可见光的波长范围
颜色 波长范围
红 770~622 nm
橙 622~597 nm
黄 597~577 nm
绿 577~492 nm
蓝、靛 492~455 nm
紫 455~350 nm
[名师点拨] (1)可见光中,红光的波长最长,紫色的波长最短。
(2)焰色反应是电子跃迁的结果,故金属的焰色反应是物理变化过程,不属于化学变化。1. Tc是医用放射性同位素。下列关于Tc的叙述正确的是( )
A.中子数是56 B.质量数是43
C.质子数是56 D.原子序数是99
2. “原子”原意是“不可再分”的意思。20世纪初,人们才认识到原子不是最小的粒子。从电子层
模型分析,Ca原子核外N能层中运动的电子数为( )
A.8 B.2
C.18 D.10
3.钼元素为人体及动植物必须的微量元素,也在钢铁工业中有着重要的作用,钼作为钢的合金化元
素,可以提高钢的强度,特别是高温强度和韧性。我国钼元素的储量丰富,在世界上占笫二位。如图所示
是钼元素的相关信息,下列有关钼的说法错误的是( )
A.95Mo18O(钼酸根离子)中共计有76个电子
B.Mo元素是第五周期的主族元素
C.92Mo、95Mo、98Mo互为同位素,化学性质几乎相同
D.98Mo的原子核内中子数比质子数多14
4.下列电子排布图能表示氮原子的最低能量状态的是( )
5.现有四种短周期元素,它们的结构、性质等信息如下表所述:
元素 结构、性质等信息
是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆
A
的导热剂
B 与A同周期,其最高价氧化物的水化物呈两性C 在空气中含量第二,在地壳中含量第一
海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常
D
用的消毒杀菌剂
请根据表中信息填写:
(1)A原子的核外电子排布式为________________。
(2)B元素在周期表中的位置是________;离子半径:B________A(填“大于”或“小于”)。
(3)C原子的电子排布图是________________,其原子核外有________个未成对电子,能量最高的电子
为____________轨道上的电子,其轨道呈________形。
(4)D原子的电子排布式为________________,D-的结构示意图是____________。
(5)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为
____________________________;B的最高价氧化物对应的水化物与D的氢化物的水溶液反应的化学方程
式为____________________________________________________________。
1. 肼(N H)是发射航天飞船常用的高能燃料,可通过反应2NH +NaClO=N H+NaCl+HO制备。下列有关
2 4 3 2 4 2
微粒的描述错误的是
A.NH 的电子式为
3
B.NH 的结构式为
2 4
C.Na+的结构示意图:
D.质子数为17、中子数为18的氯原子可表示为 Cl
2.全氮类物质具有高密度、超高能量及爆轰、产物无污染等优点。中国科学家成功合成全氮阴离子N,N
是制备全氮类物质NN的重要中间体。下列说法中,不正确的是( )
A.全氮类物质属于绿色能源
B.每个N中含有35个质子
C.NN属于离子化合物
D.NN结构中含共价键和离子键3.(江苏省南通市如皋市2021-2022学年高三下学期 4月适应性考试)配合物 可用于蚀刻
铜,蚀刻后的产物 可在氧气中再生,再生反应为
。下列说法正确的是
A.基态 的电子排布式为
B. 属于共价化合物
C. 的晶体类型为原子晶体
D. 中与 形成配位键的原子是N
4.(辽宁省辽阳市2022届高三一模)氢氟酸可用于雕刻玻璃,其反应原理为4HF+SiO =SiF ↑+2H O。下
2 4 2
列有关说法正确的是
A.HF中的共价键为s-pσ键
B.HO、SiF 均为极性分子
2 4
C.SiO 晶体为分子晶体
2
D.基态氧原子的价层电子轨道表示式为
5.如图为元素周期表前三周期的一部分。
(1)X的基态原子的电子排布图是________(填序号);
另一电子排布图不能作为基态原子的电子排布图是因为它不符合
________(填字母)。
A.能量最低原理 B.泡利原理
C.洪特规则
(2)以上五种元素中,________(填元素符号)元素第一电离能最大。
(3)由以上某种元素与氢元素组成的三角锥形分子E和由以上某种元素组成的直线形分子G反应,生成
两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10),反应如图所示,该反应的化学
方程式是____________________________________。1.(2019江苏)反应NH Cl+NaNO ===NaCl+N↑+2HO放热且产生气体,可用于冬天石油开采。下列
4 2 2 2
表示反应中相关微粒的化学用语正确的是( )
A.中子数为18的氯原子:Cl
B.N 的结构式:N===N
2
C.Na+的结构示意图:
D.HO的电子式:
2
2.(1)(2020·全国卷Ⅰ)基态Fe2+与Fe3+离子中未成对的电子数之比为________。
(2)(2020·全国卷Ⅱ)基态Ti原子的核外电子排布式为
____________。
(3)(2020·江苏高考)Fe基态核外电子排布式为________。
(4)(2020·天津等级考)Fe、Co、Ni在周期表中的位置为________。
(5)(2019·全国卷Ⅰ)下列状态的镁中,电离最外层一个电子所需能量最大的是________(填标号)。
A.[Ne] B.[Ne]
C.[Ne] D.[Ne]
(6)(2019·全国卷Ⅱ)Fe成为阳离子时首先失去____________轨道电子,Sm的价电子排布式为4f66s2,
Sm3+价电子排布式为____________。
(7)(2019·江苏高考)Cu2+基态核外电子排布式为__________________。
(8)(2019·海南高考)Mn位于元素周期表中第四周期_____族,基态Mn原子核外未成对电子有_____个。
3.(1)(2020·全国卷Ⅰ)Li及其周期表中相邻元素的第一电离能(I)如表所示。I(Li)>I(Na),原因是
1 1 1
___________________________。I(Be)>I(B)>I(Li),原因是________________________。
1 1 1
I/(kJ·mol-1)
1
Li Be B
520 900 801
Na Mg Al
496 738 578
(2)(2020·全国卷Ⅱ)CaTiO 中,其组成元素的电负性大小顺序是________。
3(3)(2020·全国卷Ⅲ)H、B、N中,原子半径最大的是________。根据对角线规则,B的一些化学性质与
元素________的相似。
(4)(2019·全国卷Ⅱ)比较离子半径:F-________O2-(填“大于”“等于”或“小于”)。
(5)(2019·全国卷 Ⅲ)在周期表中,与Li的化学性质最相似的邻族元素是________,该元素基态原子核
外M层电子的自旋状态________(填“相同”或“相反”)。
1. 【答案】A
【解析】 Tc的质子数=原子序数,均为43,质量数是99,中子数=99-43=56,所以A正确。
2. 【答案】B
【解析】Ca原子核外有4个电子层,分别对应符号K、L、M、N,其原子结构示意图为 ,第
4层有2个电子,故 N能层运动的电子数有2个;故选B。
3.【答案】B
【解析】由图中信息可知Mo原子的核外电子数=42,1个氧原子含8个电子,95Mo18O(钼酸根离子)中
含有的电子数为42+8×4+2=76(个),故A正确;Mo元素位于元素周期表第五周期第ⅥB族,属于副族
元素,故B错误;92Mo、95Mo、98Mo质子数相同、中子数不同,它们互为同位素,由于原子最外层电子数
相同,化学性质几乎相同,故C正确;98Mo的质子数为42,中子数=98-42=56,原子核内中子数比质子
数多56-42=14,故D正确。
4.【答案】A
【解析】基态氮原子的电子排布图为
,此时能量处于最低状态,A选项正确。
5. 【答案】 (1)1s22s22p63s1(或[Ne]3s1) (2)第三周期ⅢA族 小于 (3)
2 2p 哑铃
(4)1s22s22p63s23p5(或[Ne]3s23p5) (5)Al(OH) +NaOH===NaAlO+2HO Al(OH) +
3 2 2 3
3HCl===AlCl +3HO
3 2【解析】根据题中信息可推出:A为Na,B为Al,C为O,D为Cl。
(1)A为Na,其核外电子排布式为1s22s22p63s1或[Ne]3s1。(2)B为Al,其在元素周期表中的位置为第三
周期第ⅢA族,Na+与Al3+的核外电子排布相同,核电荷数Al3+大于Na+,故r(Al3+)