文档内容
考向 15 元素周期表 元素周期律
【2022·广东卷】甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对应的
水化物为强酸。下列说法不正确的是
A.原子半径:丁>戊>乙
B.非金属性:戊>丁>丙
C.甲的氢化物遇氯化氢一定有白烟产生
D.丙的最高价氧化物对应的水化物一定能与强碱反应
【答案】C
【解析】甲~戊是短周期元素,戊中的最高价氧化物对应水化物为强酸,则可能是硫酸或高氯酸,若是高
氯酸,则戊为Cl,甲为N、乙为F、丙为P、丁为S,若是硫酸,则戊为S,甲为C、乙为O、丙为Si、丁
为P。
A.根据层多径大,同电子层结构核多径小原则,则原子半径:丁>戊>乙,故A正确;
B.根据同周期从左到右非金属性逐渐增强,则非金属性:戊>丁>丙,故B正确;
C.甲的氢化物可能为氨气,可能为甲烷、乙烷等,若是氨气,则遇氯化氢一定有白烟产生;若是甲烷、
乙烷等,则遇氯化氢不反应,没有白烟生成,故C错误;
D.丙的最高价氧化物对应的水化物可能是硅酸、也可能是磷酸,都一定能与强碱反应,故D正确。
综上所述,答案为C。考点一 元素周期表的结构
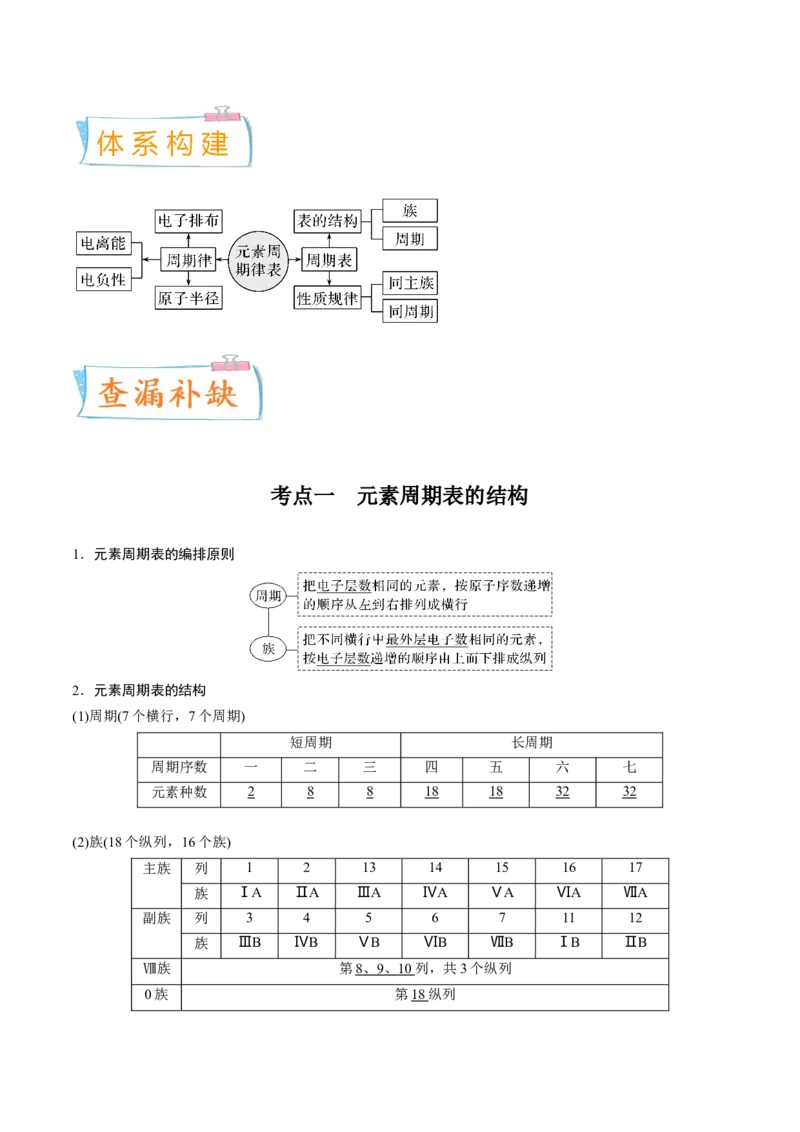
1.元素周期表的编排原则
2.元素周期表的结构
(1)周期(7个横行,7个周期)
短周期 长周期
周期序数 一 二 三 四 五 六 七
元素种数 2 8 8 18 18 32 32
(2)族(18个纵列,16个族)
主族 列 1 2 13 14 15 16 17
族 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
副族 列 3 4 5 6 7 11 12
族 ⅢB ⅣB ⅤB ⅥB ⅦB ⅠB ⅡB
Ⅷ族 第 8 、 9 、 10 列,共3个纵列
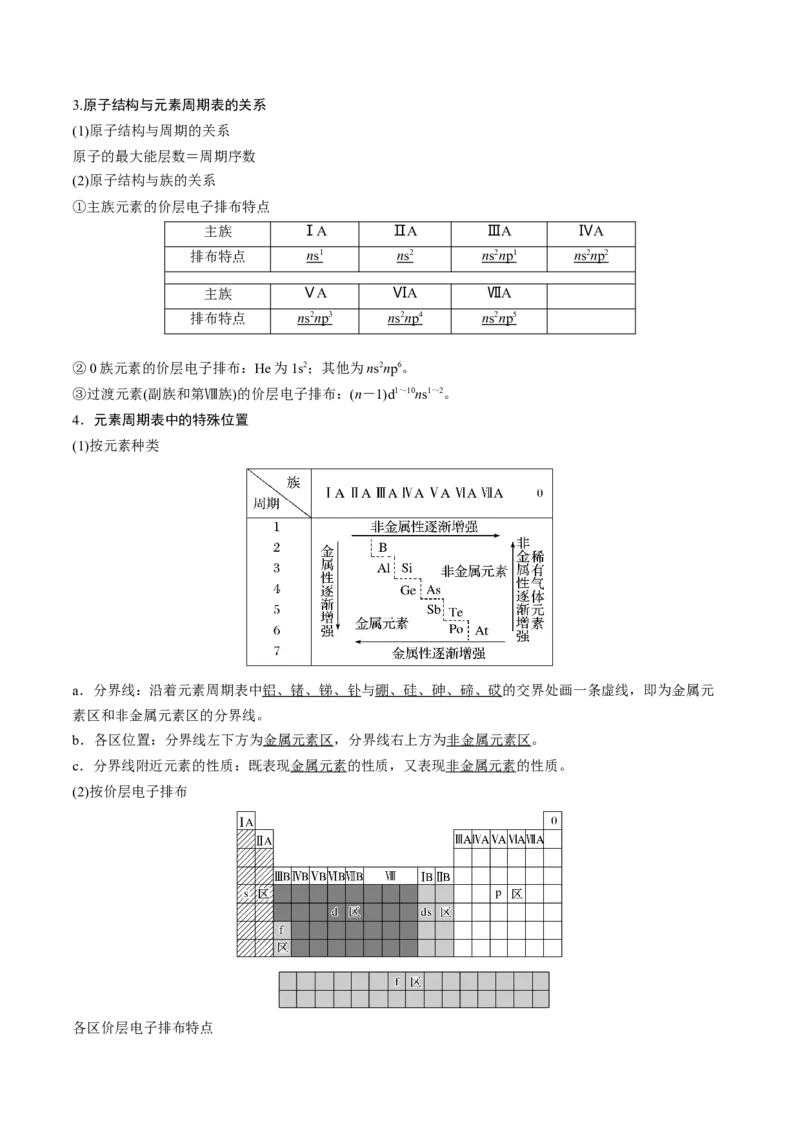
0族 第18 纵列3.原子结构与元素周期表的关系
(1)原子结构与周期的关系
原子的最大能层数=周期序数
(2)原子结构与族的关系
①主族元素的价层电子排布特点
主族 ⅠA ⅡA ⅢA ⅣA
排布特点 n s 1 n s 2 n s 2 n p 1 n s 2 n p 2
主族 ⅤA ⅥA ⅦA
排布特点 n s 2 n p 3 n s 2 n p 4 n s 2 n p 5
②0族元素的价层电子排布:He为1s2;其他为ns2np6。
③过渡元素(副族和第Ⅷ族)的价层电子排布:(n-1)d1~10ns1~2。
4.元素周期表中的特殊位置
(1)按元素种类
a.分界线:沿着元素周期表中铝、锗、锑、钋与硼、硅、砷、碲、砹的交界处画一条虚线,即为金属元
素区和非金属元素区的分界线。
b.各区位置:分界线左下方为金属元素区,分界线右上方为非金属元素区。
c.分界线附近元素的性质:既表现金属元素的性质,又表现非金属元素的性质。
(2)按价层电子排布
各区价层电子排布特点分区 价层电子排布
s区 ns1~2
p区 ns2np1~6(除He外)
d区 (n-1)d1~9ns1~2(除钯外)
ds区 (n-1)d10ns1~2
f区 (n-2)f0~14(n-1)d0~2ns2
(3)过渡元素:元素周期表中从第 Ⅲ B 族到第 Ⅱ B 族10个纵列共六十多种元素,这些元素都是金属元素。
(4)镧系:元素周期表第六周期中:57号元素镧到71号元素镥共15种元素。
(5)锕系:元素周期表第七周期中:89号元素锕到103号元素铹共15种元素。
(6)超铀元素:在锕系元素中,92号元素铀(U)以后的各种元素。
5.元素周期表的三大应用
(1)科学预测:为新元素的发现及预测它们的原子结构和性质提供了线索。
(2)寻找新材料
(3)用于工农业生产
对探矿有指导意义的是地球化学元素的分布与它们在元素周期表中的位置关系,研制农药材料等。
考点二 元素周期律 电离能 电负性
1.元素周期律
2.主族元素的周期性变化规律
项目 同周期(左→右) 同主族(上→下)核电荷数 逐渐增大 逐渐增大
电子层数 相同 逐渐增多
原子
原子半径 逐渐减小 逐渐增大
结构
阳离子逐渐减小,阴离子逐渐
离子半径 逐渐增大
减小,r(阴离子)> r(阳离子)
最高正化合价由 + 1→ + 7(O、 相同,最高正化合价
化合价 F除外),负化合价= - ( 8 -主 =主族序数(O、F除
族序数 )(H为-1价) 外)
元素的金属性和非金 金属性逐渐减弱,非金属性逐 金属性逐渐增强,非
属性 渐增强 金属性逐渐减弱
性质
第一电离能 增大的趋势 逐渐减小
电负性 逐渐增大 逐渐减小
气态氢化物的稳定性 逐渐增强 逐渐减弱
最高价氧化物对应水 碱性逐渐增强,酸性
碱性逐渐减弱,酸性逐渐增强
化物的酸碱性 逐渐减弱
3.电离能
(1)第一电离能:气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,通常用I 表
1
示,单位: kJ·mol - 1 。
(2)规律
①同周期元素:从左至右第一电离能总体呈现增大的趋势。其中第ⅡA族与第ⅢA族,第ⅤA族与第ⅥA
族元素的第一电离能出现反常。
②同族元素:从上到下第一电离能逐渐变小。
③同种原子:逐级电离能越来越大。
4.电负性
(1)含义:不同元素的原子对键合电子吸引力的大小。元素的电负性越大,表示其原子对键合电子的吸引力
越大。
(2)标准:以氟的电负性为4.0 和锂的电负性为1.0 作为相对标准,计算得出其他元素的电负性(稀有气体未
计)。
(3)变化规律
①同周期元素从左至右,元素的电负性逐渐变大;
②同族元素从上至下,元素的电负性逐渐变小。
5.对角线规则
在元素周期表中,某些主族元素与右下方的主族元素有些性质是相似的,如 。1. 已知X元素是地壳中含量最多的元素,Y元素是空气中含量最多的元素,A元素与Y同主族,且是该主
族中原子序数最大的非金属元素,D元素位于周期表中第三周期,其最高氧化态可与A形成DA。下列说
3 2
法错误的是( )
A.对应酸的酸性:AX<AX
2 5 2 3
B.简单离子半径:A>Y>X>D
C.A元素的原子结构示意图:
D.非金属性:X>Y
2. W、X、Y、Z是原子序数依次增大的短周期主族元素,位于三个周期,X原子最外层电子数等于Y、Z
原子最外层电子数之和,W与Y同主族,Z的单质是一种黄色固体。下列说法正确的是( )
A.简单离子半径:Z>X>Y
B.稳定性:WZ>WX
2
C.YWZ只含有一种化学键
D.WX和YZ溶液中由水电离出的c(H+)均大于10-7
2
3. 短周期主族元素W、X、Y和Z的原子序数依次增大,W的气态氢化物的水溶液可使酚酞变红,W与X
可形成一种红棕色有刺激性气味的气体,Y的原子半径是所有短周期主族元素中最大的,Z原子最外层电
子数与W原子的电子总数相同。下列说法中正确的是( )
A.W的氧化物对应水化物均为强酸
B.简单离子半径:W<X<Y
C.简单氢化物沸点:Z<W
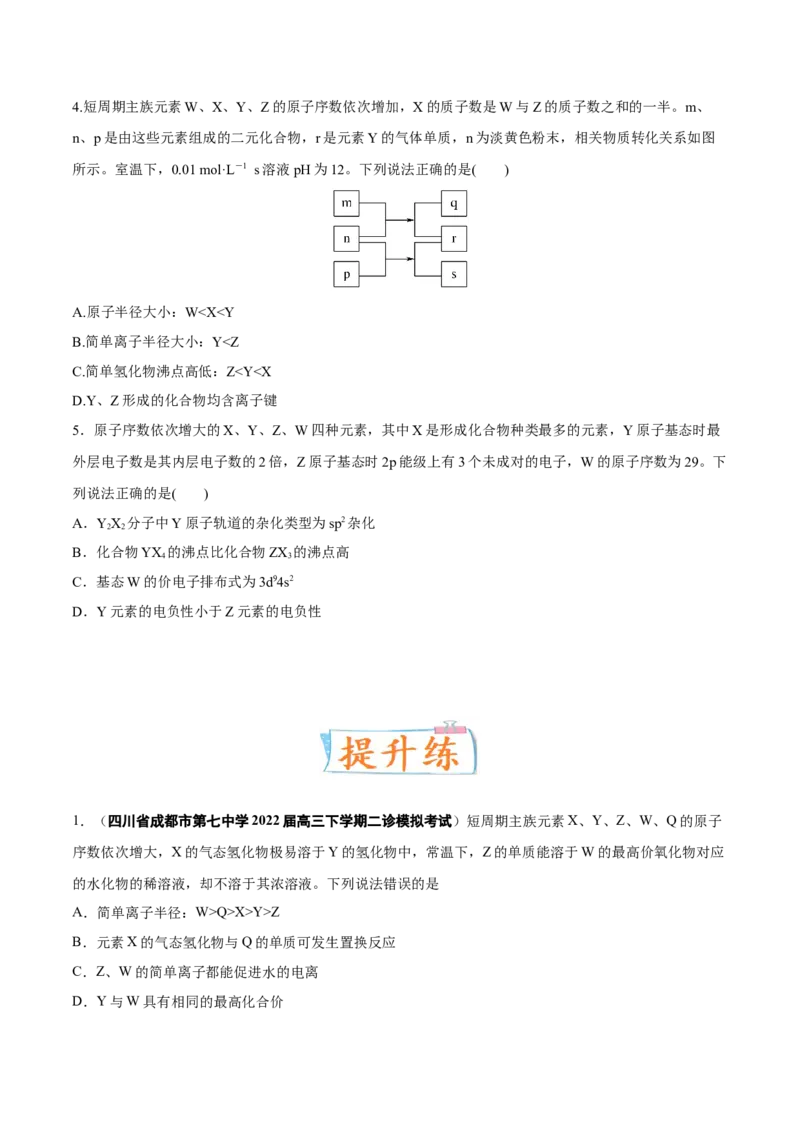
D.Y与Z形成的化合物的水溶液呈碱性4.短周期主族元素W、X、Y、Z的原子序数依次增加,X的质子数是W与Z的质子数之和的一半。m、
n、p是由这些元素组成的二元化合物,r是元素Y的气体单质,n为淡黄色粉末,相关物质转化关系如图
所示。室温下,0.01 mol·L-1 s溶液pH为12。下列说法正确的是( )
A.原子半径大小:WQ>X>Y>Z
B.元素X的气态氢化物与Q的单质可发生置换反应
C.Z、W的简单离子都能促进水的电离
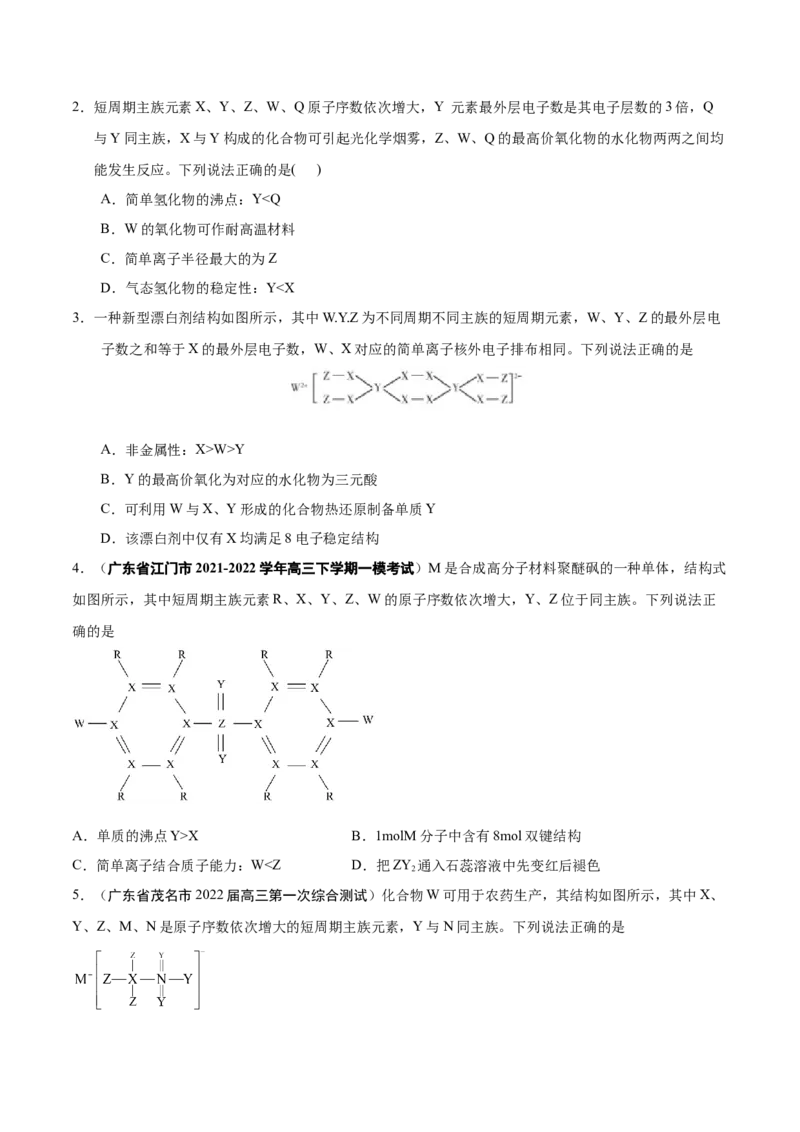
D.Y与W具有相同的最高化合价2.短周期主族元素X、Y、Z、W、Q原子序数依次增大,Y 元素最外层电子数是其电子层数的3倍,Q
与Y同主族,X与Y构成的化合物可引起光化学烟雾,Z、W、Q的最高价氧化物的水化物两两之间均
能发生反应。下列说法正确的是( )
A.简单氢化物的沸点:Y
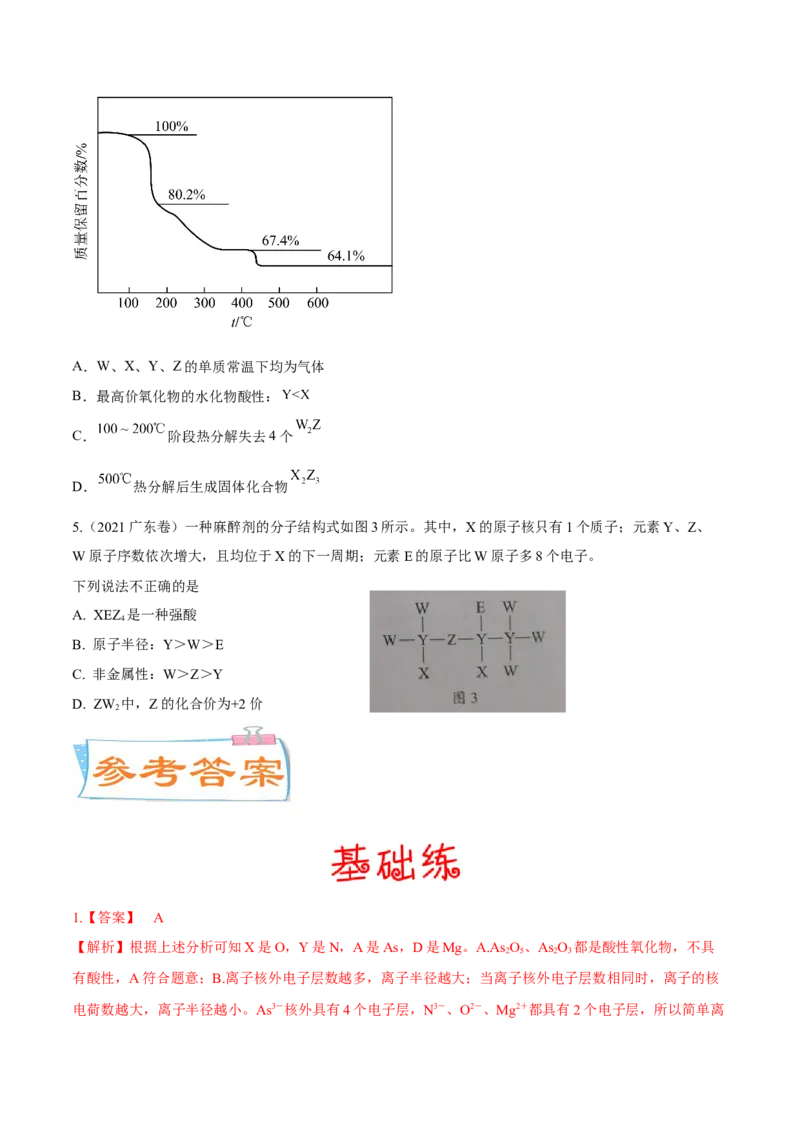
W>Y B.Y的最高价氧化为对应的水化物为三元酸 C.可利用W与X、Y形成的化合物热还原制备单质Y D.该漂白剂中仅有X均满足8电子稳定结构 4.(广东省江门市2021-2022学年高三下学期一模考试)M是合成高分子材料聚醚砜的一种单体,结构式 如图所示,其中短周期主族元素R、X、Y、Z、W的原子序数依次增大,Y、Z位于同主族。下列说法正 确的是 A.单质的沸点Y>X B.1molM分子中含有8mol双键结构 C.简单离子结合质子能力:WQ>X>Y>Z,A正确; B.N的气态氢化物为NH ,可以与Cl 发生:3Cl+2NH=N +6HCl,该反应为置换反应,B正确; 3 2 2 3 2 C.Z、W的简单离子分别为铝离子、硫离子,都可以水解,促进水的电离,C正确; D. W为S元素,Y为O元素,S的最高化合价为+6价,O不能失去最外层6个电子,没有+6价,最高 化合价不同,D错误; 故选D。 2.【答案】B 【解析】【分析】短周期主族元素X为N、Y为O、Z为Na、W为Al、Q为S; 【详解】A. Y、Q的简单氢化物分别为HO、HS,水分子间存在氢键,沸点反常,沸点HO>HS,A错 2 2 2 2 误; B. W的氧化物为氧化铝,熔点高达2000°C以上,可作耐高温材料,B正确; C. N、O、Na、Al的简单离子都是10电子,核电荷数越大,半径越小,则r(N3-)> ,氧、硫同主族,核电荷数越大,半径越大,则 ,故钠离子半 径不可能最大,C错误; D.非金属性N<O,则 气态氢化物的稳定性HO>NH ,D错误; 2 3 答案选B。 3.【答案】C 【分析】由W2+可知,W最外层有2个电子;Z形成1个键,Z是第ⅠA或ⅦA族元素;W、Y、Z的最外 层电子数之和等于X的最外层电子数,X形成2个键,X是ⅥA族元素;Z与X形成共价键,Z是H元素, X是O元素;Y是B元素;W、X对应的简单离子核外电子排布相同,W是Mg元素。【详解】A. W是镁,为金属元素,非金属性:O>B>Mg,故A错误; B. Y是B元素,B的最高价氧化为对应的水化物为HBO,HBO 中的质子无法直接电离出,HBO 结合水 3 3 3 3 3 3 中的OH-,电离出H+,HBO 是一元弱酸,故B错误; 3 3 C. 镁和B O 加热生成B和氧化镁,故C正确; 2 3 D. 该漂白剂中Mg2+、B、O均满足8电子稳定结构,故D错误。 4.【答案】C 【分析】 X构成苯环,X为C,R为H,Y能形成2条共价键,Y为O,Y、Z位于同主族,Z为S,W的原子序数比 S大且为主族元素,则W为Cl; 【详解】 分析可知,R为H,X为C,Y为O,Z为S,W为Cl; A.X为C,Y为O,C在常温下是固体,O 是气体,则单质的沸点:X>Y,A错误; 2 B.X构成的是苯环,不存在碳碳双键,只有Z=Y构成双键,则1molM分子中含有2mol双键结构,B错 误; C.盐酸是强酸,氢硫酸是二元弱酸,则硫离子结合氢离子能力比氯离子强,则简单离子结合质子的能力: W X,A错误; B.由分析可知,X为Al属于金属晶体,Y为Si属于原子晶体或共价晶体,故单质熔点Si>Al,即Y>X, B错误; C.含有氢键的物质沸点升高,由分析可知Q为N或O或F,其简单氢化物为HO或NH 或HF,Z为Cl 2 3 或S或P,其简单氢化物为HCl或HS或PH ,由于前者物质中存在分子间氢键,而后者物质中不存在, 2 3 故沸点Q>Z,C错误; D.元素的非金属性越强,其最高价含氧酸的酸性越强,P、S、Cl的非金属性均强于Si,因此最高价含氧 酸酸性:Z>Y,D正确; 故答案为:D。 4.【答案】D 【解析】化合物(YW XZ·4W Z)可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周期元素,原子序 4 5 8 2 数依次增加,且加和为21。该化合物的热重曲线如图所示,在200℃以下热分解时无刺激性气体逸出,则 说明失去的是水,即W为H,Z为O,YZ 分子的总电子数为奇数,常温下为气体,则Y为N,原子序数 2 依次增加,且加和为21,则X为B。 A.X(B)的单质常温下为固体,故A错误; B.根据非金属性越强,其最高价氧化物的水化物酸性越强,则最高价氧化物的水化物酸性:X(H BO)< 3 3 Y(HNO ),故B错误; 3 C.根据前面已知200℃以下热分解时无刺激性气体逸出,则说明失去的是水,若100~200℃阶段热分解 失去4个HO,则质量分数 ,则说明不是失去去4个HO,故C 2 2 错误; D.化合物(NH B O·4H O)在500℃热分解后若生成固体化合物XZ(B O),根据硼元素守恒,则得到关系 4 5 8 2 2 3 2 3 式2NH B O·4H O~5B O,则固体化合物B O 质量分数为 , 4 5 8 2 2 3 2 3 说明假设正确,故D正确。综上所述,答案为D。 5.【答案】B 【解析】 依题意,X的原子核只有一个质子,则X为H,由分子结构式可知,Y可形成4个共价键,Z可形成2个 共价键,W可形成一个共价键,且X、Y、Z,子序数依次增大,均位于X的下一周期,也就是第二周期, 则可推断Y为C,Z为O,W为F;元素E的原子比W原子多8个电子,则E为Cl。 故X为H,Y为C,Z为O,W为F,E为Cl。 A、Cl的非金属性强于S,则Cl的最高价氧化物(HC1O ) 对应水化物的酸性强于HSO 的酸性,则 4 2 4 HCIO,是一种强酸,A正确; B、同周期元素,原子序数越大,非金属性越强,故非金属性: W> Z>Y,B正确; C、核外电子层数不同的原子,电子层数越多,其原子半径越大,核外电子层数相同的原子,原子序数越 大,原子半径越小,故原子半径:E> Y > W,故C项错误; D、ZW 为OF ,F的非金属性强于O的,F在化合物中一般显-1价,故O的化合价为+2价,D正确。 2 2 故答案为C。