文档内容
考向 16 化学键
【2022·湖南卷】下列说法错误的是
A.氢键,离子键和共价键都属于化学键
B.化学家门捷列夫编制了第一张元素周期表
C.药剂师和营养师必须具备化学相关专业知识
D.石灰石是制造玻璃和水泥的主要原料之一
【答案】A
【解析】A.离子键和共价键都属于化学键,氢键属于分子间作用力,A说法错误;
B.第一张元素周期表是俄国化学家门捷列夫编制的,B说法正确;
C.药剂师和营养师的工作分别与药剂和营养物质有关,因此必须具备相关的化学专业知识才能胜任相关
工作,C说法正确;
D.制造玻璃的主要原料是石灰石、石英和纯碱,制造水泥的主要原料是石灰石和黏土,D说法正确;
综上所述,本题选A。1.化学键
(1)概念
使离子相结合或原子相结合的作用力。
(2)分类
2.离子键、共价键的比较
共价键
离子键
非极性键 极性键
带相反电荷的离子之
概念 原子间通过共用电子对所形成的相互作用
间的相互作用
成键微粒 阴、阳离子 原子
阴、阳离子的静电作 共用电子对不偏向任何一
成键实质 共用电子对偏向一方原子
用 方
非金属性强的元素与
形成条件 金属性强的元素经得 同种元素原子之间成键 不同种元素原子之间成键
失电子,形成离子键
形成的 非金属单质;某些共价化
离子化合物 共价化合物或离子化合物
物质 合物或离子化合物
3.离子化合物与共价化合物
4.化学键与物质类别的关系
(1)除稀有气体内部无化学键外,其他物质内部都存在化学键。
(2)只含有极性共价键的物质一般是不同种非金属元素原子形成的共价化合物,如SiO、HCl、CH 等。
2 4
(3)只含有非极性共价键的物质是同种非金属元素原子形成的单质,如Cl、P、金刚石等。
2 4(4)既有极性键又有非极性键的共价化合物一般由多个原子组成,如HO、C H 等。
2 2 2 4
(5)只含离子键的物质主要是由活泼非金属元素与活泼金属元素形成的化合物,如NaS、CaCl 、NaCl
2 2
等。
(6)既有离子键又有极性共价键的物质,如NaOH、KSO 等;既有离子键又有非极性共价键的物质,
2 4
如NaO 等。
2 2
(7)仅由非金属元素形成的离子化合物,如NH Cl、NH NO 等。
4 4 3
(8)金属元素和非金属元素间可能存在共价键,如AlCl 等。
3
5.物质的溶解或熔化与化学键变化的关系
(1)离子化合物的溶解或熔化过程
离子化合物溶于水或熔化后均电离成自由移动的阴、阳离子,离子键被破坏。
(2)共价化合物的溶解过程
①有些共价化合物溶于水后,能与水反应,其分子内的共价键被破坏,如CO 和SO 等。
2 2
②有些共价化合物溶于水后,发生电离,其分子内的共价键被破坏,如HCl、HSO 等。
2 4
③有些共价化合物溶于水后,其分子内的化学键不被破坏,如蔗糖(C H O )、酒精(C HOH)等。
12 22 11 2 5
(3)单质的溶解过程
某些活泼的非金属单质溶于水后,能与水反应,其分子内的共价键被破坏,如Cl、F 等。
2 2
6.化学键对物质性质的影响
(1)对物理性质的影响
金刚石、晶体硅、石英、金刚砂等物质硬度大、熔点高,就是因为其中的共价键很强,破坏时需消耗
很多的能量。NaCl等部分离子化合物,也有很强的离子键,故熔点也较高。
(2)对化学性质的影响
N 分子中有很强的共价键,故在通常状况下,N 很稳定;HS、HI等分子中的共价键较弱,故它们受
2 2 2
热时易分解。
7.电子式
(1)概念
在元素符号周围,用“·”或“×”来表示原子的 最外层电子 ( 价电子 )的式子。
(2)书写方法(3)电子式书写的四大误区
(4)书写示例CaCl 。
2
8.分子间作用力和氢键
(1)分子间作用力
定义 把分子聚集在一起的作用力,又称范德华力
①分子间作用力比化学键得多,它主要影响物质的熔点、沸点等物理性质,
而化学键主要影响物质的化学性质
特点 ②分子间作用力存在于由共价键形成的多数共价化合物和绝大多数气态、液
态、固态非金属单质分子之间。但像二氧化硅、金刚石等由共价键形成的物
质,微粒之间不存在分子间作用力
一般来说,对于组成和结构相似的物质,相对分子质量越大,分子间作用力
变化规律
越大,物质的熔、沸点也越高。例如,熔、沸点:IBr ClF
2 2 2 2
(2)氢键
定义 分子间存在的一种比分子间作用力稍强的相互作用
形成条件 除H外,形成氢键的原子通常是 O 、 F 、 N
氢键存在广泛,如蛋白质分子、醇、羧酸分子、HO、NH 、HF等分
存在 2 3
子之间。分子间氢键会使物质的熔点和沸点升高
①存在氢键的物质,其熔、沸点明显高于同族同类物质。如HO的
2
熔、沸点高于HS
2
②氨气极易液化,是因为液氨分子间存在氢键;NH 极易溶于水,也
性质影响 3
是因为NH 分子与HO分子间易形成氢键
3 2
③水结冰时体积膨胀、密度减小,是因为在固态水(冰)中水分子间以
氢键结合成排列规整的晶体1.下列物质中,既属于离子化合物又属于电解质且含有极性键的是( )
A.NaO B.HSO
2 2 2 4
C.CS D.BaSO
2 4
2.利用固体表面催化工艺进行NO分解的过程如图所示。下列说法不正确的是( )
A.NO属于共价化合物
B.O 含有非极性共价键
2
C.过程②吸收能量,过程③释放能量
D.标准状况下,NO分解生成11.2 L N 转移电子数为N
2 A
3.人们从冰箱中取出的“常态冰”仅是冰存在的多种可能的形式之一。目前,科学家发现了一种全
新的多孔、轻量级的“气态冰”,可形成气凝胶。下列有关说法正确的是( )
A.“常态冰”和“气态冰”结构不同,是同素异形体
B.“气态冰”因其特殊的结构而具有比“常态冰”更活泼的化学性质
C.18 g“气态冰”的体积为22.4 L
D.构成“气态冰”的分子中含有极性共价键
4.下表中相关物质的信息都正确的一项是( )
与性质相对应
选项 化学式 电子式或含有的化学键类型 物质的性质
的用途
A NaClO 离子键、共价键 强氧化性 消毒剂
不稳定,易
B HO 医用消毒剂
2 2 分解水溶液呈弱
C NH 共价键 工业制硝酸
3 碱性
D NaHCO 离子键 受热易分解 泡沫灭火器
3
5.下列叙述正确的是( )
A.24 g镁与27 g铝中含有相同的质子数
B.常温常压下,1.12 L丙烷分子中所含非极性键数目为0.1N
A
C.1 mol重水(D O)与1 mol水(H O)中,中子数之比为5∶4
2 2
D.1 mol乙烷和1 mol乙烯中,化学键数目相同
1.(2022·河南·高三开学考试)月壤中含有丰富的3He,3He发生核聚变反应为:
3He+3He→4He+2mX+12.86MeV,可控核聚变提供人类生产生活所需能量是能源发展的重要方向。下列说法
正确的是
A.3He核聚变是化学变化 B.3He与4He互为同位素
C.mX的中子数为1 D.3He、4He形成的单质中均含有共价键
2.(2022·江苏南京·高三阶段练习)双氧水和“84”消毒液两者混合时可发生反应:
NaClO+H O=NaCl+HO+O↑。下列有关说法不正确的是
2 2 2 2
A.NaO 中含有非极性共价键 B.NaClO 的电子式为
2 2
C.HO 中O元素的化合价为-1 D.HO的空间构型为直线形
2 2 2
3.(2022·河南·模拟预测)四氟肼可发生反应: ,下列有关叙述错误的是
A. 的氧化性比 的强 B. 的电子式为
C. 中既含极性键又含非极性键 D. 在水溶液中的电离方程式为
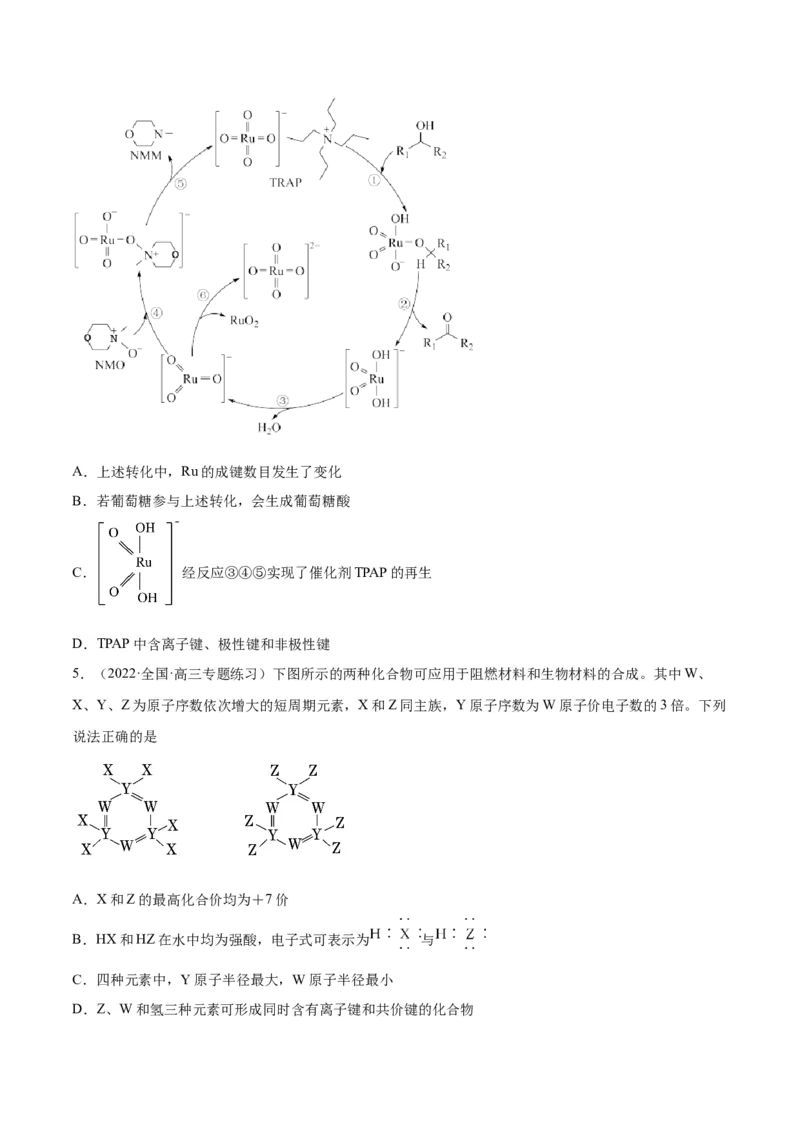
4.(2022·陕西西安·高三开学考试)在有机合成化学中,Ley-Griffith氧化法是众多将醇氧化成醛(或酮)的
方法中的一种,Ley-Griffith氧化又称为TPAP氧化,TPAP是一种高选择性氧化剂,不氧化碳碳双键或醛基。
某醇的Ley-Griffith氧化历程如图。下列说法错误的是A.上述转化中,Ru的成键数目发生了变化
B.若葡萄糖参与上述转化,会生成葡萄糖酸
C. 经反应③④⑤实现了催化剂TPAP的再生
D.TPAP中含离子键、极性键和非极性键
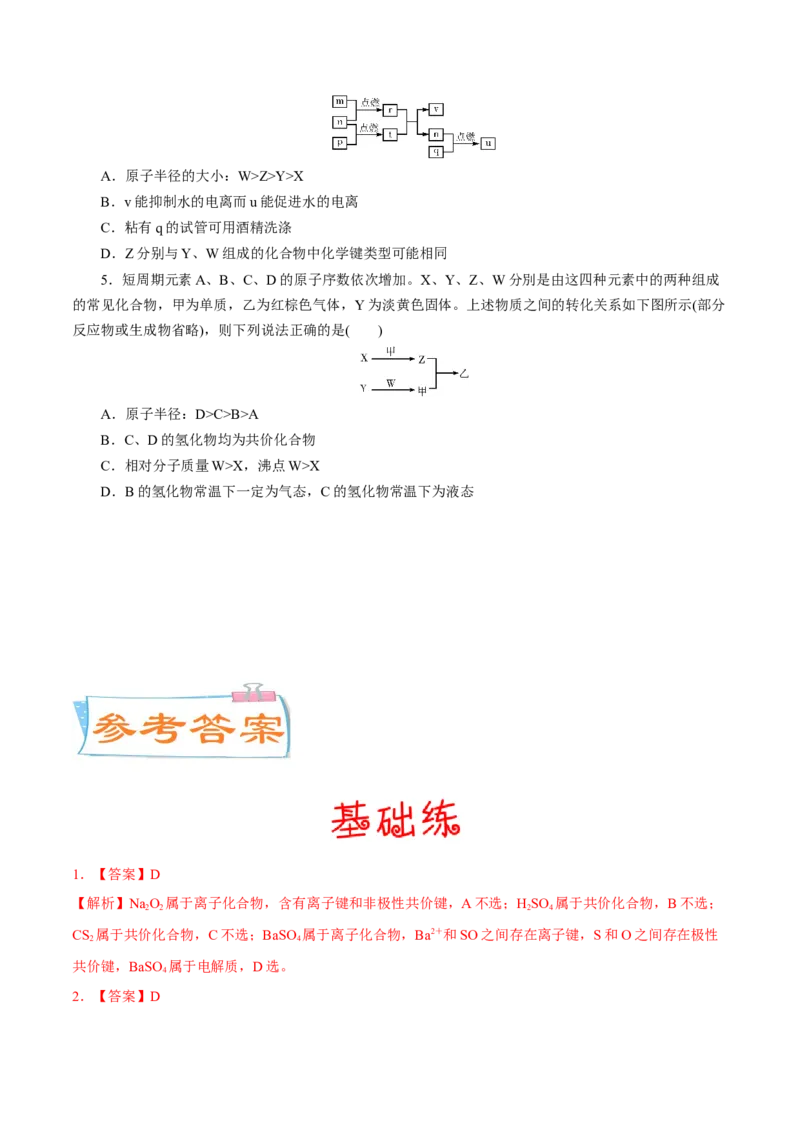
5.(2022·全国·高三专题练习)下图所示的两种化合物可应用于阻燃材料和生物材料的合成。其中W、
X、Y、Z为原子序数依次增大的短周期元素,X和Z同主族,Y原子序数为W原子价电子数的3倍。下列
说法正确的是
A.X和Z的最高化合价均为+7价
B.HX和HZ在水中均为强酸,电子式可表示为 与
C.四种元素中,Y原子半径最大,W原子半径最小
D.Z、W和氢三种元素可形成同时含有离子键和共价键的化合物1. (2022山东) 、 的半衰期很短,自然界中不能稳定存在。人工合成反应如下:
; 。下列说法正确的是
A. X的中子数为2
为
B. X、Y互 同位素
C. 、 可用作示踪原子研究化学反应历程
D. 自然界不存在 、 分子是因其化学键不稳定
2.(2021·湖南)W、X、Y、Z为原子序数依次增大的短周期主族元素,Y的原子序数等于W与X的原子序数
之和,Z的最外层电子数为K层的一半,W与X可形成原子个数比为2∶1的18e-分子。下列说法正确的是(
)
A.简单离子半径:Z>X>Y
B.W与Y能形成含有非极性键的化合物
C.X和Y的最简单氢化物的沸点:X>Y
D.由W、X、Y三种元素所组成化合物的水溶液均显酸性
3.(2021·全国乙理综)我国嫦娥五号探测器带回1.731 kg的月球土壤,经分析发现其构成与地球土壤类似。土
壤中含有的短周期元素W、X、Y、Z,原子序数依次增大,最外层电子数之和为15。X、Y、Z为同周期相邻
元素,且均不与W同族。下列结论正确的是 ( )
A.原子半径大小顺序为W>X>Y>Z
B.化合物XW中的化学键为离子键
C.Y单质的导电性能弱于Z单质的
D.Z的氧化物的水化物的酸性强于碳酸
4.短周期主族元素X、Y、Z、W的原子序数依次增大。四种元素形成的单质依次为m、n、p、q;这
些元素组成的二元化合物为r、t、u,其中u为形成酸雨的主要物质之一;25 ℃时,0.01 mol·L-1的v溶液
中pH=12。上述物质的转化关系如下图所示。下列说法正确的是( )A.原子半径的大小:W>Z>Y>X
B.v能抑制水的电离而u能促进水的电离
C.粘有q的试管可用酒精洗涤
D.Z分别与Y、W组成的化合物中化学键类型可能相同
5.短周期元素A、B、C、D的原子序数依次增加。X、Y、Z、W分別是由这四种元素中的两种组成
的常见化合物,甲为单质,乙为红棕色气体,Y为淡黄色固体。上述物质之间的转化关系如下图所示(部分
反应物或生成物省略),则下列说法正确的是( )
A.原子半径:D>C>B>A
B.C、D的氢化物均为共价化合物
C.相对分子质量W>X,沸点W>X
D.B的氢化物常温下一定为气态,C的氢化物常温下为液态
1.【答案】D
【解析】NaO 属于离子化合物,含有离子键和非极性共价键,A不选;HSO 属于共价化合物,B不选;
2 2 2 4
CS 属于共价化合物,C不选;BaSO 属于离子化合物,Ba2+和SO之间存在离子键,S和O之间存在极性
2 4
共价键,BaSO 属于电解质,D选。
4
2.【答案】D【解析】只含有共价键的化合物是共价化合物,NO属于共价化合物,A正确;同种非金属元素原子之间
形成非极性键,所以O 含有非极性共价键,B正确;由图可知,过程②NO中化学键发生断裂形成氮原子
2
和氧原子,此过程需要吸收能量,过程③形成了新的化学键N≡N键和O===O键,此过程释放能量,C正
确;根据方程式2NO===N +O,每生成1 mol氮气,转移的电子数为4 mol,生成11.2 L N(标准状况下),
2 2 2
即0.5 mol N 时,转移电子数为2N ,D错误。
2 A
3. 【答案】D
【解析】 “常态冰”和“气态冰”是水的不同存在形式,状态不同,但属于同种物质,同素异形体是针
对单质而言的,A错误;“常态冰”和“气态冰”是水的不同存在形式,物理性质不同,但化学性质相同,
B错误;“气态冰”是形成气凝胶的冰,且不知物质所处状态,不能利用标准状况下的气体摩尔体积计算
其体积,C错误;“气态冰”的分子是HO,其分子中含有极性共价键,D正确。
2
4. 【答案】A
【解析】NaClO中钠离子和次氯酸根离子之间存在离子键,O、Cl原子之间存在共价键,次氯酸钠具有强
氧化性,所以可作消毒剂,A正确;HO 是共价化合物,电子式为 ,HO 具有强氧化性,
2 2 2 2
可用于消毒,B错误;NH 在工业上用于制取硝酸是利用其还原性,与其水溶液呈碱性无关,C错误;碳
3
酸氢钠中既存在离子键又存在共价键,碳酸氢钠可与铝离子发生双水解反应生成二氧化碳,故可用于灭火,
与其稳定性强弱无关,D错误。
5. 【答案】C
【解析】24 g镁与27 g铝中含有的质子数分别是12N 和13N ,A错误;丙烷中的C—C键为非极性键,但
A A
常温常压下,无法用标准状况下气体摩尔体积计算丙烷的物质的量,B错误;每个重水(D O)分子含有10
2
个中子,每个水(H O)分子含有8个中子,所以1 mol重水(D O)与1 mol 水(H O)中的中子数之比为10∶8
2 2 2
=5∶4,C正确;乙烷结构简式为CHCH,每个分子中有7个共价键;乙烯结构简式为CH===CH ,每
3 3 2 2
个分子中有4个C—H键和1个C===C键,所以1 mol乙烷和1 mol乙烯中化学键数目不相同,D错误。
1.【答案】B
【详解】A.核聚变时原子种类发生变化,不存在旧键的断裂和新建的形成,不属于化学变化,A错误;
B. 与 是 元素的不同原子,互为同位素,B正确;C.根据守恒可得, 是 , 的中子数是0,C错误;
D. 与 都是单原子分子,无共价键,D错误;
答案选B。
2. 【答案】D
【详解】A.NaO 中O与O之间存在非极性共价键,A项正确;
2 2
B.根据次氯酸结构H-O-Cl,故NaClO 的电子式为 ,B项正确;
C.HO 中O元素的化合价为-1,C项正确;
2 2
D.HO中心原子sp3杂化,有2对孤电子对,空间构型为V形,D项错误;
2
答案选D。
3. 【答案】B
【详解】A.反应中 作氧化剂,氧气是氧化产物,所以 的氧化性比 的强,正确;
B. 中氟原子周用应满足 结构,电子式为 ,B错误。
C. 的电子式为 ,其中既含极性键又含非极性键,C正确;
D. 是一元弱酸,在水溶液中的电离方程式为 ,D正确;
答案选B。
4. 【答案】B
【详解】A.根据图示,反应①中Ru的成键数目由6变为7,故A正确;
B.TPAP是一种高选择性氧化剂,不氧化醛基,若葡萄糖参与上述转化,不会生成葡萄糖酸,故B错误;
C.根据图示, 经反应③④⑤实现了催化剂TPAP的再生,故C正确;
D.TPAP由阴阳离子构成,含有离子键,阴离子中C-H、C-C碱,故D正确;
选B。
5. 【答案】D【解析】W、X、Y、Z为原子序数依次增大的短周期元素,X和Z同主族,由原子序数可知,X处于第二
周期、Z处于第三周期,结构式中X、Z都形成1个共价键,则X为F元素、Z为Cl元素;Y形成5个共
价键,W形成3个共价键,W原子的价电子数为5,Y原子序数为W原子价电子数的3倍,则Y为P,W
为N元素。由分析可知,W为N,X为F,Y为P,Z为Cl元素;
A.氯的最高化合价为+7价,但氟的非金属性最强,F只有-1、0两种价态,没有最高正价+7价,A错误;
B.HCl为强酸,HF为弱酸,B错误;
C.同周期主族元素从左向右原子半径减小,一般电子层越多原子半径越大,四种元素原子半径由大到小
的顺序为P>Cl>N>F,即Y>Z>W>X,C错误;
D.Cl、N、H三种元素可形成离子化合物NH Cl,其既含有离子键又含有共价键,D正确;
4
故选:D。
1. 【答案】B
【解析】根据质量守恒可知,X微粒为 ,Y微粒为 ,据此分析解题。
A. 由分析可知,X微粒为 ,根据质量数等于质子数加中子数可知,该微粒的中子数为4,A错误;
B. 由分析可知,X微粒为 ,Y微粒为 ,二者具有相同的质子数而不同的中子数的原子,故互为
同位素,B正确;
C.由题干信息可知, 与 的半衰期很短,故不适宜用作示踪原子研究化学反应历程,C错误;
D.自然界中不存在 与 并不是其化学键不稳定,而是由于 与 的半衰期很短,很容易发生核
变化,转化为气体其他原子,O=O的键能与形成该键的核素无关,D错误;
故答案为:B。
2. 【答案】B
【解析】本题考查了元素推断和元素周期律的应用。首先根据“Z的最外层电子数为K层的一半”可推知
满足该条件的短周期元素有钠元素和锂元素,再依据“W、X、Y、Z为原子序数依次增大的短周期主族元
素”可排除锂元素,则Z为钠元素。再依据“W与X可形成原子个数比为2∶1的18e-分子”可推知,W为氢
元素,X为氮元素,二者所形成的18e-分子为肼(N H)。最后依据“Y的原子序数等于W与X的原子序数之
2 4和”可确定Y为氧元素。Na+、N3-和O2-具有相同的核外电子排布,根据“径小序大”规律可知,离子半径大
小顺序为N3->O2->Na+,A项错误;氢和氧可形成HO,其结构式为H—O—O—H,其中含有非极性键,B项正确;
2 2
氮元素、氧元素形成的最简单的氢化物分别为氨气和水,水的沸点高于液氨,C项错误;NH·H O由氢、氮、
3 2
氧三种元素组成,其水溶液呈碱性,D项错误。
3. 【答案】B
【解析】根据题干中有关W、X、Y、Z原子结构的信息,并结合对地球土壤中的元素组成的初步认识,可推
断出X、Y、Z分别为第三周期的Mg、Al、Si,W为O。O、Mg、Al、Si的原子半径大小顺序为
X>Y>Z>W(Mg>Al>Si>O),A项错误;化合物XW(MgO)中的化学键是离子键,B项正确;Y(Al)单质的导电性强
于Z(Si)单质的导电性,C项错误;Z的氧化物的水化物(硅酸或原硅酸)的酸性弱于碳酸的酸性,D项错误。
4. 【答案】D
【解析】短周期主族元素X、Y、Z、W的原子序数依次增大。四种元素形成的单质依次为m、n、p、q,
r、t、u是这些元素组成的二元化合物,其中u为形成酸雨的主要物质之一,u为SO ;25 ℃时,0.01 mol/L
2
的v溶液中pH=12,则v为NaOH,结合图中转化可知,m为H,n为O,p为Na,r为HO,t为
2 2 2
NaO,则X、Y、Z、W分别为H、O、Na、S,q为S单质。
2 2
5.【答案】C
【解析】Y是短周期元素形成的二元化合物,由其状态与颜色知其是NaO,由乙的状态及颜色知其是
2 2
NO ,Z与单质甲反应得到NO ,故甲是氧气,Z是NO,化合物X是NH ,W是水,故A、B、C、D依次
2 2 3
为H、N、O、Na。氮的原子半径大于氧的原子半径,A错误;NaH是离子化合物,B错误;相对分子质量:
HO>NH ,水常温下是液体,NH 的沸点比HO的低,C正确;肼(N H)在常温下是液体,D错误。
2 3 3 2 2 4