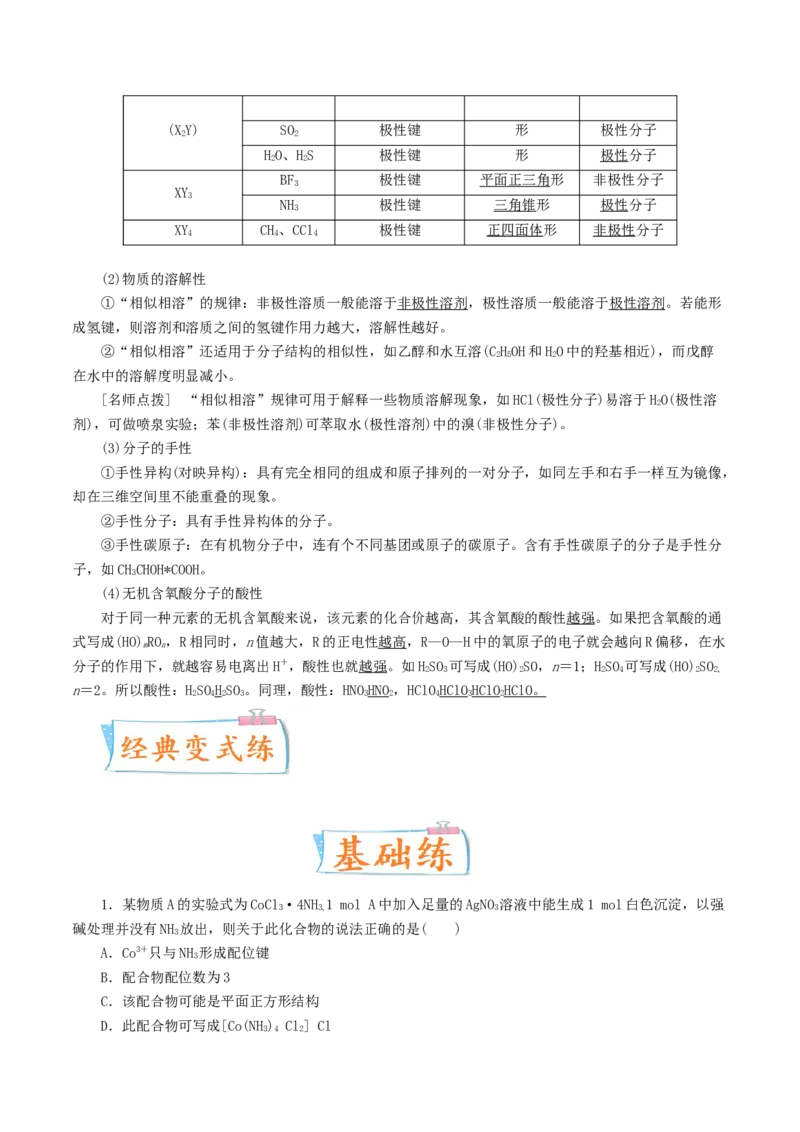
文档内容
考向 17 分子结构与性质
【2022·浙江卷6月】回答下列问题:
(1)乙醇的挥发性比水的强,原因是_______。
(2)金属氢化物是应用广泛的还原剂。KH的还原性比NaH的强,原因是_______。
【答案】(1)乙醇分子间形成氢键的数量比水分子间形成氢键的数量少,分子间作用力小
(2)Na+半径小于K+,Na+与H—的离子键作用强,H—更难失电子,还原性更弱
【解析】(1)乙醇和水均可形成分子晶体,且其均可形成分子间氢键,但是,水分子中的2个H均可参与形
成氢键,而乙醇分子中只有羟基上的1个H可以参与形成氢键,故水分子间形成氢键的数量较多,水分子
间的作用力较大,水的沸点较高而乙醇的沸点较低。因此,乙醇的挥发性比水的强的原因是:乙醇分子间
形成氢键的数量比水分子间形成氢键的数量少,分子间作用力小。
(2)KH和NaH均可形成离子晶体,Na+半径小于K+,故NaH的晶格能较大,Na+与H—的离子键作用较强,
其中的H—更难失电子、还原性更弱,因此,KH的还原性比NaH的强的原因是:Na+半径小于K+,Na+与
H—的离子键作用强,H—更难失电子,还原性更弱。知识点一 共价键
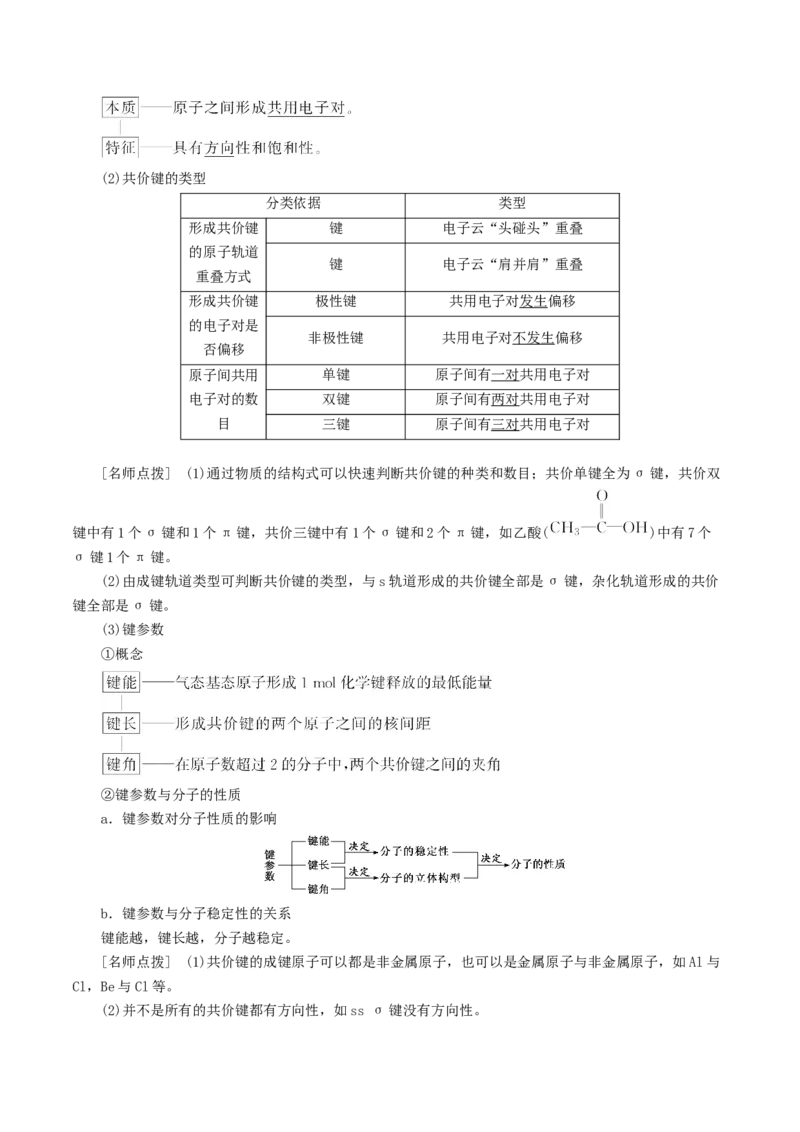
1.共价键
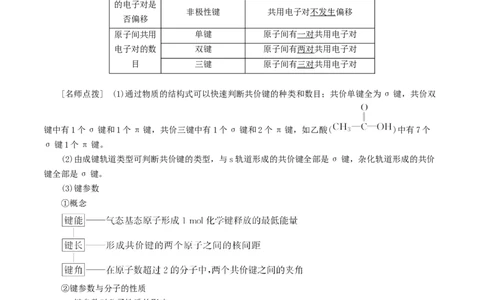
(1)共价键的本质与特征(2)共价键的类型
分类依据 类型
形成共价键 键 电子云“头碰头”重叠
的原子轨道
键 电子云“肩并肩”重叠
重叠方式
形成共价键 极性键 共用电子对发生偏移
的电子对是
非极性键 共用电子对不发生偏移
否偏移
原子间共用 单键 原子间有一对共用电子对
电子对的数 双键 原子间有两对共用电子对
目 三键 原子间有三对共用电子对
[名师点拨] (1)通过物质的结构式可以快速判断共价键的种类和数目;共价单键全为σ键,共价双
键中有1个σ键和1个π键,共价三键中有1个σ键和2个π键,如乙酸( )中有7个
σ键1个π键。
(2)由成键轨道类型可判断共价键的类型,与s轨道形成的共价键全部是σ键,杂化轨道形成的共价
键全部是σ键。
(3)键参数
①概念
②键参数与分子的性质
a.键参数对分子性质的影响
b.键参数与分子稳定性的关系
键能越,键长越,分子越稳定。
[名师点拨] (1)共价键的成键原子可以都是非金属原子,也可以是金属原子与非金属原子,如Al与
Cl,Be与Cl等。
(2)并不是所有的共价键都有方向性,如ss σ键没有方向性。(3)共价分子中原子间的键能越大,键长越短,分子的稳定性越强。如稳定性:HF>HCl>HBr>HI。
2.配位键
(1)孤电子对
分子或离子中没有跟其他原子共用的电子对称孤电子对。
(2)配位键
①配位键的形成:成键原子一方提供孤电子对,另一方提供空轨道形成共价键。
②配位键的表示:常用“→”来表示配位键,箭头指向接受孤电子对的原子,如NH可表示为
在NH中,虽然有一个N—H键形成过程与其他3个N—H键形成过程不同,但是一
旦形成之后,4个共价键就完全相同。
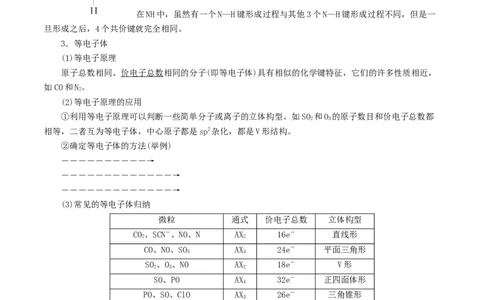
3.等电子体
(1)等电子原理
原子总数相同、价电子总数相同的分子(即等电子体)具有相似的化学键特征,它们的许多性质相近,
如CO和N。
2
(2)等电子原理的应用
①利用等电子原理可以判断一些简单分子或离子的立体构型。如SO 和O 的原子数目和价电子总数都
2 3
相等,二者互为等电子体,中心原子都是sp2杂化,都是V形结构。
②确定等电子体的方法(举例)
――――――――――→
―――――――――――――→
―――――――――――――→
(3)常见的等电子体归纳
微粒 通式 价电子总数 立体构型
CO、SCN-、NO、N AX 16e- 直线形
2 2
CO、NO、SO AX 24e- 平面三角形
3 3
SO、O、NO AX 18e- V形
2 3 2
SO、PO AX 32e- 正四面体形
4
PO、SO、ClO AX 26e- 三角锥形
3
CO、N AX 10e- 直线形
2
CH、NH AX 8e- 正四面体形
4 4
[名师点拨] 寻找等电子体的三种方法
变换过程中注意电荷变化,并伴有元素种类的改变
序号 方法 示例竖换:把同族元素(同族原子价电子数相
CO 与CS
2 2
1 同)上下交换, 即可得到相应的等电子
O 与SO
3 2
体
横换:换相邻主族元素,这时候价电子
2 发生变化,再通过得失电子使价电子总 N 与CO
2
数相等
O 与NO
3
可以将分子变换为离子,也可以将离子
3 CH 与NH
4
变换为分子
CO与CN-
知识点二 分子的立体构型
1.价层电子对互斥理论
(1)理论要点
①价层电子对在空间上彼此相距最远时,排斥力最小,体系的能量最低。
②孤电子对越多,排斥力越强,键角越小。
(2)判断分子或离子立体构型“三步骤”
第一步:确定中心原子上的价层电子对数
a为中心原子的价电子数,b为与中心原子结合的原子最多能接受的电子数,x为与中心原子结合的原
子数。如NH 的中心原子为N,a=5,b=1,x=3,所以中心原子上的孤电子对数=(a-xb)=×(5-3×1)
3
=1。
第二步:确定价层电子对的立体构型
由于价层电子对之间的相互排斥作用,使它们尽可能地相互远离,这样已知价层电子对的数目,就可
以确定它们的立体构型。
第三步:分子立体构型的确定
价层电子对有成键电子对和孤电子对之分,价层电子对的总数减去成键电子对数得孤电子对数。根据
成键电子对数和孤电子对数,可以确定相应的较稳定的分子立体构型。
(3)实用实例
价层电 σ键电 孤电子 价层电子对 分子立
实例
子对数 子对数 对数 立体构型 体构型
2 2 0 直线形 直线形 CO
2
3 0 平面三角形 BF
3
3 平面三角形
2 1 V 形 SO
2
4 0 正四面体形 CH
4
4 3 1 四面体形 三角锥形 NH
3
2 2 V形 HO
22.杂化轨道理论
(1)杂化轨道理论概述
当原子成键时,原子的价电子轨道相互混杂,形成与原轨道数相等且能量相同的杂化轨道。杂化轨道
数不同,轨道间的夹角不同,形成分子的空间结构不同。
(2)杂化轨道三种类型
(3)由杂化轨道数判断中心原子的杂化类型
杂化轨道用来形成σ键和容纳孤电子对,所以有公式:杂化轨道数=中心原子的孤电子对数+中心原
子的σ键个数。
[名师点拨] (1)价层电子对互斥理论说明的是价层电子对的立体构型,而分子的立体构型指的是成
键电子对的立体构型,不包括孤电子对。
①当中心原子无孤电子对时,两者的构型一致;
②当中心原子有孤电子对时,两者的构型不一致。如中心原子采取sp3杂化的,其价层电子对模型为
四面体形,其分子构型可以为正四面体形(如CH),也可以为三角锥形(如NH)或V形(如HO)。
4 3 2
(2)杂化轨道间的夹角与分子内的键角不一定相同,中心原子杂化类型相同时孤电子对数越多,键角
越小。
3.配合物
(1)定义:金属离子(或原子)与某些分子或离子(称为配体)以配位键结合形成的化合物。
(2)形成条件
(3)组成
[名师点拨] 1 mol[Ti(HO)Cl]Cl·HO的配合物只能电离出2 mol Cl-
2 5 2 2
知识点三 分子间作用力与分子的性质
1.分子间作用力
(1)概念:物质分子之间普遍存在的相互作用力,称为分子间作用力。
(2)分类:分子间作用力最常见的是范德华力和氢键。
(3)强弱:范德华力氢键化学键。
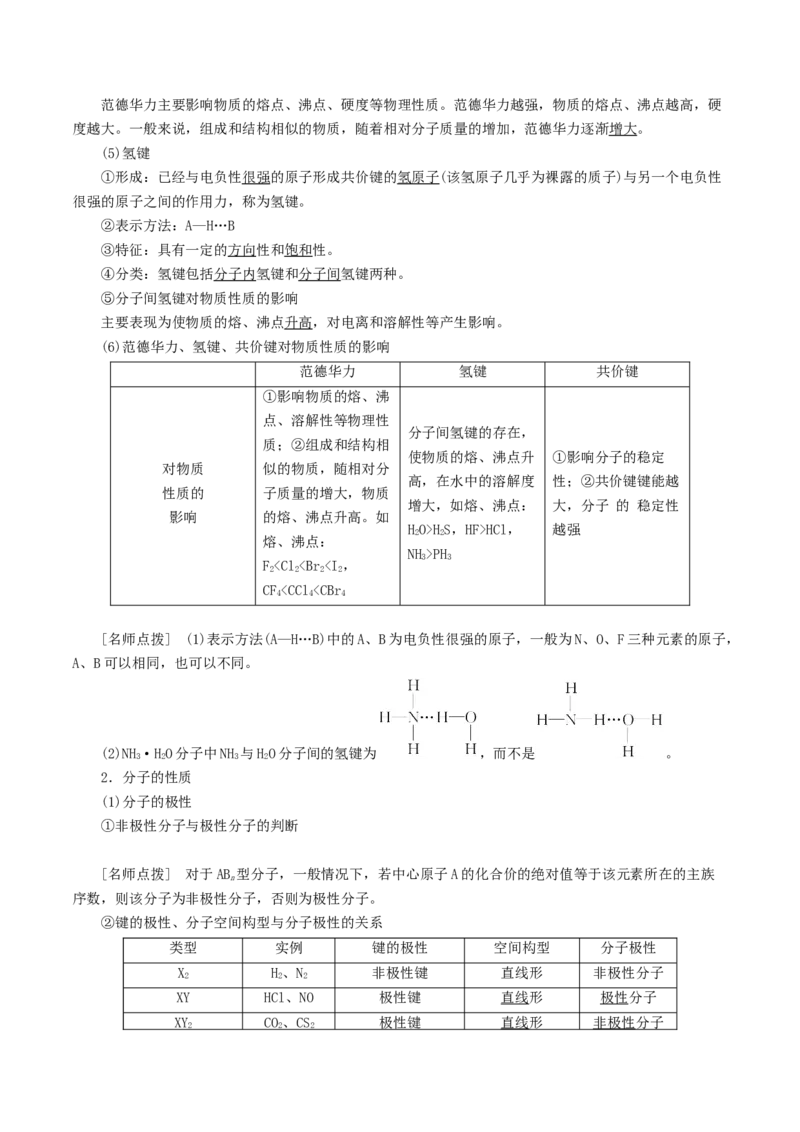
(4)范德华力范德华力主要影响物质的熔点、沸点、硬度等物理性质。范德华力越强,物质的熔点、沸点越高,硬
度越大。一般来说,组成和结构相似的物质,随着相对分子质量的增加,范德华力逐渐增大。
(5)氢键
①形成:已经与电负性很强的原子形成共价键的氢原子(该氢原子几乎为裸露的质子)与另一个电负性
很强的原子之间的作用力,称为氢键。
②表示方法:A—H…B
③特征:具有一定的方向性和饱和性。
④分类:氢键包括分子内氢键和分子间氢键两种。
⑤分子间氢键对物质性质的影响
主要表现为使物质的熔、沸点升高,对电离和溶解性等产生影响。
(6)范德华力、氢键、共价键对物质性质的影响
范德华力 氢键 共价键
①影响物质的熔、沸
点、溶解性等物理性
分子间氢键的存在,
质;②组成和结构相
使物质的熔、沸点升 ①影响分子的稳定
对物质 似的物质,随相对分
高,在水中的溶解度 性;②共价键键能越
性质的 子质量的增大,物质
增大,如熔、沸点: 大,分子 的 稳定性
影响 的熔、沸点升高。如
HO>HS,HF>HCl, 越强
2 2
熔、沸点:
NH>PH
3 3
FCH —CH。
3 3 3 3 3 3
5.【答案】(1)[Ar]3d64s2或1s22s22p63s23p63d64s2 O
(2)sp3 N>O>C (3)CH 或SiH (4)7
4 4
【解析】(1)Fe为26号,价电子数为26-18=8,在4s轨道上填充2个电子,在3d轨道上填充6个电子,
则Fe的核外电子排布为[Ar]3d64s2。
[Fe(HO)]2+中O原子有孤电子对,可以填入Fe2+的空轨道中,即O为配位原子。(2)NH 中,N有一
2 6 3
对孤电子对,价层电子对为1+3=4,则N为sp3杂化。N的最外层电子排布为2s22p3,p轨道中的电子为
半满的稳定状态,很难失去电子,故N的第一电离能比相邻的O元素要大,C的半径大,相对于O原子而
言,C易失去电子,则C的第一电离能小于O。(3)NH中,N失去一个电子为C,则CH 与NH互为等
4
电子体。(4)—COOH中,C与O形成双键以及C与O形成单键,1 mol—COOH中含有2 mol σ键,C与
羟基相连为单键,为一个σ键,所以1 mol柠檬酸中碳与氧共有7 mol σ键。