文档内容
考向 18 晶体结构与性质
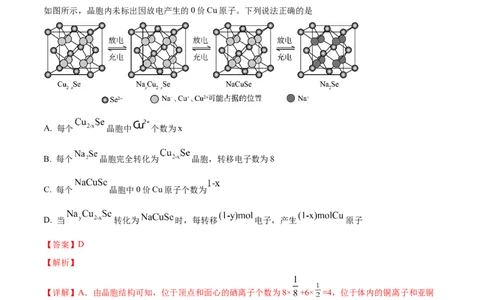
【2022·山东】 是一种钠离子电池正极材料,充放电过程中正极材料立方晶胞(示意图)的组成变化
如图所示,晶胞内未标出因放电产生的0价Cu原子。下列说法正确的是
A. 每个 晶胞中 个数为x
B. 每个 晶胞完全转化为 晶胞,转移电子数为8
C. 每个 晶胞中0价Cu原子个数为
D. 当 转化为 时,每转移 电子,产生 原子
【答案】D
【解析】
【详解】A.由晶胞结构可知,位于顶点和面心的硒离子个数为8× +6× =4,位于体内的铜离子和亚铜
离子的个数之和为8,设晶胞中的铜离子和亚铜离子的个数分别为a和b,则a+b=8-4x,由化合价代数和为
0可得2a+b=4×2,解得a=4x,故A错误;
B.由题意可知,NaSe转化为Cu Se的电极反应式为NaSe-e-+(2-x)Cu=Cu Se+Na+,由晶胞结构可知,
2 2-x 2 2-x
位于顶点和面心的硒离子个数为8× +6× =4,则每个晶胞中含有4个NaSe,转移电子数为4,故B错误;
2的
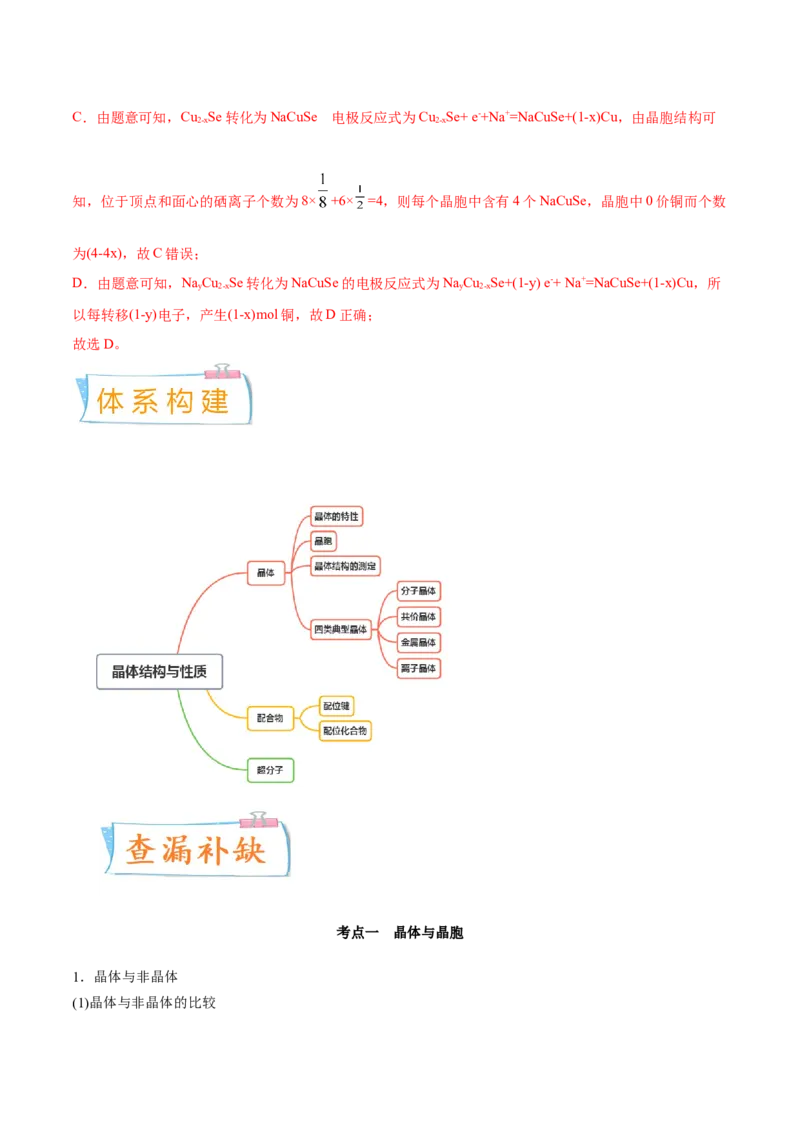
C.由题意可知,Cu Se转化为NaCuSe 电极反应式为Cu Se+ e-+Na+=NaCuSe+(1-x)Cu,由晶胞结构可
2-x 2-x
知,位于顶点和面心的硒离子个数为8× +6× =4,则每个晶胞中含有4个NaCuSe,晶胞中0价铜而个数
为(4-4x),故C错误;
D.由题意可知,NaCu Se转化为NaCuSe的电极反应式为NaCu Se+(1-y) e-+ Na+=NaCuSe+(1-x)Cu,所
y 2-x y 2-x
以每转移(1-y)电子,产生(1-x)mol铜,故D正确;
故选D。
考点一 晶体与晶胞
1.晶体与非晶体
(1)晶体与非晶体的比较晶体 非晶体
结构特征 原子在三维空间里呈周期性有序排列 原子排列相对无序
自范性 有 无
性质特征 熔点 固定 不固定
异同表现 各向异性 各向同性
二者区别 间接方法 看是否有固定的熔点或根据某些物理性质的各向异性
方法 科学方法 对固体进行 X 射线衍射 实验
(2)获得晶体的途径
①熔融态物质凝固。
②气态物质冷却不经液态直接凝固(凝华)。
③溶质从溶液中析出。
2.晶胞
(1)概念:晶胞是描述晶体结构的基本单元,是从晶体中“截取”出来具有代表性的最小重复单元。
(2)晶体中晶胞的排列——无隙并置
①无隙:相邻晶胞之间没有任何间隙。
②并置:所有晶胞平行排列、取向相同。
(3)晶胞中微粒数的计算方法——均摊法
①长方体(包括立方体)晶胞中不同位置的粒子数的计算:如某个粒子为N个晶胞所共有,则该粒子有属于
这个晶胞。中学中常见的晶胞为立方晶胞,立方晶胞中微粒数的计算方法如图1。
②非长方体晶胞
在六棱柱(如图2)中,顶角上的原子有属于此晶胞,面上的原子有属于此晶胞,因此六棱柱中镁原子个数为
12×+2×=3,硼原子个数为6。
考点二 晶体类型、结构与性质
1.四种晶体类型的比较
类型
分子晶体 共价晶体 金属晶体 离子晶体
比较
构成粒子 分子 原子 金属阳离子、自由电子 阴、阳离子
粒子间的相互 范德华力 ( 某些 共价键 金属键 离子键作用力 含氢键 )
硬度 较小 很大 有的很大,有的很小 较大
熔、沸点 较低 很高 有的很高,有的很低 较高
难溶于一般 一般不溶于水,少数与 大多易溶于水
溶解性 相似相溶
溶剂 水反应 等极性溶剂
一般不具有 晶体不导电,
一般不导电,溶
导电、传热性 导电性,个 电和热的良导体 水溶液或熔融
于水后有的导电
别为半导体 态导电
2.过渡晶体
大多数晶体是这四种晶体类型之间的过渡晶体,以离子晶体和共价晶体之间的过渡为例,如NaO、Al O
2 2 3
中既有离子键成分,也有共价键成分,NaO中离子键成分占62%,因而通常当作离子晶体来处理,Al O
2 2 3
中离子键成分占41%,因而通常当作共价晶体来处理。
3.常见晶体结构模型
(1)共价晶体
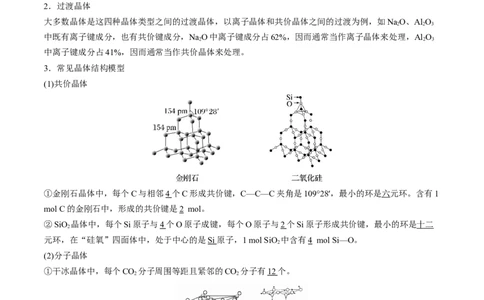
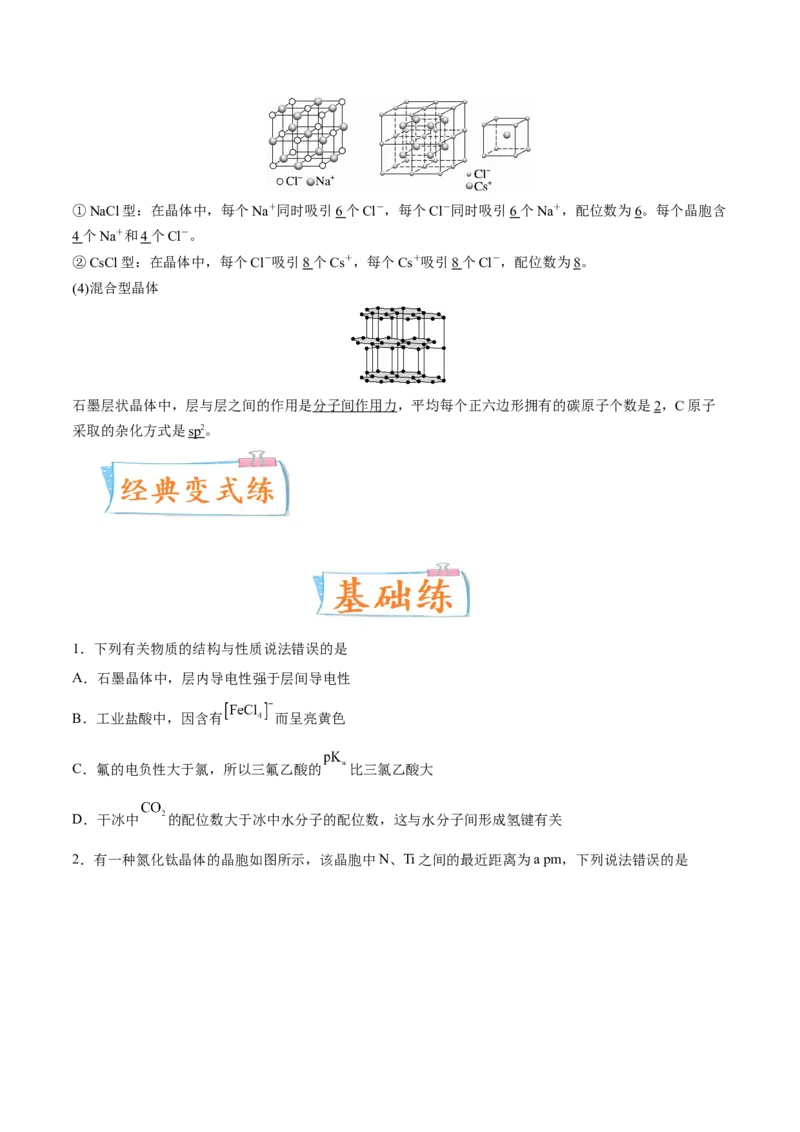
①金刚石晶体中,每个C与相邻4 个C形成共价键,C—C—C夹角是109°28′,最小的环是六元环。含有1
mol C的金刚石中,形成的共价键是2 mol。
②SiO 晶体中,每个Si原子与4 个O原子成键,每个O原子与2 个Si原子形成共价键,最小的环是十二
2
元环,在“硅氧”四面体中,处于中心的是Si 原子,1 mol SiO 中含有4 mol Si—O。
2
(2)分子晶体
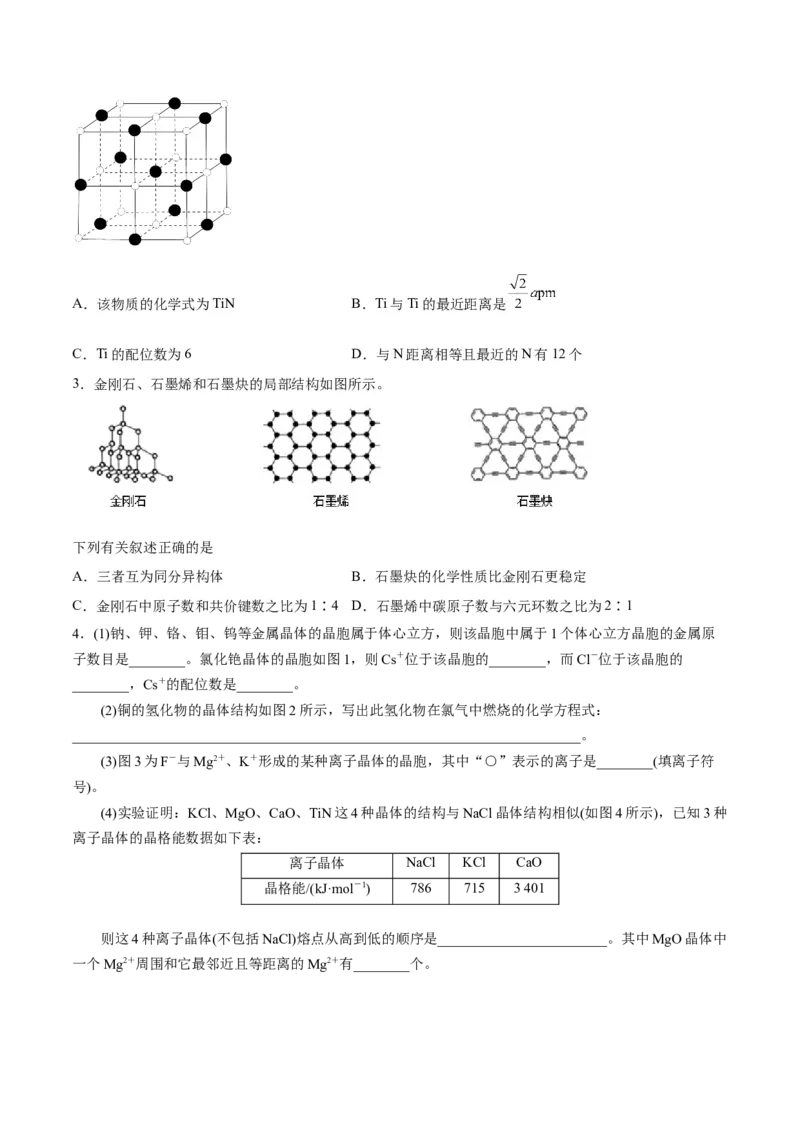
①干冰晶体中,每个CO 分子周围等距且紧邻的CO 分子有12 个。
2 2
②冰晶体中,每个水分子与相邻的4 个水分子以氢键相连接,含1 mol H O的冰中,最多可形成2 mol氢
2
键。
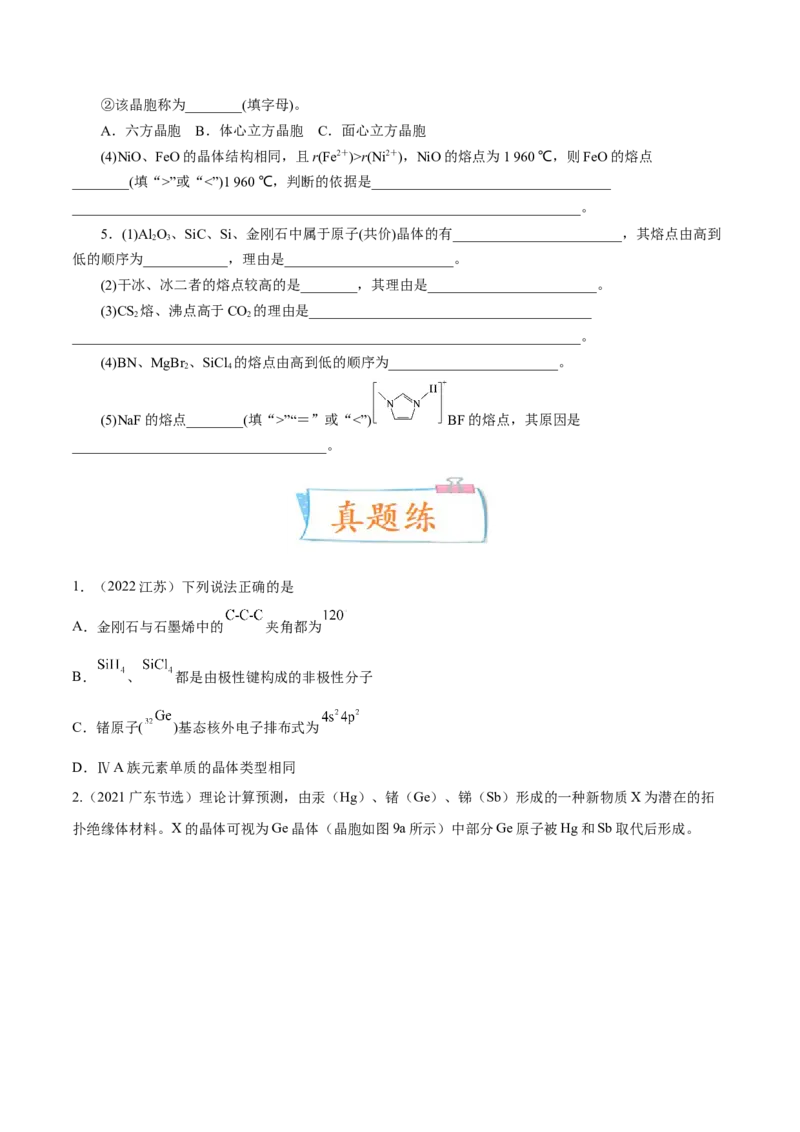
(3)离子晶体①NaCl型:在晶体中,每个Na+同时吸引6 个Cl-,每个Cl-同时吸引6 个Na+,配位数为6。每个晶胞含
4 个Na+和4 个Cl-。
②CsCl型:在晶体中,每个Cl-吸引8 个Cs+,每个Cs+吸引8 个Cl-,配位数为8。
(4)混合型晶体
石墨层状晶体中,层与层之间的作用是分子间作用力,平均每个正六边形拥有的碳原子个数是2,C原子
采取的杂化方式是 sp 2 。
1.下列有关物质的结构与性质说法错误的是
A.石墨晶体中,层内导电性强于层间导电性
B.工业盐酸中,因含有 而呈亮黄色
C.氟的电负性大于氯,所以三氟乙酸的 比三氯乙酸大
D.干冰中 的配位数大于冰中水分子的配位数,这与水分子间形成氢键有关
2.有一种氮化钛晶体的晶胞如图所示,该晶胞中N、Ti之间的最近距离为a pm,下列说法错误的是A.该物质的化学式为TiN B.Ti与Ti的最近距离是
C.Ti的配位数为6 D.与N距离相等且最近的N有12个
3.金刚石、石墨烯和石墨炔的局部结构如图所示。
下列有关叙述正确的是
A.三者互为同分异构体 B.石墨炔的化学性质比金刚石更稳定
C.金刚石中原子数和共价键数之比为1∶4 D.石墨烯中碳原子数与六元环数之比为2∶1
4.(1)钠、钾、铬、钼、钨等金属晶体的晶胞属于体心立方,则该晶胞中属于1个体心立方晶胞的金属原
子数目是________。氯化铯晶体的晶胞如图1,则Cs+位于该晶胞的________,而Cl-位于该晶胞的
________,Cs+的配位数是________。
(2)铜的氢化物的晶体结构如图2所示,写出此氢化物在氯气中燃烧的化学方程式:
________________________________________________________________________。
(3)图3为F-与Mg2+、K+形成的某种离子晶体的晶胞,其中“○”表示的离子是________(填离子符
号)。
(4)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图4所示),已知3种
离子晶体的晶格能数据如下表:
离子晶体 NaCl KCl CaO
晶格能/(kJ·mol-1) 786 715 3 401
则这4种离子晶体(不包括NaCl)熔点从高到低的顺序是________________________。其中MgO晶体中
一个Mg2+周围和它最邻近且等距离的Mg2+有________个。5.现有几组物质的熔点(℃)数据:
A组 B组 C组 D组
金刚石:3 550 ℃ Li:181 ℃ HF:—83 ℃ NaCl:801 ℃
硅晶体:1 410 ℃ Na:98 ℃ HCl:—115 ℃ KCl:776 ℃
硼晶体:2 300 ℃ K:64 ℃ HBr:—89 ℃ RbCl:718 ℃
二氧化硅:1 723 ℃ Rb:39 ℃ HI:—51 ℃ CsCl:645 ℃
据此回答下列问题:
(1)A组属于________晶体,其熔化时克服的微粒间的作用力是________。
(2)B组晶体共同的物理性质是________(填序号)。
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于________________________________________________
________________________________________________________________________。
(4)D组晶体可能具有的性质是________(填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(5)D组晶体的熔点由高到低的顺序为NaCl>KCl>RbCl>CsCl,其原因为_____________
________________________________________________________________________
________________________________________________________________________。
1.(2022·重庆巴蜀中学高三阶段练习)化学与生产、生活、科技、环境等关系密切。下列说法正确的是
A.汽车尾气催化转化器可有效减少 ,的排放,实现“碳中和”
B.制造焊锡时,把铅加入锡,形成原电池,从而增加锡的抗腐蚀能力
C.2022年冬奥会衣物采用石墨烯纺织物柔性发热材料,石墨烯属于混合型晶体
D.聚氯乙烯塑料通过加聚反应制得,可用于制作不粘锅的耐热涂层
2.(2022·湖北·高三阶段练习)砷化镓是继硅之后研究最深入、应用最广泛的半导体材料,其结构与硫化
锌相似,其晶胞结构如下图1所示,图2为晶胞沿z轴的1∶1平面投影图,已知图中 球的原子坐标参数
为(0,0,0), 球为(1,1,1),下列说法错误的是A.Ga的配位数是4
B.晶胞参数为 pm
C.晶胞中离As原子距离最近且相等的As原子有8个
D.晶胞中离 球距离最远的黑球的坐标参数为( , , )
3.(2022·重庆巴蜀中学高三阶段练习)萤石是制作光学玻璃的原料之一,其主要成分氟化钙的晶胞结构
如图1所示。下列说法错误的是
A.F位于元素周期表p区 B.该晶体属于离子晶体
C. 位于 构成的四面体空隙 D.每个 周围距离最近且等距的 有4个
4.下面是一些晶体的结构示意图。
(1)下列关于晶体的说法正确的是________(填字母)。
A.晶体的形成与晶体的自范性有关
B.可以用X射线衍射仪区分晶体和非晶体
C.石蜡是非晶体,但有固定的熔点
D.晶胞就是晶体
(2)图甲表示的是晶体的二维平面示意图,a、b中可表示化学式为AX 的化合物的是________(填“a”
3
或“b”)。
(3)图乙表示的是金属铜的晶胞。
①该晶胞“实际”拥有的铜原子数是________,铜原子的配位数为________。②该晶胞称为________(填字母)。
A.六方晶胞 B.体心立方晶胞 C.面心立方晶胞
(4)NiO、FeO的晶体结构相同,且r(Fe2+)>r(Ni2+),NiO的熔点为1 960 ℃,则FeO的熔点
________(填“>”或“<”)1 960 ℃,判断的依据是__________________________________
________________________________________________________________________。
5.(1)AlO、SiC、Si、金刚石中属于原子(共价)晶体的有________________________,其熔点由高到
2 3
低的顺序为____________,理由是________________________。
(2)干冰、冰二者的熔点较高的是________,其理由是________________________。
(3)CS 熔、沸点高于CO 的理由是________________________________________
2 2
________________________________________________________________________。
(4)BN、MgBr 、SiCl 的熔点由高到低的顺序为________________________。
2 4
(5)NaF的熔点________(填“>”“=”或“<”) BF的熔点,其原因是
____________________________________。
1.(2022江苏)下列说法正确的是
A.金刚石与石墨烯中的 夹角都为
B. 、 都是由极性键构成的非极性分子
C.锗原子( )基态核外电子排布式为
D.ⅣA族元素单质的晶体类型相同
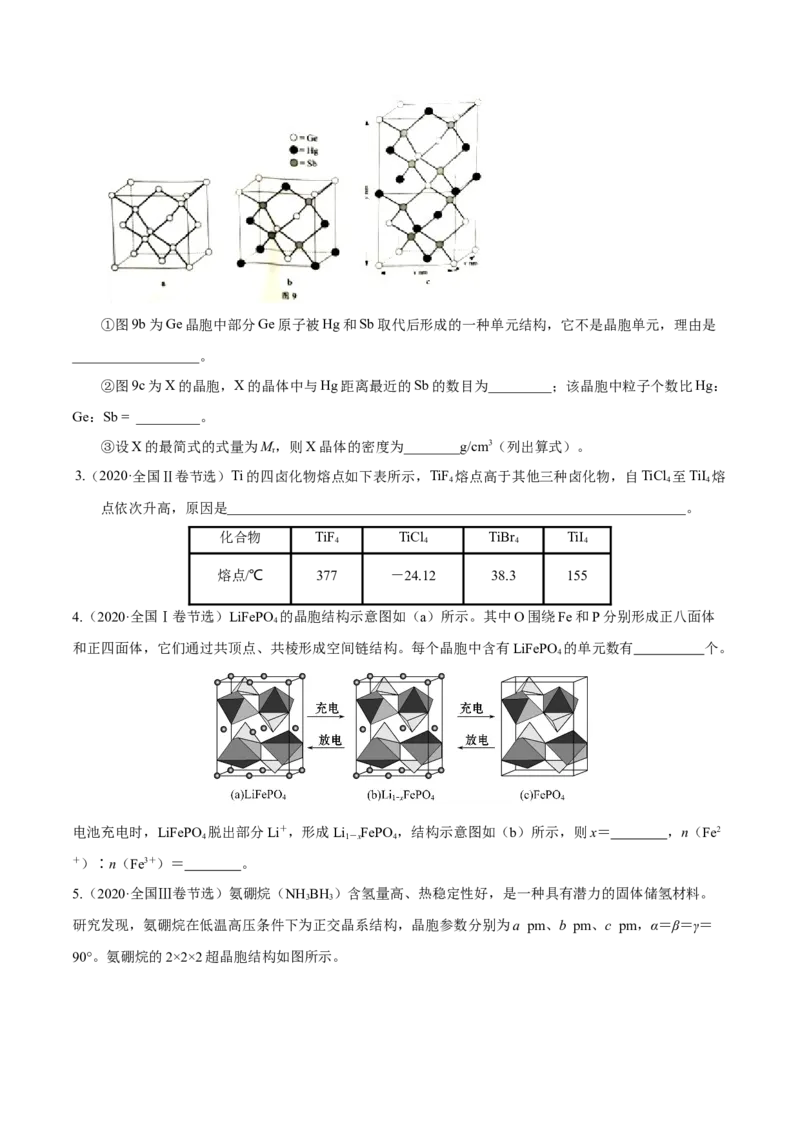
2.(2021广东节选)理论计算预测,由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓
扑绝缘体材料。X的晶体可视为Ge晶体(晶胞如图9a所示)中部分Ge原子被Hg和Sb取代后形成。①图9b为Ge晶胞中部分Ge原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞单元,理由是
__________________。
②图9c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为_________;该晶胞中粒子个数比Hg:
Ge:Sb = _________。
③设X的最简式的式量为M,则X晶体的密度为________g/cm3(列出算式)。
r
3.(2020·全国Ⅱ卷节选)Ti的四卤化物熔点如下表所示,TiF 熔点高于其他三种卤化物,自TiCl 至TiI 熔
4 4 4
点依次升高,原因是_________________________________________________________________。
化合物 TiF TiCl TiBr TiI
4 4 4 4
熔点/℃ 377 -24.12 38.3 155
4.(2020·全国Ⅰ卷节选)LiFePO 的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体
4
和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有LiFePO 的单元数有 个。
4
电池充电时,LiFePO 脱出部分Li+,形成Li FePO ,结构示意图如(b)所示,则x= ,n(Fe2
4 1-x 4
+)∶n(Fe3+)= 。
5.(2020·全国Ⅲ卷节选)氨硼烷(NH BH)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。
3 3
研究发现,氨硼烷在低温高压条件下为正交晶系结构,晶胞参数分别为a pm、b pm、c pm,α=β=γ=
90°。氨硼烷的2×2×2超晶胞结构如图所示。氨硼烷晶体的密度ρ= g·cm-3(列出计算式,设N 为阿伏加德罗常数的值)。
A
1.【答案】C
【详解】A.石墨晶体中每一层会形成大π键产生可以自由移动的电子使得石墨可以导电,因此层内导电
性强于层间导电性,A正确;
B.工业盐酸中含有部分铁离子,铁离子和氯离子生成 ,因含有 而呈亮黄色,B正确;
C.氟的电负性大于氯,使得三氟乙酸酸性强于三氯乙酸,三氟乙酸的Ka值较大,故三氟乙酸的 比三
氯乙酸更小,C错误;
D.干冰是面心立方堆积,水配位数与生成氢键有关,干冰中 的配位数大于冰中水分子的配位数,这
与水分子间形成氢键有关,D正确;
故选C。
2.【答案】B
【详解】A.该晶胞中,Ti(黑球)的个数为1+12 =4,N(白球)的个数为8 +6 =4,则Ti和N的
个数比为1:1,该物质的化学式为TiN,A正确;
B.该晶胞中N、Ti之间的最近距离为a pm,则Ti与Ti的最近距离是 a pm,B错误;C.如图所示,与Ti距离相等且最近的N有6个,则Ti的配位数为6,C正确;
D.与N距离相等且最近的N有12个,D正确;
故选B。
3.【答案】D
【详解】A.同分异构体是分子式相同、结构不同的化合物;三者不是互为同分异构体,A错误;
B.石墨炔中含碳碳叄键,化学性质较活泼,金刚石中碳原子均是饱和键,化学性质在常温下非常稳定,B
错误;
C.金刚石中1个碳原子与4个碳原子相连形成4个共价键,每个共价键为相邻2个碳原子共用,故原子数
和共价键数之比为1∶(4× )=1:2,C错误;
D.石墨烯中1个碳原子被相邻3个环共用,每个环上有6个碳原子,则碳原子数与六元环数之比为为
(6× )∶1=2∶1,D正确;
故选D。
4.【答案】(1)2 体心 顶点 8
(2)2CuH+3Cl=====2CuCl +2HCl
2 2
(3)F- (4)TiN>MgO>CaO>KCl 12
【解析】(1)体心立方晶胞中,1个原子位于体心,8个原子位于立方体的顶点,故1个晶胞中金属原
子数为8×+1=2;氯化铯晶胞中,Cs+位于体心,Cl-位于顶点,Cs+的配位数为8。(2)由晶胞可知,微粒
个数比为1∶1,化学式为CuH,CuH与Cl 反应,产物为CuCl 和HCl,化学方程式为2CuH+
2 2
3Cl=====2CuCl +2HCl。(3)由晶胞结构可知,黑球有1个,灰球有1个,白球有3个,由电荷守恒可知
2 2
n(Mg2+)∶n(K+)∶n(F-)=1∶1∶3,故白球为F-。(4)从3种离子晶体的晶格能数据知道,离子所带电荷越
多、离子半径越小,离子晶体的晶格能越大,离子所带电荷数:Ti3+>Mg2+,离子半径:Mg2+<Ca2+,所
以熔点:TiN>MgO>CaO>KCl;MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有12个。
5.【答案】(1)原子 共价键 (2)①②③④
(3)HF分子间能形成氢键,其熔化时需要消耗的能量更多(只要答出HF分子间能形成氢键即可)
(4)②④ (5)D组晶体都为离子晶体,r(Na+)Ni2+,则晶格能:FeOFeO。
5.【答案】(1)SiC、Si、金刚石 金刚石>SiC>Si C—C键、C—Si键、Si—Si键的键长依次增大,键能
依次减小,熔点依次降低
(2)冰 冰晶体中分子间存在氢键
(3)CS 和CO 均为分子晶体,CS 的相对分子质量大,分子间作用力大,因此CS 熔、沸点高于CO
2 2 2 2 2
(4)BN>MgBr >SiCl
2 4
(5)> 两者均为离子化合物,且离子所带电荷数均为1,但后者离子半径大,离子键较弱,因此熔点较低
【解析】(1)SiC、Si、金刚石为原子晶体,原子晶体中共价键键长越短,键能越大,熔、沸点越高。(2)冰
晶体中含有氢键,熔点比干冰高。(3)CS 、CO 均为分子晶体,组成、结构相似,相对分子质量越大,范
2 2
德华力越大,熔、沸点越高。(4)BN为原子晶体,MgBr 为离子晶体,SiCl 为分子晶体,故熔点:
2 4
BN>MgBr >SiCl 。
2 4
1.【答案】B
【详解】
A.金刚石中的碳原子为正四面体结构, 夹角为109°28′,故A错误;
B. 的化学键为Si-H,为极性键,为正四面体,正负电荷中心重合,为非极性分子; 的化学键为
Si-Cl,为极性键,为正四面体,正负电荷中心重合,为非极性分子,故B正确;
C.锗原子( )基态核外电子排布式为[Ar]3d10 ,故C错误;
D.ⅣA族元素中的碳元素形成的石墨为混合晶体,而硅形成的晶体硅为原子晶体,故D错误;
故选B。
2.【答案】由图9c可知,图9b中Sb、Hg原子取代位置除图9b外还有其它形式 4 1:1:2
【详解】(6)①对比图9b和图9c可得X晶体的晶胞中上下两个单元内的原子位置不完全相同,不符合晶胞晶胞是晶
体的最小重复单位要求,故答案为:由图9c可知,图9b中Sb、Hg原子取代位置除图9b外还有其它形式。
②以晶胞上方立方体中右侧面心中Hg原子为例,同一晶胞中与Hg距离最近的Sb的数目为2,右侧晶胞中
有2个Sb原子与Hg原子距离最近,因此X的晶体中与Hg距离最近的Sb的数目为4;该晶胞中Sb原子均
位于晶胞内,因此1个晶胞中含有Sb原子数为8,Ge原子位于晶胞顶点、面心、体心,因此1个晶胞中含
有Ge原子数为1+8× +4× =4,Hg原子位于棱边、面心,因此1个晶胞中含有Hg原子数为6× +4×
=4,则该晶胞中粒子个数比Hg:Ge:Sb =4:4:8=1:1:2,故答案为:4;1:1:2。
③1个晶胞的质量m= ,1个晶胞的体积V=(x×10-7cm)2×(y×10-7cm)=x2y×10-21cm3,则X晶体的
密度为 = = g/cm3,故答案为: 。
3.【答案】TiF 为离子化合物,熔点高,其他三种均为共价化合物,随相对分子质量的增大分子间作用力
4
增大,熔点逐渐升高
【解析】F的电负性强,故TiF 属于离子化合物,形成离子晶体,熔点较高,而自TiCl 至TiI 均为共价化
4 4 4
合物,形成分子晶体,熔沸点很低,且随相对分子质量的增大分子间作用力增大,熔点逐渐升高。
4.【答案】4 或0.187 5 13∶3
【解析】由题干可知,LiFePO 的晶胞中,Fe存在于由O构成的正八面体内部,P存在于由O构成的正四
4
面体内部;再分析题干中给出的(a)、(b)和(c)三个不同物质的晶胞结构示意图,对比(a)和(c)
的差异可知,(a)图所示的LiFePO 的晶胞中,小球表示的即为Li+,其位于晶胞的8个顶点,4个侧面
4
面心以及上下底面各自的相对的两条棱心处,经计算一个晶胞中Li+的个数为8×+4×+4×=4(个);进
一步分析(a)图所示的LiFePO 的晶胞中,八面体结构和四面体结构的数目均为4,即晶胞中含Fe和P的
4
数目均为4;考虑到化学式为LiFePO ,并且一个晶胞中含有的Li+、Fe和P的数目均为4,所以一个晶胞
4
中含有4个LiFePO 单元。对比(a)和(b)两个晶胞结构示意图可知,
4
Li FePO 相比于LiFePO 缺失一个面心的Li+以及一个棱心的Li+;结合上一个空的分析可知,LiFePO 晶
1-x 4 4 4
胞的化学式为LiFe PO ,那么Li FePO 晶胞的化学式为Li Fe PO ,所以有1-x=即x=0.187 5。结
4 4 4 16 1-x 4 3.25 4 4 16
合上一个空计算的结果可知,Li FePO 即Li FePO ;假设Fe2+和Fe3+数目分别为x和y,则列方程组:
1-x 4 0.812 5 4x+y=1,0.812 5+2x+3y+5=4×2,解得x=0.812 5,y=0.187 5,则Li FePO 中n(Fe2+)∶n(Fe3+)
1-x 4
=0.812 5∶0.187 5=13∶3。
5.【答案】
【解析】由图可知晶胞体积为2a×2b×2c=8abc (pm3)=8abc×10-30(cm3);而每个晶胞中氨硼烷质量为
g,所以晶体的密度ρ= g·cm-3。