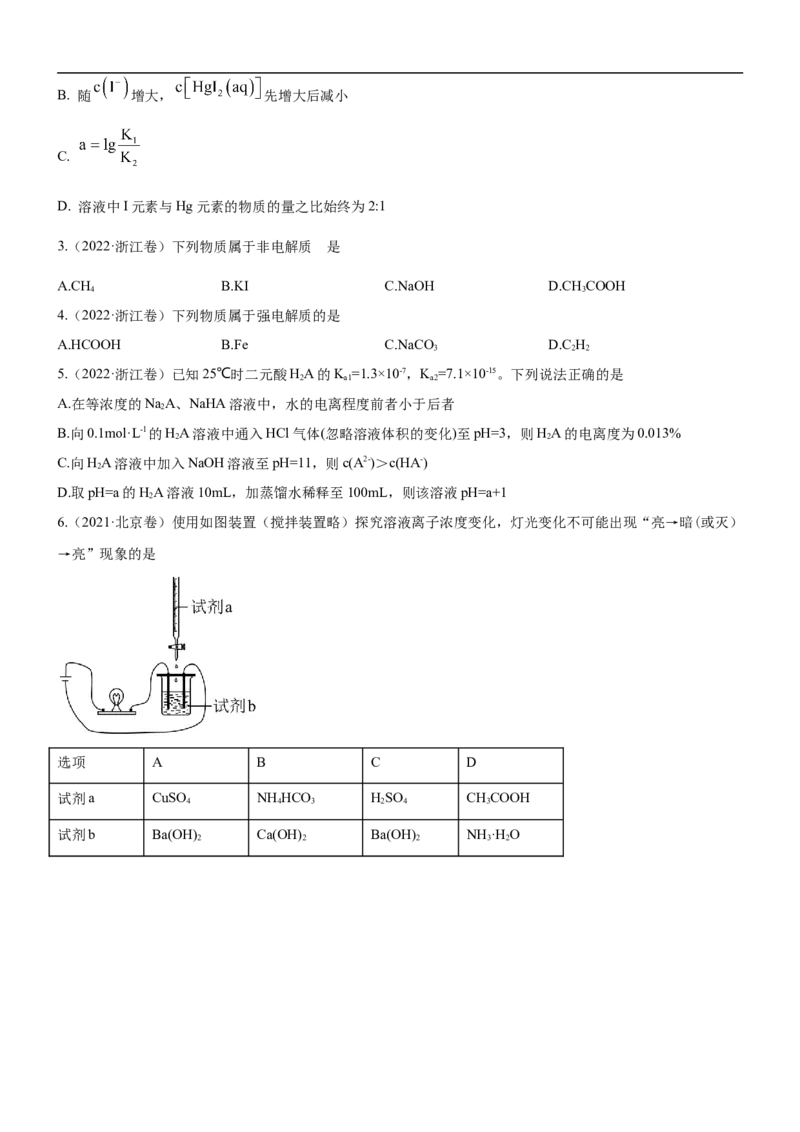
文档内容
考点 1 电离平衡
1.3年真题考点分布
考点分布
年份 卷区
电解质的判断 强、弱电解质的判断 弱电解质的电离影响因素
山东 √
2023
浙江 √
2022 浙江 √ √
北京 √ √
2021
浙江 √ √
2.命题规律及备考策略
【命题规律】近3年新高考卷对于该专题主要考查:
1.强、弱电解质的判断
2.电离方程式
3.弱电解质的电离平衡
【备考策略】掌握弱电解质的电离有一定限度,是可以调控的,能多角度、动态地分析弱电解质的电离平衡,
并运用平衡移动原理解决实际问题。
【命题预测】预测2024年高考,考查电离平衡的移动及影响因素,重在考查现象的本质和规律。
考法 1 电离平衡
一、弱电解质的电离平衡
1.弱电解质
强电解质 弱电解质
定义 在水溶液中能完全电离的电解质 在水溶液中只能部分电离的电解质
电离过程 不可逆,无电离平衡 可逆,存在电离平衡
在溶液中的
只有离子 既有离子,又有电解质分子
存在形式
①强酸,如HCl、HSO ①弱酸,如CHCOOH、HClO
2 4 3
物质类别
②强碱,如KOH、Ba(OH) ②弱碱,如NH ·H O、Mg(OH)
2 3 2 2
及示例
③大部分盐,如NaCl、BaSO ③水
4
(2)与化合物类型的关系
强电解质主要是大部分离子化合物及某些共价化合物,弱电解质主要是某些共价化合物。
2.弱电解质的电离概念(1)电离平衡的建立
在一定条件下(如温度、压强等),当弱电解质电离产生离子的速率和离子结合成分子的速率相等时,电离过程
达到了平衡。
(2)电离平衡的建立与特征
①开始时,v(电离)最大,而v(结合)为0。
②平衡的建立过程中,v(电离)>v(结合)。
③当v(电离)=v(结合)时,电离过程达到平衡状态。
二、电离方程式的书写
强酸 完全电离,如HCl === H+ + Cl-
强碱 完全电离,如Ba(OH) === Ba2+ + 2OH-
2
强 正盐 完全电离,如NaCO === 2Na+ + CO2-
电 2 3 3
解 强酸的酸式盐 完全电离,如NaHSO === Na+ + H+ + SO2-
质 盐 4 4
第一步完全电离,第二步弱酸酸根部分电离,如
弱酸的酸式盐
NaHCO 3 === Na+ + HCO 3 -,HCO 3 - ⇌ H+ + CO 3 2-
一元弱酸 部分电离,如CH 3 COOH ⇌ CH 3 COO- + H+
一元弱碱 部分电离,如 NH 3 ·H 2 O ⇌ NH+ 4 + OH-
弱
电 H 2 O 部分电离, H 2 O ⇌ H+ + OH-
解
分步电离,必须分步写出,不可合并(以第一步电离为主)
质
多元弱酸
如H 2 CO 3 ⇌ H+ + HCO 3 -,HCO 3 - ⇌ H+ + CO 3 2-
多元弱碱 分步电离,中学阶段要求一步写出。如Fe(OH) 3 ⇌ Fe3+ + 3OH-
【特别提醒】强酸的酸式盐在熔融状态和水溶液中,电离方程式是不同的。
(1)熔融状态时:NaHSO === Na+ + HSO- ;
4 4
(2)溶于水时:NaHSO === Na+ + H+ + SO2-杨sir
4 4
三、电离平衡的影响因素
1.外因对电离平衡的影响
(1)浓度:在一定温度下,同一弱电解质溶液,浓度越小,越易电离。
(2)温度:温度越高,电离程度越大。
(3)同离子效应:加入与弱电解质具有相同离子的电解质时,可使电离平衡向结合成弱电解质分子的方向移动。
(4)化学反应:加入能与弱电解质电离出的离子反应的物质时,可使电离平衡向电离方向移动。如:以0.1 mol·L-1 CHCOOH溶液为例,填写外界条件对CHCOOH CHCOO-+H+ ΔH>0的影响。
3 3 3
改变条件 平衡移动方向 n(H+) c(H+) 导电能力 K
a
加水稀释 向右 增大 减小 减弱 不变
加入少量冰醋酸 向右 增大 增大 增强 不变
通入HCl(g) 向左 增大 增大 增强 不变
加NaOH(s) 向右 减小 减小 增强 不变
加CHCOONa(s) 向左 减小 减小 增强 不变
3
加入镁粉 向右 减小 减小 增强 不变
升高温度 向右 增大 增大 增强 增大
2.一元强酸(HCl)与一元弱酸(CHCOOH)的比较
3
(1)相同物质的量浓度、相同体积的盐酸与醋酸溶液的比较
比较项目 与活泼金属反应产 开始与金属反应
c(H+) pH 中和碱的能力
酸 生H 2 的量 的速率
盐酸 大 小 大
相同 相同
醋酸溶液 小 大 小
(2)相同pH、相同体积的盐酸与醋酸溶液的比较
比较项目 与足量活泼金属反 开始与金属反
c(H+) c(酸) 中和碱的能力
酸 应产生H 2 的量 应的速率
盐酸 小 小 少
相同 相同
醋酸溶液 大 大 多
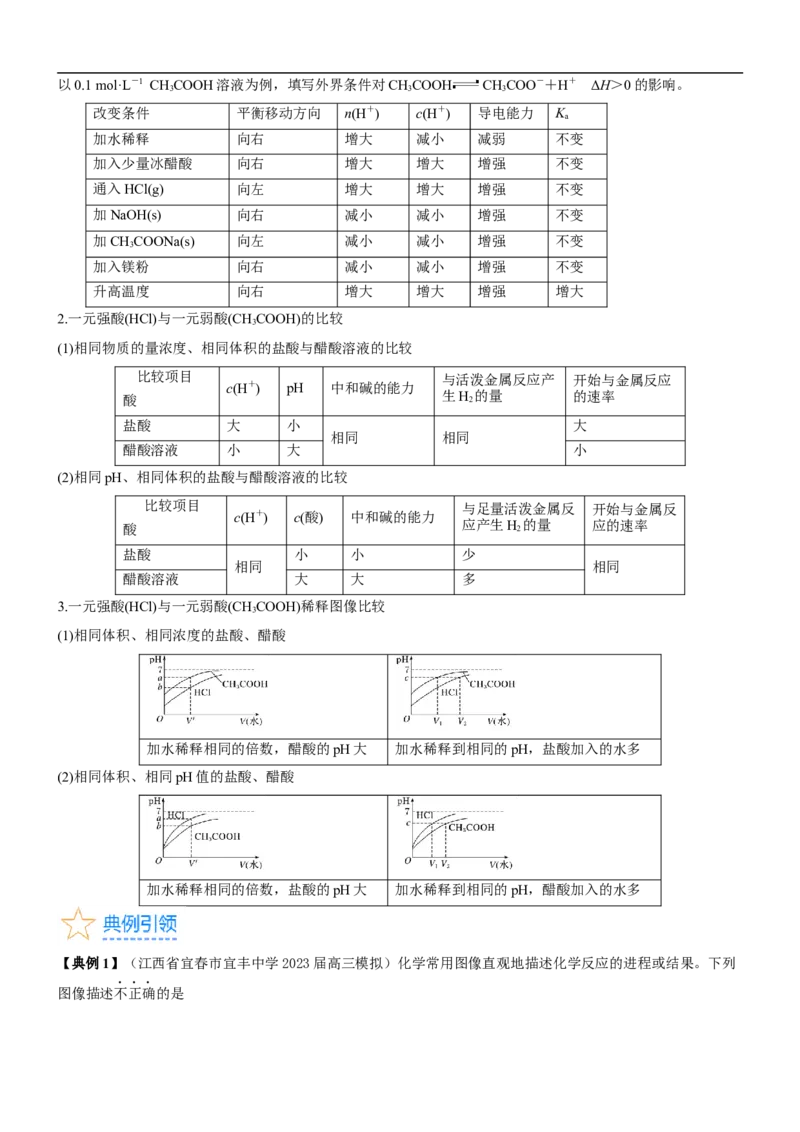
3.一元强酸(HCl)与一元弱酸(CHCOOH)稀释图像比较
3
(1)相同体积、相同浓度的盐酸、醋酸
加水稀释相同的倍数,醋酸的pH大 加水稀释到相同的pH,盐酸加入的水多
(2)相同体积、相同pH值的盐酸、醋酸
加水稀释相同的倍数,盐酸的pH大 加水稀释到相同的pH,醋酸加入的水多
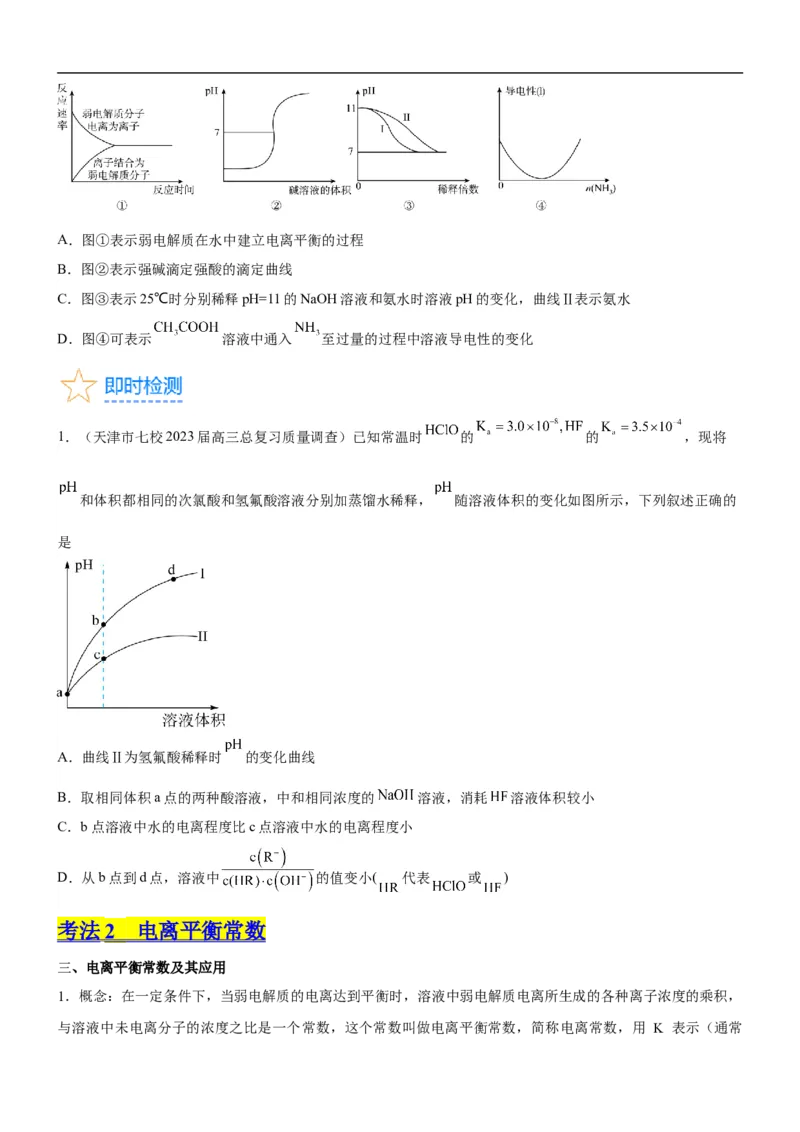
【典例1】(江西省宜春市宜丰中学2023届高三模拟)化学常用图像直观地描述化学反应的进程或结果。下列
图像描述不正确的是A.图①表示弱电解质在水中建立电离平衡的过程
B.图②表示强碱滴定强酸的滴定曲线
C.图③表示25℃时分别稀释pH=11的NaOH溶液和氨水时溶液pH的变化,曲线Ⅱ表示氨水
D.图④可表示 溶液中通入 至过量的过程中溶液导电性的变化
1.(天津市七校2023届高三总复习质量调查)已知常温时 的 的 ,现将
和体积都相同的次氯酸和氢氟酸溶液分别加蒸馏水稀释, 随溶液体积的变化如图所示,下列叙述正确的
是
A.曲线Ⅱ为氢氟酸稀释时 的变化曲线
B.取相同体积a点的两种酸溶液,中和相同浓度的 溶液,消耗 溶液体积较小
C.b点溶液中水的电离程度比c点溶液中水的电离程度小
D.从b点到d点,溶液中 的值变小( 代表 或 )
考法 2 电离平衡常数
三、电离平衡常数及其应用
1.概念:在一定条件下,当弱电解质的电离达到平衡时,溶液中弱电解质电离所生成的各种离子浓度的乘积,
与溶液中未电离分子的浓度之比是一个常数,这个常数叫做电离平衡常数,简称电离常数,用 K 表示(通常用K、K 分别表示弱酸、弱碱的电离平衡常数)。
a b 杨sir化学,侵权必究
2.表达式
(1)一元弱酸HA的电离常数:根据HA H++A-,可表示为K=。
a
(2)一元弱碱BOH的电离常数:根据BOH B++OH-,可表示为K =。
b
(3)多元弱酸、弱碱
电离方程式 电离常数表达式
c(H+)·c(HCO-)
K = 3
H 2 CO 3 ⇌ H+ +HCO 3 - 1 c(H2CO3)
HCO
2 3 HCO 3 - ⇌ H+ +CO 3 2- K = c(H+)·c(CO 3 2-)
2 c(HCO-)
3
c(Cu2+ )·c2(OH-)
Cu(OH) 2 Cu(OH) 2 ⇌ Cu2+ + 2OH- K= c[Cu(OH)2]
3.特点
(1)电离平衡常数与温度有关,与浓度无关,升高温度,K值增大。
(2)电离平衡常数反映弱电解质的相对强弱,K越大,表示弱电解质越易电离,酸性或碱性越强。
例如,在25 ℃时,K(HNO)=4.6×10-4,K(CHCOOH)=1.8×10-5,因而HNO 的酸性比CHCOOH强。
2 3 2 3
(3)多元弱酸的各级电离常数的大小关系是K ≫K ≫K ……,故其酸性取决于第一步电离。
1 2 3
4.电离度
(1)概念:弱电解质达电离平衡时,已电离的电解质分子数占原来总分子数(包括已电离的和未电离的)的百
分数。
(2)表示方法
α=×100%
也可表示为α=×100%
(3)影响因素
①相同温度下,同一弱电解质,浓度越大,其电离度(α)越小。
②相同浓度下,同一弱电解质,温度越高,其电离度(α)越大。
(4)意义:表示不同弱电解质在水溶液中的电离程度,在相等条件下可用电离度比较弱电解质的相对强弱。
【典例2】 (安徽省黄山市2023届高三下学期三模)HX是一种二元弱酸。常温下向HX溶液中滴加NaOH溶液,
2 2
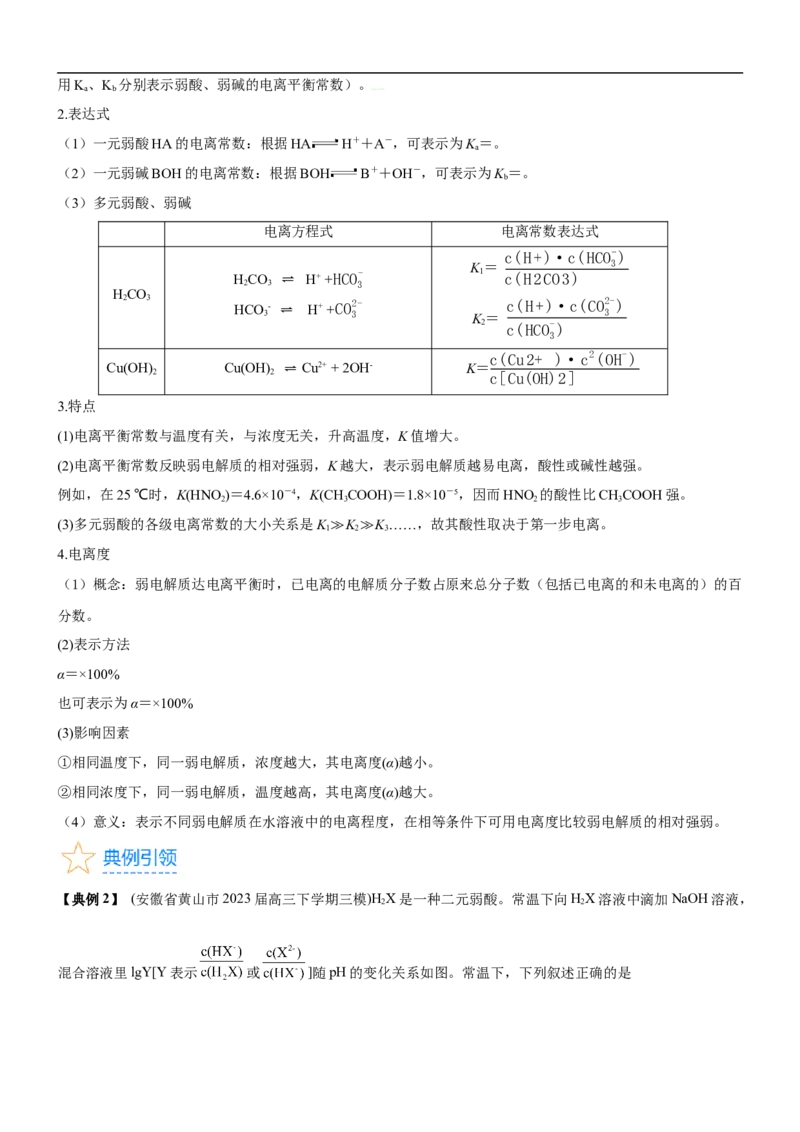
混合溶液里lgY[Y表示 或 ]随pH的变化关系如图。常温下,下列叙述正确的是A.直线Ⅰ中Y表示的是
B.电离平衡常数Ka(H X)的数量级为10-4
2 2
C.pH=7.2时,c(HX-)=1000c(X2-)
D.当c(X2-)=c(H X)时,溶液的pH为2.7
2
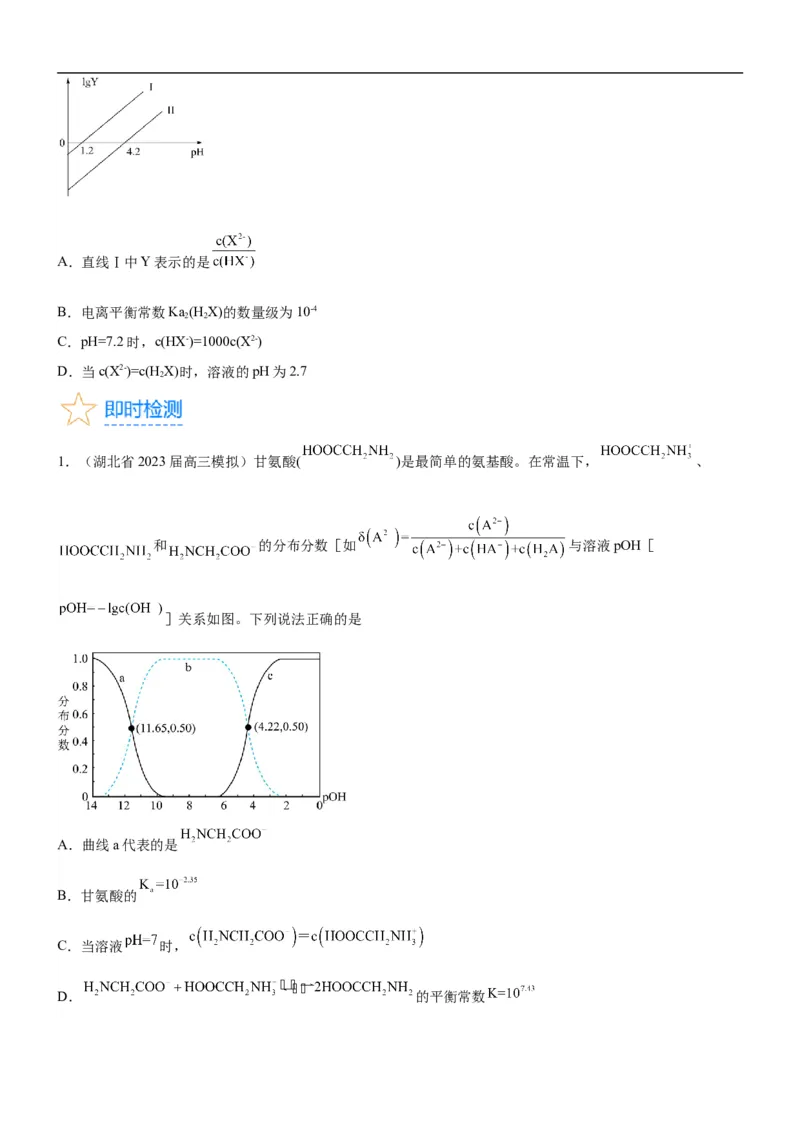
1.(湖北省2023届高三模拟)甘氨酸( )是最简单的氨基酸。在常温下, 、
和 的分布分数[如 与溶液pOH[
]关系如图。下列说法正确的是
A.曲线a代表的是
B.甘氨酸的
C.当溶液 时,
D. 的平衡常数【基础过关】
1.(辽宁省鞍山市2023-2024学年高三上学期第一次质量监测)HA、HB为两种一元酸,为研究25°C时反应
的相关性质,查阅此温度下相关数据: H=+29.1kJ/mol; S=+150.0J/
△ △
(K·mol),下列说法正确的是
A.由于此过程 H>0,故HB比HA内能更低
B. S对该反应△自发性的影响小于 H
C.△相对于B-,A-与质子的结合能力△更强
D.体积和物质的量浓度均相同的NaA和NaB两溶液中,前者离子总数更多
2.(河南省郑州外国语学校2023届高三下学期模拟)已知电离常数:K(HCN)=5×10-10,HCO:K =4.3×10-
a 2 3 a1
7,K =5.6×10-11,下列离子方程式书写正确的是
a2
A.向KCN(aq)中通入少量的CO 气体:CO+H O+2CN-=2HCN+CO
2 2 2
B.少量SO 通入Ca(ClO) 溶液中:SO +H O+Ca2++2ClO-=CaSO ↓+2HClO
2 2 2 2 3
C.氢氧化铁沉淀溶解于过量氢碘酸溶液中:2Fe(OH) +6H++2I-=2Fe2++6H O+I
3 2 2
D.向Ba(OH) 溶液中加入少量的NaHCO 溶液:2HCO +Ba2++2OH-=BaCO ↓+CO +2H O
2 3 3 2
3.(河北省衡水市第二中学2023届高三调研)常温常压下,下列物质的物理量种前者是后者两倍的是
A.28 g 和28g 中所含的中子数
B.2.24 L 和2.24 L 原子数
C.1mol 和2mol 的密度
D.0.1mol·L 和0.1 mol·L 的
4.(辽宁省沈阳市第二中学2023届高三下学期第六次模拟)下列操作能实现相应的实验目的的是
选
实验目的 操作步骤及现象
项
加入酚酞做指示剂,用同浓度的烧碱溶液滴定,终点消耗烧碱溶液体积与
A 证明HA是强酸
HA相同
证明H 与I(g)的反应为可 将物质的量之比为2:1的H 与I(g)混合气体在一定条件下充分反应,混
B 2 2 2 2
逆反应 合气体呈紫色向麦芽糖溶液中加稀硫酸并加热,冷却后加入烧碱中和过量硫酸再加入银
C 证明麦芽糖能水解
氨溶液加热,析出银镜
D 证明氧化性: 将硫酸酸化的HO 滴入Fe(NO ) 溶液中,再滴入KSCN溶液,溶液变红
2 2 3 2
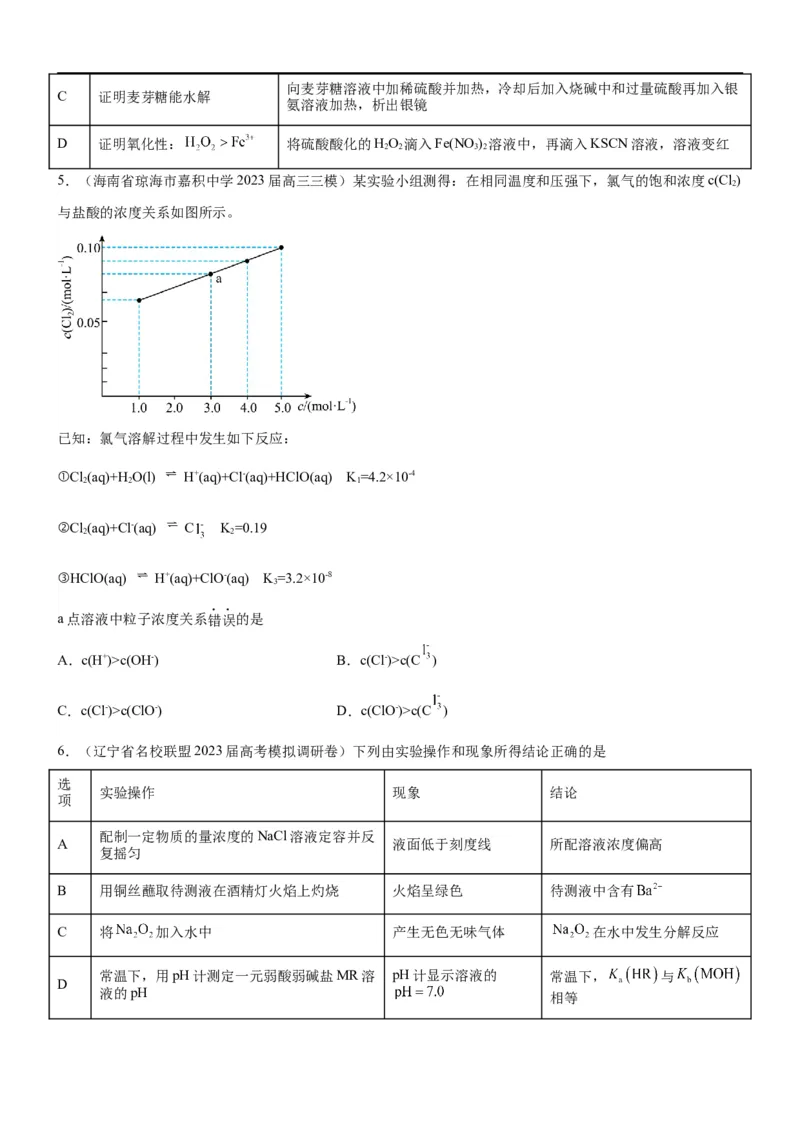
5.(海南省琼海市嘉积中学2023届高三三模)某实验小组测得:在相同温度和压强下,氯气的饱和浓度c(Cl )
2
与盐酸的浓度关系如图所示。
已知:氯气溶解过程中发生如下反应:
①Cl(aq)+H O(l) H+(aq)+Cl-(aq)+HClO(aq) K=4.2×10-4
2 2 1
②Cl (aq)+Cl-(aq) C K=0.19
2 2
③HClO(aq) H+(aq)+ClO-(aq) K=3.2×10-8
3
a点溶液中粒子浓度关系错误的是
A.c(H+)>c(OH-) B.c(Cl-)>c(C )
C.c(Cl-)>c(ClO-) D.c(ClO-)>c(C )
6.(辽宁省名校联盟2023届高考模拟调研卷)下列由实验操作和现象所得结论正确的是
选
实验操作 现象 结论
项
配制一定物质的量浓度的NaCl溶液定容并反
A 液面低于刻度线 所配溶液浓度偏高
复摇匀
B 用铜丝蘸取待测液在酒精灯火焰上灼烧 火焰呈绿色 待测液中含有
C 将 加入水中 产生无色无味气体 在水中发生分解反应
常温下,用pH计测定一元弱酸弱碱盐MR溶 pH计显示溶液的 常温下, 与
D
液的pH
相等7.(福建省三明市2022-2023学年普通高中高三下学期质量检测)将等量的 分别快速通入等体积等物质的
量浓度的 溶液和 溶液中(除无氧 溶液外,都产生白色沉淀),测得各溶液pH随时间变化曲
线如图所示。下列说法正确的是
A.曲线a所示溶液pH降低的原因: 、
B.依据曲线b可推知无氧 溶液能氧化 溶液
C.曲线c所示溶液中发生反应的离子方程式为:
D.曲线d所表示的过程中氧化 的主要微粒是
8.(江苏省盐城市2023届高三下学期三模)周期表中VIIA元素及其化合物应用广泛。氢氟酸可用作雕刻玻璃;
卤化银具有感光性( 的电离平衡常数分别为: 、 ;HClO的电离平衡常数为:
)。下列物质性质与用途具有对应关系的是
A.氢氟酸具有酸性,可用于雕刻玻璃 B. 受热可分解,可用作食盐碘添加剂
C.碘化银具有感光性,可用于人工降雨 D. 有强氧化性,可用作水体杀菌消毒剂
【能力提升】
1.(辽宁省东北育才学校2023届高三模拟)25 ℃时,用同一NaOH溶液分别滴定一元酸HA溶液和 溶液,pM[p表示负对数,M表示 、 ]与溶液pH的变化关系如图所示。已知: 易溶于水,一
般认为反应的平衡常数 时反应进行完全。下列说法错误的是
A.HA为一元弱酸,25 ℃时
B.线①代表滴定 溶液时pM与溶液pH的变化关系
C.滴定HA溶液至x点时,溶液中
D.滴定 溶液至x点时,改为滴加HA溶液,沉淀逐渐完全溶解
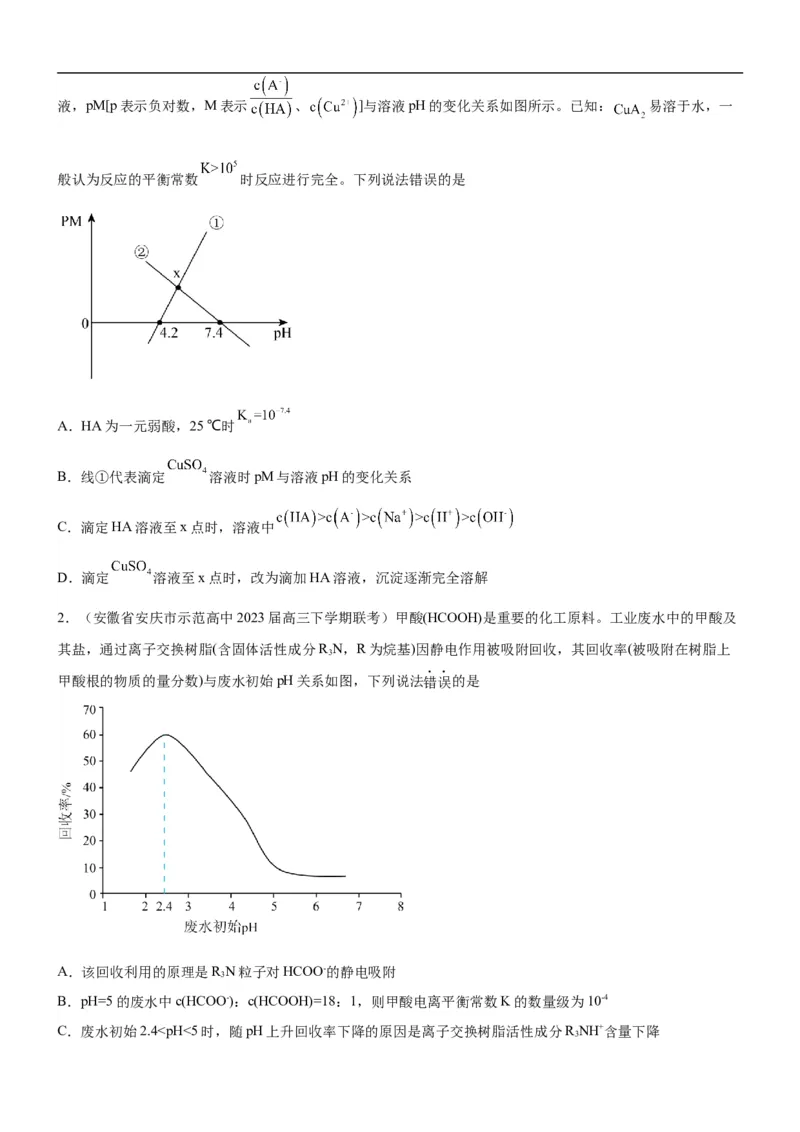
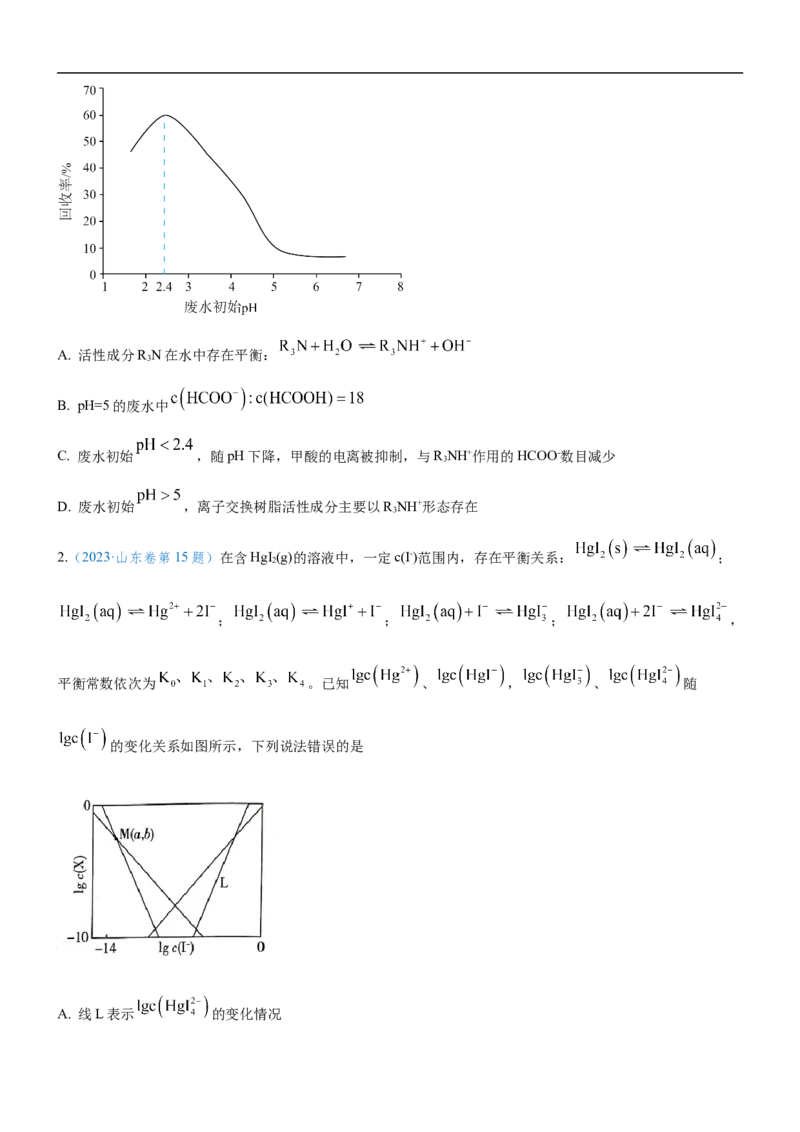
2.(安徽省安庆市示范高中2023届高三下学期联考)甲酸(HCOOH)是重要的化工原料。工业废水中的甲酸及
其盐,通过离子交换树脂(含固体活性成分R N,R为烷基)因静电作用被吸附回收,其回收率(被吸附在树脂上
3
甲酸根的物质的量分数)与废水初始pH关系如图,下列说法错误的是
A.该回收利用的原理是R N粒子对HCOO-的静电吸附
3
B.pH=5的废水中c(HCOO-):c(HCOOH)=18:1,则甲酸电离平衡常数K的数量级为10-4
C.废水初始2.4