文档内容
考点 23 化学平衡常数
分析近年来各省市高考卷均对化学平衡常数都作了考查。主要考查形式有四种:书写化学平衡常数表
达式;计算平衡常数;运用平衡常数判断反应方向;判断平衡常数与外界因素关系等。计算平衡常数易错
点主要有:用物质的量替代浓度直接计算,忘了体积;固体或液体物质引入平衡常数表达式中;读图像不
精确等。
预测2023年必将把握化学平衡常数这一平衡理论核心,关注考查方向:(1)根据图像、数据表、或转
化率、各物质浓度求平衡常数K;(2)根据平衡常数、-lgK与温度关系图像判断正反应是吸热还是放热;
(3)在平衡状态投入反应物和产物,利用平衡常数数据和判断反应方向;(4)有关有机反应、溶液中反应的平
衡常数计算或转化率的计算,可能涉及pH、Ksp、Kw等常数计算。可以预计选择有机反应、溶液中进行
的反应考查化学平衡问题成为命题热点。
一、化学平衡常数
二、化学反应速率常数
化学平衡常数
1.概念
在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一
个常数,用符号K 表示。
2.数学表达式:对于反应mA(g)+nB(g) pC(g)+qD(g)来说,K=。
注意:①不要把反应体系中纯固体、纯液体以及稀水溶液中水的浓度写进平衡常数表达式。例如:
CaCO (s) CaO(s)+CO(g) K=c(CO)
3 2 2
Cr O(aq)+HO(l) 2CrO(aq)+2H+(aq) K=
2 2
②同一化学反应,化学反应方程式写法不同,其平衡常数表达式亦不同。例如:
NO(g) 2NO (g) K=
2 4 2
NO(g) NO (g) K′==
2 4 22NO (g) NO(g) K″==
2 2 4
因此书写平衡常数表达式时,要与化学反应方程式相对应,否则意义就不明确。
(2)对于气体反应,写平衡常数表达式时,除可以用平衡时的物质的量浓度表示外,也可以用平衡时各
气体的分压来表示。例如:
N(g)+3H(g) 2NH (g) K =
2 2 3 p
其中:p(NH )、p(N )、p(H )分别为NH 、N 、H 的平衡分压,某气体平衡分压=平衡时总压×该气体
3 2 2 3 2 2
的物质的量分数。
3.平衡常数的意义
(1)平衡常数可表示反应进行的程度。K越大,反应进行的程度越大,K>105时,可以认为该反应已经
进行完全。转化率也能表示反应进行的程度,转化率不仅与温度有关,而且与起始条件有关。
(2)K的大小只与温度有关,与反应物或生成物起始浓度的大小无关。
4.浓度商:可逆反应进行到某时刻(包括化学平衡)时,生成物浓度幂之积与反应物浓度幂之积的比值
称为浓度商(Q)。对于化学反应aA(g)+bB(g) cC(g)+dD(g)的任意状态,浓度商:Q=。
Q<K,反应向正反应方向进行;
Q=K,反应处于平衡状态;
Q>K,反应向逆反应方向进行。
【易混易错】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)平衡常数表达式中,可以是物质的任一浓度( )
(2)催化剂既能改变速率常数,也能改变化学平衡常数( )
(3)对于同一可逆反应,升高温度,则化学平衡常数增大( )
(4)增大反应物的浓度,平衡正向移动,化学平衡常数增大( )
(5)Cl +HO HCl+HClO的平衡常数表达式 ( )
2 2
(6)某一化学反应的平衡常数与反应的温度有关,还与反应本身有关( )
(7)与某一化学反应的平衡常数化学反应本身和温度有关,并且会受到起始浓度的影响( )
(8)两种物质反应,不管怎样书写化学方程式,平衡常数不变( )
(9)温度一定时,对于给定的化学反应,正、逆反应的平衡常数互为倒数( )
(10)当生成物浓度幂之积与反应物浓度幂之积比值小于K时,v H O>CO
2 2 2 2 2
D.温度升高,上述三个反应的平衡常数均增大
【答案】C
【解析】A项,NO(g) N(g)+O(g)的平衡常数为()=1015,错误;B项,H 和O 之间的反应需
2 2 2 2
要点燃才能进行,错误;C项,常温下,NO、HO、CO 三种物质分解放出O 的平衡常数依次为1×1030、
2 2 2
5×10-82、4×10-92,平衡常数越大,则反应进行的程度越大,正确;D项,反应②为放热反应,升高温度平
衡逆向移动,平衡常数减小,错误。
例2 某温度下,在一个2 L的密闭容器中,加入4 mol X和2 mol Y进行如下反应:3X(g)+2Y(g)
4Z(s)+2W(g),反应一段时间后达到平衡,测得生成1.6 mol Z,则下列说法正确的是( )
A.该反应的化学平衡常数表达式是
B.此时,Y的平衡转化率是40%
C.增大该体系的压强,化学平衡常数增大
D.增加Y,Y的平衡转化率增大
【答案】B
【解析】化学平衡常数的表达式中不能出现固体或纯液体,而物质Z是固体,A错误;根据化学方程
式可知,平衡时减少的Y的物质的量是1.6 mol×=0.8 mol,所以Y的转化率为×100%=40%,B正确;平
衡常数只与温度有关,增大压强时平衡常数不变,C错误;增加Y后平衡右移,X的转化率增大,而Y的
转化率减小,D错误。
【对点提升】
对点1 在淀粉KI溶液中存在下列平衡:I(aq)+I-(aq) I(aq)。测得不同温度下该反应的平衡常
2
数K如表所示:
t/℃ 5 15 25 35 50
K 1 100 841 689 533 409
下列说法正确的是( )
A.反应I(aq)+I-(aq) I(aq)的ΔH>0
2
B.其他条件不变,升高温度,溶液中c(I)减小
C.该反应的平衡常数表达式为
D.25 ℃时,向溶液中加入少量KI固体,平衡常数K小于689
【答案】B
【解析】A项,温度升高,平衡常数减小,因此该反应是放热反应,ΔH<0,错误;B项,温度升高,平衡逆向移动,c(I)减小,正确;C项, ,错误;D项,平衡常数仅与温度有关,25 ℃
时,向溶液中加入少量KI固体,平衡正向移动,但平衡常数不变,仍然是689,错误。
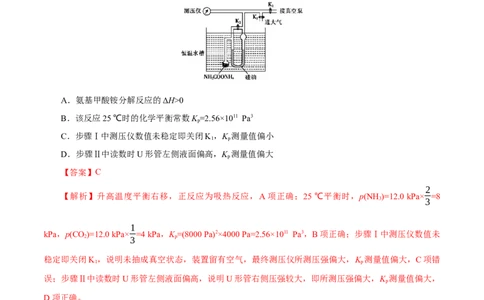
对点2 氨基甲酸铵发生分解的化学方程式为NH COONH(s) 2NH (g)+CO (g)。利用如下装置测定
2 4 3 2
不同温度下该反应以分压表示的化学平衡常数K 。
p
步骤Ⅰ:关闭K,打开K 和K,开启真空泵抽气至测压仪数值稳定后关闭K;
3 1 2 1
步骤Ⅱ:关闭K,缓慢开启K 至U形管两边液面相平并保持不变,读取压强数值。
2 3
记录25 ℃、30 ℃下压强分别为12.0 kPa、17.1 kPa。下列说法错误的是( )。
A.氨基甲酸铵分解反应的ΔH>0
B.该反应25 ℃时的化学平衡常数K =2.56×1011 Pa3
p
C.步骤Ⅰ中测压仪数值未稳定即关闭K,K 测量值偏小
1 p
D.步骤Ⅱ中读数时U形管左侧液面偏高,K 测量值偏大
p
【答案】C
2
【解析】升高温度平衡右移,正反应为吸热反应,A项正确;25 ℃平衡时,p(NH )=12.0 kPa× =8
3 3
1
kPa,p(CO)=12.0 kPa× =4 kPa,K =(8000 Pa)2×4000 Pa=2.56×1011 Pa3,B项正确;步骤Ⅰ中测压仪数值未
2 3 p
稳定即关闭K ,说明未抽成真空状态,装置留有空气,最终测压仪所测压强偏大,K 测量值偏大,C项错
1 p
误;步骤Ⅱ中读数时U形管左侧液面偏高,说明U形管右侧压强较大,即所测压强偏大,K 测量值偏大,
p
D项正确。
【巧学妙记】
化学平衡计算模式
对以下反应:mA(g)+nB(g) pC(g)+qD(g),令A、B起始物质的量(mol)分别为a、b,达到平衡
后,A的消耗量为mx,容器容积为V L。
mA(g)+nB(g) pC(g)+qD(g)
起始(mol) a b 0 0
变化(mol) mx nx px qx
平衡(mol) a-mx b-nx px qx(1)v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q(未达到平衡时,用于确定化学方程式中未知的化学计量数)。
(2)K==(Q是任意时刻的,则有Q>K,v v )。
正 逆 正 逆
(3)c(A) ==。
平
(4)α(A)=×100%=×100%。
(5)φ(A)=×100%。
(6)平衡时与起始时的压强比==(同T、V时),混合气体的密度比=(同T、P时),=(同质量的气体时)
等。
(7)混合气体的密度(混)==(g·L-1)(T、V不变时,不变)。
(8)混合气体的平均摩尔质量==(g·mol-1)。
化学反应速率常数
1.速率常数的含义
速率常数(k)是指在给定温度下,反应物浓度皆为1 mol·L-1时的反应速率。在相同的浓度条件下,可用
速率常数大小来比较化学反应的反应速率。
化学反应速率与反应物浓度(或浓度的次方)成正比,而速率常数是其比例常数,在恒温条件下,速率
常数不随反应物浓度的变化而改变。因此,可以应用速率方程求出该温度下任意浓度时的反应速率。
2.速率方程
对于反应:aA(g)+bB(g) gG(g)+hH(g),v =k ·cm(A)·cn(B)(其中k 为正反应的速率常数),v
正 正 正 逆
=k ·cp(G)·cq(H)(其中k 为逆反应的速率常数)。
逆 逆
m、n、p、q为实验测得数据,与计算系数不一定相等。
3.基元反应速率常数与化学平衡常数之间的关系
一定温度下,可逆反应:aA(g)+bB(g) gG(g)+hH(g),达到平衡状态时,v =k ·ca(A)·cb(B),v
正 正 逆
k cg(G)·cℎ(H)
正
=k ·cg(G)·ch(H),因平衡时v =v ,则k ·ca(A)·cb(B)=k ·cg(G)·ch(H), = =K。
逆 正 逆 正 逆 k ca(A)·cb(B)
逆
【典例】
例1 (2021·河北卷)室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:
①M+N X+Y;②M+N X+Z。反应①的速率可表示为 v=kc2(M),反应②的速率可表示为
1 1
v=kc2(M)(k 、k 为速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图。下列说法错误的是(
2 2 1 2
)。A.0~30 min 时间段内,Y的平均反应速率为6.67×10-8 mol·L-1·min-1
B.反应开始后,体系中Y 和Z的浓度之比保持不变
C.如果反应能进行到底,反应结束时 62.5%的M转化为Z
D.反应①的活化能比反应②的活化能大
【答案】A
【解析】依据三段式法,设第①个反应中M的起始物质的量浓度为a mol·L-1,N的起始物质的量浓度
为b mol·L-1,则:
①M +N X + Y
起始(mol·L-1): a b 0 0
反应(mol·L-1): c c c c
平衡(mol·L-1): a-c b-c c c
②M + N X+Z
起始(mol·L-1): 0.5-a 0.5-b 0 0
1 1 1 1
反应(mol·L-1):
8 8 8 8
1 1 1 1
平衡(mol·L-1): 0.5-a- 0.5-b-
8 8 8 8
1 0.075
30 min时,a-c+0.5-a- =0.3,可得到c=0.075,则v(Y)= mol·L-1·min-1=0.0025 mol·L-1·min-1,A
8 30
k
1
项错误;由题中信息可知,反应①和反应②的速率之比为 ,Y和Z分别为反应①和反应②的产物,且两
k
2
k
1
者与M的化学计量数相同(化学计量数均为1),因此反应开始后,体系中Y和Z的浓度之比等于 ,由于
k
2v k
1 1
k 、k 为速率常数,故该比值保持不变,B项正确;30 min内,v=kc2(M),v=kc2(M),可求得 = =
1 2 1 1 2 2 v k
2 2
0.075 3 5
= ,若反应能进行到底,反应结束时,有 的M转化为Z,即62.5%的M转化为Z,C项正确;由
0.125 5 8
上述分析知,在相同时间内生成Z较多,生成Y较少,因此反应①的化学反应速率小,在同一体系中,活
化能较小的化学反应速率较快,故反应①的活化能比反应②的活化能大,D项正确。
例2 温度为T 时,在三个容积均为1 L的恒容密闭容器中仅发生反应:2NO (g) 2NO(g)+O (g)
1 2 2
(正反应吸热)。实验测得:v =v(NO ) =k ·c2(NO ),v =v(NO) =2v(O ) =k ·c2(NO)·c(O ),k 、k 为
正 2 消耗 正 2 逆 消耗 2 消耗 逆 2 正 逆
速率常数,受温度影响。下列说法正确的是( )
容器 物质的起始浓度(mol·L-1) 物质的平衡浓度(mol·L-1)
编号 c(NO ) c(NO) c(O ) c(O )
2 2 2
Ⅰ 0.6 0 0 0.2
Ⅱ 0.3 0.5 0.2
Ⅲ 0 0.5 0.35
k
逆
A.设K为该反应的化学平衡常数,则有K=
k
正
B.达平衡时,容器Ⅱ与容器Ⅲ中的总压强之比为20∶17
C.容器Ⅱ中起始时平衡正向移动,达到平衡时,容器Ⅱ中NO 的转化率比容器Ⅰ中的小
2
D.若改变温度为T,且T>T ,则k ∶k <0.8
2 2 1 正 逆
【答案】C
【解析】平衡时,正、逆反应速率相等,则有 k ·c2(NO )=k ·c2(NO)·c(O ),所以 K=
正 2 逆 2
c2(NO)·c(O ) k
2 = 正,A 项错误。根据化学方程式和容器 Ⅰ 中 O 的平衡浓度可知,平衡时,
c2(NO ) k 2
2 逆
c2(NO)·c(O )
2
c(NO)=0.4 mol·L-1,c(NO )=0.2 mol·L-1,则 T 温度下,该反应的平衡常数 K= =
2 1 c2(NO )
2
0.42×0.2 0.2×0.52
=0.8;容器Ⅱ中浓度商Q= ≈0.56<0.8,反应正向进行,气体的总物质的量大于 1
0.22 c 0.32
mol,而容器Ⅲ中反应向左进行,气体的总物质的量小于0.85 mol,所以达到平衡时,容器Ⅱ与容器Ⅲ中的0.4 2
总压强之比大于20∶17,B项错误。容器Ⅰ中NO 的转化率为 = ,假设容器Ⅱ中NO 的转化率也为
2 0.6 3 2
2
,反应正向进行:
3
2NO (g) 2NO(g)+O (g)
2 2
起始量(mol·L-1) 0.3 0.5 0.2
变化量(mol·L-1) 0.2 0.2 0.1
平衡量(mol·L-1) 0.1 0.7 0.3
0.3×0.72 2
平衡常数K= =14.7>0.8,所以容器Ⅱ中NO 的转化率小于 ,即容器Ⅱ中起始平衡正向移
0.12 2 3
动,达到平衡时,容器Ⅱ中NO 的转化率比容器Ⅰ中的小,C项正确。因为该反应的正反应是吸热反应,
2
温度T>T ,所以T 时平衡常数增大,则k ∶k >0.8,D项错误。
2 1 2 正 逆
【对点提升】
对点1 氨气去除NO的反应原理为:4NH (g)+6NO(g) 5N(g)+6HO(g) ΔH<0,反应速率与浓度
3 2 2
之间存在如下关系:v =k ·c4(NH )·c6(NO),v =k ·c5(N )·c6(H O),k 、k 为速率常数,只受温度影响。
正 正 3 逆 逆 2 2 正 逆
350℃时,在2L恒容密闭容器中,通入0.9molNH (g)和1.2molNO(g)发生反应,保持温度不变,5min后反
3
应达平衡,NO的转化率为50%。下列说法正确的是( )
A.用NH 表示的化学反应速率为0.06mol·L-1·min-1
3
B.350℃时,该反应的平衡常数为0.5
C.其他条件不变,往反应后的容器中再通入0.9molNH (g)和1.2molNO(g),重新达平衡时NO的体积
3
分数增大
D.当温度改变为T°C时,若k =k ,则T>350
正 逆
【答案】C
【解析】由题意可得如下三段式:
A项,由三段式数据可知,用氨气表示的化学反应速率为 =0.04mol·L-1·min-1,故A错误;B项,由三段式数据可知,350℃时,反应的平衡常数为 =0.25,故B错误;C项,
其他条件不变,往反应后的容器中再通入0.9mol氨气和1.2mol一氧化氮相当于增大压强,该反应是气体体
积增大的反应,增大压强,平衡向逆反应方向移动,一氧化氮的体积分数增大,故C正确;D项,反应达
到平衡时,正反应速率和逆反应速率相等,则反应速率k ·c4(NH )·c6(NO) =k ·c5(N )·c6(H O), =
正 3 逆 2 2
=K,当k =k 时,平衡常数K=1>0.25说明平衡向正反应方向移动,该反应为放热反应,
正 逆
则反应温度小于350℃,故D错误;故选C。
对点2 T 温度下,在三个容积均为1L的恒容密闭容器中发生如下反应:2NO (g) NO(g)
1 2
+O (g) ΔH>0。实验测得: , , 、
2
为速率常数,受温度影响。下列说法正确的是( )
物质的起始浓度(mol·L-1) 物质的平衡浓度(mol·L-1)
容器编号
c(NO ) c(NO) c(O) c(O)
2 2 2
I 0.6 0 0 0.2
II 0.3 0.5 0.2
III 0 0.5 0.35
A.设K为该反应的化学平衡常数,则有
B.若改变温度为 ,且 ,则
C.容器II中起始时平衡正向移动,达平衡时,容器II中 的转化率比容器I中的大
D.达平衡时,容器II与容器III中的总压强之比大于20:17
【答案】D【解析】根据反应方程式和容器Ⅰ中O 的平衡浓度可知:平衡时,c(NO)=0.4mol·L-1,
2
c(NO )=0.2mol·L-1,则T 温度下,该反应的平衡常数 。A项,平衡时,
2 1
正、逆反应速率相等,则有 ,所以K= = ;A错误;B项,由
于该反应正反应是吸热反应,温度T>T,所以T 时平衡常数增大,则k :k >0.8,B错误;C项,针
2 1 2 正 逆
对于容器Ⅰ内反应可知:NO 的转化率为 ,容器II中起始时平衡正向移动,假设容器Ⅱ中NO 的转
2 2
化率也为 ,则:
浓度商Q = =14.7>0.8,所以容器Ⅱ中NO 的转化率小于 ,即容器Ⅱ中起始平衡正向移动,
C 2
达平衡时,容器Ⅱ中NO 的转化率比容器Ⅰ中的小,C错误;D项,T 温度下,该反应的平衡常数
2 1
K=0.8,容器Ⅱ中浓度商Q = =0.56<0.8,反应正向移动,气体的总量大于1mol,而容器Ⅲ中反应
C
向左进行,气体的总量小于0.85mol,所以达平衡时,容器Ⅱ与容器Ⅲ中的总压强之比大于20∶17,D正
确;故选D。
1.下列关于化学平衡常数的说法中错误的是( )
A.某特定反应的平衡常数只与温度有关
B.催化剂不能改变平衡常数的大小
C.平衡常数发生改变,化学平衡必发生改变
D.化学平衡移动时,平衡常数必改变【答案】D
【解析】A项,平衡常数只与温度有关,A项不符合题意;B项,平衡常数只受到温度的影响,催化
剂不能改变平衡常数的大小,B项不符合题意;C项,平衡常数变大,平衡正向移动,平衡常数减小,平
衡逆向移动,平衡常数改变,化学平衡必然移动,C项不符合题意;D项,平衡常数只受温度的影响,能
引起平衡移动的因素有多个,只有平衡因为温度变化而移动时,平衡常数才会改变,D项符合题意;故正
确选项为D
2.只改变一个影响化学平衡的因素,平衡常数K与化学平衡移动的关系叙述不正确的是( )
A.K值不变,平衡可能移动
B.平衡向右移动时,K值不一定变化
C.K值有变化,平衡一定移动
D.相同条件下,同一个反应的方程式的化学计量数增大2倍,K值也增大两倍
【答案】D
【解析】因改变压强或浓度引起化学平衡移动时,K值不变,A项和B项均正确;K值只与温度有关,
K值发生了变化,说明体系的温度改变,则平衡一定移动,C项正确;相同条件下,同一个反应的方程式
的化学计量数增大2倍,K值应该变为K,D项错误。
3.在25 ℃时,密闭容器中X、Y、Z三种气体的起始浓度和平衡浓度如下表,下列说法错误的是(
)
物质 X Y Z
起始浓度/(mol·L-1) 0.1 0.2 0
平衡浓度/(mol·L-1) 0.05 0.05 0.1
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y 2Z,平衡常数为1 600
C.其他条件不变时,增大压强可使平衡常数增大
D.改变温度可以改变该反应的平衡常数
【答案】C
【解析】达到平衡消耗 X 的物质的量浓度为(0.1-0.05)mol·L-1=0.05 mol·L-1,因此转化率为
0.05/0.1×100%=50%,A项正确;根据化学反应速率之比等于化学计量数之比,因此三种组分的系数之比
为:(0.1-0.05)∶(0.2-0.05)∶0.1=1∶3∶2,因此反应方程式为:X+3Y 2Z,根据化学平衡常数的
表达式,K=0.12/(0.05×0.053)=1 600,B项正确;化学平衡常数只受温度的影响,与浓度、压强无关,C
项错误、D项正确。
4.在恒温条件下,向盛有食盐的2L恒容密闭容器中加入0.2mol NO 、0.2moI NO 和0.1mol Cl ,发
2 2生如下两个反应:
①2NO (g)+NaCl(s) NaNO (s)+ClNO(g) H<0平衡常数 K
2 3 1 1
②2NO(g)+Cl (g) 2ClNO(g) H<0平衡常数 K
2 2 2
10 分钟时反应达到平衡,测得容器内体系的压强减少 20%,10 分钟内用ClNO(g)表示 的平均反应
速率v(ClNO)=7.5×10-3mol/(L·min)。下列说法正确的是
A.平衡时 NO 的转化率为50%
2
B.平衡后 c(NO)=2.5×10-2mol·L-1
C.其它条件保持不变,反应在恒压条件下进行,则平衡常数K 增大
2
D.反应 4NO (g)+2NaCl(s) 2NaNO (s)+2NO(g)+Cl (g)的平衡常数为K 2-K
2 3 2 2 1
【答案】A
【解析】A项,10min时反应达到平衡,测得容器内体系的压强减少20%,则平衡时混合气体总物质
的量为(0.2+0.2+0.1)mol×(1-20%)=0.4mol,10min内用ClNO(g)表示的平均反应速率v(ClNO)=7.5×10-3mol/
(L·min),则平衡时n(ClNO)=7.5×10-3mol/(L•min)×10min×2L=0.15mol,设①中反应的NO 为x mol,②中反
2
应的Cl 为ymol,则:
2
则0.5x+2y=0.15,(0.2-x+0.2-2y+0.1-y)+0.5x+2y=0.4,联立方程,解得x=0.1、y=0.05,故平衡时NO 的
2
转化率为 ,故A正确;B项,由A项分析,平衡后c(NO)=
,故B错误;C项,平衡常数只受温度影响,温度不变,平
衡常数不变,则其它条件保持不变,反应在恒压条件下进行,平衡常数K 不变,故C错误;D项,
2
①2NO (g)+NaCl(s) NaNO (s)+ClNO(g) H<0平衡常数K ;②2NO(g)+Cl (g) 2ClNO(g)
2 3 1 1 2
△H<0平衡常数K ;由盖斯定律可知,由①×2-②可得反应4NO (g)+2NaC1(s) 2NaNO (s)+2NO(g)
2 2 2 3
△
+Cl(g),则4NO (g)+2NaC1(s) 2NaNO (s)+2NO(g)+Cl (g)的平衡常数 ,故D错误;故选
2 2 3 2
A。
5.CO 是目前大气中含量最高的一种温室气体。因此,控制和治理CO 是解决温室效应的有效途径。
2 2
已知反应Fe(s)+CO (g) FeO(s)+CO(g)的平衡常数为K;
2 1
反应Fe(s)+H O(g) FeO(s)+H (g)的平衡常数为K。
2 2 2
在不同温度时K、K 的值如下表:
1 2
温度(绝对温度) K K
1 2
973 1.47 2.38
1173 2.15 1.67
(1)推导反应CO(g)+H(g) CO(g)+HO(g)的平衡常数K与K、K 的关系式:
2 2 2 1 2
_____________________。
(2)通过K值的计算,(1)中的反应是_________反应(填“吸热”或“放热”)。
(3)在一体积为10L的密闭容器中,加入一定量的CO 和HO(g),在1173开时发生反应并记录前5min
2 2
的浓度,第6min时改变了反应的条件。各物质的浓度变化如下表:
时间/min CO HO CO H
2 2 2
0 0.2000 0.3000 0 0
2 0.1740 0.2740 0.0260 0.0260
3 c c c c
1 2 3 3
4 c c c
1 2 3
5 0.0727 0.1727 0.1273 0.1273
6 0.0350 0.1350 0.1650
①前2min,用CO表示的该化学反应的速率是:_______________________。
②在3~4min之间,反应处于___________状态(填“平衡”或“非平衡”)。
③第6min时,平衡向_________方向移动,可能的原因是______________________。
【答案】(1)K= (2)吸热 (3)①v(CO)=0.0130mol·L-1·nin-1 ②平衡③右或正反应 升高温度或降低了H 浓度
2
【解析】(1)CO (g)+H(g) CO(g)+HO(g)平衡常数K的表达式K= ;Fe(s)
2 2 2
+CO (g) FeO(s)+CO(g)的平衡常数为K= ;Fe(s)+H O(g) FeO(s)+H (g)的平衡常数为
2 1 2 2
K= ,由平衡常数分析计算可知,K与K、K 二者的关系为K= ;(2)973时,K= =
2 1 2
=0.68;1173时,K= = =1.43;故升高温度,K值增大,平衡正向移动,(1)中的反应是吸热反应;
(3)①前2min,用CO表示的该化学反应的速率c(CO)= =0.013mol/(L•min);②由表中数据可知,
3min、 4min时, 反应混合物对应物质的浓度不变,处于与平衡状态; ③表6min时, CO 浓度降低、
2
HO的浓度减小、CO的浓度增大,说明平衡向正反应移动,正反应为吸热反应,可能是升高温度,由于
2
氢气物质的量未知,也可能是降低氢气浓度。
6.CO 是目前大气中含量最高的一种温室气体。因此,控制和治理CO 是解决温室效应的有效途径。
2 2
已知反应Fe(s)+CO (g) FeO(s)+CO(g)的平衡常数为K;
2 1
反应Fe(s)+H O(g) FeO(s)+H (g)的平衡常数为K。
2 2 2
在不同温度时K、K 的值如下表:
1 2
温度(绝对温度) K K
1 2
973 1.47 2.38
1173 2.15 1.67
(1)推导反应CO(g)+H(g) CO(g)+HO(g)的平衡常数K与K、K 的关系式:
2 2 2 1 2
_____________________。
(2)通过K值的计算,(1)中的反应是_________反应(填“吸热”或“放热”)。(3)在一体积为10L的密闭容器中,加入一定量的CO 和HO(g),在1173开时发生反应并记录前5min
2 2
的浓度,第6min时改变了反应的条件。各物质的浓度变化如下表:
时间/min CO HO CO H
2 2 2
0 0.2000 0.3000 0 0
2 0.1740 0.2740 0.0260 0.0260
3 c c c c
1 2 3 3
4 c c c
1 2 3
5 0.0727 0.1727 0.1273 0.1273
6 0.0350 0.1350 0.1650
①前2min,用CO表示的该化学反应的速率是:_______________________。
②在3~4min之间,反应处于___________状态(填“平衡”或“非平衡”)。
③第6min时,平衡向_________方向移动,可能的原因是______________________。
【答案】(1)K= (2)吸热 (3)①v(CO)=0.0130mol·L-1·nin-1 ②平衡
③右或正反应 升高温度或降低了H 浓度
2
【解析】(1)CO (g)+H(g) CO(g)+HO(g)平衡常数K的表达式K= ;Fe(s)
2 2 2
+CO (g) FeO(s)+CO(g)的平衡常数为K= ;Fe(s)+H O(g) FeO(s)+H (g)的平衡常数为
2 1 2 2
K= ,由平衡常数分析计算可知,K与K、K 二者的关系为K= ;(2)973时,K= =
2 1 2
=0.68;1173时,K= = =1.43;故升高温度,K值增大,平衡正向移动,(1)中的反应是吸热反应;(3)①前2min,用CO表示的该化学反应的速率c(CO)= =0.013mol/(L•min);②由表中数据可知,
3min、 4min时, 反应混合物对应物质的浓度不变,处于与平衡状态; ③表6min时, CO 浓度降低、
2
HO的浓度减小、CO的浓度增大,说明平衡向正反应移动,正反应为吸热反应,可能是升高温度,由于
2
氢气物质的量未知,也可能是降低氢气浓度。
7.100 kPa时,反应2NO(g)+O(g) 2NO (g)中NO的平衡转化率与温度的关系曲线如图1,反
2 2
应2NO (g)NO(g)中NO 的平衡转化率与温度的关系曲线如图2。
2 2 4 2
(1)图1中A、B、C三点表示不同温度、压强下2NO(g)+O(g)2NO (g)达到平衡时NO的转化率,
2 2
则________点对应的压强最大。
(2)100 kPa、25 ℃时,2NO (g)NO(g)平衡体系中NO 的物质的量分数为________,NO 的分压
2 2 4 2 4 2 4
p(N O)=__________kPa,列式计算平衡常数K =__________(K 用平衡分压代替平衡浓度计算,分压=总
2 4 p p
压×物质的量分数)。
(3)100 kPa、25 ℃时,V mL NO与0.5V mL O 混合后最终气体的体积为________ mL。
2
【答案】(1)B (2)66.7% 66.7 = kPa-1≈0.06 kPa-1
(3)0.6V
【解析】(1)图1中曲线为等压线,A、C在等压线下方,B在等压线上方,A、C点相对等压线,NO
的平衡转化率减小,则平衡逆向移动,为减小压强所致,B点相对等压线,NO的平衡转化率增大,则平
衡正向移动,为增大压强所致,故压强最大的点为 B点。(2)100 kPa、25 ℃时,NO 的平衡转化率为
2
80%,设起始时NO 的浓度为a,则平衡时NO 的浓度为0.2a、NO 的浓度为0.4a,故NO 的物质的量分
2 2 2 4 2 4
数为×100%≈66.7%。NO 的分压 p(N O)=100 kPa×66.7%=66.7 kPa。K == kPa-1≈0.06 kPa-1。(3)100
2 4 2 4 p
kPa、25 ℃时,V mL NO与0.5V mL O
2
生成V mL NO
2,
2NO
2
(g)N
2
O
4
(g)平衡体系中NO
2
的转化率为
80%,知平衡时气体的体积为V mL×(1-80%)+V mL×80%×=0.6V mL。
8.许多含氮物质是农作物生长的营养物质。
(1)一定温度下,向某密闭容器中充入1 mol NO ,发生反应:2NO (g) NO(g)。测得反应体系
2 2 2 4中两种气体的体积分数与压强之间的关系如图所示:
①a、b、c三点逆反应速率由大到小的顺序为 。平衡时若保持压强、温度不变,再向体系中
加入一定量的Ne,则平衡 (填“正向”、“逆向”或“不”)移动。
②a点时NO 的转化率为 ,用平衡分压代替平衡浓度可求出平衡常数K ,则该温度下K =
2 p p
(用含p 的代数式表示)。
0
(2)已知在一定温度下的可逆反应NO(g) 2NO (g) ΔH>0中,v =k ·c(N O),v =k ·c2(NO )
2 4 2 正 正 2 4 逆 逆 2
(k 、k 只与温度有关)。若该温度下的平衡常数K=10,则k = k ,升高温度,k 增大的倍数
正 逆 正 逆 正
(填“大于”、“小于”或“等于”)k 增大的倍数。
逆
600
【答案】(1)①c>b>a 逆向 ②66.7%
p
0
(2)10 大于
【解析】(1)①由图可知,a点到c点的过程中,NO 的体积分数不断增大,故逆反应速率不断增大;
2 4
一定温度下,保持压强不变,加入稀有气体,相当于减小压强,故平衡逆向移动。②a点时,设消耗了x
2
mol NO ,则生成0.5x mol N O ,剩余(1-x) mol NO ,由图可知1-x=0.5x,x= ,此时NO 的转化率为
2 2 4 2 3 2
600
66.7%;平衡时p(N O)=0.96p ,p(NO )=0.04p ,由此可求出K = 。(2)当反应达到平衡时,v =v ,即
2 4 0 2 0 p p 正 逆
0
k ·c2(NO )
k ·c(N O)=k ·c2(NO ),k = 逆 2 =k ·K=10k ;该反应是吸热反应,升高温度,平衡向正反
正 2 4 逆 2 正 c(N O ) 逆 逆
2 4
应方向移动,k 增大的倍数大于k 增大的倍数。
正 逆
1.(2022·全国金太阳大联考)一定温度下,反应MgCl (l) Mg(l)+Cl (g)达到平衡时,下列说法错
2 2
误的是A.该反应的平衡常数K=c(Cl )
2
B.将容器体积压缩为原来一半,当体系再次达到平衡时,Cl 的浓度增大
2
C.减小氯气浓度,平衡正向移动,平衡常数不变
D.温度升高该反应的化学平衡常数K增大
【答案】B
【解析】A项,化学平衡常数(固体或液体纯物质一般不列入平衡常数)是指反应达到平衡时,各生成
物浓度的化学计量数次幂的乘积与各反应物浓度的化学计量数次幂的乘积的比值,则该反应的平衡常数
K=c(Cl ),故A正确;B项,K=c(Cl ),温度不变,平衡常数不变,因此将容器体积压缩为原来一半,当体
2 2
系再次达到平衡时,Cl 的浓度不变,故B错误;C项,平衡常数只与温度有关,温度不变,平衡常数不变,
2
故C正确;D项,镁在氯气中燃烧是放热反应,则MgCl (l) Mg(l)+Cl (g)为吸热反应,升高温度,平
2 2
衡正向移动,平衡常数K增大,故D正确;故选B。
2.(2022·河北省秦皇岛市二模)在二氧化碳加氢制甲烷的反应体系中,除主反应(反应Ⅰ)外,还会发生
副反应(反应Ⅱ)。
反应Ⅰ:CO(g)+4H(g) CH(g)+2HO(g) K I
2 2 4 2 I
反应Ⅱ:CO(g)+H(g) CO(g)+HO(g) K
2 2 2 II
一定压强下,向某容积可变的密闭容器中通入CO 和H 的混合气体(其中CO 和H 的物质的量之比为
2 2 2 2
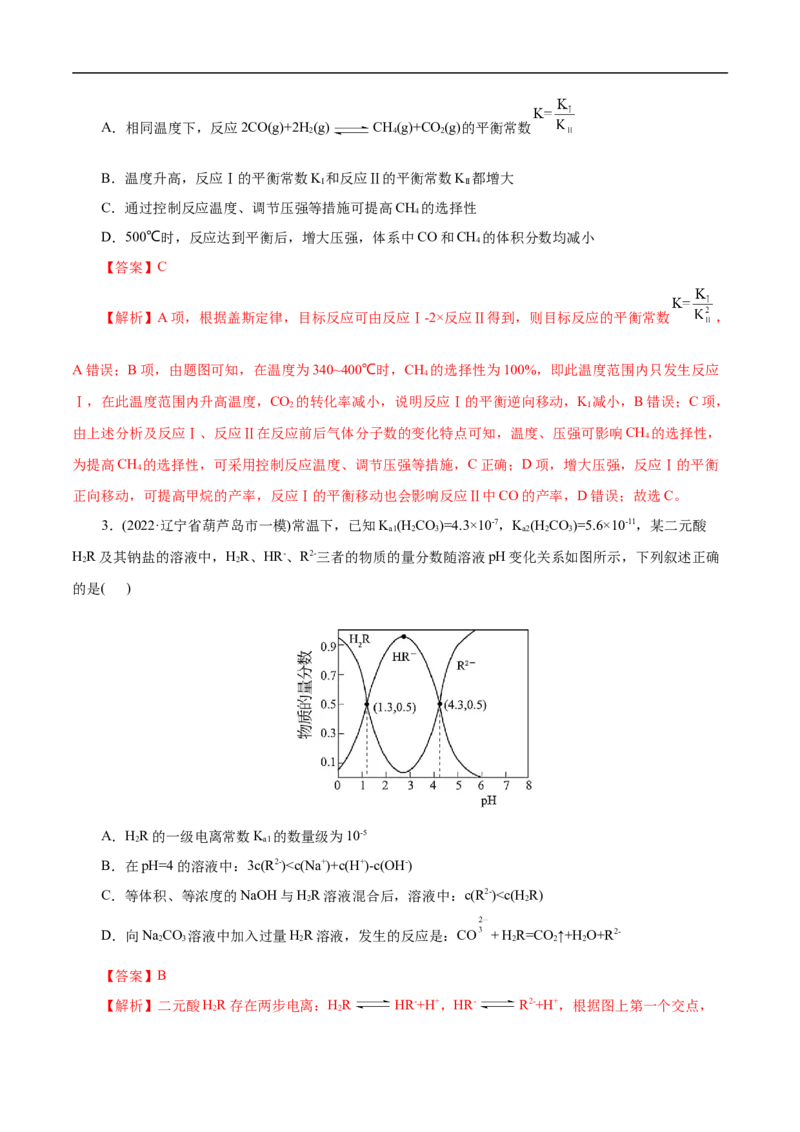
1∶4),在某催化剂的作用下同时发生反应Ⅰ和反应Ⅱ,测得CO 的转化率、CH 的选择性、CO的选择性
2 4
随反应温度的变化情况如图所示。
已知:CH 或CO的选择性指反应生成CH 或CO时所消耗的CO 的物质的量占参与反应的CO 总物质
4 4 2 2
的量的百分比。
下列说法正确的是( )A.相同温度下,反应2CO(g)+2H(g) CH(g)+CO (g)的平衡常数
2 4 2
B.温度升高,反应Ⅰ的平衡常数K 和反应Ⅱ的平衡常数K 都增大
I II
C.通过控制反应温度、调节压强等措施可提高CH 的选择性
4
D.500℃时,反应达到平衡后,增大压强,体系中CO和CH 的体积分数均减小
4
【答案】C
【解析】A项,根据盖斯定律,目标反应可由反应Ⅰ-2×反应Ⅱ得到,则目标反应的平衡常数 ,
A错误;B项,由题图可知,在温度为340~400℃时,CH 的选择性为100%,即此温度范围内只发生反应
4
Ⅰ,在此温度范围内升高温度,CO 的转化率减小,说明反应Ⅰ的平衡逆向移动,K 减小,B错误;C项,
2 I
由上述分析及反应Ⅰ、反应Ⅱ在反应前后气体分子数的变化特点可知,温度、压强可影响CH 的选择性,
4
为提高CH 的选择性,可采用控制反应温度、调节压强等措施,C正确;D项,增大压强,反应Ⅰ的平衡
4
正向移动,可提高甲烷的产率,反应Ⅰ的平衡移动也会影响反应Ⅱ中CO的产率,D错误;故选C。
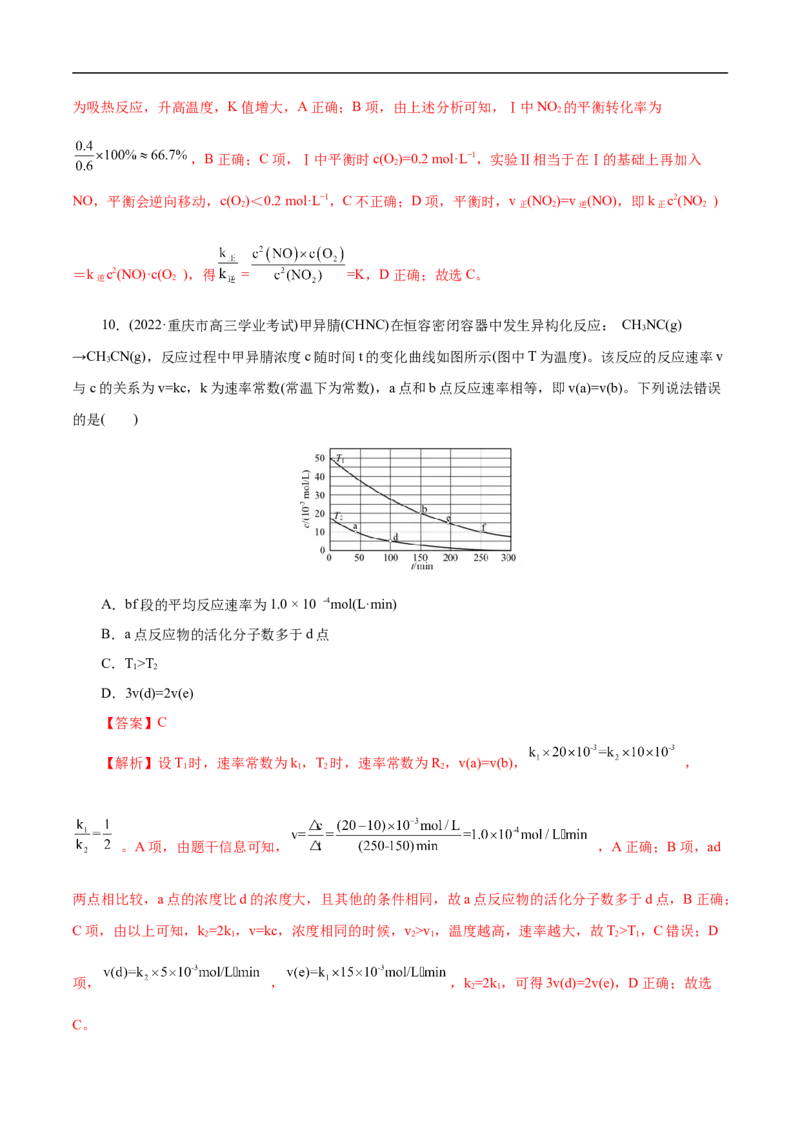
3.(2022·辽宁省葫芦岛市一模)常温下,已知K (H CO)=4.3×10-7,K (H CO)=5.6×10-11,某二元酸
a1 2 3 a2 2 3
HR及其钠盐的溶液中,HR、HR-、R2-三者的物质的量分数随溶液pH变化关系如图所示,下列叙述正确
2 2
的是( )
A.HR的一级电离常数K 的数量级为10-5
2 a1
B.在pH=4的溶液中:3c(R2-)K ,说明
2 a2 h2
电离程度大于水解程度,溶液显酸性,故电离产物c(R2-)大于水解产物c(HR),即c(R2-)>c(H R),故C错误:
2 2
D项,根据弱酸的电离平衡常数越大酸性越强,由于K (H R)>K (H R)>K (H CO)>K (H CO),可得酸性
a1 2 a2 2 a1 2 3 a2 2 3
HR>HR->H CO>HCO-,向NaCO 溶液中加入过量HR溶液,因为根据强酸制弱酸的原理,CO2-转化为
2 2 3 3 2 3 2 3
CO,并生成HR-,发生的反应是CO2-+2H R=CO ↑+H O+2HR-,故D错误;故选 B。
2 3 2 2 2
4.(2022·江苏省南通市高三模拟预测)室温时,通过实验探究(NH )C O 溶液的性质,操作及现象如下
4 2 2 4
表所示。
实
实验操作及现象
验
1 测定0.1mol·L-1(NH )C O 溶液的pH,测得溶液pH <7
4 2 2 4
2 向0.1mol·L-1(NH )C O 溶液中加入等体积0.1mol·L-1 CaCl 溶液,产生白色沉淀,过滤
4 2 2 4 2
3 向实验2所得白色沉淀中加入10mL0.1mol·L-1 Na CO 溶液,浸泡一段时间,无明显现象
2 3
下列说法正确的是( )
A.0.1mol·L-1(NH )C O 溶液中存在:
4 2 2 4
B.由实验1可得:
C.由实验2可得:
D.由实验3可得浸泡所得溶液中存在:【答案】C
【解析】A项,0.1mol·L-1(NH )C O 溶液中存在物料守恒
4 2 2 4
,电荷守恒
,所以溶液中存在
,故A错误;B项,0.1mol·L-1(NH )C O 溶液的pH<
4 2 2 4
7,溶液显酸性,但由于铵根的浓度是草酸根浓度的2倍,所以不能说明二者水解程度的相对大小,故B
错误;C项,向0.1mol·L-1(NH )C O 溶液中加入等体积0.1mol·L-1 CaCl 溶液,产生白色沉淀,则Q>
4 2 2 4 2 c
K (CaC O),即K (CaC O)<Q=c(Ca2+)• = =2.5×10-3,故C正确;D项,由于碳酸钙也是
sp 2 4 sp 2 4 c
不溶于水的白色沉淀,所以由实验3不能得出浸泡所得溶液中存在: ,故D
错误;故选C。
5.(2022·辽宁省锦州市一模)精炼铜工业中阳极泥的综合利用具有重要意义,从中间产品分金渣(主要
成分为:AgCl、Ag S、PbSO 、BaSO)中获取高纯银的流程如下图所示。下列说法错误的是( )
2 4 4
已知:在上述反应的温度下
① , ;
②[Ag(SO )]3- Ag++2SO 2- K=1.0×10-8.68 。
3 2 3
A.“分银”时AgCl与NaSO 反应生成[Ag(SO )]3-的离子方程式为AgCl+2SO 2- Ag(SO )]3-
2 3 3 2 3 3 2
+Cl-,该反应的化学平衡常数为
B.“分银渣”的主要成分为PbSO 、BaSO、Ag S
4 4 2
C.“沉银”时为防止产生污染性有毒气体,盐酸不宜过量D.若“还原”时有CO 生成,则该反应中氧化剂与还原剂的物质的量之比为4:1
2
【答案】B
【解析】A项,离子方程式为AgCl+2SO2- [Ag(SO)]3-+Cl-,该反应的化学平衡常数表达式为
3 3 2
,A项正确;B项,加入氯化铁进行预处理,氯化铁
具有氧化性,能与硫化银发生氧化还原反应生成硫单质,“分银”时加入亚硫酸钠,AgCl与NaSO 反应
2 3
生成[Ag(SO)]3-,而“分银渣”的主要成分为PbSO 、BaSO、S,B项错误;C项,“沉银”时加入盐酸,
3 2 4 4
使[Ag(SO)]3-生成氯化银沉淀,盐酸会与亚硫酸钠反应产生二氧化硫有毒气体,故盐酸不宜过量,C项正
3 2
确;D项,“还原”时氯化银和甲醛反应生成CO、单质银和氯化氢,化学方程式为:
2
4AgCl+HCHO+H O=4Ag+CO+4HCl,氧化剂为AgCl,还原剂为HCHO,则该反应中氧化剂与还原剂的物
2 2
质的量之比为4:1,D项正确;故选B。
6.(2022·江苏省扬州市高三阶段检测)室温下:K (H C O)=10-1.26、K (H C O)=10-4.27、
a1 2 2 4 a2 2 2 4
K (CaC O)=10-8.64,实验室进行多组实验测定某些酸、碱、盐性质,相关实验记录如下:
sp 2 4
实验1测定某浓度NaHC O 溶液的pH=4.3
2 4
实验2配制pH相等的(NH )SO 、NH Cl、NH HSO 三种溶液
4 2 4 4 4 4
实验3向0.10mol·L-1NaC O 溶液中滴加等浓度盐酸后,混合溶液的pH=7
2 2 4
实验4向0.10mol·L-1NaHC O 溶液加入一定体积的等浓度CaCl 溶液产生白色沉淀,测得上层清液
2 4 2
pH=4,c(Ca2+)=10-4mol·L-1
下列所得结论正确的是( )
A.实验1中 c(HC O) = 103.07c(C O2-)
2 2 4 2 4
B.实验2中溶液浓度的大小关系为:c(NH Cl)c[(NH )SO ]>c(NH HSO ),
4 4 4 2 4 4 4
故B错误;C项,混合溶液中存在电荷守恒: ,混
合溶液的pH=7,即 ,则有 ,故C错误;D项,上层
清液c(Ca2+)=10-4mol·L-1,则 ,pH=4,即 ,则
,故D正确;故选D。
7.(2022·浙江省镇海市高三选考模拟)硫酸工业中,将SO 氧化为SO 是生产工艺中的重要环节。在温
2 3
度为T 条件下,在三个容积均为1L的恒容密闭容器中仅发生反应:2SO (g)+O(g) 2SO (g)ΔH<0,实
1 2 2 3
验测得:v =k ·c2(SO )·c(O),v =k ·c2(SO )。
正 正 2 2 逆 逆 3
起始浓度/(mol·L-1) 平衡浓度/(mol·L-1)
容器编号
c(SO ) c(O) C(SO ) c(O)
2 2 3 2
I 0.6 0.3 0 0.2
II 0.5 x 0.3
III 0.3 0.25 0.2
已知:k 、k 为速率常数,仅受温度的影响。
正 逆
下列说法错误的是( )
A.达到平衡时,平衡常数和速率常数的关系:B.若容器II中达到平衡时 =1,则x=0.85
C.容器III中达到平衡时,c(O)<0.25mol·L-1
2
D.当温度升高为T 时,k 、k 分别增大m倍和n倍,则mK,
此时平衡向逆反应方向移动,则平衡时O 的浓度c(O)>0.25mol·L-1,C项错误;D项,ΔH<0,温度升高,
2 2
平衡向逆反应方向移动,k 增大的幅度更大,n>m,D项正确。故选C。
逆
8.(2022·河北省张家口市高三联考)在一定温度下的可逆反应X(g)= 2Y(g) ,
, ,若该温度下的平衡常数K=10,下列说法错误的是( )
A.该温度下
B.升高温度, 增大的倍数大于 增大的倍数
C.有利于测定X的相对分子质量的条件为低温高压
D.恒压条件下,向平衡体系中充入惰性气体He,X的转化率减小【答案】D
【解析】A项,达到平衡时, ,则 ,平衡常数 ,即
,故A正确;B项,该反应的正反应为吸热反应,升高温度,平衡正向移动,所以 增大的倍
数大于 增大的倍数,故B正确;C项,测定X的相对分子质量时应该使平衡尽可能逆向移动,该反应的
正反应为气体分子数增多的吸热反应,所以条件为低温高压,故C正确;D项,恒压条件下,向平衡体系
中充入惰性气体He,体积增大,压强减小,平衡正向移动,X的转化率增大,故D错误;故选D。
9.(2022·北京市人大附中三模)某温度时两个恒容密闭容器中仅发生反应2NO(g)+O (g)
2
2NO (g) ΔH>0。实验测得: , , 、 为速率常数,
2
只受温度影响。
起始浓度 (mol/L) 平衡浓度(mol/L)
容器编号
c(NO ) c(NO) c(O) c(O)
2 2 2
Ⅰ 0.6 0 0 0.2
Ⅱ 0.6 0.1 0
下列说法不正确的是( )
A.升高温度,该反应的化学平衡常数增大
B.Ⅰ中NO 的平衡转化率约为66.7%
2
C.Ⅱ中达到平衡状态时,c(O)>0.2 mol·L−1
2
D.该反应的化学平衡常数可表示为
【答案】C
【解析】先用三段式法计算出实验Ⅰ中各组分的改变浓度和平衡浓度:
而实验Ⅱ相当于在Ⅰ的基础上再加入NO,平衡会逆向移动,再判断各量的变。A项,该反应ΔH>0,为吸热反应,升高温度,K值增大,A正确;B项,由上述分析可知,Ⅰ中NO 的平衡转化率为
2
,B正确;C项,Ⅰ中平衡时c(O)=0.2 mol·L−1,实验Ⅱ相当于在Ⅰ的基础上再加入
2
NO,平衡会逆向移动,c(O)<0.2 mol·L−1,C不正确;D项,平衡时,v (NO )=v (NO),即k c2(NO )
2 正 2 逆 正 2
=k c2(NO)·c(O ),得 = =K,D正确;故选C。
逆 2
10.(2022·重庆市高三学业考试)甲异腈(CHNC)在恒容密闭容器中发生异构化反应: CHNC(g)
3
→CHCN(g),反应过程中甲异腈浓度c随时间t的变化曲线如图所示(图中T为温度)。该反应的反应速率v
3
与c的关系为v=kc,k为速率常数(常温下为常数),a点和b点反应速率相等,即v(a)=v(b)。下列说法错误
的是( )
A.bf段的平均反应速率为1.0 × 10 -4mol(L·min)
B.a点反应物的活化分子数多于d点
C.T>T
1 2
D.3v(d)=2v(e)
【答案】C
【解析】设T 时,速率常数为k,T 时,速率常数为R ,v(a)=v(b), ,
1 1 2 2
。A项,由题干信息可知, ,A正确;B项,ad
两点相比较,a点的浓度比d的浓度大,且其他的条件相同,故a点反应物的活化分子数多于d点,B正确;
C项,由以上可知,k=2k,v=kc,浓度相同的时候,v>v,温度越高,速率越大,故T>T,C错误;D
2 1 2 1 2 1
项, , ,k=2k,可得3v(d)=2v(e),D正确;故选
2 1
C。11.(2022·重庆市育才中学模拟预测)在密闭容器中充入1 和1 ,在一定条件下发生反
2NO(g)+2CO(g) N(g)+2CO (g),测得 的平衡转化率与温度及压强的关系如图所示。实验测得,
2 2
, ( 、 为速率常数,只与温度有关),下列说法错误的是(
)
A.达到平衡后,仅升高温度, 增大的倍数小于 增大的倍数
B.若密闭容器( 对应压强下)体积为1L,则b点
C. 的物质的量浓度:b点 点
D.逆反应速率:a点 点
【答案】B
【解析】A项,平衡时,v =v ,即k c2(NO)∙c2(CO)= k c(N )∙c2(CO),升高温度后,正、逆反应的
正 逆 正 逆 2 2
速率增大,但NO的平衡转化率降低,平衡逆向移动,说明逆反应增大的幅度大于正反应,而体系中各组
分的瞬时浓度不变,故k 增大的倍数小于 k 增大的倍数,A正确;B项,a点NO的平衡转化率为80%,
正 逆
CO和NO起始的物质的量均为1mol,根据化学方程式可知CO、NO、N、CO 转化的物质的量分别为
2 2
0.8mol、0.8mol、0.2mol、0.8mol,则CO、NO、N、CO 平衡时的物质的量分别为0.2mol、0.2mol、
2 2
0.2mol、0.8mol,由于容器体积为1L,故CO、NO、N、CO 平衡时的浓度分别为0.2mol/L、0.2mol/L、
2 2
0.2mol/L、0.8mol/L,a点 = = =160;p1对应压强下,b点NO
的平衡转化率还未达到80%,则反应正向进行,即v >v ,故 >160,B错误;C项,a点和b点的
正 逆
NO的起始物质的量相同,a点NO的转化率大于b点,则a点NO转化的物质的量大于b点,故a点剩余NO的物质的量小于b点,由于体积相同,故b点NO的物质的量浓度大于a点,C正确;D项,设压强为
p,温度与a点相同时的点为d点,由C选项可知,d点NO的物质的量浓度大于a点,则a点N、CO 的
2 2 2
浓度大于d点,故a点逆反应速率大于d点;d点和c点的压强相同,d点的温度高于c点,则d点的逆反
应速率大于c点,故a点逆反应速率大于c点,D正确;故选B。
12.(2022·湖北省华中师大一附中高三模拟预测)一步合成甲基丙烯酸甲酯的反应如下(其他产物已省
略)。科学家为了研究甲醇的脱氢过程对反应速率的影响,进行了下表所示动力学同位素效应实验(其他条
件均相同)。
实验编
反应物 反应速率常数 数据分析
号
Ⅰ 丙酸甲酯 甲醇(CHOH)
3
Ⅱ 丙酸甲酯 氘代甲醇D1(CD OH)
3
Ⅲ 丙酸甲酯 氘代甲醇D2(CH OD)
3
下列说法正确的是( )
A.CHOH、CDOH和HOD互为同素异形体
3 3 3
B.相比于甲醇,氘代甲醇参与的反应活化能较小
C.相比于C—H键,C—D键断裂的速率较慢
D.相比于O—H键,C—H的断裂对反应速率的影响较小
【答案】C
【解析】A项,同素异形体是同一种元素组成的不同种单质,CHOH、CDOH和HOD为化合物,不
3 3 3
是互为同素异形体,A错误;B项,根据速率常数, , ,甲醇参与反应时反应速
率常数更大,反应速率更快,则反应的活化能更小,B错误;C项,由B可知,甲醇参与反应时反应速率
更快,则相比于C—H键,C—D键断裂的速率较慢,C正确;D项,由实验Ⅱ和Ⅲ分析可知,氘代甲醇
D1参与的反应速率更慢,则相比于O—H键,C—H的断裂对反应速率的影响更大,D错误;故选C。
13.(2022·山东省德州市二模)在恒温恒容密闭容器中发生反应2H(g)+2NO(g) 2HO(g)
2 2
+N (g),N 的瞬时生成速率v=k·cm(H )c2 (NO)。控制NO起始浓度为0.5 mol/L,N 的瞬时生成速率和H 起
2 2 2 2 2始浓度的关系如图所示,下列说法正确的是( )
A.由题可知,该反应的速率常数k为15
B.随着H 起始浓度增大,该反应平衡常数增大
2
C.达平衡后,H 和NO的浓度均增加一倍,则NO转化率减小
2
D.H 起始浓度0.2 mol/L,某时刻NO的浓度为0.4 mol/L,则N 的瞬时生成速率为0.24 mol/L
2 2
【答案】A
【解析】A项,NO起始浓度为0.5 mol/L,由图像可知,N 的瞬时生成速率与H 起始浓度呈直线关系,
2 2
则m=1,将数据(0.2,0.75)代入v=k·c(H )c2 (NO),该反应的速率常数 ,A
2
项正确;B项,反应一定,平衡常数只与温度有关,温度不变,平衡常数不变,B项错误;C项,达平衡
后,H 和NO的浓度均增加一倍,新平衡与原平衡相比,相当于加压,平衡正向移动,则NO转化率增大,
2
C项错误;D项,由2H(g)+2NO(g) 2HO(g) +N (g)可知,NO起始浓度为0.5 mol/L,某时刻NO的浓
2 2 2
度为0.4 mol/L,变化量为0.1 mol/L,则时刻H 的浓度为0.2mol/L-0.1mol/L =0.1mol/L,N 的瞬时生成速率
2 2
为 ,单位错误,D项错误;故选A。
14.(2022·辽宁省高三适应性模拟)含氮化合物在生活、生产、研究领域至关重要。我国学者在容积不
变的刚性容器中按投料比 =1发生反应2H(g)+2NO(g) N(g)+2HO(g) H=-664.1kJ/mol,不同催化
2 2 2 2
⇌ △
剂条件下,反应相同时间测得NO转化率与温度的关系如图所示。且研究表明该反应v=kcm(H )c2(NO),其
2
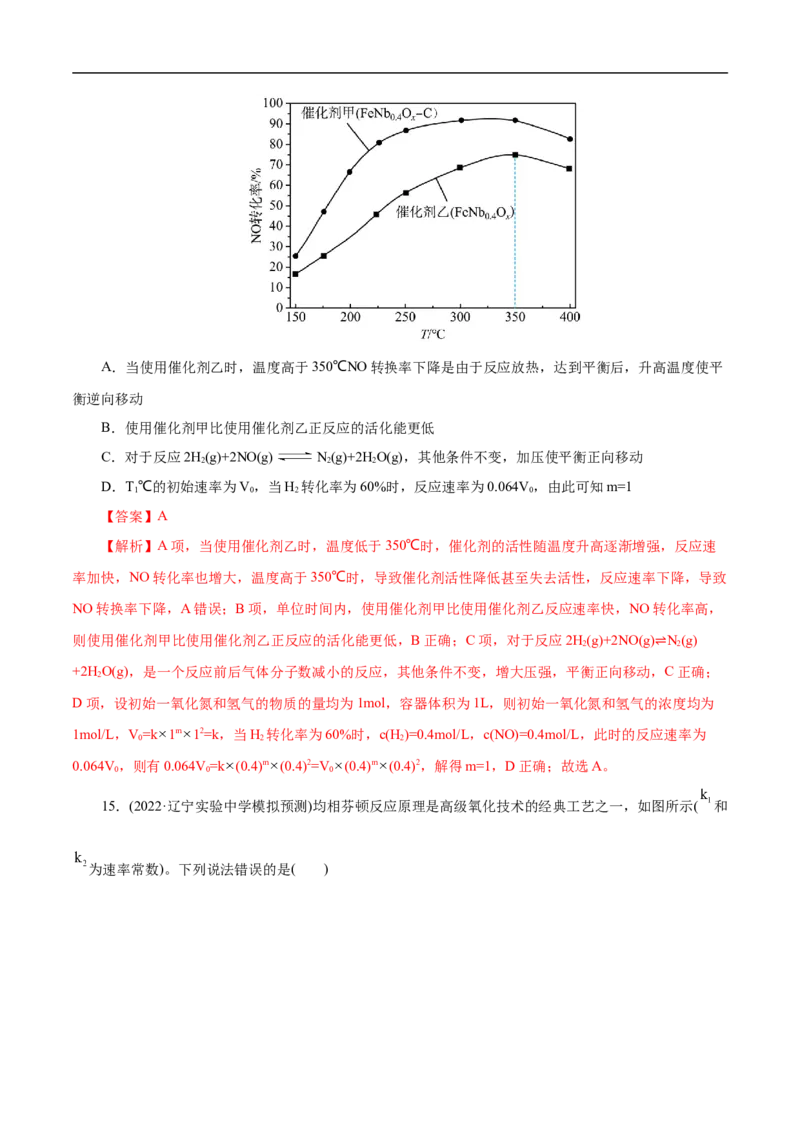
中k为速率常数。下列说法错误的是( )A.当使用催化剂乙时,温度高于350℃NO转换率下降是由于反应放热,达到平衡后,升高温度使平
衡逆向移动
B.使用催化剂甲比使用催化剂乙正反应的活化能更低
C.对于反应2H(g)+2NO(g) N(g)+2HO(g),其他条件不变,加压使平衡正向移动
2 2 2
D.T℃的初始速率为V,当H 转化率为60%时,反应速率为0.064V ,由此可知m=1
1 0 2 0
【答案】A
【解析】A项,当使用催化剂乙时,温度低于350℃时,催化剂的活性随温度升高逐渐增强,反应速
率加快,NO转化率也增大,温度高于350℃时,导致催化剂活性降低甚至失去活性,反应速率下降,导致
NO转换率下降,A错误;B项,单位时间内,使用催化剂甲比使用催化剂乙反应速率快,NO转化率高,
则使用催化剂甲比使用催化剂乙正反应的活化能更低,B正确;C项,对于反应2H(g)+2NO(g) N(g)
2 2
+2H O(g),是一个反应前后气体分子数减小的反应,其他条件不变,增大压强,平衡正向移动,⇌C正确;
2
D项,设初始一氧化氮和氢气的物质的量均为1mol,容器体积为1L,则初始一氧化氮和氢气的浓度均为
1mol/L,V=k 1m 12=k,当H 转化率为60%时,c(H)=0.4mol/L,c(NO)=0.4mol/L,此时的反应速率为
0 2 2
0.064V ,则有0.064V =k (0.4)m (0.4)2=V (0.4)m (0.4)2,解得m=1,D正确;故选A。
0 0 0
15.(2022·辽宁实验中学模拟预测)均相芬顿反应原理是高级氧化技术的经典工艺之一,如图所示( 和
为速率常数)。下列说法错误的是( )A.相同条件下,基元反应Ⅰ比Ⅱ的活化能低
B.基元反应Ⅰ中氧元素的化合价发生变化
C.基元反应Ⅱ的化学方程式为HO+Fe3+=HO·+Fe2++H+
2 2 2
D.芬顿反应进行的过程中,整个体系的 几乎不变(忽略体积变化)
【答案】D
【解析】A中根据图中速率公式,根据反应速率与活化能之间的关系进行判断;B中根据图中铁元素
的化合价的变化判断,发生氧化还原反应;C中根据图示进行书写化学方程式;D中根据总反应过程中溶
质的变化,根据浓度的变化判断进行判断酸碱性。A项,由题干信息可知,k>k,说明相同条件下,基
1 2
元反应Ⅰ比Ⅱ的反应速率更快,活化能越低反应速率越快,即基元反应Ⅰ比Ⅱ的活化能低,A正确;B项,
由题干信息可知,基元反应Ⅰ为:H++H O+Fe2+=Fe3++·OH+HO,故基元反应I中氧元素的化合价发生变化,
2 2 2
B正确;C项,由题干信息可知,基元反应Ⅱ的化学方程式为HO+Fe3+=HO·+Fe2++H+,C正确;D项,基
2 2 2
元反应Ⅰ为:H++H O+Fe2+=Fe3++·OH+HO,基元反应Ⅱ的化学方程式为 HO+Fe3+=HO·+Fe2++H+,而基
2 2 2 2 2 2
元反应Ⅰ比Ⅱ的反应速率更快,总反应不是简单基元反应Ⅰ加上基元反应Ⅱ,则芬顿反应进行的过程中,
整个体系的pH会发生变化 (忽略体积变化),D错误;故选D。
16.(2022·河北省九师联盟高三质量检测联考)向2L恒容密闭容器中充入2mol SO (g)和2mol Cl (g),
2 2
发生如下反应:SO (g)+ Cl (g) SO Cl(g),测得不同温度下SO (g)的转化率 与时间(t)的关系
2 2 2 2 2
如图所示。假设反应速率方程为 , (k是速率常数,只与温度有
关),下列说法错误的是( )A.该反应的ΔH<0
B. 时,
C.M点:
D.升高温度, 增大的倍数大于 增大的倍数
【答案】D
【解析】A项,由图知,T>T,温度越高,SO的转化率越小,说明正反应是放热反应,ΔH<0,A
2 1
项正确;B项,T 时,SO 的转化率为80%,平衡时, , ,
1 2
,可算出 ,B项正确;C项,M点为非平衡点,反应正向进行,浓度商小
于K,C项正确;D项,由于该反应ΔH<0,升高温度,平衡逆向移动, , 增大的倍数小于
增大的倍数,D项错误;故选D。
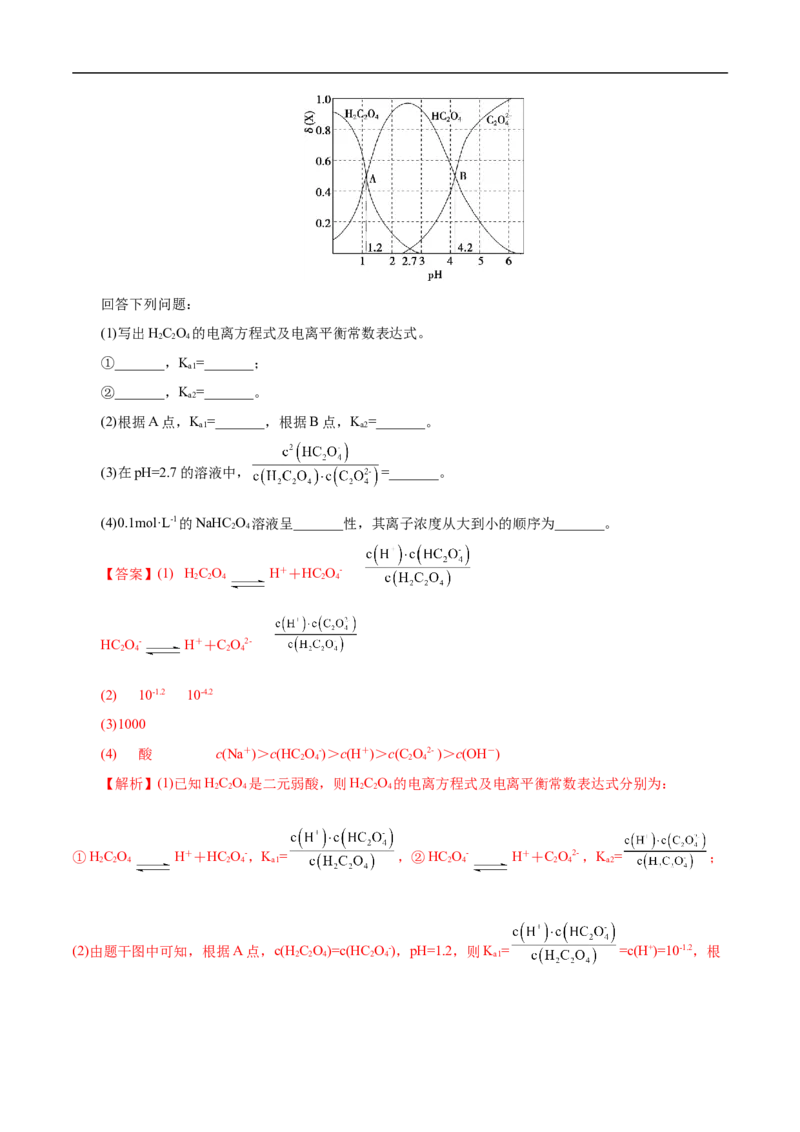
17.(2022·浙江省杭州市高三模拟)T℃时,向某浓度的草酸溶液中逐滴加入一定浓度的NaOH溶液,
所得溶液中三种微粒HC O、HC O-、C O2-的物质的量分数(δ)与pH的关系如图所示:
2 2 4 2 4 2 4回答下列问题:
(1)写出HC O 的电离方程式及电离平衡常数表达式。
2 2 4
①_______,K =_______;
a1
②_______,K =_______。
a2
(2)根据A点,K =_______,根据B点,K =_______。
a1 a2
(3)在pH=2.7的溶液中, =_______。
(4)0.1mol·L-1的NaHC O 溶液呈_______性,其离子浓度从大到小的顺序为_______。
2 4
【答案】(1) HC O H++HC O-
2 2 4 2 4
HC O- H++C O2-
2 4 2 4
(2) 10-1.2 10-4.2
(3)1000
(4) 酸 c(Na+)>c(HC O-)>c(H+)>c(C O2- )>c(OH-)
2 4 2 4
【解析】(1)已知HC O 是二元弱酸,则HC O 的电离方程式及电离平衡常数表达式分别为:
2 2 4 2 2 4
①HC O H++HC O-,K = ,②HC O- H++C O2- ,K = ;
2 2 4 2 4 a1 2 4 2 4 a2
(2)由题干图中可知,根据A点,c(HC O)=c(HC O-),pH=1.2,则K = =c(H+)=10-1.2,根
2 2 4 2 4 a1据B点,c(C O2- )=c(HC O-),pH=4.2,K = =c(H+)=10-4.2;(3)在pH=2.7的溶液中,已知
2 4 2 4 a2
= = =1000;(4)由上述分析可知,HC O 的Ka=10-1.2,Ka=10-4.2,则有Kh =
2 2 4 1 2 2
=10-12.8<Ka,即HC O-电离程度大于水解程度,则0.1mol·L-1的NaHC O 溶液呈酸性,其离子
2 2 4 2 4
浓度从大到小的顺序为c(Na+)>c(HC O-)>c(H+)>c(C O2- )>c(OH-)。
2 4 2 4
18.(2022·山东省聊城市三模)COCl 常用于有机合成,工业上采用高温活性炭催化CO与Cl 合成
2 2
COCl 。
2
(1)Burns和Dainton研究了反应Cl(g)+CO(g) COCl (g)的动力学,获得其速率方程v=kc
2 2
(Cl )c(CO),k为速率常数(只受温度形响),该反应的历程如下:
2
第一步:Cl 2Cl• H=+243kJ·mol-1
2 1
第二步:Cl•+CO COC△l• H
2
=-20kJ·mol-1
第三步:COCl•+Cl
2
COCl
2
+C△l• H
3
=-88kJ·mol-1
② 反应Cl
2
(g)+CO(g) C△OCl
2
(g)的△H=____kJ·mol-1。
②已知活化络合物分子中含有的原子数目等于反应速率方程中物质的原子数与指数的积,如
H+Cl=2HCl的反应速率方程为v=kc (Cl )•c(H ),可推测反应决速步中活化络合物的可能存在形式为
2 2 2 2
ClH 、HCl或H+Cl•,则Cl(g)+CO(g) COCl (g)反应中的活化络合物的可能存在形式为____(任写
2 2 2 2 2
一个即可),请判断第____步的活化能最高。
(2)在100kPa、恒压的密闭容器中,充入1molCO、1molCl 和适量的活性炭,发生反应Cl(g)+CO(g)
2 2
COCl (g),其压强平衡常数(用平衡分压代替平衡浓度,分压=总压×物质的量分数)的对数lgK 。与
2 p
温度倒数 呈线性关系,如图。①能正确表示上述反应线性关系的直线为____(填“L”或“L”),理由是___。
1 2
②图中Q点的坐标为(2.2,-2.0),已知 =1.4,则平衡时CO的转化率为____。若保持温度不变,将
该容器增压再次达到平衡,其状态可能为图中Q、M、N中的____点,此时混合气中COCl 的体积分数是
2
50%,则再次达到平衡状态的气体总压强是____kPa。
【答案】(1) -108 Cl CO、COCl 或COCl +Cl•、COCl•+Cl 三
3 3 2 2
(2) L 反应放热, 增大,温度降低,平衡正向移动,lgK 增大 30% Q 800
1 p
【解析】(1)①由题干信息可知,第二步:Cl•+CO COCl• H=-20kJ·mol-1第三步:COCl•+Cl
2 2
COCl +Cl• H=-88kJ·mol-1,第二步反应和第三步反应相加即△得
2 3
反应Cl
2
(g)+CO△(g) COCl
2
(g),根据该盖斯定律可知,△H= H
2
+ H
3
=(-20kJ·mol-1)+
△ △
(-88kJ·mol-1)=-108kJ·mol-1;②由题干信息可知,Cl(g)+CO(g) COCl (g) 速率方程v=kc (Cl )c(CO)可
2 2 2
知,反应中的活化络合物的可能存在形式为ClCO、COCl 或COCl +Cl•、COCl•+Cl ,由速率方程可,第
3 3 2 2
三步反应为决速步骤,故可判断第三步的活化能最高;(2)①由(1)分析可知,反应Cl(g)+CO(g)
2
COCl (g) H=-108kJ·mol-1,正反应是一个放热反应,即升高温度平衡逆向移动,Kp减小,故能正确表示
2
上述反应线△性关系的直线为L;②根据三段式分析可知:
1
图中Q点的坐标为(2.2,-2.0),即lgKp=-2,即 =10-2,已知 =1.4,解得
x=0.3mol,则平衡时CO的转化率为 =30%,若保持温度不变,温度不变平衡常数不变,将该容器增压再次达到平衡,其状态可能为图中Q、M、N中的Q点,此时混合气中COCl 的体积分数是
2
50%,则CO和Cl 的体积分数分别为25%,则Kp= =10-2,解得P总=800kPa,则再次达
2
到平衡状态的气体总压强是800kPa。
19.(2022·江西省重点中协作体第二次联考)我国力争在2060年前实现“碳中和”,体现了中国对解决
气候问题的担当。高效经济性的CO 捕集及利用是有效应对全球气候变化、促进低碳社会构建的重要方法。
2
(1)在催化剂作用下,可用CO 与H 反应制取甲酸。已知:
2 2
共价键 C=O C-O H-H H-O C-H
键能(kJ·mol-1) 799 343 436 463 413
则CO(g)+H(g)=HCOOH(g)的△H=_______kJ/mol。
2 2
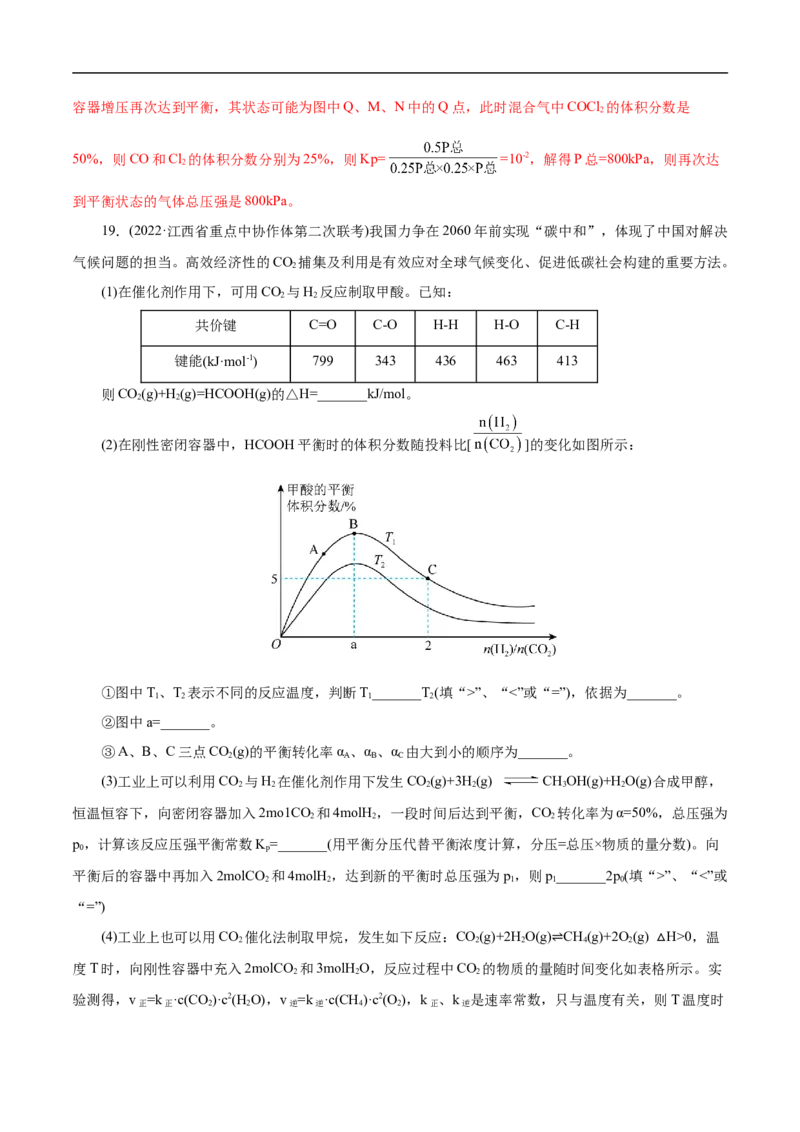
(2)在刚性密闭容器中,HCOOH平衡时的体积分数随投料比[ ]的变化如图所示:
①图中T、T 表示不同的反应温度,判断T_______T(填“>”、“<”或“=”),依据为_______。
1 2 1 2
②图中a=_______。
③A、B、C三点CO(g)的平衡转化率α 、α 、α 由大到小的顺序为_______。
2 A B C
(3)工业上可以利用CO 与H 在催化剂作用下发生CO(g)+3H(g) CHOH(g)+H O(g)合成甲醇,
2 2 2 2 3 2
恒温恒容下,向密闭容器加入2mo1CO 和4molH ,一段时间后达到平衡,CO 转化率为α=50%,总压强为
2 2 2
p,计算该反应压强平衡常数K=_______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。向
0 p
平衡后的容器中再加入2molCO 和4molH ,达到新的平衡时总压强为p,则p_______2p(填“>”、“<”或
2 2 1 1 0
“=”)
(4)工业上也可以用CO 催化法制取甲烷,发生如下反应:CO(g)+2HO(g) CH(g)+2O(g) H>0,温
2 2 2 4 2
度T时,向刚性容器中充入2molCO 和3molH O,反应过程中CO 的物质的量⇌随时间变化如表格△所示。实
2 2 2
验测得,v =k ·c(CO)·c2(H O),v =k ·c(CH)·c2(O ),k 、k 是速率常数,只与温度有关,则T温度时
正 正 2 2 逆 逆 4 2 正 逆=_______。若升高温度, _______(增大、减小或者不变)
时间/min 5 10 15 20
CO 的物质的量/mol 1.4 1.0 0.8 0.8
2
【答案】(1)+16
(2) > 该反应为吸热反应,升高温度,平衡正向移动,在相同投料比时,T 温度下产物的体积分数
1
大于T 温度下产物的体积分数,则T>T 1 α >α >α
2 1 2 C B A
(3) < (4) 减小
【解析】(1) H =反应物的总键能-生成物的总键能=2 799kJ·mol-1+436kJ·mol-1-
(799+343+463+41△3)kJ·mol-1=+16kJmol-1。(2)①该反应为吸热反应,升高温度,平衡正向移动,从图像中可
知在相同投料比时,T 温度下HCOOH的体积分数大于T 温度下产物的体积分数,则T>T;②根据反应
1 2 1 2
CO(g)+H(g) HCOOH(g)可知,当投料比[ ]=1,即a=1时,恰好达到最大转化,HCOOH平
2 2
衡时的体积分数最大;③氢气的量越大,即投料比[ ]越大,CO的转化率越大,故A、B、C三点
CO(g)的平衡转化率由大到小的顺序为α >α >α ;(3)由已知信息可列三段式求得平衡时CO,H,HOH,
C B A 2 2 3
HO的物质的量均1mol,具体如下:
2
总压强为p,则CO,3H,HOH,HO的分压均为 ,带入平衡常数表达式得:K= ,向平衡
0 2 2 3 2 p
后的容器中再加入2molCO 和4molH ,即与初始投料相比反应物的量增加一倍,即增大压强平衡正向移动,
2 2
总压强变小,可得p<2p;(4)由题意知,v =k ·c(CO)·c2(H O),v =k ·c(CH)·c2(O ), 当反应达到平衡
1 0 正 正 2 2 逆 逆 4 2时v = v ,k ·c(CO)·c2(H O) =k ·c(CH)·c2(O )即 ,由表格可知反应在15min时
正 正 正 2 2 逆 4 2
达到平衡,列三段式可得平衡常数K=24, ,由于反应为吸热反应,升
高温度平衡常数K变大, 减小。
20.(2022·甘肃省兰州市一模)我国力争2060年前实现碳中和。CH 与CO 催化重整是实现碳中和的热
4 2
点研究课题。该催化重整反应体系主要涉及以下反应:
反应I:主反应CH(g)+CO (g) 2CO(g)+2H(g) ΔH K
4 2 2 1 p1
反应II:副反应CO(g)+H(g) CO(g)+HO(g) ΔH K
2 2 2 2 p2
反应III:积碳反应2CO(g) CO(g)+C(s) ΔH K
2 3 p3
反应IV:积碳反应CH(g) C(s)+2H(g) ΔH K
4 2 4 p4
(1)已知H(g)、CO(g)的燃烧热ΔH分别为-285.8kJ·mol-1、-283.0lkJ·mol-1,HO(l)= H O(g)
2 2 2
ΔH=+44kJ·mol-1,则反应II的ΔH=____kJ·mol-1。
5 2
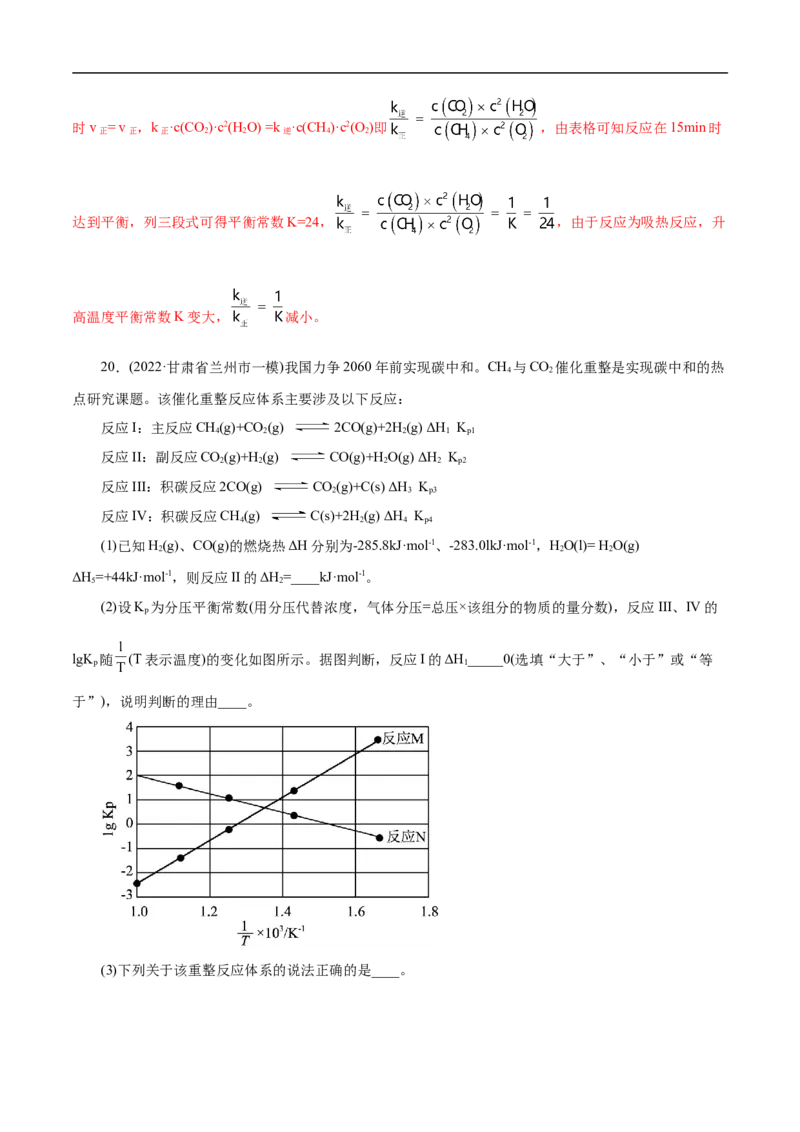
(2)设K 为分压平衡常数(用分压代替浓度,气体分压=总压×该组分的物质的量分数),反应III、IV的
p
lgK 随 (T表示温度)的变化如图所示。据图判断,反应I的ΔH_____0(选填“大于”、“小于”或“等
p 1
于”),说明判断的理由____。
(3)下列关于该重整反应体系的说法正确的是____。A.在投料时适当增大 的值,有利于减少积碳
B.在一定条件下建立平衡后,移去部分积碳,反应III和反应IV平衡均向右移
C.随着投料比 的增大,达到平衡时CH 的转化率增大
4
D.降低反应温度,反应I、II、IV的正反应速率减小,逆反应速率增大;反应III的正反应速率增大,
逆反应速率减小
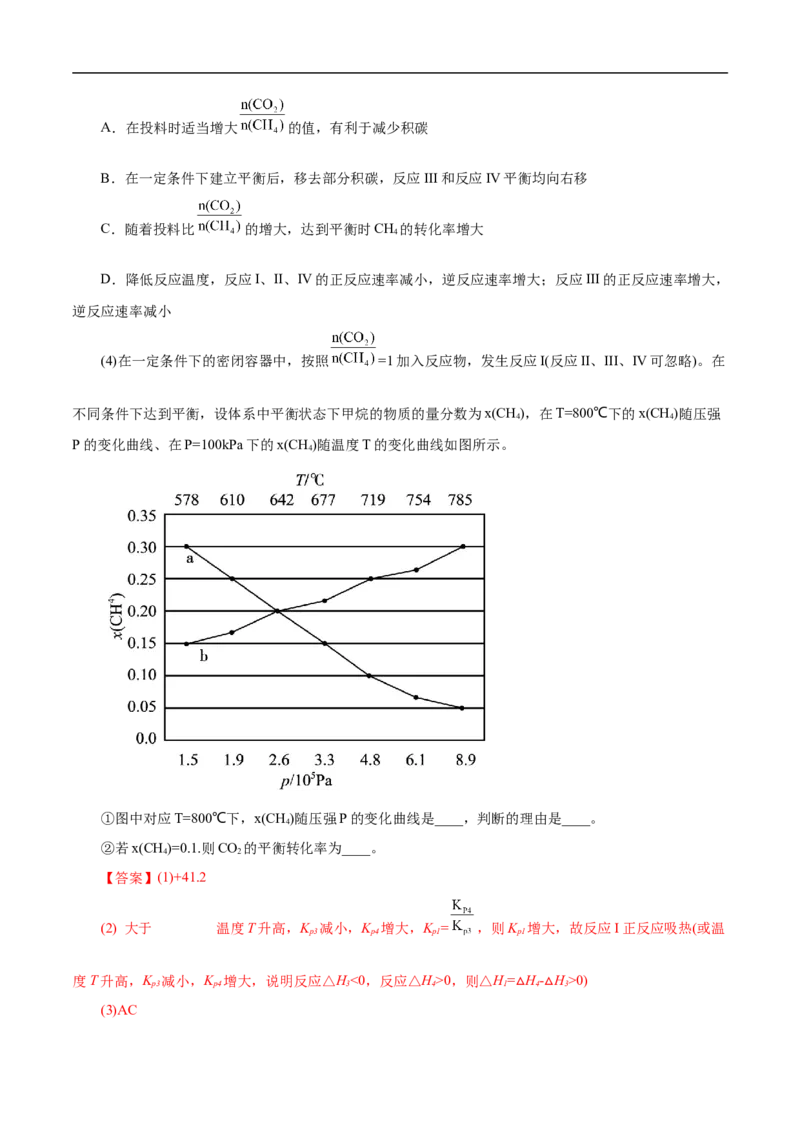
(4)在一定条件下的密闭容器中,按照 =1加入反应物,发生反应I(反应II、III、IV可忽略)。在
不同条件下达到平衡,设体系中平衡状态下甲烷的物质的量分数为x(CH),在T=800℃下的x(CH)随压强
4 4
P的变化曲线、在P=100kPa下的x(CH)随温度T的变化曲线如图所示。
4
①图中对应T=800℃下,x(CH)随压强P的变化曲线是____,判断的理由是____。
4
②若x(CH)=0.1.则CO 的平衡转化率为____。
4 2
【答案】(1)+41.2
(2) 大于 温度T升高,K 减小,K 增大,K = ,则K 增大,故反应I正反应吸热(或温
p3 p4 p1 p1
度T升高,K 减小,K 增大,说明反应△H<0,反应△H>0,则△H= H- H>0)
p3 p4 3 4 1 4 3
(3)AC △ △(4) b 反应I正反应方向气体分子数增大,其他条件不变时,增大压强,平衡逆移,x(CH)增
4
大
【解析】(1)由题意可得如下热化学方程式①H(g)+ O(g)= H O(l) ΔH=—285.8kJ/mol,②CO(g)+
2 2 2
O(g)= CO (g) ΔH=—283.0kJ/mol,③HO(l)= H O(g) ΔH=+44kJ/mol,由盖斯定律可知,①—②+③得到反
2 2 2 2 5
应II,则反应热ΔH=(—285.8kJ/mol)—(—283.0kJ/mol)+( +44kJ/mol)= +41.2kJ/mol;(2)由盖斯定律可知,反
2
应IV—反应III得到反应I,则ΔH=ΔH—ΔH ,由图可知,温度升高,反应III分压平衡常数减小,该反
1 4 ,3
应为放热反应,反应△H<0,反应IV分压平衡常数增大,该反应为吸热反应,反应△H>0,则△H= H-
3 4 1 4
△
H>0(或由盖斯定律可知,反应IV—反应III得到反应I,则反应I分压平衡常数为K = ,由图可知,
3 p1
△
温度升高,反应III分压平衡常数减小,反应IV分压平衡常数增大,K 增大,则该反应为吸热反应);
p1
(3)A.在投料时适当增大 相当于增大二氧化碳的浓度,反应I平衡向正反应方向移动,一氧化碳和
氢气的浓度增大,反应III、IV的平衡向逆反应方向移动,碳的物质的量减小,所以在投料时适当增大
的值,有利于减少积碳,故正确;B.在一定条件下建立平衡后,移去浓度为定值的碳固体,化学
反应速率不变,反应III和反应IV的平衡均不移动,故错误;C.投料比 增大相当于增大二氧化碳
的浓度,反应I平衡向正反应方向移动,甲烷的转化率增大,故正确;D.降低反应温度,反应I、II、
III、IV的正、逆反应速率均减小,故错误;故选AC;(4)①反应I为气体体积增大的反应,温度一定时,
增大压强,平衡向逆反应方向移动,甲烷的物质的量分数增大,则800℃下,甲烷的物质的量分数随压强
的变化曲线是b;②设起始甲烷和二氧化碳的物质的都为1mol,二氧化碳的转化率为a,由题意可建立如
下三段式:由甲烷的物质的量分数为0.1可得: =0.1,解得a= 。
21.(2022·河北省保定市高三阶段练习)以CO 为碳源选择性加氢合成甲醇一直是研究的热点,涉及的
2
主要反应如下:
ⅰ. CO(g)+3H(g) CHOH(g)+H O(g) ΔH <0
2 2 3 2 1
ⅱ. CO(g)+H(g) CO(g)+HO(g) ΔH
2 2 2 2
回答下列问题:
(1)已知:C(s)+O(g)==CO (g)) ΔH=-393.5kJ·mol−1
2 2
则ΔH=_______ kJ·mol-1。
2
(2)反应ⅱ的反应速率 ,其中 、 分别为正、逆反
应速率常数。则反应ⅱ的平衡常数 _______(用 、 表示),升高温度, _______(填“增大”
“减小”或“不变”)。
(3)240℃时,向 恒容密闭容器中通入 和 ,起始总压强为 。发生反
应ⅰ和反应ⅱ.实验测得 的平衡转化率和平衡时 的选择性随温度变化如图所示:已知: 的选择性 。
①图中表示平衡时CHOH的选择性的曲线为_______(填“X”或“Y”)。温度高于 时,曲线Y随
3
温度升高而升高的原因是_______。
②若在240℃恒温条件下,该 恒容密闭容器内反应经过 达到平衡状态。则 内,平均
反应速率v(CO )=_______。已知反应ⅱ在240℃时的浓度平衡常数 ,则初始充入 的物质的量
2
_______ 。反应ⅰ在 时的压强平衡常数 _______ (保留两位小数)。
(4)工业上按一定体积比加入CO 和CH,在恒压下发生催化重整反应制得合成气:CO(g)+CH (g)
2 4 2 4
2CO(g)+HO(g) ΔH>0,温度对CO和H,产率的影响如图所示。工业上此反应优选温度为
2 2
的原因是_______。
【答案】(1) +41.2
(2) 增大(3) X 温度高于280℃时,以反应ⅱ为主,反应ⅱ为吸热反应,温度升高,平衡正向移动,CO 的
2
平衡转化率增大 0.02mol·L-1·min-1 1.12 4.17
(4) 900℃时,合成气产率已经较高,再升高温度产率增幅不大,但能耗升高,经济效益降低
【解析】(1)已知:③C(s)+O(g)==CO (g)) ΔH=-393.5kJ·mol−1
2 2
④
⑤
根据盖斯定律,由⑤-③+④得反应ⅱ. CO(g)+H(g) CO(g)+HO(g) ΔH =-241.8kJ/mol-
2 2 2 2
(-393.5kJ/mol)+(-110.5kJ/mol)=+41.2kJ/mol;(2)当反应达平衡时,反应ⅱCO(g)+H(g) CO(g)
2 2
+H O(g)的反应速率 ,其中 、 分别为正、逆反应速
2
率常数, , ,故反应ⅱ的平衡常数 ,
该反应为吸热反应,升高温度,K值增大,则 增大;(3)反应为放热反应,升高温度,平衡向逆反应
方向进行,CHOH的物质的量降低,反应ii为吸热反应,升高温度,平衡正反应方向进行,CO 的转化率
3 2
增大,根据甲醇的选择性定义,甲醇的选择性降低,依据图像可知,表示平衡时CHOH的选择性的曲线
3
是X,曲线Y表示平衡CO 转化率;温度高于280℃时,反应ii为吸热反应,升高温度,平衡正反应方向
2
进行,CO 的转化率增大,以反应ii为主;高于280℃时,以反应ii为主,反应ii为吸热反应,温度升高,
2
平衡正向移动,CO 的平衡转化率增大;②240℃时,CO 的转化率为40%,CHOH的选择性为80%,根
2 2 3
据化学反应速率的数学表达式,v(CO)= = =0.02mol/ (L·min);达到平衡时,消耗n(CO) =
2 2
1mol×40% = 0.4mol,则产生甲醇的物质的量为0.4mol ×80% = 0.32mol,则:
反应ⅰ:
反应ⅰⅰ:反应ⅰⅰ的平衡常数K= = = ,解得n(H )=0.08mol,
2
即被始时通入氢气的物质的量为(0.08+0.08+0.96)mol=1.12mol,相同条件下,压强之比等于气体物质的量
之比,有: = ,解得p =14.8MPa,反应ⅰ的K= =
平 p
(MPa)-2 4.17(MPa)-2;(4)根据图中曲线可知,900℃时,合成气产率已经较高,
再升高温度产率增幅不大,但能耗升高,经济效益降低。
22.(2022·甘肃省高三第二次高考诊断性考试)绿色能源的开发利用是未来能源发展的重要方向,也是
实现“碳中和”目标的重要举措。氢能是重要的绿色能源,利用甲烷来制取氢气的总反应可表示为:
CH(g)+2HO(g)=CO(g)+4H(g),该反应可通过如下过程来实现:
4 2 2 2
反应I:CH(g)+HO(g)=3H (g)+CO(g) H=+206.3kJ·mol-1
4 2 2 1
反应II:CO(g)+H
2
O(g)=CO
2(
g)+H
2
(g) △H
2
=-41.2kJ·mol-1
(1)总反应的△H=_______kJ·mol-1 △
(2)反应I在恒压条件下,不同进气比[n(CH):n(H O)]和不同温度时测得相应的CH 平衡转化率见
4 2 4
下表。
平衡点 a b c d
n(CH):n(H O) 0.5 0.5 1 1
4 2
CH 平衡转化率/% 50 69 50 80
4
①c点平衡混合物中H 的体积分数为_______,a、b两点对应的反应速率v______________v(填
2 a b
“<”“=”或“〉”),判断的理由为_______。
②若d点的总压强为aMPa,则d点的分压平衡常数K 为_______(用平衡分压代替浓度计算,分压=总
P
压×物质的量分数,计算结果精确到0.01)。
(3)反应II在工业上称为一氧化碳的催化变换反应,研究表明该反应用Fe O 作催化剂,反应历程如下:
3 4
第一步:Fe O+4CO=3Fe+4CO 第二步:3Fe+4H O=Fe O+4H
3 4 2 2 3 4 2已知第一步为慢反应,则第一步反应的活化能比第二步反应_______ (填“大”或“小”)。由于
CO还原性较强,若将Fe O 还原成Fe,并以Fe的形式大量存在于反应体系中,会使催化剂失去活性,但
3 4
在实际生产中一般不会发生催化剂失去活性的情况,请结合一氧化碳的催化变换反应历程说明理由
_______。
(4)研究表明,CO催化变换反应的速率方程为 ,该表达式中
分别表示相应的物质的量分数,K 为分压平衡常数,k为反应的速率常数,温度升髙
P
时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如下图所示。温度升髙时,
CO催化变换反应的K _______ (填“增大”或“减小”)。根据速率方程分析,T>T 时r逐渐减小的原
P m
因是_______。
【答案】(1)+165.1
(2) 0.50或50% < 反应I为吸热反应,投料比相同时平衡转化率越高则体系的温度越高,
反应速率越快 21.33a2(MPa)2
(3)大 由于第二步反应快,催化剂不会以铁的形式大量存在于反应体系中,所以不会出现催
化剂的失活
(4) 减小 K 减小对v的降低大于k增大对v的提高
p
【解析】(1)已知:反应I:CH(g)+HO(g)=3H (g)+CO(g) ΔH =+206.3kJ·mol-1
4 2 2 1
反应II:CO(g)+HO(g)=CO g)+H (g) ΔH =-41.2kJ·mol-1
2 2( 2 2
根据盖斯定律可知两式相加即得到总反应CH(g)+2HO(g)=CO(g)+4H(g)的ΔH=+165.1kJ·mol-1;(2)①
4 2 2 2
根据三段式可知所以c点平衡混合物中H 的体积分数为 ;由于反应I为吸热反应,投料比相同时平衡
2
转化率越高则体系的温度越高,反应速率越快,因此a、b两点对应的反应速率v<v。②根据三段式可知
a b
d点的总压强为aMPa,则d点的分压平衡常数K = MPa2≈21.33a2(MPa)2。(3)由于第
P
一步为慢反应,则第一步反应的活化能比第二步反应大。由于第二步反应快,催化剂不会以铁的形式大量
存在于反应体系中,所以不会出现催化剂的失活。(4)CO催化变换反应是放热反应,温度升髙时,平衡逆
向进行,所以CO催化变换反应的K 减小。根据速率方程可知当T>T 时K 减小对v的降低大于k增大对v
P m p
的提高,所以r逐渐减小。
23.(2022·辽宁省高三模拟预测)我国科学家成功开发Pd—Fe/Fe O 催化剂在低温条件下高选择性合成
2 3
高纯度的乙烯,化学原理如下:
主反应:C H(g)+H(g) C H(g) H
2 2 2 2 4 1
副反应:C
2
H
2
(g)+2H
2
(g) C
2
H
6
(g)△ H
2
(1)已知:A.几种共价键的键能如下表所△示:
共价键 H-C H-H C=C C≡C
键能/(kJ·mol-1) 413.4 436 615 812
B.C H(g)、H(g)、C H(g)的燃烧热△H分别为-1299.6kJ·mol-1、-285.8kJ·mol-1、-1559.8kJ·mol-1。
2 2 2 2 6
则△H=_______kJ·mol-1;乙烯加氢生成乙烷的热化学方程式是_______。
1
(2)在刚性密闭容器中充入一定量的C H(g)和H(g),发生反应:C H(g)+H(g) C H(g)。其他条件相
2 2 2 2 2 2 2 4
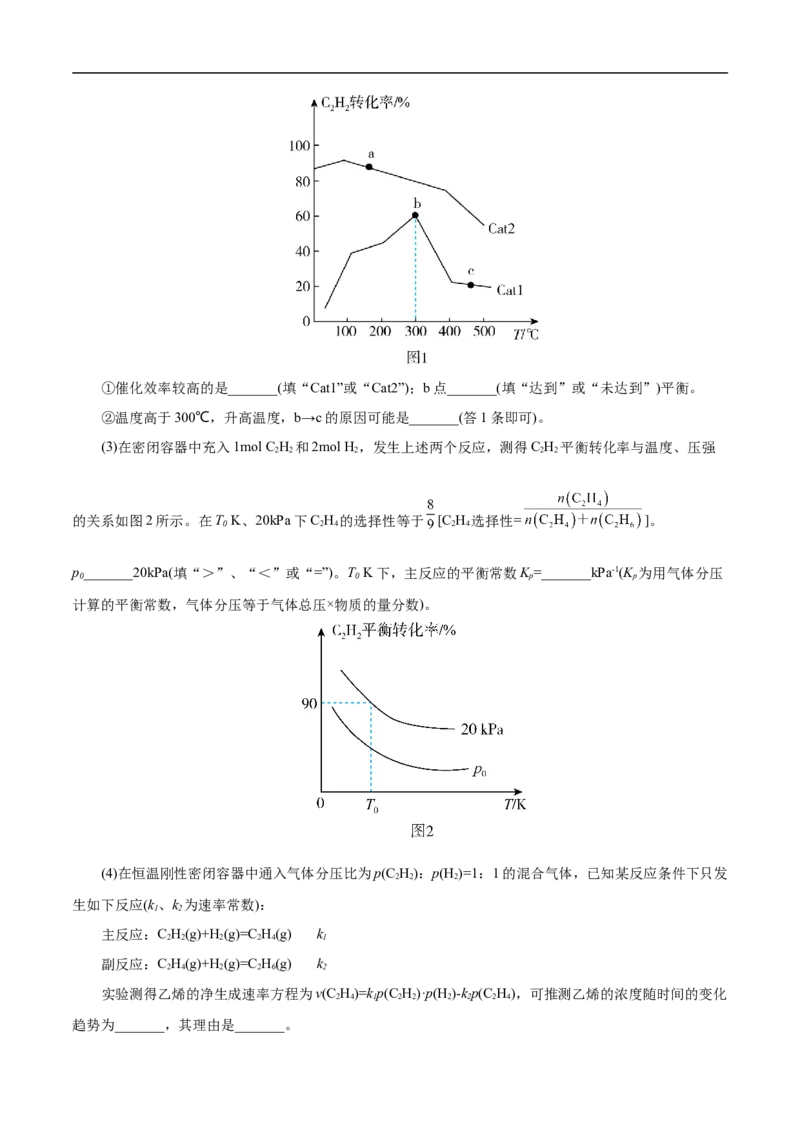
同,在Cat1、Cat2两种催化剂作用下,反应相同时间时C H 的转化率与温度的关系如图1所示。
2 2①催化效率较高的是_______(填“Cat1”或“Cat2”);b点_______(填“达到”或“未达到”)平衡。
②温度高于300℃,升高温度,b→c的原因可能是_______(答1条即可)。
(3)在密闭容器中充入1mol C H 和2mol H,发生上述两个反应,测得C H 平衡转化率与温度、压强
2 2 2 2 2
的关系如图2所示。在T K、20kPa下C H 的选择性等于 [C H 选择性= ]。
0 2 4 2 4
p_______20kPa(填“>”、“<”或“=”)。T K下,主反应的平衡常数K =_______kPa-1(K 为用气体分压
0 0 p p
计算的平衡常数,气体分压等于气体总压×物质的量分数)。
(4)在恒温刚性密闭容器中通入气体分压比为p(C H):p(H )=1:1的混合气体,已知某反应条件下只发
2 2 2
生如下反应(k、k 为速率常数):
1 2
主反应:C H(g)+H(g)=C H(g) k
2 2 2 2 4 1
副反应:C H(g)+H(g)=C H(g) k
2 4 2 2 6 2
实验测得乙烯的净生成速率方程为v(C H)=kp(C H)·p(H )-kp(C H),可推测乙烯的浓度随时间的变化
2 4 1 2 2 2 2 2 4
趋势为_______,其理由是_______。【答案】(1) -193.8 C H(g)+H(g) C H(g) H=-117.6kJ·mol-1
2 4 2 2 6
(2) Cat2 未达到 催化剂的活性降低 △
(3) < 0.8
(4)先变大后变小 反应开始时,C H 浓度最大,C H 浓度最小,此时生成乙烯速率快,浓度
2 2 2 4
变大;随着反应进行,C H 浓度变小,C H 浓度变大,副反应速率变大,乙烯的浓度又会减小
2 2 2 4
【解析】(1)反应的焓变△H=反应物的总键能-生成物的总键能;由化学方程式和键能数据可知,
△H=(812+2×413.4+436-4×413.4-615) kJ·mol-1=-193.8kJ·mol-1;C H(g)、H(g)、C H(g)的燃烧热△H分别
1 2 2 2 2 6
为-1299.6kJ·mol-1、-285.8kJ·mol-1、-1559.8kJ·mol-1;则有:③C H(g)+ O(g)=2CO (g)+HO(l)
2 2 2 2 2
H=-1299.6kJ·mol-1;④H(g)+ O(g)=HO(l) H=-285.8kJ·mol-1;⑤C H(g)+ O(g)=2CO (g)+3HO(l)
3 2 2 2 4 2 6 2 2 2
△ △
H=-1559.8kJ·mol-1;③+④×2-⑤得副反应:C H(g)+2H(g) C H(g)
5 2 2 2 2 6
△H=(-1299.6kJ·mol-1)+2(-285.8kJ·mol-1)-(-1559.8kJ·mol-1)=-311.4 kJ·mol-1,副反应-主反应得:C H(g)
2 2 4
△+H (g) C H(g) H=(-311.4 kJ·mol-1)-(-193.8kJ·mol-1)=-117.6 kJ·mol-1。(2)①由图可知,温度相同时间
2 2 6
相同时Cat2做催化剂,△C H 的转化率更高,故Cat2的催化效率较高;催化剂改变反应速率,不改变平衡
2 2
时物质的转化率,由图可知,b点时使用Cat2做催化剂C H 的转化率高于b点,说明b点未达到平衡。②
2 2
温度高于300℃,升高温度,b→c段C H 的转化率降低,原因可能是催化剂的活性降低导致。
2 2
(3)主反应:C H(g)+H(g) C H(g)和副反应:C H(g)+2H(g) C H(g);反应均为气体分子
2 2 2 2 4 2 2 2 2 6
数减小的反应,增大压强,平衡正向移动,C H 的转化率升高,结合图像可知,p<20kPa;T K时,设
2 2 0 0
平衡时C H(g)、C H(g)的物质的量分别为x、y;
2 4 2 6
由图可知,在T K、20kPa下C H 的平衡转化率为90%,则 ;在T K、20kPa下
0 2 2 0
C H 的选择性等于 ,则 ;解得x=0.8mol,y=0.1mol;平衡时C H(g)、C H(g)、C H(g)、H(g)的
2 4 2 2 2 6 2 4 2物质的量分别为0.1mol、0.1mol、0.8mol、1.0mol,总的物质的量为2.0mol,则T K下,主反应的平衡常
0
数K = kPa-1。(4)推测乙烯的浓度随时间的变化趋势为先变大后变小;反应开始时
p
C H 浓度最大、C H 浓度最小,由乙烯的净生成速率方程可知,此时生成乙烯速率快、浓度变大;随着反
2 2 2 4
应进行,C H 浓度变小,C H 浓度变大,副反应速率变大,乙烯的浓度又会减小。
2 2 2 4
24.(2022·广东省梅州市二模)工业合成氨是人类科学技术的一项重大突破。
(1)已知:3H(g)+N(g) 2NH (g) ΔH= -92.2 kJ/mol ,若起始时向容器内放入2mol N 和6 mol H ,
2 2 3 2 2
达平衡时放出的热量为Q,则Q_______184.4kJ(填“>”“<”或“=”)。
(2)合成氨生产流程如图所示。
流程中,有利于提高原料利用率的措施是_______(任写两种)。
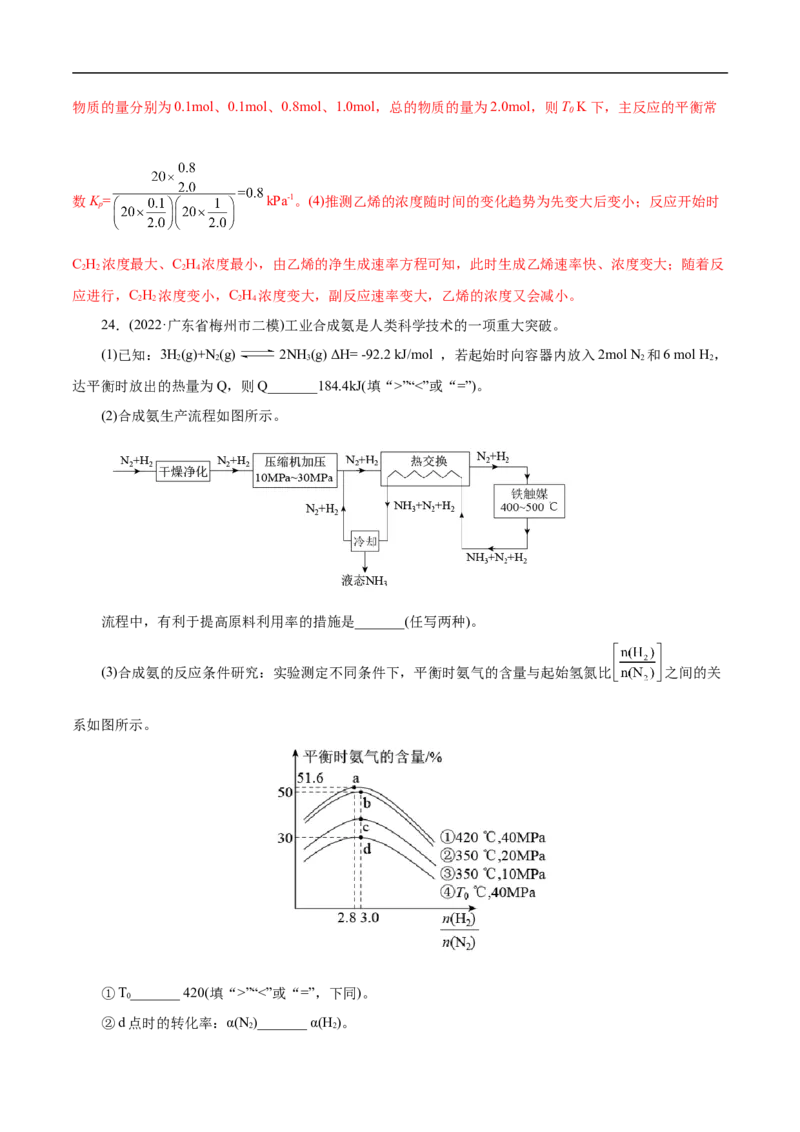
(3)合成氨的反应条件研究:实验测定不同条件下,平衡时氨气的含量与起始氢氮比 之间的关
系如图所示。
①T_______ 420(填“>”“<”或“=”,下同)。
0
②d点时的转化率:α(N )_______ α(H )。
2 2③a、b、c三点对应平衡常数的大小关系为_______ (用 K、K、K 表示)。
a b c
④p(N )、p(H )、p( NH)分别代表N、H、NH 的分压,K 代表压力平衡常数(用平衡时的分压代替平
2 2 3 2 2 3 p
衡时的浓度表示),一定条件下,上述合成氨反应接近平衡时,遵循如下方程: v(NH )=k ×p(N )
3 正 2
。其中v(NH )为氨合成反应的净速率(即正逆反应速率差),a为常数,与催化
3
剂性质及反应条件有关, k 、k 为速率常数,该条件下,实验测得a =0.5,则反应达到平衡时,k 、k 、
正 逆 正 逆
K 三者的关系式为_______。
p
(4)可用作合成氨的催化剂有很多,如Os、Fe、Pt、Mn、Co等金属及相应的合金或化合物。该反应在
LaCoSi催化作用的化学吸附及初步表面反应历程如下:
注:方框内包含微粒种类及个数、微粒的相对总能量(括号里数字的单位:eV)其中,TS表示过渡态,
*表示吸附态。
①请写出N 参与化学吸附的反应方程式_______。
2
②以上历程须克服的最大势垒为_______kJ/mol(列出计算式)。(已知:1 eV=1.6 ×10-22 kJ)
【答案】(1)<
(2)加压10 Mpa~30 Mpa、冷却液化氨、原料气循环利用
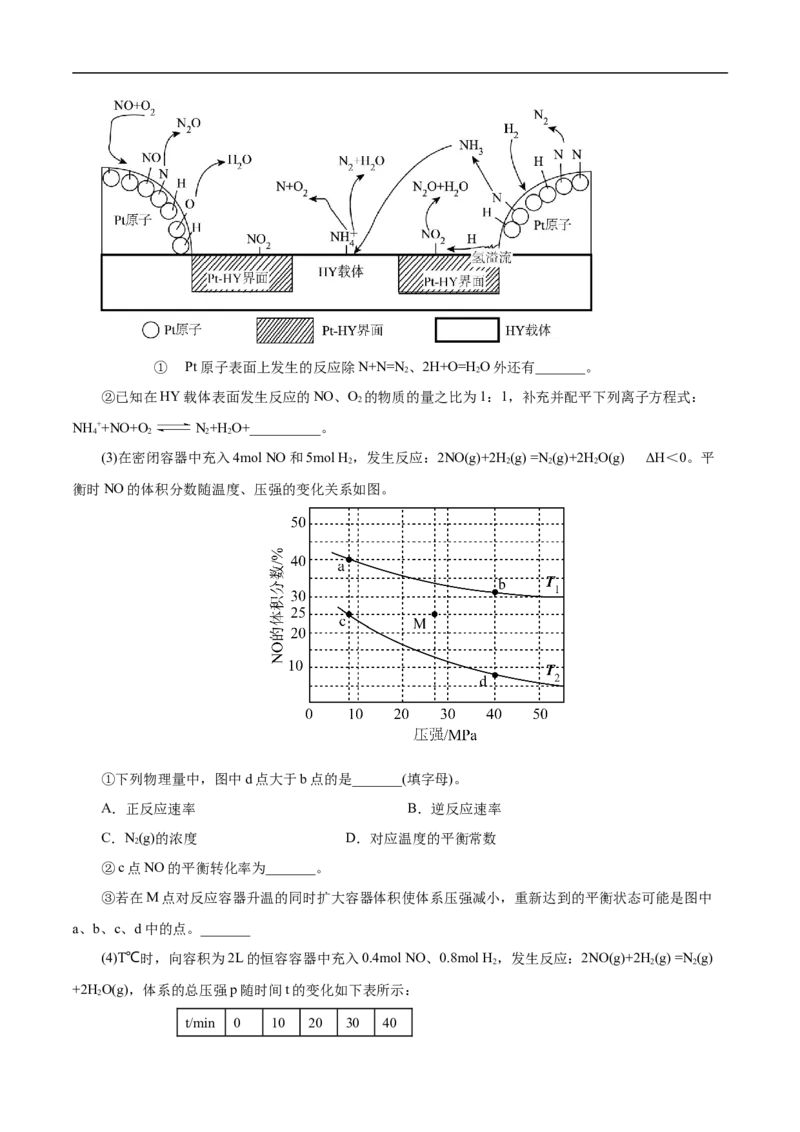
(3) > = K=K>K(或K0
2 2
B.图中X点所示条件下,延长反应时间能提高NO转化率
C.图中Y点所示条件下,增加O 的浓度不能提高NO转化率
2
D.380℃下,c (O )=5.0×10−4 mol·L−1,NO平衡转化率为50%,则平衡常数K>2000
起始 2
【答案】BD
【解析】A.随温度升高NO的转化率先升高后降低,说明温度较低时反应较慢,一段时间内并未达
到平衡,分析温度较高时,已达到平衡时的 NO转化率可知,温度越高NO转化率越低,说明温度升高平
衡向逆方向移动,根据勒夏特列原理分析该反应为放热反应,∆H<0,故A错误;B.根据上述分析,X点
时,反应还未到达平衡状态,平衡正向移动,所以延长反应时间能提高 NO的转化率,故B正确;C.Y
点,反应已经达到平衡状态,此时增加O 的浓度,使得正反应速率大于逆反应速率,平衡向正方向移动,
2可以提高NO的转化率,故C错误;D.设NO起始浓度为a,NO的转化率为50%,则平衡时NO、O 和
2
NO 的 浓 度 分 别 为 0.5amol/L 、 (5×10-4-0.25a)mol/L 、 0.5amol/L , 根 据 平 衡 常 数 表 达 式 K=
2
> =2000,故D正确;选BD。
5.【2017•天津卷】常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g) Ni(CO) (g)。230℃时,该
4
反应的平衡常数K=2×10−5。已知:Ni(CO) 的沸点为42.2℃,固体杂质不参与反应。
4
第一阶段:将粗镍与CO反应转化成气态Ni(CO) ;
4
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是( )
A.增加c(CO),平衡向正向移动,反应的平衡常数增大
B.第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
C.第二阶段,Ni(CO) 分解率较低
4
D.该反应达到平衡时,v [Ni(CO) ]=4v (CO)
生成 4 生成
【答案】B
【解析】A项,平衡常数只与温度有关,与浓度无关,A错误;B项,50时,Ni(CO) 以气态存在,有
4
利于分离,从而促使平衡正向移动,B正确;C项,230时,Ni(CO) 分解的平衡常数为5×106,可知分解率
4
较高,C错误;D项,平衡时,4v [Ni(CO) ]= v (CO),D错误。故选B。
生成 4 生成
6.【2022•全国甲卷】金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前生产钛的方法
之一是将金红石(TiO)转化为TiCl ,再进一步还原得到钛。回答下列问题:
2 4
(1) TiO 转化为TiCl 有直接氯化法和碳氯化法。在 时反应的热化学方程式及其平衡常数如下:
2 4
(ⅰ)直接氯化:TiO(s)+2Cl(g)= TiCl (g)+O(g) ΔH =172kJ·mol−1 Kp =1.0×10-2
2 2 4 2 1 1
(ⅱ)碳氯化:TiO(s)+2Cl(g)+2C(s)=TiCl (g)+2CO(g) ΔH =-51kJ·mol−1 Kp =1.2×1012Pa
2 2 4 2 2
①反应2C(s)+O(g)=2CO(g)的ΔH为_______ kJ·mol−1,Kp=_______Pa。
2
②碳氯化的反应趋势远大于直接氯化,其原因是_______。
③对于碳氯化反应:增大压强,平衡_______移动(填“向左”“向右”或“不”);温度升高,平衡转
化率_______(填“变大”“变小”或“不变”)。
(2)在1.0×105Pa,将TiO、C、Cl 以物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质
2 2
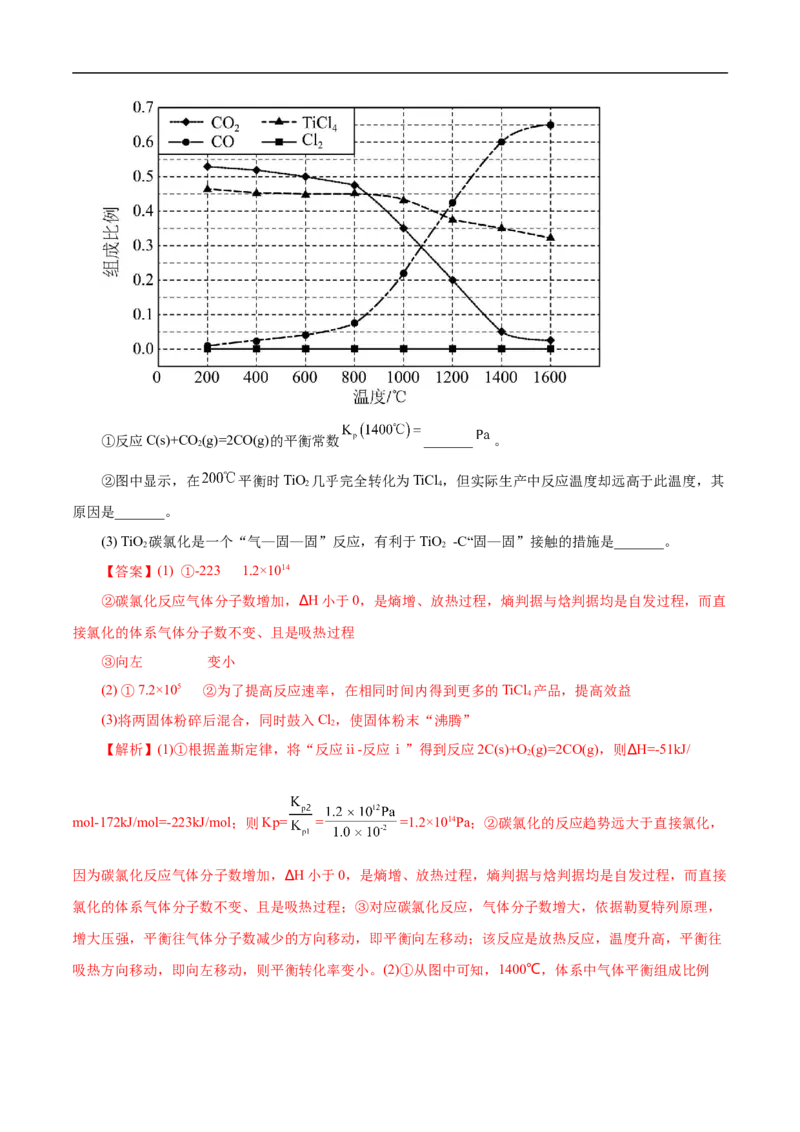
的量分数)随温度变化的理论计算结果如图所示。①反应C(s)+CO(g)=2CO(g)的平衡常数 _______ 。
2
②图中显示,在 平衡时TiO 几乎完全转化为TiCl ,但实际生产中反应温度却远高于此温度,其
2 4
原因是_______。
(3) TiO 碳氯化是一个“气—固—固”反应,有利于TiO -C“固—固”接触的措施是_______。
2 2
【答案】(1) ①-223 1.2×1014
②碳氯化反应气体分子数增加,∆H小于0,是熵增、放热过程,熵判据与焓判据均是自发过程,而直
接氯化的体系气体分子数不变、且是吸热过程
③向左 变小
(2) ①7.2×105 ②为了提高反应速率,在相同时间内得到更多的TiCl 产品,提高效益
4
(3)将两固体粉碎后混合,同时鼓入Cl,使固体粉末“沸腾”
2
【解析】(1)①根据盖斯定律,将“反应ⅱ-反应ⅰ”得到反应2C(s)+O(g)=2CO(g),则∆H=-51kJ/
2
mol-172kJ/mol=-223kJ/mol;则Kp= = =1.2×1014Pa;②碳氯化的反应趋势远大于直接氯化,
因为碳氯化反应气体分子数增加,∆H小于0,是熵增、放热过程,熵判据与焓判据均是自发过程,而直接
氯化的体系气体分子数不变、且是吸热过程;③对应碳氯化反应,气体分子数增大,依据勒夏特列原理,
增大压强,平衡往气体分子数减少的方向移动,即平衡向左移动;该反应是放热反应,温度升高,平衡往
吸热方向移动,即向左移动,则平衡转化率变小。(2)①从图中可知,1400℃,体系中气体平衡组成比例CO 是0.05,TiCl 是0.35,CO是0.6,反应C(s)+CO(g)=2CO(g)的平衡常数Kp(1400℃)= =
2 4 2
Pa=7.2×105Pa;②实际生产中需要综合考虑反应的速率、产率等,以达到最佳效益,实际
反应温度远高于200℃,就是为了提高反应速率,在相同时间内得到更多的TiCl 产品。(3)固体颗粒越小,
4
比表面积越大,反应接触面积越大。有利于TiO – C“固-固”接触,可将两者粉碎后混合,同时鼓入Cl,
2 2
使固体粉末“沸腾”,增大接触面积。
7.【2022·浙江省1月选考】工业上,以煤炭为原料,通入一定比例的空气和水蒸气,经过系列反应
可以得到满足不同需求的原料气。请回答:
(1)在C和O 的反应体系中:
2
反应1:C(s)+O(g)=CO (g) ΔH =-394kJ·mol-1
2 2 1
反应2:2CO(g)+O(g)=2CO (g) ΔH =-566kJ·mol-1
2 2 2
反应3:2C(s)+O(g)=2CO(g) ΔH 。
2 3
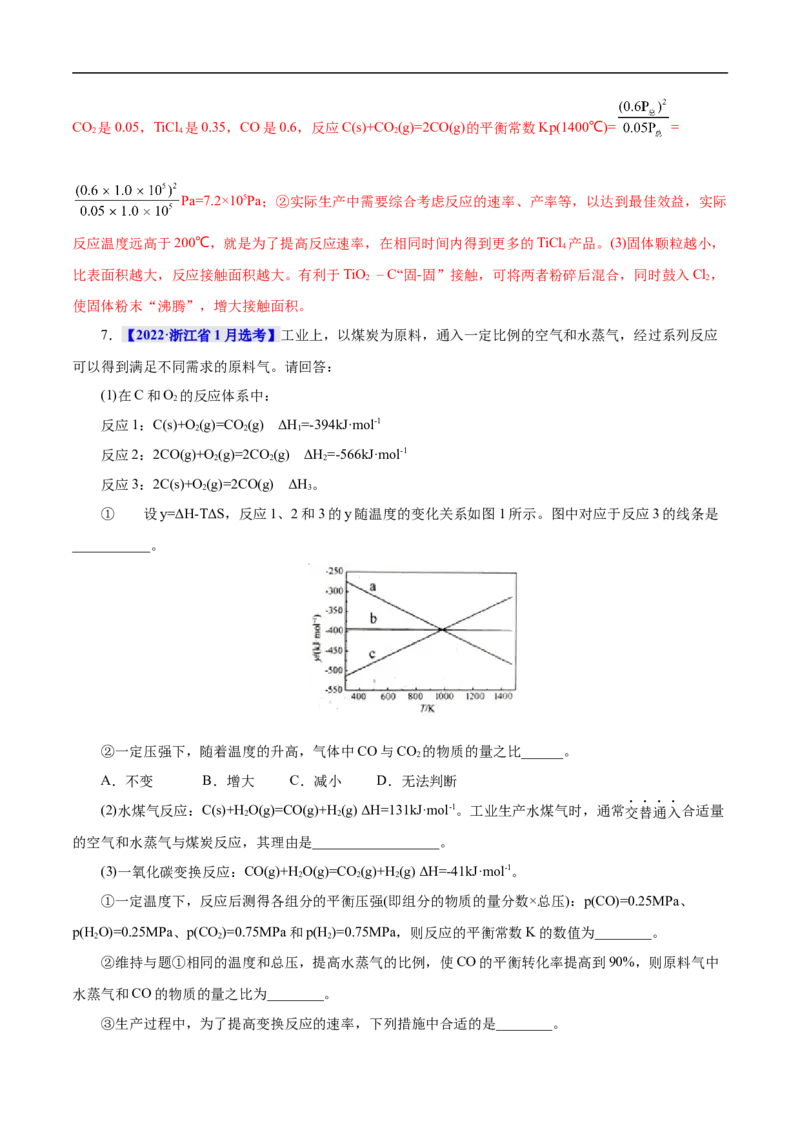
① 设y=ΔH-TΔS,反应1、2和3的y随温度的变化关系如图1所示。图中对应于反应3的线条是
___________。
②一定压强下,随着温度的升高,气体中CO与CO 的物质的量之比______。
2
A.不变 B.增大 C.减小 D.无法判断
(2)水煤气反应:C(s)+HO(g)=CO(g)+H (g) ΔH=131kJ·mol-1。工业生产水煤气时,通常交替通入合适量
2 2
的空气和水蒸气与煤炭反应,其理由是__________________。
(3)一氧化碳变换反应:CO(g)+HO(g)=CO(g)+H(g) ΔH=-41kJ·mol-1。
2 2 2
①一定温度下,反应后测得各组分的平衡压强(即组分的物质的量分数×总压):p(CO)=0.25MPa、
p(H O)=0.25MPa、p(CO)=0.75MPa和p(H )=0.75MPa,则反应的平衡常数K的数值为________。
2 2 2
②维持与题①相同的温度和总压,提高水蒸气的比例,使CO的平衡转化率提高到90%,则原料气中
水蒸气和CO的物质的量之比为________。
③生产过程中,为了提高变换反应的速率,下列措施中合适的是________。A.反应温度愈高愈好 B.适当提高反应物压强
C.选择合适的催化剂 D.通入一定量的氮气
④以固体催化剂M催化变换反应,若水蒸气分子首先被催化剂的活性表面吸附而解离,能量-反应过
程如图2所示。
用两个化学方程式表示该催化反应历程(反应机理):步骤Ⅰ:__________________;步骤Ⅱ:
_______________________。
【答案】(1)a B
(2)水蒸气与煤炭反应吸热,氧气与煤炭反应放热,交替通入空气和水蒸气有利于维持体系热量平衡,
保持较高温度,有利于加快化学反应速率
(3)①9.0 ②1.8:1 ③BC ④M+HO=MO+H MO+CO=M+CO
2 2 2
【解析】1)①由已知方程式:(2×反应1-反应2)可得反应3,结合盖斯定律得:ΔH=2ΔH -
3 1
ΔH=[2×(-394)-(-566)]kJ·mol-1=-222 kJ·mol-1,反应1前后气体分子数不变,升温y不变,对应线条b,升温
2
促进反应2平衡逆向移动,气体分子数增多,熵增,y值增大,对应线条c,升温促进反应3平衡逆向移动,
气体分子数减少,熵减, y值减小,对应线条a,故此处填a;②温度升高,三个反应平衡均逆向移动,
由于反应2焓变绝对值更大,故温度对其平衡移动影响程度大,故CO 物质的量减小,CO物质的量增大,
2
所以CO与CO 物质的量比值增大,故选B;(2)由于水蒸气与煤炭反应吸热,会引起体系温度的下降,从
2
而导致反应速率变慢,不利于反应的进行,通入空气,利用煤炭与O 反应放热从而维持体系温度平衡,维
2
持反应速率,故此处填:水蒸气与煤炭反应吸热,氧气与煤炭反应放热,交替通入空气和水蒸气有利于维
持体系热量平衡,保持较高温度,有利于加快反应速率;(3)①该反应平衡常数K=
;②假设原料气中水蒸气为x mol,CO为1 mol,由题意列三段式如
下:则平衡常数K= ,解得x=1.8,故水蒸气与CO物质的量之比为1.8:1;③A项,反应温
度过高,会引起催化剂失活,导致反应速率变慢,A不符合题意;B项,适当增大压强,可加快反应速率,
B符合题意;C项,选择合适的催化剂有利于加快反应速率,C符合题意;D项,若为恒容条件,通入氮
气对反应速率无影响,若为恒压条件,通入氮气后,容器体积变大,反应物浓度减小,反应速率变慢,D
不符合题意;故故选BC;④水分子首先被催化剂吸附,根据元素守恒推测第一步产生H,第二步吸附CO
2
产生CO,对应反应历程依次为:M+HO=MO+H 、MO+CO=M+CO 。
2 2 2 2
8.【2021•广东选择性考试】我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH 与CO 重
4 2
整是CO 利用的研究热点之一。该重整反应体系主要涉及以下反应:
2
a)CH(g)+CO (g) 2CO(g)+2H(g) ∆H
4 2 2 1
b)CO(g)+H(g) CO(g)+HO(g) ∆H
2 2 2 2
c)CH(g) C(s)+2H(g) ∆H
4 2 3
d)2CO(g) CO(g)+C(s) ∆H
2 4
e)CO(g)+H(g) HO(g)+C(s) ∆H
2 2 5
(1)根据盖斯定律,反应a的∆H=_______(写出一个代数式即可)。
1
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______。
A.增大CO 与CH 的浓度,反应a、b、c的正反应速率都增加
2 4
B.移去部分C(s),反应c、d、e的平衡均向右移动
C.加入反应a的催化剂,可提高CH 的平衡转化率
4
D.降低反应温度,反应a~e的正、逆反应速率都减小
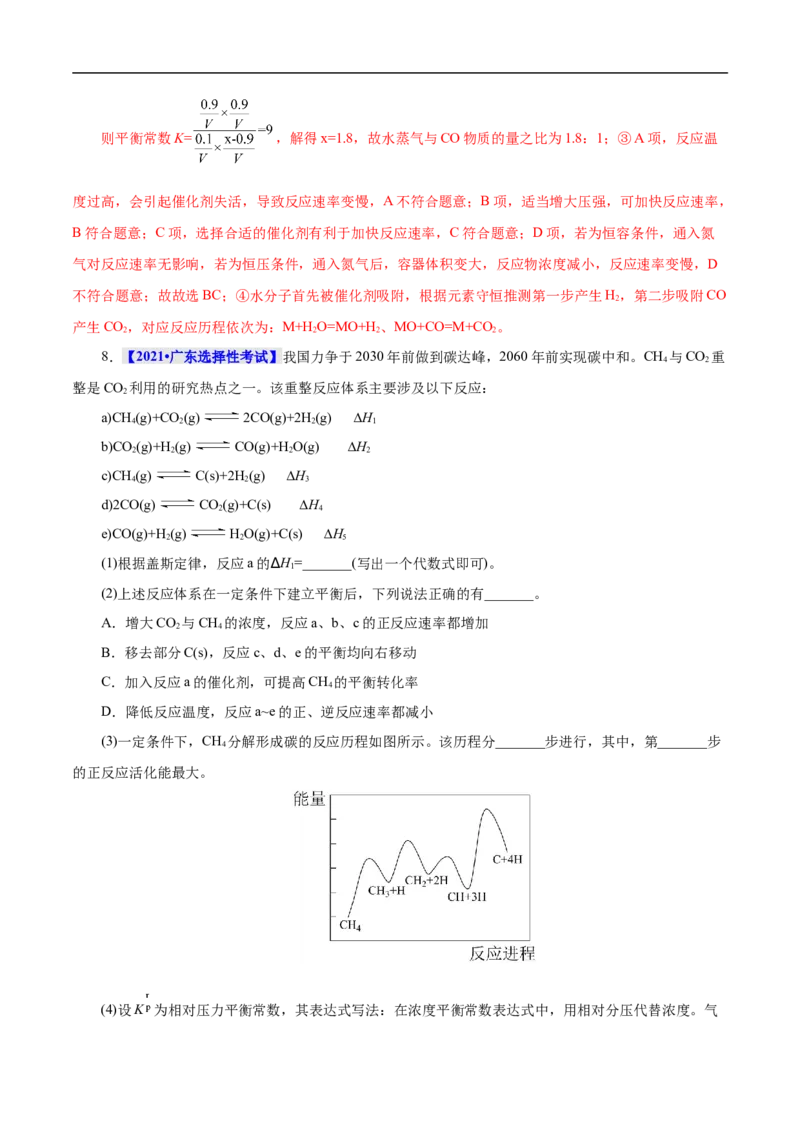
(3)一定条件下,CH 分解形成碳的反应历程如图所示。该历程分_______步进行,其中,第_______步
4
的正反应活化能最大。
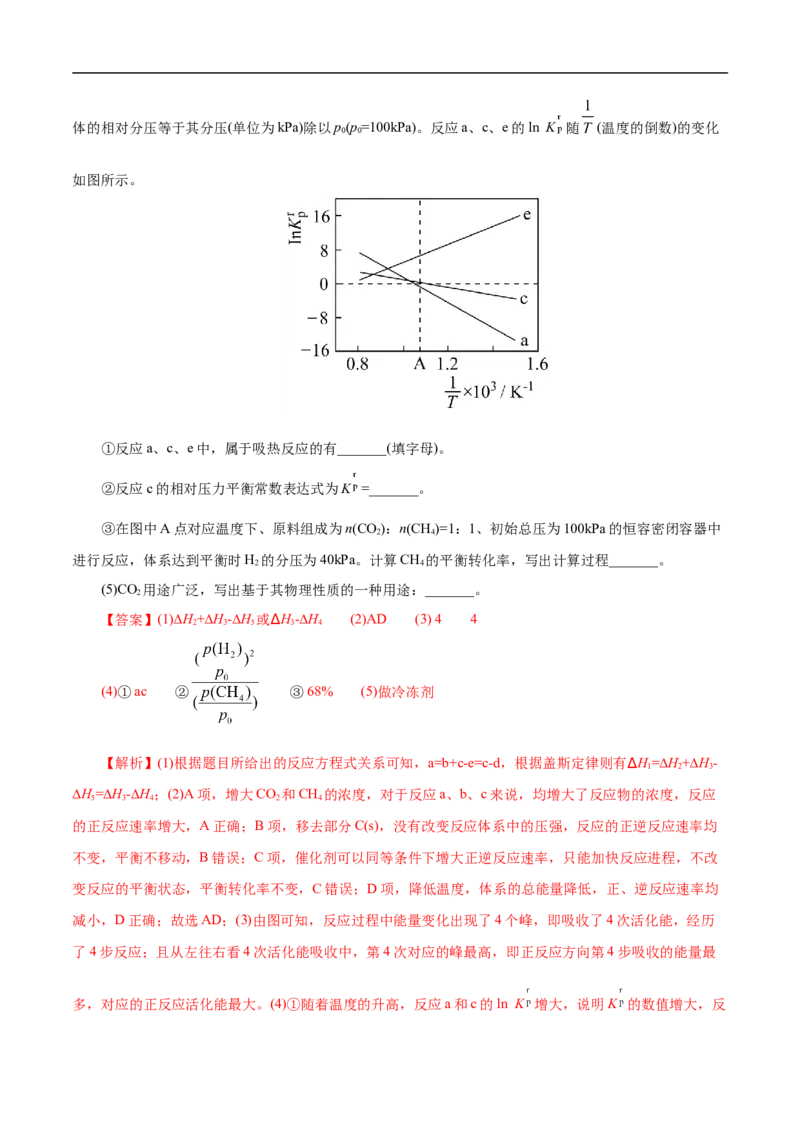
(4)设K 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p(p=100kPa)。反应a、c、e的ln K 随 (温度的倒数)的变化
0 0
如图所示。
①反应a、c、e中,属于吸热反应的有_______(填字母)。
②反应c的相对压力平衡常数表达式为K =_______。
③在图中A点对应温度下、原料组成为n(CO):n(CH)=1:1、初始总压为100kPa的恒容密闭容器中
2 4
进行反应,体系达到平衡时H 的分压为40kPa。计算CH 的平衡转化率,写出计算过程_______。
2 4
(5)CO 用途广泛,写出基于其物理性质的一种用途:_______。
2
【答案】(1)∆H+∆H-∆H 或∆H-∆H (2)AD (3) 4 4
2 3 5 3 4
(4)①ac ② ③68% (5)做冷冻剂
【解析】(1)根据题目所给出的反应方程式关系可知,a=b+c-e=c-d,根据盖斯定律则有∆H=∆H+∆H-
1 2 3
∆H=∆H-∆H;(2)A项,增大CO 和CH 的浓度,对于反应a、b、c来说,均增大了反应物的浓度,反应
5 3 4 2 4
的正反应速率增大,A正确;B项,移去部分C(s),没有改变反应体系中的压强,反应的正逆反应速率均
不变,平衡不移动,B错误;C项,催化剂可以同等条件下增大正逆反应速率,只能加快反应进程,不改
变反应的平衡状态,平衡转化率不变,C错误;D项,降低温度,体系的总能量降低,正、逆反应速率均
减小,D正确;故选AD;(3)由图可知,反应过程中能量变化出现了4个峰,即吸收了4次活化能,经历
了4步反应;且从左往右看4次活化能吸收中,第4次对应的峰最高,即正反应方向第4步吸收的能量最
多,对应的正反应活化能最大。(4)①随着温度的升高,反应a和c的ln K 增大,说明K 的数值增大,反应向正反应方向进行,反应a和c为吸热反应,同理反应e的ln K 减小,说明K 的减小,反应向逆反应
方向进行,反应e为放热反应,故答案为ac;②用相对分压代替浓度,则反应c的平衡常数表达式K =
;③由图可知,A处对应反应c的ln K =0,即K = =1,解方程的p2(H )=p(CH),
2 4
已知反应平衡时p(H )=40kPa,则有p(CH)=16kPa,且初始状态时p(CH)= ×100kPa=50kPa,故CH 的
2 4 4 4
平衡转化率为 ×100%=68%;(5)固态CO 即为干冰,干冰用于制冷或人工降雨均是利用其物
2
理性质。
9.【2021•全国乙卷】一氯化碘(ICl)是一种卤素互化物,具有强氧化性,可与金属直接反应,也可用
作有机合成中的碘化剂。回答下列问题:
(1)历史上海藻提碘中得到一种红棕色液体,由于性质相似,Liebig误认为是ICl,从而错过了一种新
元素的发现,该元素是_______。
(2)氯铂酸钡(BaPtCl )固体加热时部分分解为BaCl 、Pt和Cl,376.8℃时平衡常数K=1.0×104Pa2,在一
6 2 2 p
硬质玻璃烧瓶中加入过量BaPtCl ,抽真空后,通过一支管通入碘蒸气(然后将支管封闭),在376.8℃,碘
6
蒸气初始压强为 。376.8℃平衡时,测得烧瓶中压强为32.5 kPa,则P =_______ kPa,反应
Icl
2ICl(g)=I(g) +Cl(g)的平衡常数K=_______(列出计算式即可)。
2 2
(3)McMorris测定和计算了在136~180℃范围内下列反应的平衡常数K。
p
2NO(g)+2ICl(g) 2NOCl (g)+ I (g) K
2 p1
2NOCl (g) 2NO (g)+ Cl(g) K
2 p2
得到 和 均为线性关系,如下图所示:①由图可知,NOCl分解为NO和Cl 反应的ΔH_______0(填“大于”或“小于”)
2
②反应2ICl(g)=I(g) +Cl(g)的K=_______(用K 、K 表示):该反应的ΔH _______0(填“大于”或“小
2 2 p1 p2
于”),写出推理过程_______。
(4)Kistiakowsky曾研究了NOCl光化学分解反应,在一定频率(v)光的照射下机理为:
NOCl+ →
+NOCl→2NO+Cl
2
其中 表示一个光子能量, 表示NOCl的激发态。可知,分解1mol的NOCl需要吸收
_______mol光子。
【答案】(1)溴(或Br) (3)24.8
(3)①大于 ②K ·K 大于 设T/>T,即 ,由图可知:
p1 p2
则:
,即 ,因此该反应正反应为吸热反应,即ΔH大于0
(4)0.5
【解析】(1)红棕色液体,推测为溴单质,因此错过发现的元素是溴(或Br);
(2)由题意玻376.8℃时璃烧瓶中发生两个反应:BaPtCl (s) BaCl (s)+ Pt (s)+2 Cl (g)、Cl(g)
6 2 2 2
+I (g) 2ICl(g)。BaPtCl (s) BaCl (s)+ Pt (s)+2 Cl (g)的平衡常数K=1.0×104Pa2,则平衡时
2 6 2 2 p
p2(Cl )= 1.0×104Pa2,平衡时p(Cl )=100Pa,设到达平衡时I(g)的分压减小pkPa,则:
2 2 2
376.8℃平衡时,测得烧瓶中压强为32.5kPa,则0.1+20.0+p=32.5,解得p=12.4,则平衡时
P =2pkPa=2×12.4kPa=24.8kPa;则平衡时,I(g)的分压为(20.0-p)kPa=(20×103-12.4×103)Pa,
Icl 2
24.8kPa=24.8×103Pa,p(Cl )=0.1kPa=100Pa,因此反应2ICl(g)=I (g) +Cl (g)的平衡常数K=
2 2 2
;(3)①结合图可知,温度越高, 越小,lgKp 越大,即Kp 越大,说明升高
2 2
温度平衡2NOCl (g) 2NO (g)+ Cl (g)正向移动,则NOCl分解为NO和Cl 反应的大于0;②Ⅰ.
2 2
2NO(g)+2ICl(g) 2NOCl (g)+ I (g) K ;Ⅱ.2NOCl (g) 2NO (g)+ Cl (g) K ;Ⅰ+Ⅱ得
2 p1 2 p2
2ICl(g)=I (g) +Cl (g),则2ICl(g)=I (g) +Cl (g)的K= K ·K ;该反应的ΔH大于0;推理过程如下:设
2 2 2 2 p1 p2
,即 ,由图可知: 则:
,即 ,因此该反应正反应为吸热反应,即ΔH大
于0;(4)Ⅰ. NOCl+ → ,Ⅱ. +NOCl→2NO+Cl ,Ⅰ+Ⅱ得总反应为
2
2NOCl+hv=2NO+Cl ,因此2molNOCl分解需要吸收1mol光子能量,则分解1mol的NOCl需要吸收0.5mol
2
光子。10.【2021•湖南选择性考试】氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可
通过下面两种方法由氨气得到氢气。
方法Ⅰ.氨热分解法制氢气
相关化学键的键能数据
化学键 N≡N H﹣H N﹣H
键能E/(kJ•mol﹣1) 946 436.0 390.8
在一定温度下,利用催化剂将NH 分解为N 和H。回答下列问题:
3 2 2
(1)反应2NH (g) N(g)+3H(g) H= kJ•mol﹣1;
3 2 2
(2)已知该反应的△S=198.9J•mol﹣1•△K﹣1,在下列哪些温度下反应能自发进行? (填标号);
A.25℃ B.125℃ C.225℃ D.325℃
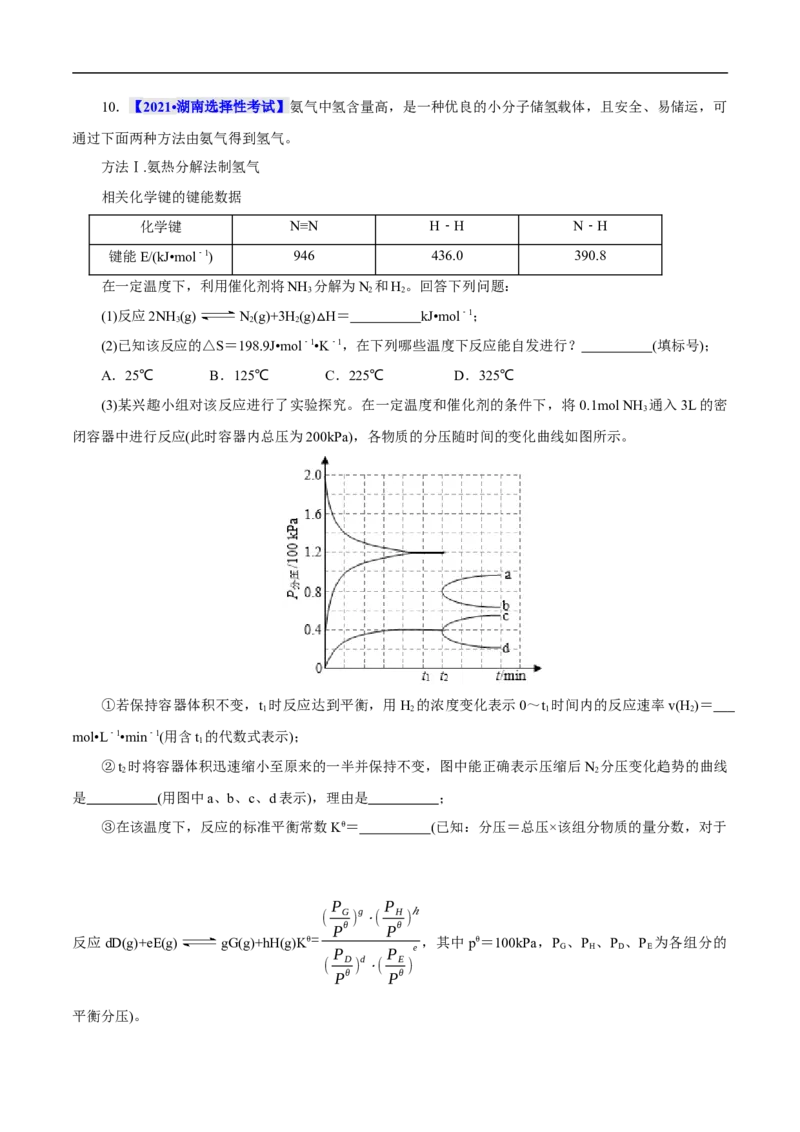
(3)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将 0.1mol NH 通入3L的密
3
闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
①若保持容器体积不变,t 时反应达到平衡,用H 的浓度变化表示0~t 时间内的反应速率v(H )=
1 2 1 2
mol•L﹣1•min﹣1(用含t 的代数式表示);
1
②t 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N 分压变化趋势的曲线
2 2
是 (用图中a、b、c、d表示),理由是 ;
③在该温度下,反应的标准平衡常数Kθ= (已知:分压=总压×该组分物质的量分数,对于
P P
( G ) g ⋅( H )ℎ
Pθ Pθ
反应dD(g)+eE(g) gG(g)+hH(g)Kθ= ,其中pθ=100kPa,P 、P 、P 、P 为各组分的
P P e G H D E
D d E
( ) ⋅( )
Pθ Pθ
平衡分压)。方法Ⅱ.氨电解法制氢气
利用电解原理,将氨转化为高纯氢气,其装置如图所示。
(4)电解过程中OH﹣的移动方向为 (填“从左往右”或“从右往左”);
(5)阳极的电极反应式为 。
【答案】(1)+90.8 (2)CD
(3)① ②b 开始体积减半,N 分压变为原来的2倍,随后由于加压平衡逆向移动,N 分
2 2
压比原来2倍要小 ③0.48
(4)从右往左 (5)2NH -6e-+6OH-= N +6H O
3 2 2
【解析】(1)由△H=反应物键能和﹣生成物键能和可知,该反应的△H=2×(390.8kJ•mol﹣1×3)﹣
[(946kJ•mol﹣1)+(436.0kJ•mol﹣1×3)]=+90.8kJ•mol﹣1;(2)在等温等压的反应中△G=△H﹣T S<0时,正反
△
应能自发进行,其中△H=+90.8kJ•mol﹣1,△S=198.9J•mol﹣1•K﹣1,则T △H 90.8×103J/mol
> = =
△S 198.9J⋅mol−1 ⋅K−1
456.5k=183.52℃,故选 C、D;(3)①密闭容器中 0.1molNH 总压为 200kPa,则如图 t 时 H 的分压为
3 1 2
0.06mol
120kPa
120kPa,则H 的物质的量为 ×0.1mol=0.06mol,故v(H ) △c 3L 0.02mol•L﹣1•min﹣
2 200kPa 2 = = =
△t t min t
1 1
1;②容器体积迅速缩小到原来的一半,则氮气的分压迅速增大到原来的2倍,故cd错误;压强增大,平
衡向气体总体积减小的方向移动,即平衡逆向移动,N 的分压应比原来2倍小,故b正确,a错误;③在
2
该温度下,达到平衡时,p(N )=40kPa=0.4pθ、p(H )=120kPa=1.2pθ、p(NH )=120kPa=1.2pθ,则Kθ
2 2 3p(N ) p(H ) 3
( 2 )×( 2 )
pθ pθ 0.4×1.23
0.48;(4)电解池中,左侧消耗NH 生成N ,发生氧化反应是阳极,
= = = 3 2
p(N H ) 1.22
3 2
( )
pθ
消耗了OH﹣,右侧水中H+得电子生成H ,发生还原反应,是阴极,电极反应中生成OH﹣,故OH﹣从右向
2
左移动;(5)阳极是NH 失电子发生氧化反应生成N,则电极反应式为6OH﹣+2NH﹣6e﹣=N+6H O。
3 2 3 2 2
11.【2019•新课标Ⅲ卷】近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之
迅速增长。因此,将氯化氢转化为氯气的技术成为科学研究的热点。回答下列问题:
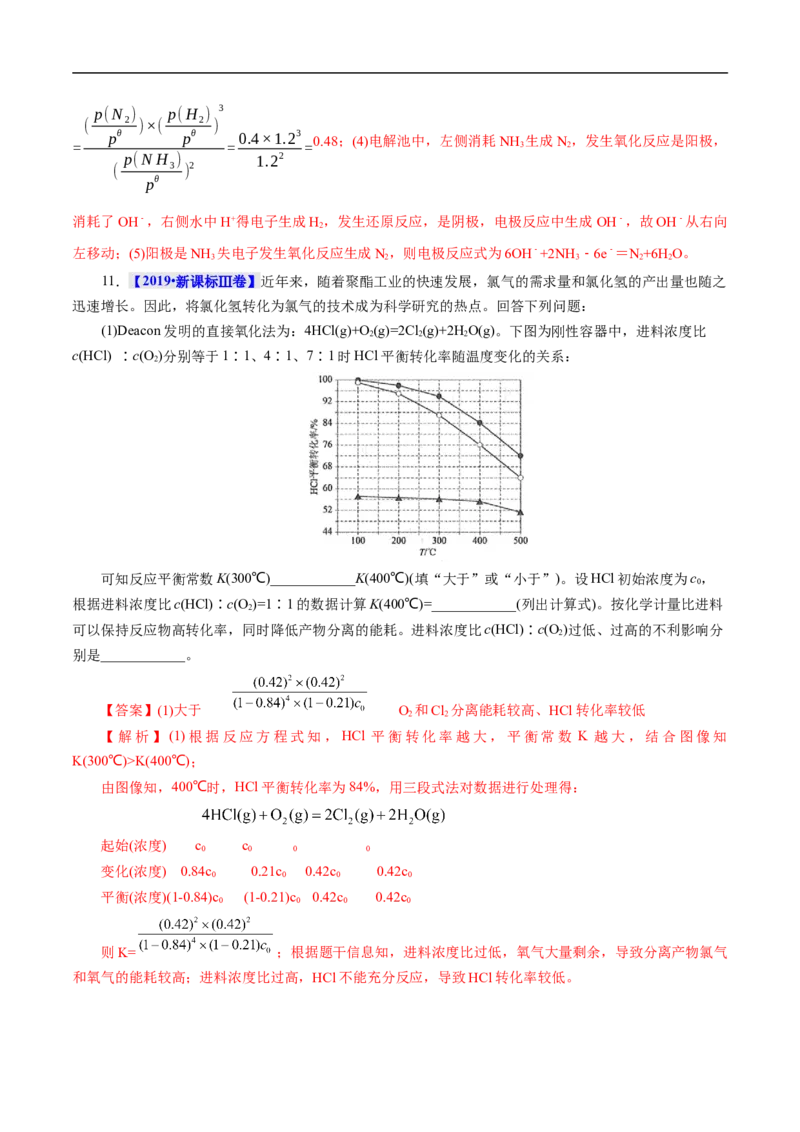
(1)Deacon发明的直接氧化法为:4HCl(g)+O (g)=2Cl (g)+2HO(g)。下图为刚性容器中,进料浓度比
2 2 2
c(HCl) ∶c(O )分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系:
2
可知反应平衡常数K(300℃)____________K(400℃)(填“大于”或“小于”)。设HCl初始浓度为c,
0
根据进料浓度比c(HCl)∶c(O )=1∶1的数据计算K(400℃)=____________(列出计算式)。按化学计量比进料
2
可以保持反应物高转化率,同时降低产物分离的能耗。进料浓度比c(HCl)∶c(O )过低、过高的不利影响分
2
别是____________。
【答案】(1)大于 O 和Cl 分离能耗较高、HCl转化率较低
2 2
【解析】(1)根据反应方程式知,HCl 平衡转化率越大,平衡常数 K 越大,结合图像知
K(300℃)>K(400℃);
由图像知,400℃时,HCl平衡转化率为84%,用三段式法对数据进行处理得:
起始(浓度) c c
0 0 0 0
变化(浓度) 0.84c 0.21c 0.42c 0.42c
0 0 0 0
平衡(浓度)(1-0.84)c (1-0.21)c 0.42c 0.42c
0 0 0 0
则K= ;根据题干信息知,进料浓度比过低,氧气大量剩余,导致分离产物氯气
和氧气的能耗较高;进料浓度比过高,HCl不能充分反应,导致HCl转化率较低。