文档内容
考点 26 弱电解质的电离
【基础过关】
1.下列事实或实验现象不能证明一元酸HX为弱酸的是
A.测得0.01mol/LHX溶液的pH=3.6
B.在KX稀溶液中滴加酚酞试剂,溶液变红
C.将稀HX溶液滴加到石灰石中,生成CO
2
D.在HX稀溶液中加入少许NaX粉末,溶液pH增大
【答案】C
【解析】A项,测得0.01mol/LHX溶液的pH=3.6,即氢离子物质的量浓度为1×10−3.6mol∙L−1,说明HX
是部分电离即一元酸HX为弱酸,故A不符合题意;B项,在KX稀溶液中滴加酚酞试剂,溶液变红,溶
液显碱性,说明是强碱弱酸盐即一元酸HX为弱酸,故B不符合题意;C项,将稀HX溶液滴加到石灰石
中,生成CO,说明酸性比碳酸强,不能证明一元酸HX为弱酸,故C符合题意;D项,在HX稀溶液中
2
加入少许NaX粉末,溶液pH增大,氢离子浓度减小,X-浓度增大,HX电离平衡逆向移动,说明一元酸
HX为弱酸,故D不符合题意。故选C。
2.(2023·北京市牛栏山一中高三检测)室温下,对于1L 醋酸溶液,下列判断正确的是( )
A.该溶液中CHCOO-的粒子数为 个
3
B.加入少量CHCOONa固体后,溶液的pH升高
3
C.滴加NaOH溶液过程中,c(CHCOO-)与c(CHCOOH)之和始终为0.1mol/L
3 3
D.与NaCO 溶液反应的离子方程式为CO2-+2H+=H O+CO↑
2 3 3 2 2
【答案】B
【解析】A项, 1L 0.1mol•L-1醋酸溶液中醋酸的物质的量为0.1mol,醋酸属于弱酸,是弱电解质,在
溶液中部分电离,则CHCOO-的粒子数小于6.02×1022,A项错误;B项,加入少量CHCOONa固体后,溶
3 3
液中CHCOO-的浓度增大,根据同离子效应,会抑制醋酸的电离,溶液中的氢离子浓度减小,酸性减弱,
3
则溶液的pH升高,B项正确;C项,1L 0.1mol•L-1醋酸溶液中醋酸的物质的量为0.1mol,滴加NaOH溶液
过程中,溶液中始终存在物料守恒,n(CHCOO-)+n(CH COOH)=0.1mol,但溶液体积不确定,故二者浓度
3 3
之和无法计算,C项错误;D项,醋酸是弱电解质,离子反应中不能拆写,则离子方程式为CO2-
3
+2CH COOH=H O+CO↑+2CH COO-,D项错误;故选B。
3 2 2 3
3.醋酸溶液中存在电离平衡:CHCOOH H++CHCOO-,下列叙述不正确的是
3 3
A.0.1 mol/L 的CHCOOH 溶液加水稀释或加热均可使CHCOO-的物质的量增多
3 3
B.0.1 mol/L 的CHCOOH 溶液加水稀释,c(CHCOO-)/[c(CHCOOH) ·c(OH-)]不变
3 3 3
资料整理【淘宝店铺:向阳百分百】C.向0.1 mol/L CH COOH溶液中加入少量纯醋酸,平衡向右移动,电离程度增大
3
D.0.1 mol/L CH COOH溶液加水稀释后,溶液中c(CHCOOH)/c(CHCOO-)的值减小
3 3 3
【答案】C
【解析】A项,0.1 mol/L 的CHCOOH 溶液加水稀释或加热,平衡正向移动,均可使CHCOO-的物
3 3
质的量增多,故不选A;B项,0.1 mol/L 的CHCOOH 溶液加水稀释,c(CHCOO-)/[c(CHCOOH)
3 3 3
·c(OH-)]=K/K ,只受温度影响,加水稀释不发生变化,故不选B;C项,向0.1 mol/L CH COOH溶液中
a w 3
加入少量纯醋酸,平衡向右移动,电离程度减小,故选C;D项,0.1 mol/L CH COOH溶液加水稀释,平
3
衡正向移动,溶液中c(CHCOOH)/c(CHCOO-)= n(CHCOOH)/n(CHCOO-)的值减小,故不选D。
3 3 3 3
4.(2023·浙江省宁波市高三选考模拟考试)下列说法正确的是( )
A.25℃时,将pH=5的醋酸溶液与pH=5的盐酸等体积混合,混合后溶液pH>5
B.25℃时,等浓度的盐酸与醋酸分别稀释相同倍数,稀释后溶液pH:盐酸<醋酸
C.25℃时,等体积、等pH的盐酸与醋酸分别用等浓度的NaOH溶液中和,盐酸消耗NaOH溶液多
D.25℃时,pH=3的一元酸HA溶液与pH=11的一元碱MOH溶液等体积混合后溶液呈酸性,则HA
是强酸
【答案】B
【解析】A项,pH=5的醋酸溶液与pH=5的盐酸中氢离子浓度相同,都是10-5mol/L,等体积混合后,
氢离子浓度不变,故pH为5,A错误;B项,等浓度的盐酸与醋酸分别稀释相同倍数后其浓度依然相同,
醋酸是弱酸,部分电离,氢离子浓度较小,pH大,B正确;C项,等体积、等pH的盐酸与醋酸,其中醋
酸的浓度大,用氢氧化钠中和时消耗的氢氧化钠较多,C错误;D项,混合后溶液呈酸性,说明酸的浓度
较大,则酸HA为弱酸,MOH是相对较强的碱,但是不一定是强碱,D错误;故选B。
5.已知某温度下 CHCOOH 和 NH ·H O 的电离常数相等,现向 10 mL 浓度为 0.1 mol·L-1的
3 3 2
CHCOOH溶液中滴加相同浓度的氨水,在滴加过程中( )
3
A.水的电离程度始终增大
B.c(NH)/c(NH ·H O)先增大再减小
3 2
C.c(CHCOOH)与c(CHCOO-)之和始终保持不变
3 3
D.当加入氨水的体积为10 mL时,c(NH)=c(CHCOO-)
3
【答案】D
【解析】开始滴加氨水时,水的电离程度增大,二者恰好完全反应时,水的电离程度最大,再继续滴
加氨水时,水的电离程度减小,A项错误;向醋酸中滴加氨水,溶液的酸性减弱,碱性增强,c(OH-)增大,
由 NH ·H O NH+OH-可知 K=,则=,故减小,B 项错误;根据原子守恒知 n(CHCOO-)与
3 2 3
n(CHCOOH)之和不变,但滴加氨水过程中,溶液体积不断增大,故 c(CHCOO-)与c(CHCOOH)之和减小,
3 3 3
C项错误;由CHCOOH和NH ·H O的电离常数相等可知当二者恰好完全反应时,溶液呈中性,结合电荷
3 3 2
守恒知c(CHCOO-)+c(OH-)=c(NH)+c(H+),则c(CHCOO-)=c(NH),D项正确。
3 3
资料整理【淘宝店铺:向阳百分百】6.(2023·浙江省诸暨市高三适应性考试)已知HR为二元弱酸,K (H R)=5.4×10-2,K (H R)=5.4×10-
2 a1 2 a2 2
5。室温下,下列说法不正确的是( )
A.0.1mol/L NaHR溶液pH<7
B.用NaOH溶液中和一定量的HR溶液至呈中性时,溶液中c(HR-)<c(R2-)
2
C.0.1mol/L H R溶液:.2mol/L+c(OH-)=c(H+)+c(H R)+c(HR-)
2 2
D.0.01mol/L的HR溶液与pH=12的NaOH溶液完全中和时,消耗酸与碱溶液的体积比为1∶2
2
【答案】C
【解析】A项,NaHR是弱酸HR的酸式盐,存在电离和水解, ,电离强于
2
水解,0.1mol/L NaHR溶液pH<7,A正确;B项,用NaOH溶液中和一定量的 HR溶液至呈中性时,
2
c(OH-)=c(H+)=10-7mol/L, ,故溶液中c(HR-)<c(R2-),B
正确;C 项,0.1mol/L H R 溶液中根据电荷守恒和元素守恒可得 c(HR)+c(HR-)+c(R2-)=0.1mol/L,
2 2
c(H+)=c(HR-)+2c(R2-)+c(OH-) , 故 .2mol/L+c(OH-)=c(H+)+2c(H R)+c(HR-) , C 错 误 ; D 项 ,
2
HR+2NaOH=2HO+Na R,0.01mol/L的HR(二元酸)溶液与pH=12即0.01mol/L的NaOH溶液完全中和时,
2 2 2 2
消耗酸与碱溶液的体积比为1∶2,D正确;故选C。
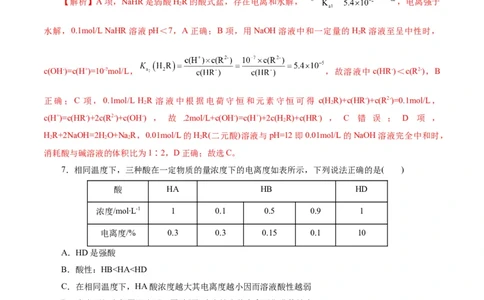
7.相同温度下,三种酸在一定物质的量浓度下的电离度如表所示,下列说法正确的是( )
酸 HA HB HD
浓度/mol∙L-1 1 0.1 0.5 0.9 1
电离度/% 0.3 0.3 0.15 0.1 10
A.HD是强酸
B.酸性:HB苯甲酸溶液
D.C HCOONa溶液中存在关系:c(C HCOO—)=c(Na+)=c(H+)=c(OH—)
6 5 6 5
【答案】B
【解析】A项,苯甲酸钠是强碱弱酸盐,在溶液中水解使溶液呈碱性,则常温下,0.1mol/L的苯甲酸
钠溶液的pH小于13,故A错误;B项,苯甲酸是一种有机弱酸,在溶液中部分电离出氢离子,相同浓度
的盐酸与苯甲酸溶液中盐酸中氢离子浓度大于苯甲酸溶液,溶液的pH大于苯甲酸溶液,故B正确;C项,
等体积等物质的量浓度的盐酸与苯甲酸溶液的中和能力相同,完全反应消耗氢氧化钠的物质的量相等,故
C错误;D项,苯甲酸钠是强碱弱酸盐,在溶液中水解使溶液呈碱性,则溶液中离子浓度的大小顺序为
c(Na+)>c(C HCOO—)>c(OH—) >c(H+),故D错误;故选B。
6 5
9.下列叙述正确的是( )
A.常温下 的HA溶液与 的BOH等体积混合,溶液 ,则BOH为强碱
B.含1molKOH的溶液与1molCO 完全反应后的溶液中:c(K+) =c(HCO -)
2 3
C. 氨水的,pH=a,加入适量的氯化铵固体可使溶液pH=a+1
D.物质的量浓度相等的(NH )SO 溶液与(NH )CO 溶液中, 前者大于后者
4 2 4 4 2 3
【答案】D
【解析】A项,常温下pH=2的HA溶液与pH=12的BOH等体积混合,则酸和碱电离出的n(H+) =
n(OH-),最后溶液pH>7,说明BOH有剩余,证明BOH未完全电离,所以BOH为弱碱,A项错误;B项,
含1molKOH的溶液与1molCO2完全反应后,溶液的溶质为KHCO ,HCO -在水中会水解和电离,浓度会
3 3
减少,所以c(K+) >c(HCO -),B项错误;C项,0.1 molL−1氨水的pH=a,溶液中存在电离平衡:NH ·H O
3 3 2
NH
4
++OH-+,加入适量的氯化铵固体,c(NH
4
+)增⋅ 大,平衡逆向移动,c(OH-)减小,pH会小于a,所
以C项错误;D项,物质的量浓度相等的(NH )SO 溶液与(NH )CO 都会存在水解平衡NH ++H O
4 2 4 4 2 3 4 2
NH ·H O+H+,与硫酸根比,碳酸根水解呈碱性促进水解平衡正向移动,c(NH ·H O)会变大,c(NH +)会减
3 2 3 2 4
小,使得 变小,所以物质的量浓度相等的(NH )SO 溶液与(NH )CO 中,(NH )CO 前者大于后者,
4 2 4 4 2 3 4 2 3
D项正确;故选D。
资料整理【淘宝店铺:向阳百分百】10.下列说法正确的是( )
A.相同温度下,等pH的盐酸和醋酸加水稀释10倍后,c(Cl-)<c(CHCOO-)
3
B.0.1 mol·L-1的KA溶液pH=6.5,则HA为弱酸
C.常温下pH=3的盐酸和pH=11的氨水等体积混合:c(Cl-)+c(H+)=c(NH+)+c(OH-)
4
D.某温度下,向氨水中通入CO,随着CO 的通入, 不断增大
2 2
【答案】A
【解析】A项,盐酸为强酸,醋酸为弱酸,相同pH时,醋酸物质的量浓度大于盐酸浓度,相同pH时,
溶液中c(Cl-)=c(CH COO-),加水稀释相同倍数,促进醋酸的电离,推出c(Cl-)<c(CHCOO-),故A正确;B
3 3
项,没有指明温度是否是常温,因此无法判断HA是否是弱酸,故B错误;C项,一水合氨为弱碱,常温
下pH=3的盐酸和pH=11的氨水等体积混合,混合后溶质为NH Cl和NH ·H O,溶液显碱性,c(OH-)>
4 3 2
c(H+),c(NH +)>c(Cl-),即c(Cl-)+c(H+)<c(NH +)+c(OH-),故C错误;D项,
4 4
,K 只受温度影响,向氨水中通入二氧化碳气体,生成碳酸
b
铵或碳酸氢铵,溶液c(NH +)增大,该比值减小,故D错误;答案为A。
4
11.相同温度下,根据三种酸的电离常数,下列判断正确的是( )
酸 HX HY HZ
电离常数K/(mol·L-1) 9×10-7 9×10-6 1×10-2
A.三种酸的强弱关系:HX>HY>HZ
B.反应HZ+Y-===HY+Z-不能够发生
C.V升HY溶液,加入水使溶液体积为2V,则Q=K(HY),平衡正向移动,促进HY电离
D.0.1 mol·L-1 HX溶液加水稀释,值变小
【答案】C
【解析】相同温度下,酸的电离常数越大,则酸的电离程度越大,酸的酸性越强,则酸根离子水解程
度越小,根据电离平衡常数知,这三种酸的强弱顺序是HZ>HY>HX,故A错误;由A知,HZ的酸性大
于HY,根据强酸制取弱酸知,HZ+Y-===HY+Z-能发生,故B错误;K(HY)=,加水后Q= =K(HY),
Q<K,平衡正向移动,促进HY电离,故C正确;=,加水稀释时,c(H+)减小,K 值不变,则增大,故
a
D错误。
12.下列曲线中,可以描述乙酸(甲,K=1.8×10-5)和一氯乙酸(乙,K=1.4×10-3)在水中的电离程度和
a a
浓度关系的是( )
资料整理【淘宝店铺:向阳百分百】【答案】B
【解析】根据甲、乙的电离平衡常数得,这两种物质都是弱电解质,在温度不变、浓度相等时,电离
程度:CHCOOH<CHClCOOH,可以排除A、C;当浓度增大时,物质的电离程度减小,排除D选项,
3 2
故B项正确。
13.在稀氨水中存在下列平衡:NH + H O NH ·H O NH ++ OH— ,对于该平衡,下列叙
3 2 3 2 4
述正确的是( )
A.加入少量NH Cl固体,平衡逆向移动,溶液的pH减小
4
B.通入少量氨气,平衡正向移动,c (NH·H O) 减小
3 2
C.加入少量NaOH固体,并恢复至室温,平衡逆向移动,NH ·H O的电离平衡常数减小
3 2
D.加水稀释,NH ·H O的电离程度及c ( OH— ) 都增大
3 2
【答案】A
【解析】A项,加入少量NH Cl固体,导致溶液中铵根离子浓度增大,NH ·H O的电离平衡逆向移动,
4 3 2
氢氧根离子浓度减小,溶液的pH减小,A正确;B项,通入少量氨气,导致氨气与水的反应平衡正向移动,
c(NH ·H O)增大,B错误;C项,加入少量NaOH固体,并恢复至室温,NH ·H O的电离平衡逆向移动,
3 2 3 2
但NH ·H O的电离平衡常数与温度有关,温度未变,平衡常数不变,C错误;D项,加水稀释,NH ·H O
3 2 3 2
的电离平衡正向移动,电离程度增大,但c(OH-)减小,D错误;故选A。
14.下表是几种弱酸在常温下的电离平街常数:
CHCOOH HCO HS HPO
3 2 3 2 3 4
K =7.5×10-3
a1
K =4.3×10-7 K =9.1×10-8
a1 a1
1.8×10-5 K =6.2×10-8
a2
K =5.6×10-11 K =1.1×10-12
a2 a2
K =2.2×10-13
a3
则下列说法中不正确的是( )
A.碳酸的酸性强于氢硫酸
B.多元弱酸的酸性主要由第一步电离决定
C.常温下,加水稀释醋酸, 增大
D.向弱酸溶液中加少量NaOH溶液,电离平衡常数不变
【答案】D
【解析】A项,多元弱酸的酸性主要由第一步电离决定。弱酸的电离平衡常数越大,该酸的酸性就越
资料整理【淘宝店铺:向阳百分百】强。由于碳酸的电离平衡常数K =4.3×10-7比HS氢硫酸的电离平衡常数K = K =9.1×10-8大,所以酸性:
a1 2 a1 a1
碳酸比氢硫酸的酸性强,A正确;B项,多元弱酸一级电离产生的氢离子会抑制二级电离,所以多元弱酸
的二级电离程度远小于一级电离,故多元弱酸的酸性主要由第一步电离决定,B正确;C项,醋酸是一元
弱酸,在溶液中存在电离平衡:CHCOOH CHCOO-+H+,加水稀释,使电离平衡正向移动,导致溶
3 3
液中n(H+)有所增加,n(CHCOOH)减小,在同一溶液中,体积相同,所以加水稀释导致 增
3
大,C正确;D项,向弱酸溶液中加少量NaOH溶液,二者发生中和反应,放出热量,使溶液的温度升高;
升高温度,能够促进电解质的电离,使弱电解质电离平衡正向移动,导致其电离平衡常数增大,D错误;
故选D。
15.高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在
冰醋酸中的电离常数:
酸 HClO HSO HCl HNO
4 2 4 3
K 1.6×10-5 6.3×10-9 1.6×10-9 4.2×10-10
a
从以上表格中判断以下说法中不正确的是( )。
A.在冰醋酸中这4种酸都没有完全电离
B.在冰醋酸中高氯酸是这4种酸中最强的酸
C.在冰醋酸中硫酸的电离方程式为:HSO ===2H++SO
2 4
D.水对于这4种酸的强弱没有区分能力,但醋酸可以区别这4种酸的强弱
【答案】C
【解析】在冰醋酸中四种酸的电离常数均很小,可以判断其电离都是不完全的,A正确;HClO 的电
4
离常数最大,酸性最强,B正确;在冰醋酸中HSO 是弱酸,其电离是不完全的,且为分步电离,C错;
2 4
四种酸在水中都是完全电离而在冰醋酸中呈现不同的电离常数,其酸性得以区分,D正确。
16.已知部分弱酸的电离平衡常数如下表:
下列离子方程式正确的是( )
A.少量CO 通入NaClO溶液中:CO + H O + 2ClO-===CO 2-+ 2HClO
2 2 2 3
B.少量的SO 通入Ca(ClO) 溶液中:SO + H O + Ca2+ + 2ClO-===CaSO ↓+2HClO
2 2 2 2 3
C.少量的SO 通入NaCO 溶液中:SO + H O + 2CO 2-===SO2-+ 2HCO -
2 2 3 2 2 3 3 3
D.相同浓度NaHCO 溶液与NaHSO 溶液等体积混合:H+ + HCO -===CO ↑+ H O
3 3 3 2 2
【答案】C
资料整理【淘宝店铺:向阳百分百】