文档内容
考点 41 原子结构与性质
【基础过关】
1.(2023·湖南省衡阳市期末)磷灰石是制造磷肥和含磷化合物的最主要矿物原料,可表示为
Ca(PO )(F,Cl,OH)。下列有关化学用语或图示表达正确的是( )
5 4 3
A.OH-的电子式:
B.基态磷原子的最外层电子的轨道表示式:
C.基态Ca原子最高能级的电子云轮廓图:
D.中子数为20的氯原子:
2.(2023·安徽省黄山市期末)下列各项叙述中,正确的是( )
A.所有原子任一能层的s电子云轮廓图都是球形,但球的半径大小不同
B.价电子排布式为5s25p1的元素位于第五周期第ⅠA族,是s区元素
C.钠原子由1s22s22p63s1→1s22s22p63p1时,原子释放能量,由基态转化成激发态
D. Cr原子的电子排布式是1s22s22p63s23p63d44s2
24
3.(2023·广东省佛山市期末)人类对核外电子运动的认知不断进步。下列说法正确的是( )
A.电子在线性轨道上绕核运行
B.电子从激发态跃迁到基态时能产生吸收光谱
C. 、 、 轨道相互平行、能量相等
D.2s轨道比1s轨道大,其空间包含了 轨道
4.(2023·四川省成都市联考)下列说法错误的是( )
A.可用光谱仪摄取某元素原子由基态跃迁到激发态的发射光谱,从而进行元素鉴定
B.夜空中的激光与电子跃迁释放能量有关
C.若基态氮原子价电子排布式为2s22p 2p ,则违反洪特规则
D.若某基态原子有n种不同运动状态的电子,则该原子的原子序数为n
5.(2023·江西省宜春市期末)下列说法错误的是( )
A.所有非金属元素都分布在p区
B.同一原子中,2p、3p、4p电子的能量依次增大C.元素周期表中从第ⅢB族到第ⅡB族的10个纵列的元素都是金属元素
D.N能层中有4s、4p、4d、4f四个能级,共16个轨道,可容纳32种运动状态的电子
6.工业上通过Al O+N +3C 2AlN+3CO可制得高温陶瓷材料AlN。下列说法正确的是( )
2 3 2
A.N 的电子式为: B.AlN是分子晶体
2
C.27Al用原子中的中子数为14 D.基态氮原子轨道表示式:
7.“结构决定性质”是学习化学的重要思维方法,下列说法正确的是( )
A.同一元素不可能既表现金属性,又表现非金属性
B.第三周期元素的最高正化合价等于它所处的主族序数
C.核外电子排布相同的微粒,化学性质一定相同
D.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
8.(2023·重庆市南开中学校考三模)白铜是一种延展性好、硬度高、色泽美观、耐腐蚀的合金材料,
其主要成分为Cu、Ni、Zn,还含有少量S、P、As等元素。关于上述涉及到的元素,下列说法正确的是(
)
A.基态Ni原子的简化电子排布式为:
B.基态As原子最高能级的轨道形状为哑铃形
C.第一电离能:S>P>Cu
D.S、P为p区元素,Cu、Zn为d区元素
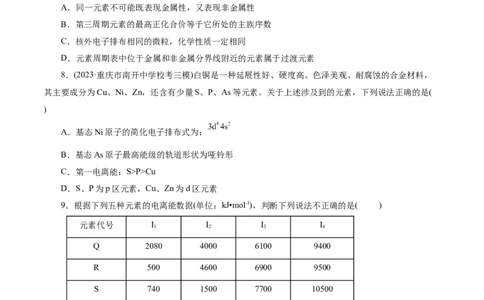
9.根据下列五种元素的电离能数据(单位:kJ•mol-1),判断下列说法不正确的是( )
元素代号 I I I I
1 2 3 4
Q 2080 4000 6100 9400
R 500 4600 6900 9500
S 740 1500 7700 10500
T 580 1800 2700 11600
U 420 3100 4400 5900
A.元素的第一电离能最大的可能是Q元素
B.R和S均可能与U在同一主族
C.U元素可能在元素周期表的s区
D.原子的价电子排布为ns2np1的可能是T元素
10.下列关于原子核外电子排布与元素在周期表中位置关系的表述正确的是( )A.原子的价电子排布式为ns2np1~6的元素一定是主族元素
B.基态原子的p能级上有5个电子的元素一定是第ⅦA族元素
C.原子的价电子排布式为(n-1)d6~8ns2的元素一定位于第ⅢB~第ⅦB族
D.基态原子的N层上只有1个电子的元素一定是主族元素
11.元素的原子结构决定其性质和在周期表中的位置。下列说法正确的是( )
A.按电子排布,可把周期表里的元素划分成5个区,Zn元素属于d区
B.多电子原子中,在离核较近的区域内运动的电子能量较高
C.P、S、Cl的第一电离能、电负性和最高价氧化物对应的水化物的酸性均依次增大或增强
D.某同学给出的Fe原子的3d能级电子排布图为 ,此排布图违反了洪特规则
12.下列说法正确的是( )
A.金属钠的焰色是黄色,它的产生与电子的跃迁吸收能量有关
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.氢原子核外只有一个电子,它产生的原子光谱中只有一根或明或暗的线
D.光谱分析就是利用原子光谱上的特征谱线来鉴定元素
13.气态原子生成+1价气态阳离子所需要的能量称为第一电离能。元素的第一电离能是衡量元素金
属性强弱的一种尺度。下列有关说法不正确的是( )
A.元素的第一电离能越大,其金属性越弱
B.元素的第一电离能越小,其金属性越强
C.金属单质跟酸反应的难易,只跟该金属元素的第一电离能有关
D.金属单质跟酸反应的难易,除跟该金属元素的第一电离能有关外,还与该金属原子失去电子后在
水溶液里形成水合离子的变化有关
14.玻尔理论、量子力学理论都是对核外电子运动状态的描述,根据对它们的理解,判断下列叙述正
确的是( )
A.因为s轨道的形状是球形的,所以s电子做圆周运动
B.3p、3p、3p 的差异之处在于三者中电子(基态)的能量不同
x y z
C.在同一能级上运动的电子,其运动状态肯定相同
D.原子轨道和电子云都是用来形象地描述电子运动状态的
15.某元素的最外层电子数为2,价电子数为5,并且该元素是同族中原子序数最小的元素,关于该元
素的判断错误的是( )
A.该元素原子的电子排布式为[Ar]3d34s2B.该元素为Ⅴ
C.该元素属于ⅢA族元素 D.该元素属于过渡元素
16.某短周期元素R的各级电离能数据(用I、I……表示,单位为kJmol-1)如表所示。关于元素R的
1 2
判断中正确的是( ) ⋅I I I I
1 2 3 4
R 740 1500 7700 10500
A.R元素基态原子的电子排布式为ns1 B.R的最高正价为+4价
C.R元素可能属于非金属元素 D.R元素位于元素周期表中第ⅡA族
17.第一电离能、第二电离能、第三电离能分别用I 、I 、I 表示,下表是第三周期部分元素的电离能
1 2 3
[单位:eV(电子伏特)]数据。
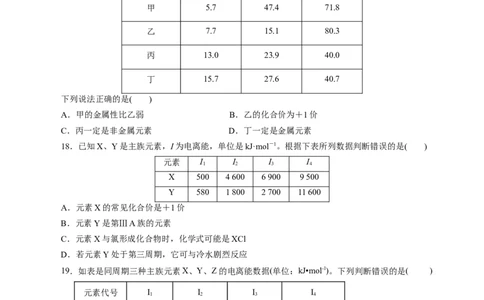
元素 I/eV I/eV I/eV
1 2 3
甲 5.7 47.4 71.8
乙 7.7 15.1 80.3
丙 13.0 23.9 40.0
丁 15.7 27.6 40.7
下列说法正确的是( )
A.甲的金属性比乙弱 B.乙的化合价为+1价
C.丙一定是非金属元素 D.丁一定是金属元素
18.已知X、Y是主族元素,I为电离能,单位是kJ·mol-1。根据下表所列数据判断错误的是( )
元素 I I I I
1 2 3 4
X 500 4 600 6 900 9 500
Y 580 1 800 2 700 11 600
A.元素X的常见化合价是+1价
B.元素Y是第ⅢA族的元素
C.元素X与氯形成化合物时,化学式可能是XCl
D.若元素Y处于第三周期,它可与冷水剧烈反应
19.如表是同周期三种主族元素X、Y、Z的电离能数据(单位:kJ•mol-1)。下列判断错误的是( )
元素代号 I I I I
1 2 3 4
X 496 4562 6912 9543
Y 578 1817 2745 11575
Z 738 1451 7733 10540
A.X为第IA族元素 B. 的价电子排布式为ns2np1
C.Z位于元素周期表s区 D.金属性:X>Y>Z20.四种常见元素基态原子的结构信息如下表。下列大小关系不一定正确的是( )
元素 X Y Z Q
价电子排
结构 有5个原子轨道填充有电子, 有8个不同运动 能级上
布式为
信息 有3个未成对电子 状态的电子 有2个电子
A.电负性: B.第一电离能:
C.单质的硬度: D.最高价含氧酸的酸性:
21.(2022·山东省实验中学模拟预测)含有N-、N+的材料Pb(N )、NAsF 可以用于炸药。下列说法正
3 5 3 2 5 6
确的是( )
A.Pb属于d区元素
B.基态As原子的d轨道与p轨道上的电子数之比为3:2
C.N-的空间构型为直线形
3
D.基态F原子中,核外电子的空间运动状态有9种
22.实验室中利用CoCl 制取配合物[Co(NH )]Cl 的反应为2CoCl + 10NH + 2NH Cl+H O
2 3 6 3 2 3 4 2 2
=2[Co(NH)]Cl +2H O。下列叙述正确的是( )
3 6 3 2
A.Co2+的价电子排布图为
B.1 mol [Co(NH)]3+中含σ键为18 mol
3 6
C.HO 中氧原子采用sp3杂化
2 2
D.氨分子间存在氢键,因而NH 易溶于水
3
23.(2023·福建龙岩高三联考)短周期元素X、Y、Z、W、Q原子序数依次增大,且X、Z、Q原子均
有两个单电子,W为地壳中含量最高的金属元素。下列说法正确的是( )
A.X易与多种元素形成离子键 B.简单氢化物的稳定性:Z<Q
C.第一电离能:Y>Z D.电负性:W>Z
24.(2023·山东烟台二模)短周期元素X、Y、Z、W原子序数依次增大。基态X原子有两个单电子,Z
的简单离子在同周期离子中半径最小,基态W原子的价电子排布式为ns(n-1)np(n-1),且Y、W同主族。下列
说法错误的是( )
A.电负性:Y>W>X>Z B.四种元素均位于元素周期表的p区
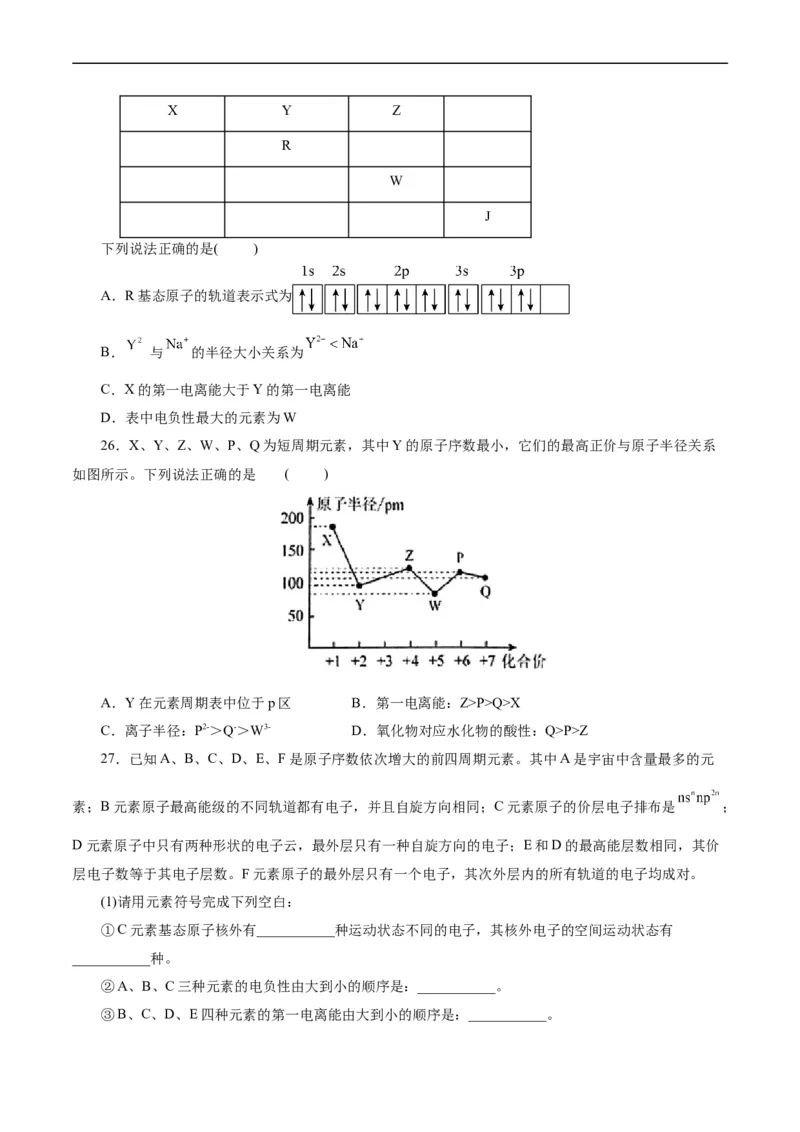
C.简单氢化物沸点:XP>Q>X
C.离子半径:P2->Q->W3- D.氧化物对应水化物的酸性:Q>P>Z
27.已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元
素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布是 ;
D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E和D的最高能层数相同,其价
层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
(1)请用元素符号完成下列空白:
①C元素基态原子核外有___________种运动状态不同的电子,其核外电子的空间运动状态有
___________种。
②A、B、C三种元素的电负性由大到小的顺序是:___________。
③B、C、D、E四种元素的第一电离能由大到小的顺序是:___________。(2)下表是A~F元素中某种元素的部分电离能,由此可判断该元素是___________(填元素名称)。
电离能/(kJ·mol-1)
元素
I I I I I
1 2 3 4 5
某种元素 578 1817 2745 11575 14830
(3)F元素位于周期表的___________区,该元素的价层电子排布图为___________。
28.嫦娥五号返回器带回月球土壤样品。研究发现,月球土壤样品中存在铁、金、银、铅、锌、铜等
矿物颗粒。请回答下列问题:
(1)基态Fe原子的价电子排布式为_______,在元素周期表中的位置为_______,基态Fe2+与Fe3+离子中
未成对电子数之比为_______。
(2)写出基态硅原子的电子轨道表示式_______,其中具有最高能级轨道电子云轮廓图的形状为_______。
(3)碳、氮和氧3种元素第一电离能由小到大的顺序为_______(填元素符号),碳、氮和氧3种元素的电
负性最大的是_______(填元素符号)。
(4)分析Cu、Zn的核外电子排布,推测Cu的第二电离能I_______Zn的第二电离能I(填写“大于”、
2 2
“小于”或“等于”)。
(5)资料显示:N元素电负性略大于Cl;NCl 可溶于水发生水解反应。试判断NCl 可能的水解方程式
3 3
为_______。
29.现有A、B、C、D、E、F、G、H八种元素,均为前四周期元素,它们的原子序数依次增大。请
根据下列相关信息,回答有关问题。
A元素的核外电子数和电子层数相等,也是宇宙中含量最丰富的元素
B元素是形成化合物种类最多的元素
C元素基态原子的核外p电子数比s电子数少1
D元素基态原子的核外p轨道中有两个未成对电子
E元素的气态基态原子的第一至第四电离能分别如下:I=738kJ/mol、
1
I=1451kJ/mol、I=7733kJ/mol、I=10540kJ/mol
2 3 4
F元素的主族序数与周期数的差为4
G元素是前四周期中电负性最小的元素
H元素位于元素周期表中的第八纵列
(1) 的电子式为_______(用元素符号表示,下同),其易溶于水的原因为_______。
(2)B元素的原子核外共有_______种不同运动状态的电子,基态原子中能量最高的电子所占据的原子轨道呈_______形。B元素的一种单质B 分子中每个B原子只跟相邻的3个碳原子形成共价键,且每个碳
60
原子最外层都满足8电子稳定结构,则一个B 分子中π键的数目为_______个。
60
(3)E元素的原子I 远远大于I,其原因是_______。
3 2
(4)D、E、F三种元素的简单离子半径由大到小的顺序是_______(用离子符号表示)。
(5)H位于元素周期表中_______区(按电子排布分区),其基态原子的价层电子轨道表示式为_______,
实验室用一种含G元素的黄色溶液检验 时产生蓝色沉淀,该反应的离子方程式为_______。
【能力提升】
30.(2023·湖南邵阳三模)金属M在潮湿的空气中会形成一层致密稳定的MZX•3M(XY) 薄膜。X、
3 2
Y、Z为短周期主族元素,X的原子序数是Y的8倍,X和Z同周期且X和Z基态原子的未成对电子数相
同,M是人体必需的微量元素之一。1molMZX 含有60mol质子。下列说法正确的是( )
3
A.原子半径:X>Z>Y
B.基态M原子的价层电子排布式为4s2
C.X、Y、Z三种元素的电负性:X>Z>Y
D.同周期元素中第一电离能比X大的有2种
31.短周期主族元素X、Y、Z、M、N的原子序数依次增大,其中基态Y原子s能级电子数是p能级
的两倍,Z和M位于同一主族,由上述五种元素形成的化合物可作离子导体,结构如图所示。下列说法正
确的是( )
A.原子半径:M>Y>Z>X
B.非金属性:M>N,Y>Z
C.氢化物沸点:Z>N>M>Y
D.同周期中第一电离能小于Z的元素有4种
32(2023·浙江杭州联考)X、Y、Z、W、Q五种短周期元素,原子序数依次增大。X元素基态原子电子
排布式为 ,Y元素的第一电离能大于同周期相邻元素的第一电离能,Z元素基态原子2p轨道有
一个未成对电子,W元素基态原子s能级上的电子总数与p能级上电子总数相等,Q是地壳中含量最多的金属元素。下列说法不正确的是( )
A.最高价氧化物对应水化物的碱性:
B.Y和原子序数为51的元素位于同一主族
C.同周期元素中Z的第一电离能最大
D.X、Q的氧化物、氢氧化物都有两性
33.合成氨是人类科学技术发展史上的一项重大成㩆,在很大程度上解决了地球上因粮食不足而导致
的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为___________,占据最高能级电子的电子云轮廓图为___________形。
②NH 分子中,与N原子相连的H显正电性。N、H电负性大小顺序为___________。
3
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al O、KO、CaO、MgO、Cr O 等
2 3 2 2 3
氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中d区的元素是________。
②比较Mg、Ca第一电离能的大小:_______。O的第一电离能小于N,原因是________。
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
元素 Na Mg Al
496 738 578
4562 1451 1817
电离能(kJ/mol)
6912 7733 2745
9543 10540 11575
结合数据说明Mg的常见化合价为+2价的原因___________。:
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成
氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为___________,铁在元素周期表中的位置为___________。
②比较Li+与H-的半径大小关系:r(Li+) ___________r(H-)((填“>”或“<”)。
34.铊的相关信息卡片如图所示:(1)铊的原子序数为81,铊在元素周期表中位置_______。
(2)根据所学知识,下列推断正确的是_______。
A.单质的还原性:Tl>Al B.原子半径:Al>Tl
C.碱性:Al(OH) >Tl(OH) D.氧化性:Tl3+>Al3+
3 3
(3)铊(Tl)是某超导材料的组成元素之一。Tl3+与Ag在酸性介质中发生反应:Tl3++2Ag=Tl++2Ag+。下列
推断正确的是_______。
A.Tl+最外层有1个电子 B.Tl能形成+3价和+1价的化合物
C.Tl3+的氧化性比Ag+弱 D.Tl+的还原性比Ag强
(4)随着科技的不断发展,人类对原子结构的认识不断深入,新型材料层出不穷。表中列出了第三周期
的几种元素的部分性质:请按要求回答下列问题:
元素编号 a b c d e
电负性 3.0 2.5 X 1.5 0.9
主要化合价 -1,+7 -2,+6 -3,+5 +3 +1
①写出基态a原子的价层电子轨道表示式:_______。
②预测X值的范围:_______<X<_______。
③表中五种元素的第一电离能由大到小排第二的是_______(写元素符号)。
(5)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂、钛酸锂等正极材料研究方面的卓越贡献而
获得2019年诺贝尔化学奖。回答下列问题:
①基态Ti原子的核外电子排布式为:_______。
②基态Fe3+、Fe2+离子中未成对的电子数之比为_______。
③元素Li为_______区元素。
35.有a、b、c、d、e、f、g七种元素,原子序数依次增大,前5种为短周期主族元素,f、g为第四
周期的元素。有关信息如下表,请回答以下问题:
a a能形成一种硬度最大的固体单质
c c元素基态原子的电子排布式为
d d基态原子的I=578kJ/mol、I=1817kJ/mol、I=2745kJ/mol、I=11575kJ/mol
1 2 3 4
e e基态原子核外3p轨道半满
f f在周期表中第11纵行
g g基态原子最外层电子数为2
(1)a、f的元素符号为_______、_______,分别位于元素周期表的_______分区和_______分区。
(2)e的基态原子中能量最高的电子所占的轨道形状是_______,其电子云在空间有_______个伸展方向。(3)d基态原子的价层电子的轨道表示式为_______,某元素在元素周期表中位置处于d元素的左上角对
角线处,它们具有部分相似的性质,请写出该元素组成的单质与氢氧化钠溶液反应的化学方程式_______
(4)b、c两种元素基态原子的第一电离能由大到小的顺序为_______(用元素符号表示)。解释造成两者
电离能大小差别的主要原因:_______。
(5)g基态原子的简化电子排布式为_______。
(6)元素f基态原子的第二电离能_______元素g基态原子的第二电离能(填“>”、“<”或“=”)
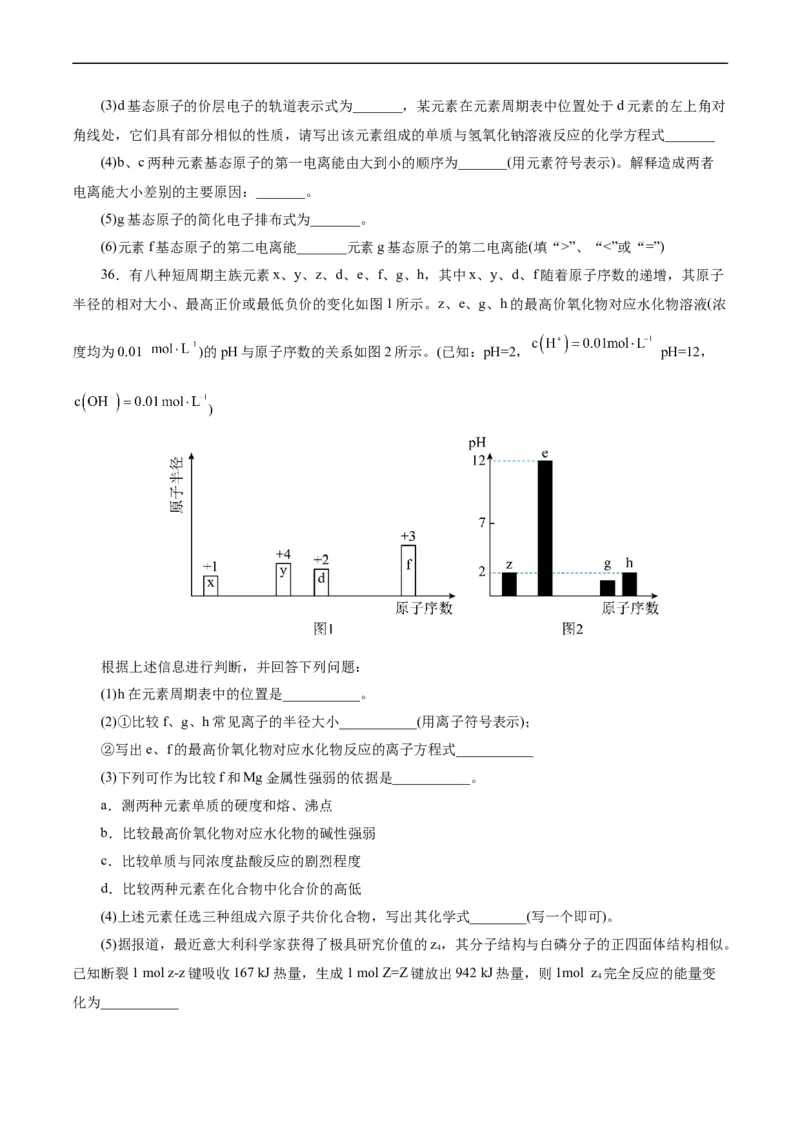
36.有八种短周期主族元素x、y、z、d、e、f、g、h,其中x、y、d、f随着原子序数的递增,其原子
半径的相对大小、最高正价或最低负价的变化如图1所示。z、e、g、h的最高价氧化物对应水化物溶液(浓
度均为0.01 )的pH与原子序数的关系如图2所示。(已知:pH=2, pH=12,
)
根据上述信息进行判断,并回答下列问题:
(1)h在元素周期表中的位置是___________。
(2)①比较f、g、h常见离子的半径大小___________(用离子符号表示);
②写出e、f的最高价氧化物对应水化物反应的离子方程式___________
(3)下列可作为比较f和Mg金属性强弱的依据是___________。
a.测两种元素单质的硬度和熔、沸点
b.比较最高价氧化物对应水化物的碱性强弱
c.比较单质与同浓度盐酸反应的剧烈程度
d.比较两种元素在化合物中化合价的高低
(4)上述元素任选三种组成六原子共价化合物,写出其化学式________(写一个即可)。
(5)据报道,最近意大利科学家获得了极具研究价值的z,其分子结构与白磷分子的正四面体结构相似。
4
已知断裂1 mol z-z键吸收167 kJ热量,生成1 mol Z=Z键放出942 kJ热量,则1mol z 完全反应的能量变
4
化为___________(6)由上述元素中的y、z、e组成的某剧毒化合物eyz不慎泄漏时,消防人员通常采用喷洒过氧化氢溶
液的方式处理,以较少污染。反应生成一种酸式盐和一种气体,二者溶于水均呈碱性,该反应的化学方程
式为________。已知eyz含有z 分子中类似的化学键,写出化合物eyz的电子式________。
2
(7)①将xyzd的电负性按照从大到小的顺序排序___________(用元素符号表示)
②将efgh的第一电离能按照从小到大的顺序排序___________(用元素符号表示)
(8)将23.9 g表面已锈蚀成铜绿[Cu (OH) CO]的铜片投入100 mL一定浓度的Z的最高价含氧酸中,充
2 2 3
分反应后,该酸被还原成ZO 和ZO,反应后溶液中H+的物质的量为0.160mol。往反应后的溶液中加入过
2
量的NaOH溶液,滤出沉淀,洗涤,干燥后得到29.4 g蓝色固体。
①铜片中单质铜的质量分数为___________。
②铜片与该酸充分反应后,溶液中ZO-的物质的量浓度(假设反应前后溶液的体积不变)为______。
3