文档内容
考点巩固卷 08 化学反应与能量(二)
考法01 电解原理
考点03 电解池、金属的腐蚀与防护
考法02 电解原理的应用
(限时:20min)
考法03 金属的腐蚀与防护
考法01 电解原理在物质制备中的应用
考点04 电化学原理的综合应用 考法02 电解原理应用与污水处理
(限时:30 min) 考法03 电解原理在大气治理方面的应用
考法04 电解原理应用与金属处理
考点05 多池、多室的电化学装置 考法01 多池串联的两大模型
(限时:20 min) 考法02 离子交换膜电解池
考点03 电解池、金属的腐蚀与防护
考法01 电解原理
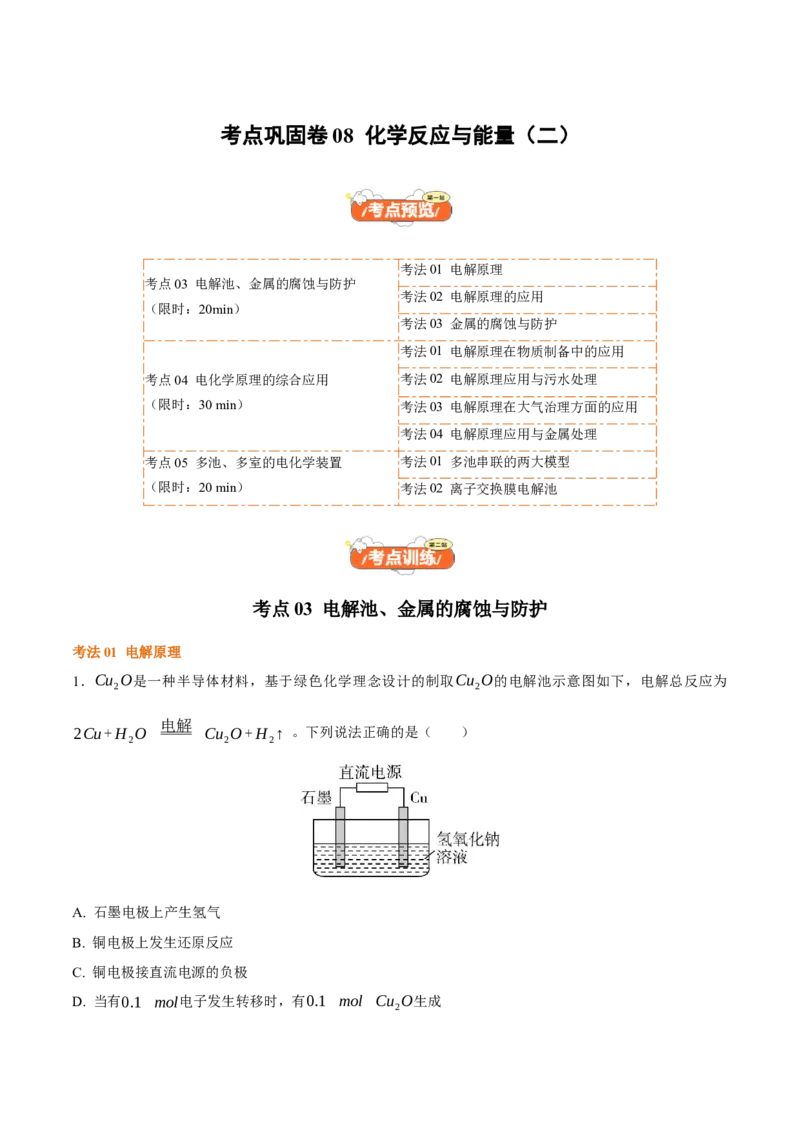
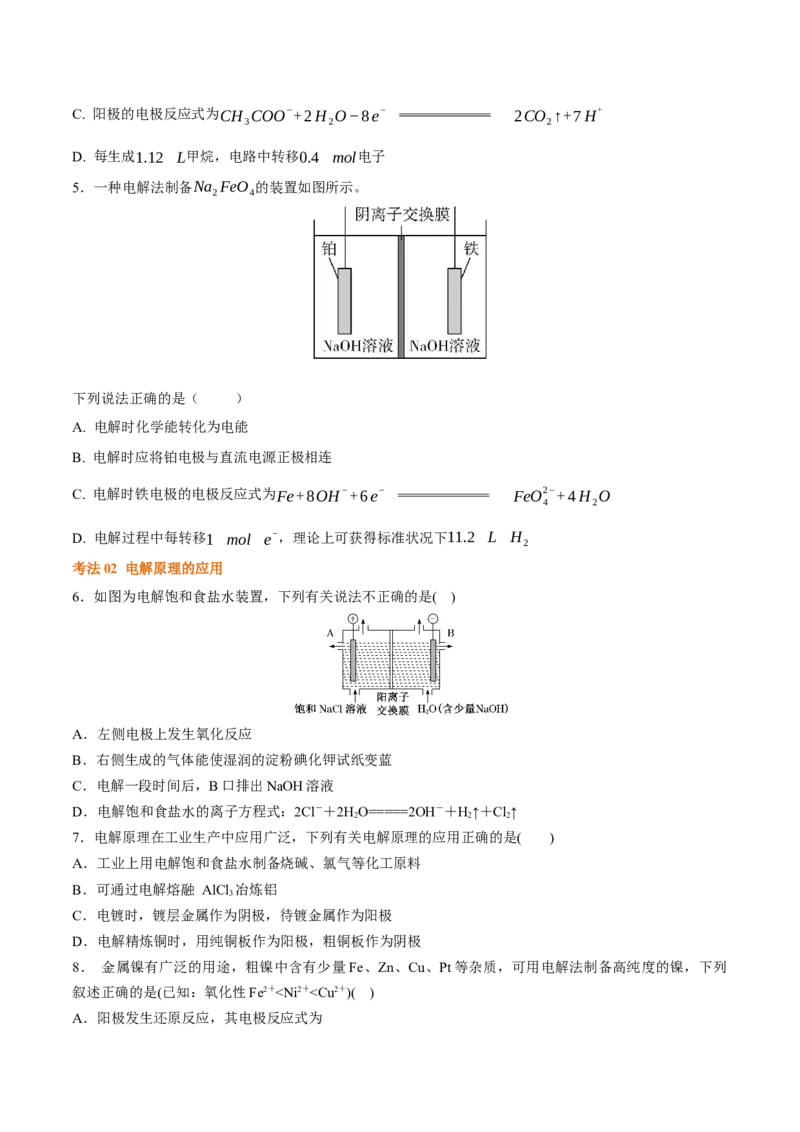
1.Cu O是一种半导体材料,基于绿色化学理念设计的制取Cu O的电解池示意图如下,电解总反应为
2 2
电解
2Cu+H O Cu O+H ↑ 。下列说法正确的是( )
2 2 2
A. 石墨电极上产生氢气
B. 铜电极上发生还原反应
C. 铜电极接直流电源的负极
D. 当有0.1 mol电子发生转移时,有0.1 mol Cu O生成
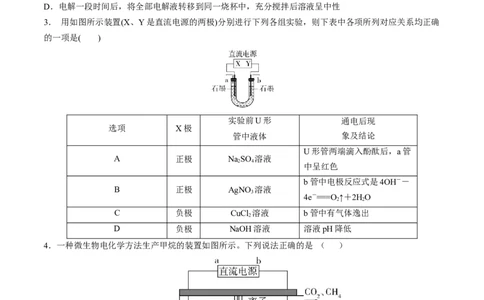
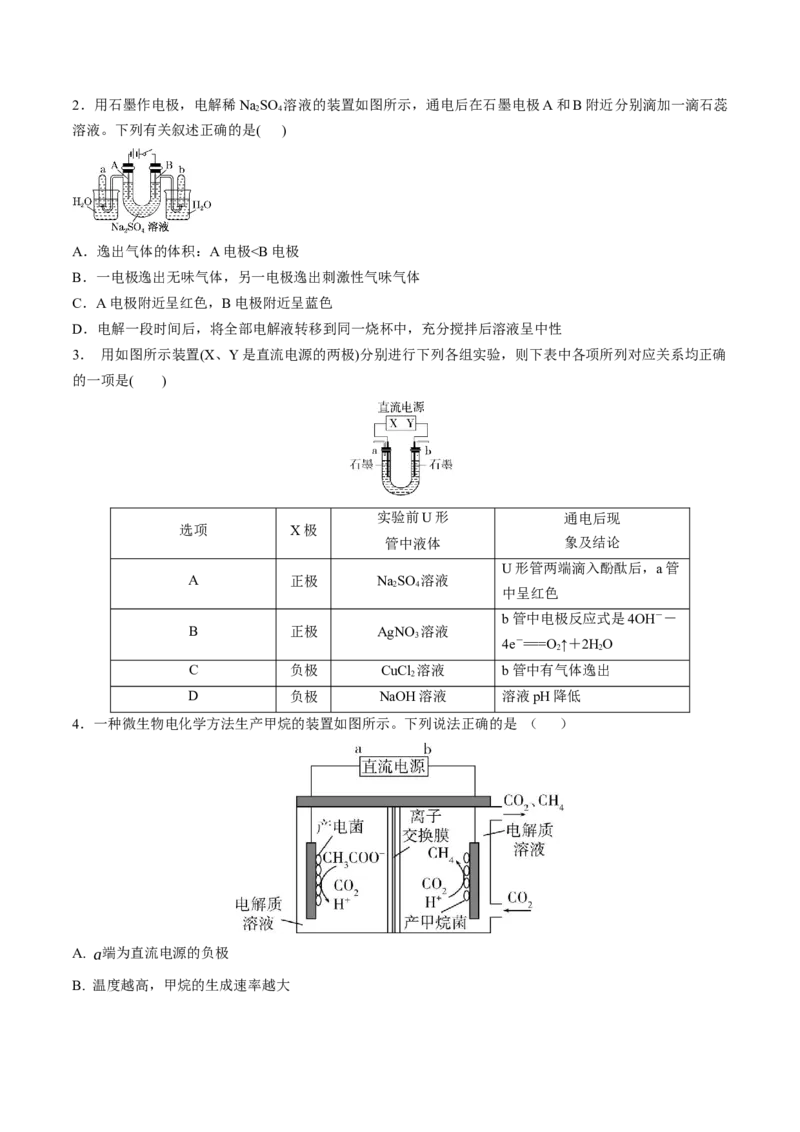
22.用石墨作电极,电解稀NaSO 溶液的装置如图所示,通电后在石墨电极A和B附近分别滴加一滴石蕊
2 4
溶液。下列有关叙述正确的是( )
A.逸出气体的体积:A电极a>b
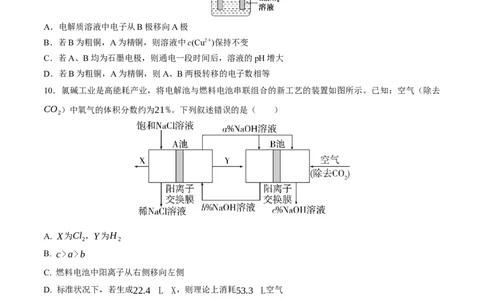
C. 燃料电池中阳离子从右侧移向左侧
D. 标准状况下,若生成22.4 L X,则理论上消耗53.3 L空气
考法03 金属的腐蚀与防护
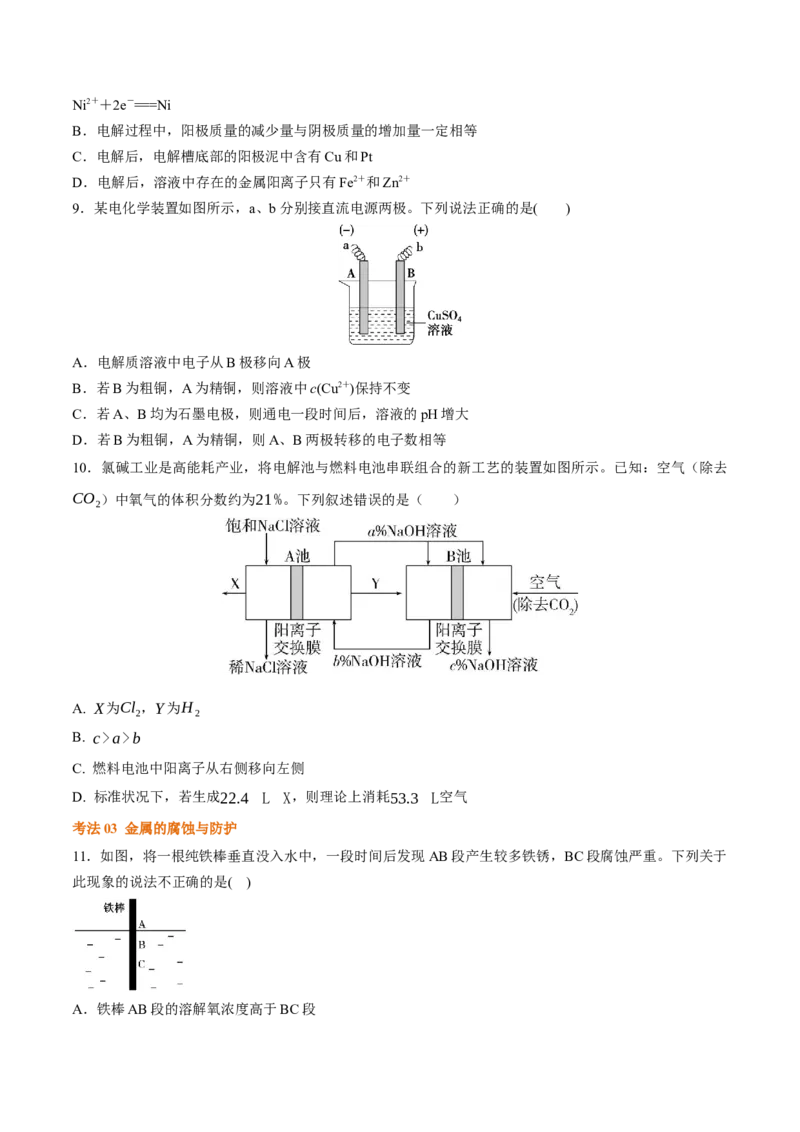
11.如图,将一根纯铁棒垂直没入水中,一段时间后发现AB段产生较多铁锈,BC段腐蚀严重。下列关于
此现象的说法不正确的是( )
A.铁棒AB段的溶解氧浓度高于BC段B.铁棒AB段电极反应为O+2HO+4e-===4OH-
2 2
C.铁棒AB段的Fe2+浓度高于BC段
D.该腐蚀过程属于电化学腐蚀
12.我国多条高压直流电线路的瓷绝缘子出现铁帽腐蚀现象,在铁帽上加锌环能有效防止铁帽的腐蚀,防
护原理如图所示。
下列说法错误的是( )
A.通电时,锌环是阳极,发生氧化反应
B.通电时,阴极上的电极反应为2HO+2e-===H ↑+2OH-
2 2
C.断电时,锌环上的电极反应为Zn+2e-===Zn2+
D.断电时,仍能防止铁帽被腐蚀
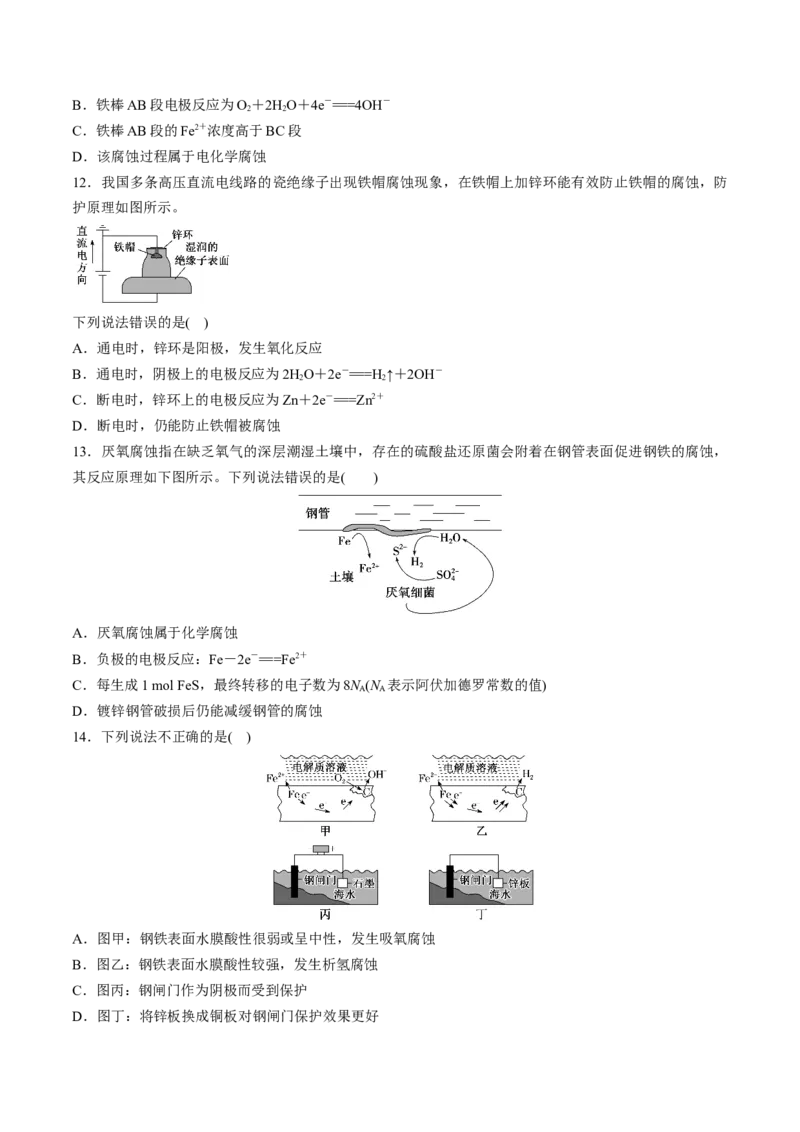
13.厌氧腐蚀指在缺乏氧气的深层潮湿土壤中,存在的硫酸盐还原菌会附着在钢管表面促进钢铁的腐蚀,
其反应原理如下图所示。下列说法错误的是( )
A.厌氧腐蚀属于化学腐蚀
B.负极的电极反应:Fe-2e-===Fe2+
C.每生成1 mol FeS,最终转移的电子数为8N (N 表示阿伏加德罗常数的值)
A A
D.镀锌钢管破损后仍能减缓钢管的腐蚀
14.下列说法不正确的是( )
A.图甲:钢铁表面水膜酸性很弱或呈中性,发生吸氧腐蚀
B.图乙:钢铁表面水膜酸性较强,发生析氢腐蚀
C.图丙:钢闸门作为阴极而受到保护
D.图丁:将锌板换成铜板对钢闸门保护效果更好15.(2024·辽宁六校联考)将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图所示装置中,进行铁的
电化学腐蚀实验。下列有关该实验的说法正确的是( )
A.铁被氧化的电极反应式为Fe-3e-===Fe3+
B.铁腐蚀过程中化学能全部转化为电能
C.活性炭的存在会加速铁的腐蚀
D.以水代替NaCl溶液,铁不能发生吸氧腐蚀
考点04 电化学原理的综合应用
考法01 电解原理在物质制备中的应用
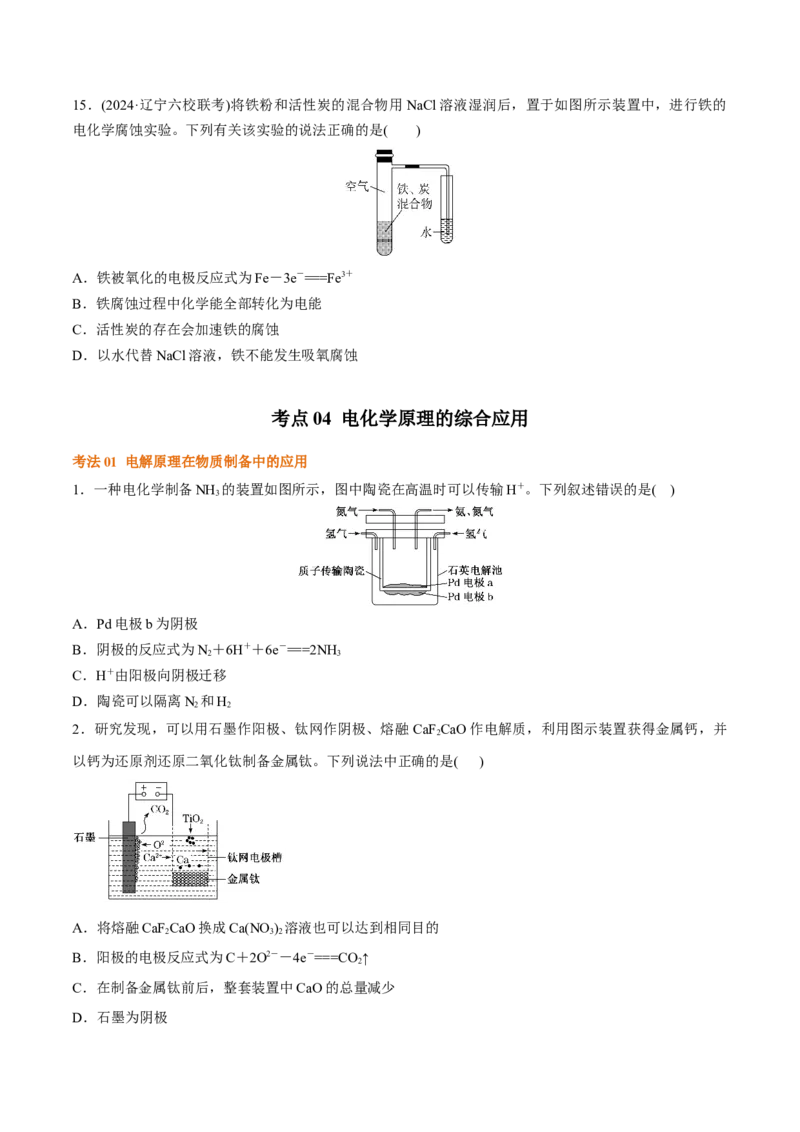
1.一种电化学制备NH 的装置如图所示,图中陶瓷在高温时可以传输H+。下列叙述错误的是( )
3
A.Pd电极b为阴极
B.阴极的反应式为N+6H++6e-===2NH
2 3
C.H+由阳极向阴极迁移
D.陶瓷可以隔离N 和H
2 2
2.研究发现,可以用石墨作阳极、钛网作阴极、熔融 CaF CaO作电解质,利用图示装置获得金属钙,并
2
以钙为还原剂还原二氧化钛制备金属钛。下列说法中正确的是( )
A.将熔融CaF CaO换成Ca(NO ) 溶液也可以达到相同目的
2 3 2
B.阳极的电极反应式为C+2O2--4e-===CO ↑
2
C.在制备金属钛前后,整套装置中CaO的总量减少
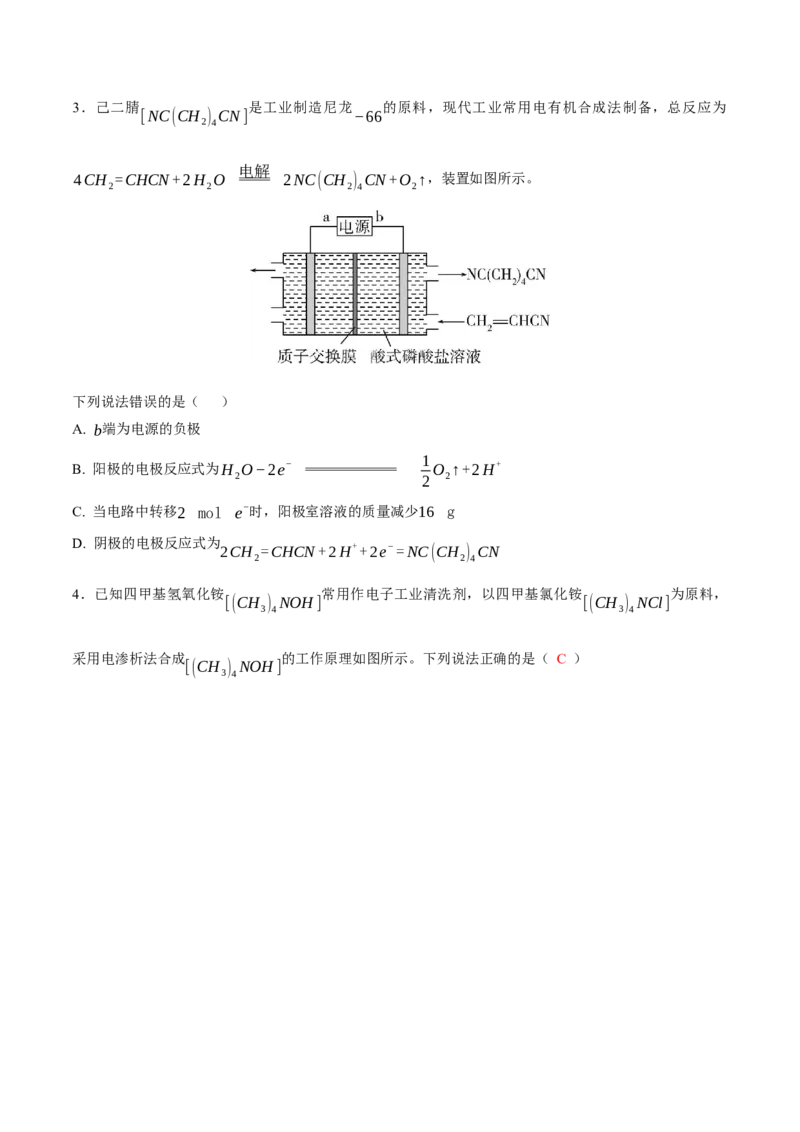
D.石墨为阴极3.己二腈 是工业制造尼龙 的原料,现代工业常用电有机合成法制备,总反应为
[NC(CH ) CN] −66
2 4
电解
4CH =CHCN+2H O 2NC(CH ) CN+O ↑,装置如图所示。
2 2 2 4 2
下列说法错误的是( )
A. b端为电源的负极
1
B. 阳极的电极反应式为H O−2e− O ↑+2H+
2 2 2
C. 当电路中转移2 mol e−时,阳极室溶液的质量减少16 g
D. 阴极的电极反应式为 2CH =CHCN+2H++2e−=NC(CH ) CN
2 2 4
4.已知四甲基氢氧化铵 常用作电子工业清洗剂,以四甲基氯化铵 为原料,
[(CH ) NOH] [(CH ) NCl]
3 4 3 4
采用电渗析法合成 的工作原理如图所示。下列说法正确的是( C )
[(CH ) NOH]
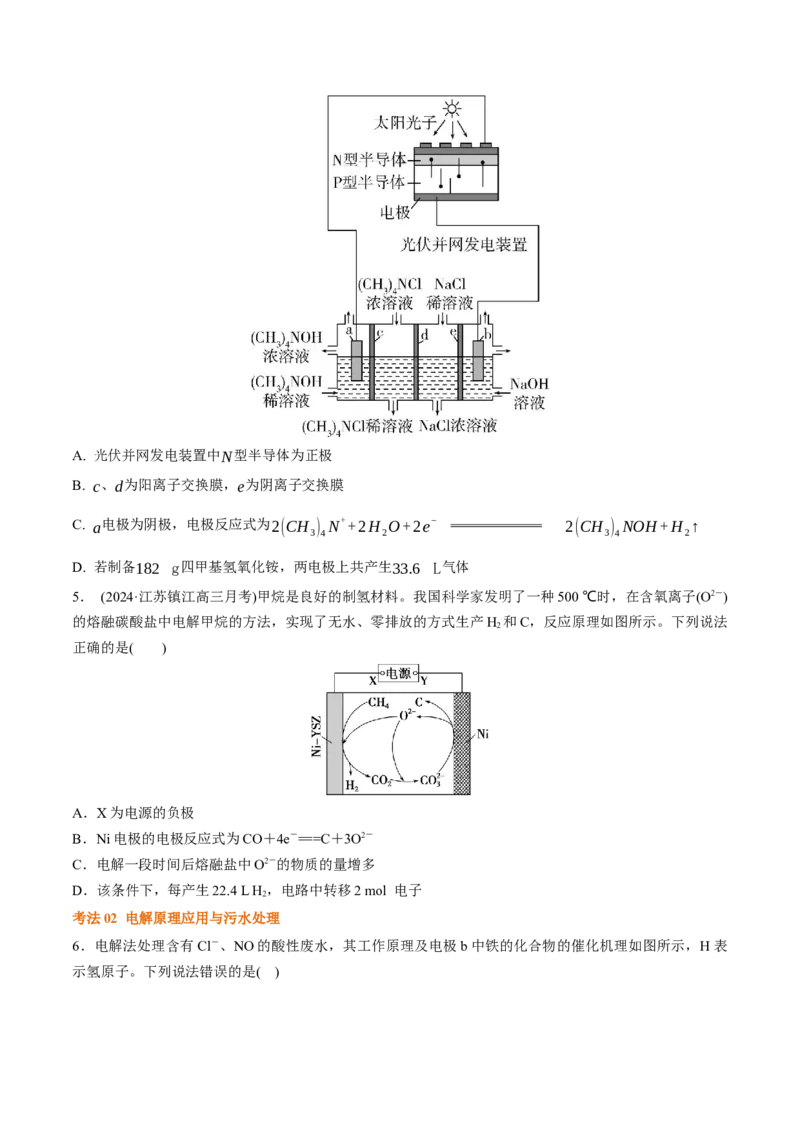
3 4A. 光伏并网发电装置中N型半导体为正极
B. c、d为阳离子交换膜,e为阴离子交换膜
C. a电极为阴极,电极反应式为2(CH ) N++2H O+2e− 2(CH ) NOH+H ↑
3 4 2 3 4 2
D. 若制备182 g四甲基氢氧化铵,两电极上共产生33.6 L气体
5. (2024·江苏镇江高三月考)甲烷是良好的制氢材料。我国科学家发明了一种500 ℃时,在含氧离子(O2-)
的熔融碳酸盐中电解甲烷的方法,实现了无水、零排放的方式生产H 和C,反应原理如图所示。下列说法
2
正确的是( )
A.X为电源的负极
B.Ni电极的电极反应式为CO+4e-===C+3O2-
C.电解一段时间后熔融盐中O2-的物质的量增多
D.该条件下,每产生22.4 L H ,电路中转移2 mol 电子
2
考法02 电解原理应用与污水处理
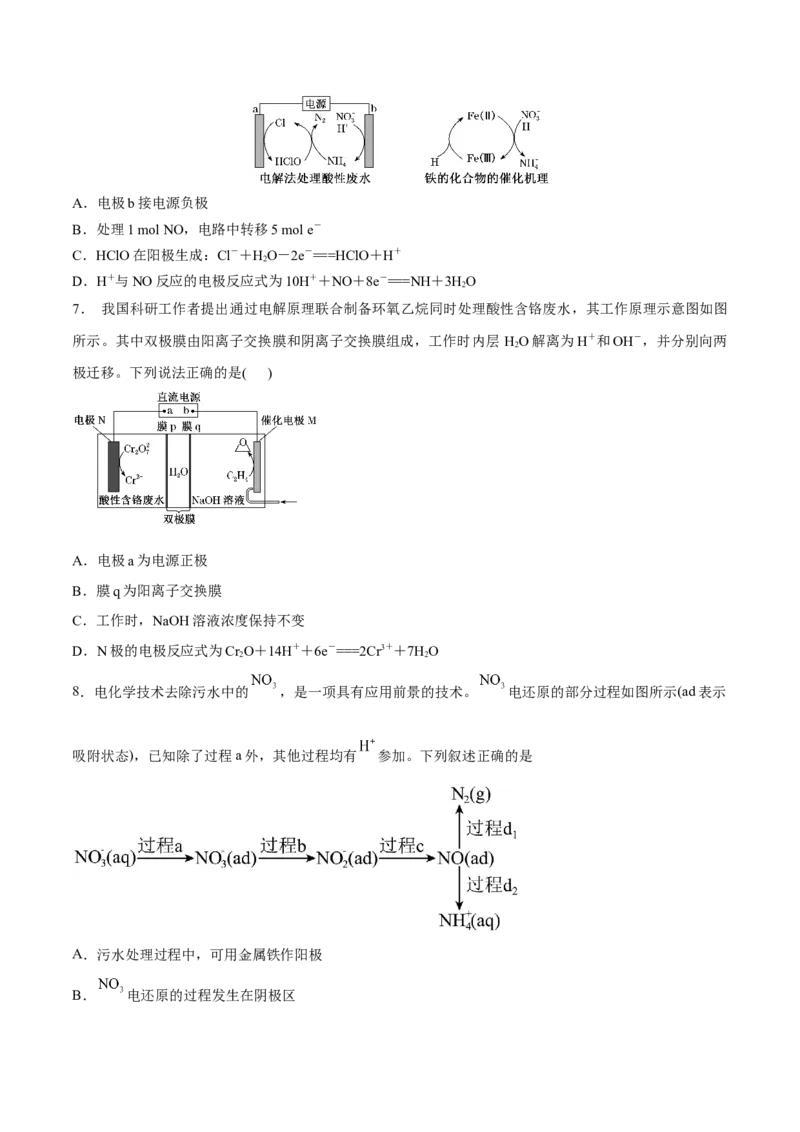
6.电解法处理含有Cl-、NO的酸性废水,其工作原理及电极b中铁的化合物的催化机理如图所示,H表
示氢原子。下列说法错误的是( )A.电极b接电源负极
B.处理1 mol NO,电路中转移5 mol e-
C.HClO在阳极生成:Cl-+HO-2e-===HClO+H+
2
D.H+与NO反应的电极反应式为10H++NO+8e-===NH+3HO
2
7. 我国科研工作者提出通过电解原理联合制备环氧乙烷同时处理酸性含铬废水,其工作原理示意图如图
所示。其中双极膜由阳离子交换膜和阴离子交换膜组成,工作时内层 HO解离为H+和OH-,并分别向两
2
极迁移。下列说法正确的是( )
A.电极a为电源正极
B.膜q为阳离子交换膜
C.工作时,NaOH溶液浓度保持不变
D.N极的电极反应式为Cr O+14H++6e-===2Cr3++7HO
2 2
8.电化学技术去除污水中的 ,是一项具有应用前景的技术。 电还原的部分过程如图所示(ad表示
吸附状态),已知除了过程a外,其他过程均有 参加。下列叙述正确的是
A.污水处理过程中,可用金属铁作阳极
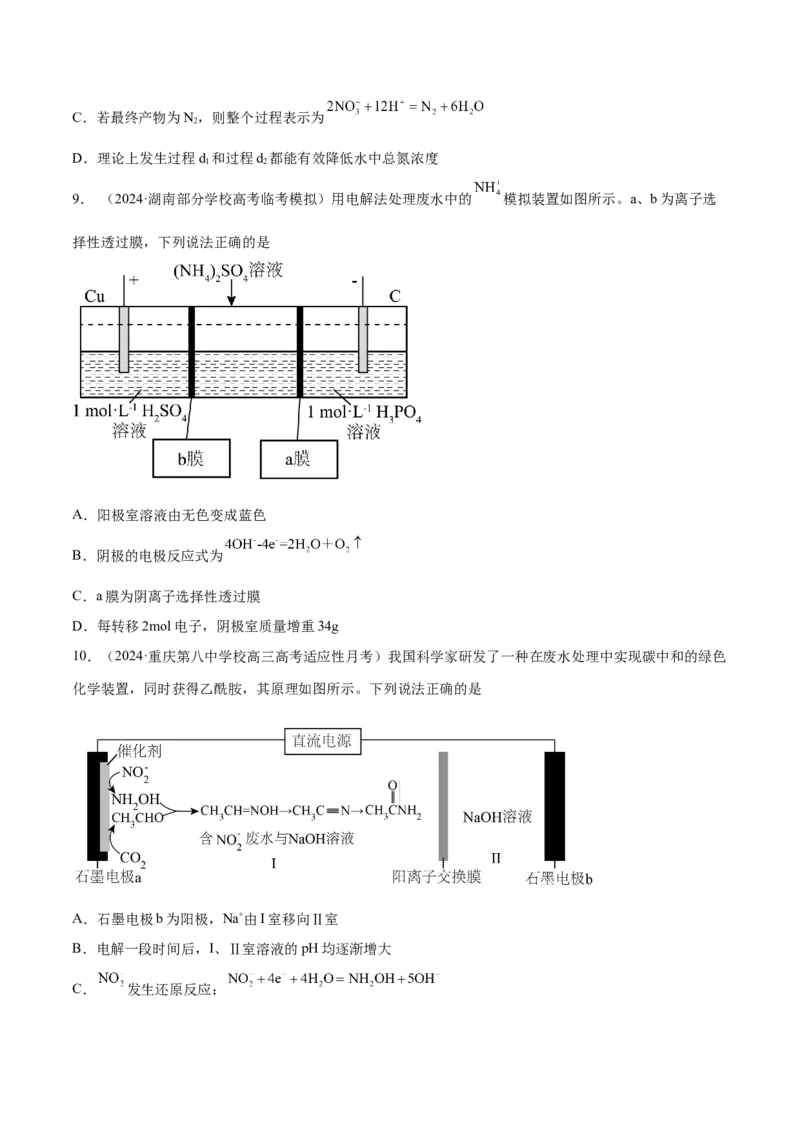
B. 电还原的过程发生在阴极区C.若最终产物为N,则整个过程表示为
2
D.理论上发生过程d 和过程d 都能有效降低水中总氮浓度
1 2
9. (2024·湖南部分学校高考临考模拟)用电解法处理废水中的 模拟装置如图所示。a、b为离子选
择性透过膜,下列说法正确的是
A.阳极室溶液由无色变成蓝色
B.阴极的电极反应式为
C.a膜为阴离子选择性透过膜
D.每转移2mol电子,阴极室质量增重34g
10.(2024·重庆第八中学校高三高考适应性月考)我国科学家研发了一种在废水处理中实现碳中和的绿色
化学装置,同时获得乙酰胺,其原理如图所示。下列说法正确的是
A.石墨电极b为阳极,Na+由I室移向Ⅱ室
B.电解一段时间后,I、Ⅱ室溶液的pH均逐渐增大
C. 发生还原反应:D.理论上,每产生0.1mol乙酰胺的同时电极b至少有15.68L(标况)O 生成
2
考法03 电解原理在大气治理方面的应用
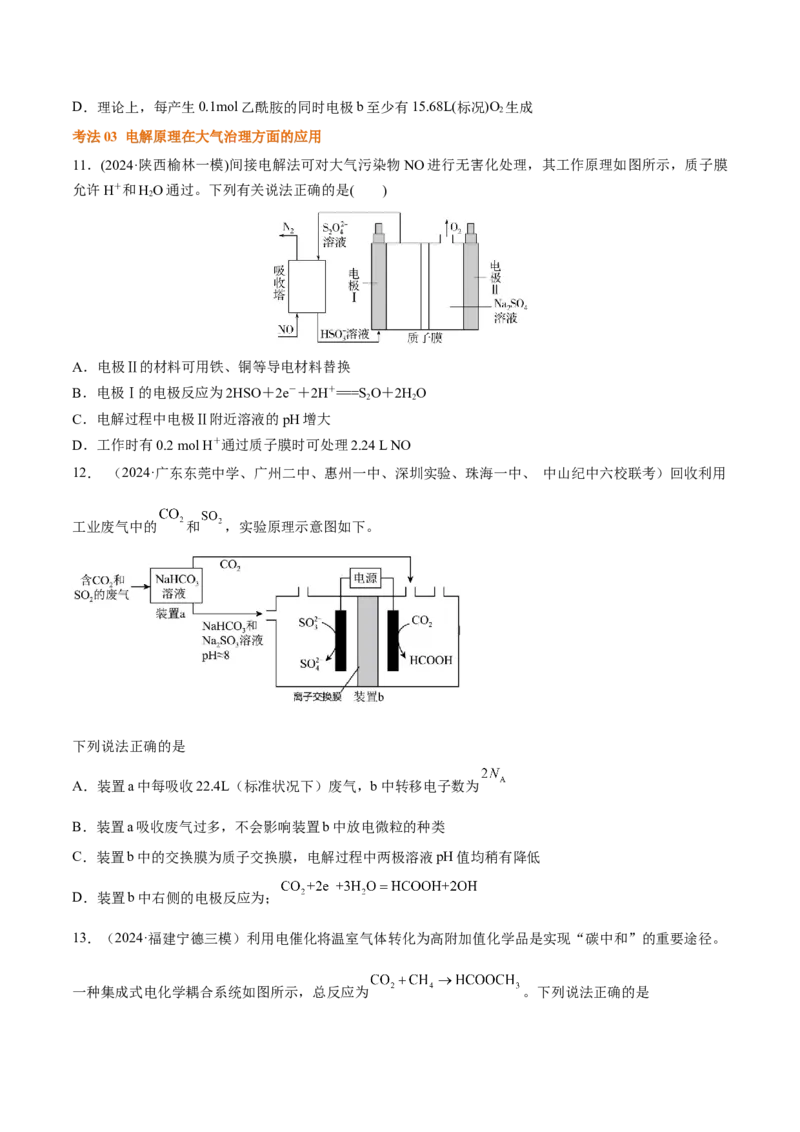
11.(2024·陕西榆林一模)间接电解法可对大气污染物NO进行无害化处理,其工作原理如图所示,质子膜
允许H+和HO通过。下列有关说法正确的是( )
2
A.电极Ⅱ的材料可用铁、铜等导电材料替换
B.电极Ⅰ的电极反应为2HSO+2e-+2H+===S O+2HO
2 2
C.电解过程中电极Ⅱ附近溶液的pH增大
D.工作时有0.2 mol H+通过质子膜时可处理2.24 L NO
12. (2024·广东东莞中学、广州二中、惠州一中、深圳实验、珠海一中、 中山纪中六校联考)回收利用
工业废气中的 和 ,实验原理示意图如下。
下列说法正确的是
A.装置a中每吸收22.4L(标准状况下)废气,b中转移电子数为
B.装置a吸收废气过多,不会影响装置b中放电微粒的种类
C.装置b中的交换膜为质子交换膜,电解过程中两极溶液pH值均稍有降低
D.装置b中右侧的电极反应为;
13.(2024·福建宁德三模)利用电催化将温室气体转化为高附加值化学品是实现“碳中和”的重要途径。
一种集成式电化学耦合系统如图所示,总反应为 。下列说法正确的是A. 接直流电源负极
B.产物中可能有
C. 为阳离子交换膜
D.右室的电极反应式为:
14.(2024·广东江门第一中学高三月考)以丙烯腈( )为原料,利用电解原理合成己二腈[
],可减少氮氧化物的排放,其总反应为: 电解
过程会产生丙腈( )等副产物(已知: )。下列说法正
确的是
A.电子的流向为电源b极→Pb电极→电解质溶液 电极→电源a极
B.Pb电极主要发生的电极反应式为:
C.工作一段时间后, 电极附近pH增大
D.若 电极产生33.6L(标准状况)气体,Pb电极区生成了2.5mol己二腈[ ],则电
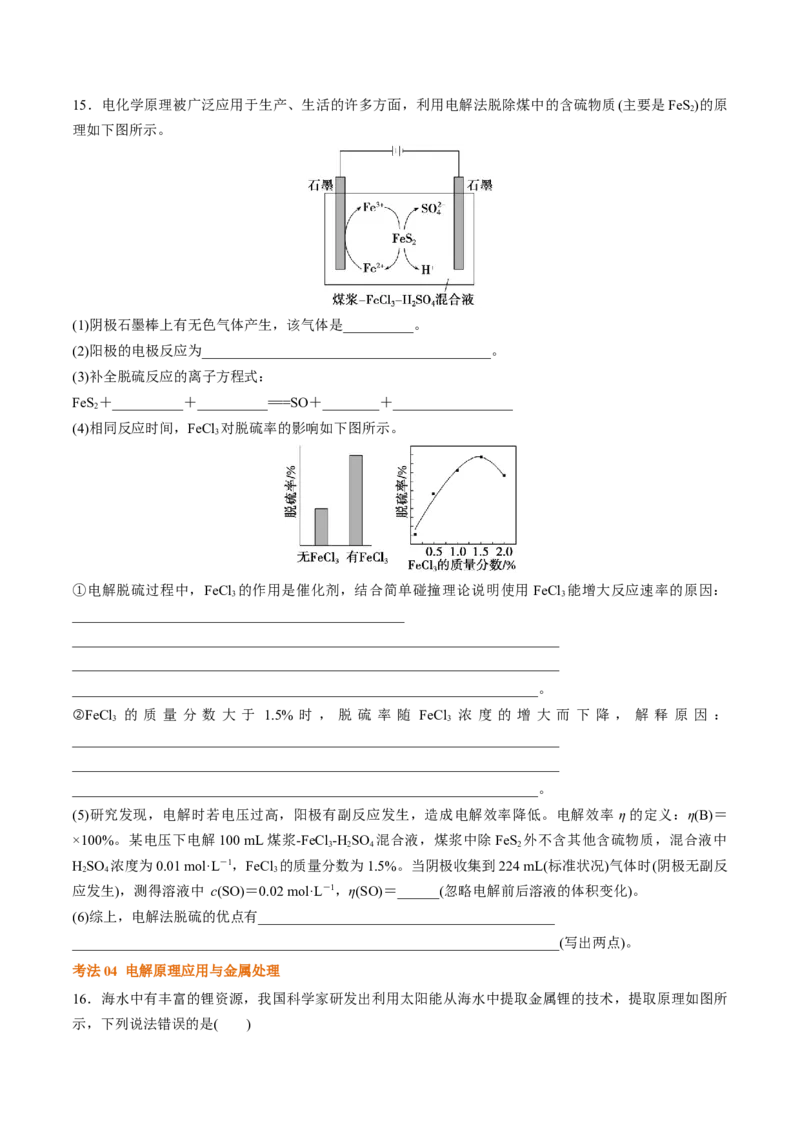
流效率高于90%15.电化学原理被广泛应用于生产、生活的许多方面,利用电解法脱除煤中的含硫物质(主要是FeS)的原
2
理如下图所示。
(1)阴极石墨棒上有无色气体产生,该气体是__________。
(2)阳极的电极反应为_________________________________________。
(3)补全脱硫反应的离子方程式:
FeS+__________+__________===SO+________+_________________
2
(4)相同反应时间,FeCl 对脱硫率的影响如下图所示。
3
①电解脱硫过程中,FeCl 的作用是催化剂,结合简单碰撞理论说明使用 FeCl 能增大反应速率的原因:
3 3
_______________________________________________
_____________________________________________________________________
_____________________________________________________________________
__________________________________________________________________。
②FeCl 的 质 量 分 数 大 于 1.5% 时 , 脱 硫 率 随 FeCl 浓 度 的 增 大 而 下 降 , 解 释 原 因 :
3 3
_____________________________________________________________________
_____________________________________________________________________
__________________________________________________________________。
(5)研究发现,电解时若电压过高,阳极有副反应发生,造成电解效率降低。电解效率 η的定义:η(B)=
×100%。某电压下电解100 mL煤浆-FeCl -H SO 混合液,煤浆中除FeS 外不含其他含硫物质,混合液中
3 2 4 2
HSO 浓度为0.01 mol·L-1,FeCl 的质量分数为1.5%。当阴极收集到224 mL(标准状况)气体时(阴极无副反
2 4 3
应发生),测得溶液中 c(SO)=0.02 mol·L-1,η(SO)=______(忽略电解前后溶液的体积变化)。
(6)综上,电解法脱硫的优点有__________________________________________
_____________________________________________________________________(写出两点)。
考法04 电解原理应用与金属处理
16.海水中有丰富的锂资源,我国科学家研发出利用太阳能从海水中提取金属锂的技术,提取原理如图所
示,下列说法错误的是( )A.该装置将光能间接转化为化学能
B.a极为阴极,电极上发生还原反应
C.电解过程中可监测到b极附近溶液的pH减小
D.固体陶瓷膜允许Li+、HO等较小微粒通过
2
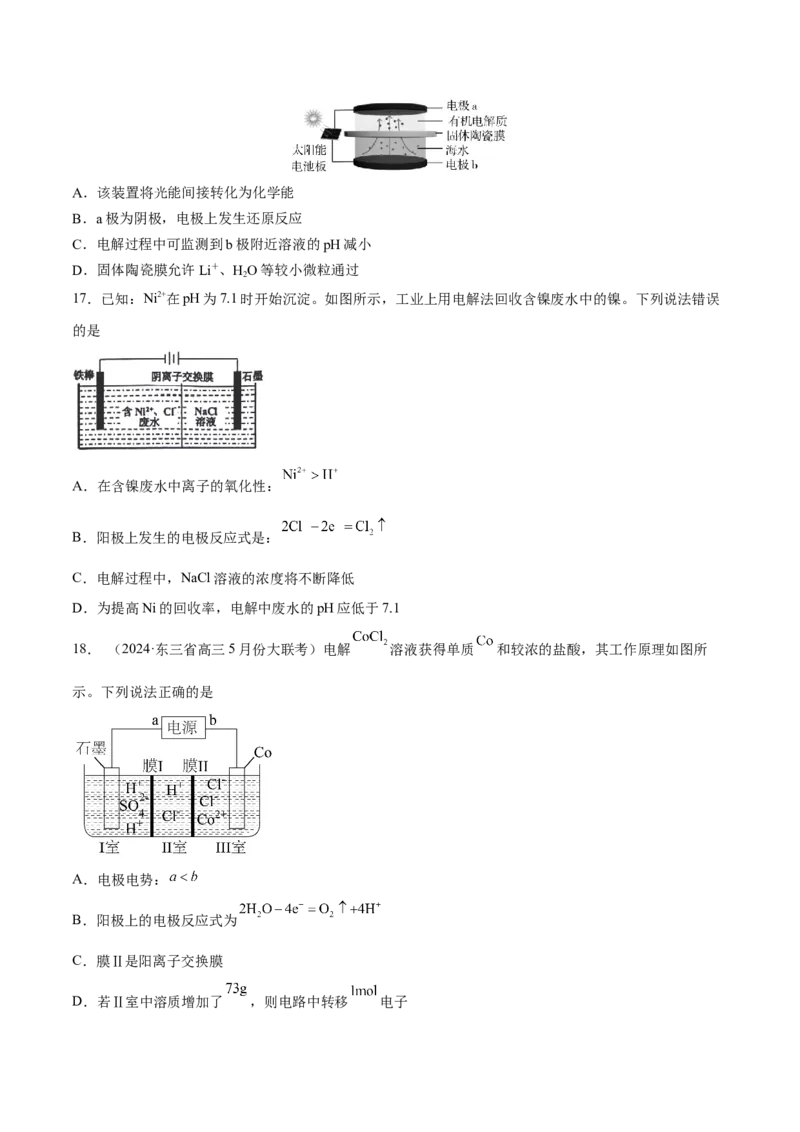
17.已知:Ni2+在pH为7.1时开始沉淀。如图所示,工业上用电解法回收含镍废水中的镍。下列说法错误
的是
A.在含镍废水中离子的氧化性:
B.阳极上发生的电极反应式是:
C.电解过程中,NaCl溶液的浓度将不断降低
D.为提高Ni的回收率,电解中废水的pH应低于7.1
18. (2024·东三省高三5月份大联考)电解 溶液获得单质 和较浓的盐酸,其工作原理如图所
示。下列说法正确的是
A.电极电势:
B.阳极上的电极反应式为
C.膜Ⅱ是阳离子交换膜
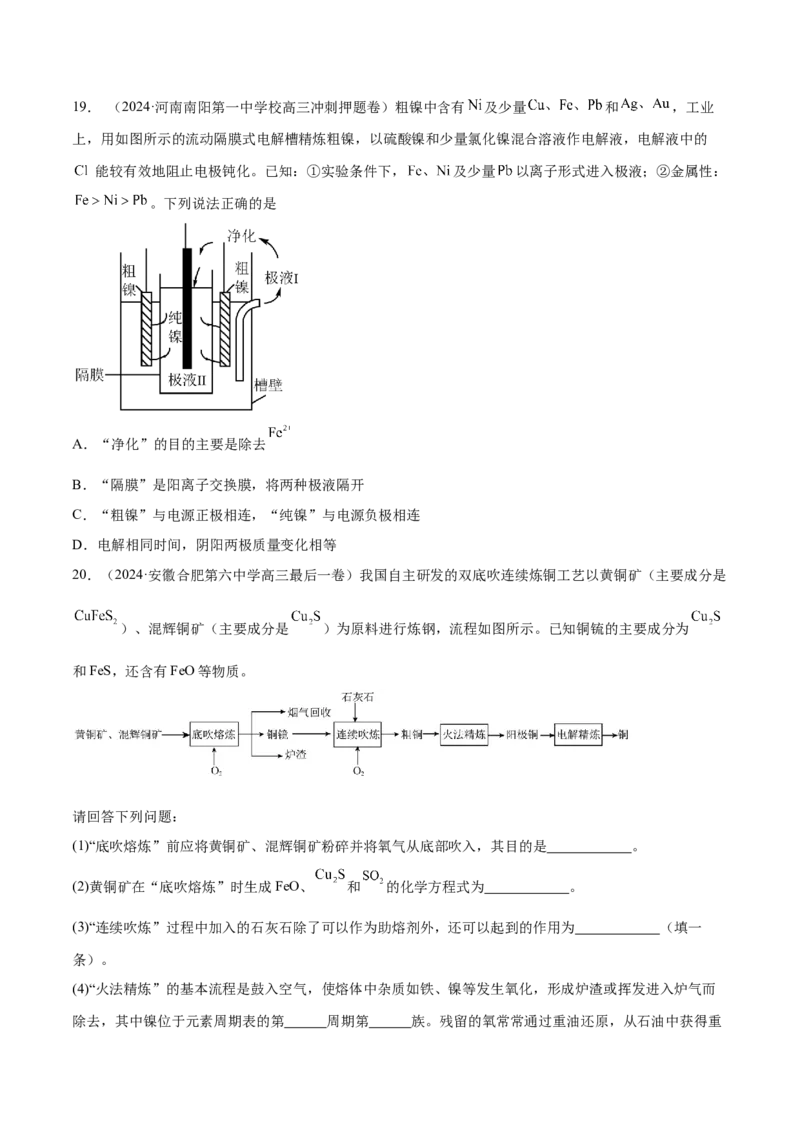
D.若Ⅱ室中溶质增加了 ,则电路中转移 电子19. (2024·河南南阳第一中学校高三冲刺押题卷)粗镍中含有 及少量 和 ,工业
上,用如图所示的流动隔膜式电解槽精炼粗镍,以硫酸镍和少量氯化镍混合溶液作电解液,电解液中的
能较有效地阻止电极钝化。已知:①实验条件下, 及少量 以离子形式进入极液;②金属性:
。下列说法正确的是
A.“净化”的目的主要是除去
B.“隔膜”是阳离子交换膜,将两种极液隔开
C.“粗镍”与电源正极相连,“纯镍”与电源负极相连
D.电解相同时间,阴阳两极质量变化相等
20.(2024·安徽合肥第六中学高三最后一卷)我国自主研发的双底吹连续炼铜工艺以黄铜矿(主要成分是
)、混辉铜矿(主要成分是 )为原料进行炼钢,流程如图所示。已知铜锍的主要成分为
和FeS,还含有FeO等物质。
请回答下列问题:
(1)“底吹熔炼”前应将黄铜矿、混辉铜矿粉碎并将氧气从底部吹入,其目的是 。
(2)黄铜矿在“底吹熔炼”时生成FeO、 和 的化学方程式为 。
(3)“连续吹炼”过程中加入的石灰石除了可以作为助熔剂外,还可以起到的作用为 (填一
条)。
(4)“火法精炼”的基本流程是鼓入空气,使熔体中杂质如铁、镍等发生氧化,形成炉渣或挥发进入炉气而
除去,其中镍位于元素周期表的第 周期第 族。残留的氧常常通过重油还原,从石油中获得重油的分离方法的名称为 。
(5)“电解精炼”铜时阴极的电极反应式为 ;若采用硫酸酸化的硫酸铜溶液作电解质溶液.电解过程
中 向 极移动(填“阴”或“阳”)。
(6)某次生产时原料黄铜矿、混辉铜矿的总质量为3.2吨(其中Cu元素的含量为20.14%),“电解精炼”
全过程转移的电子数为 ,本次生产中铜的产率为 (结果保留两位小数)。
考点05 多池、多室的电化学装置
考法01 多池串联的两大模型
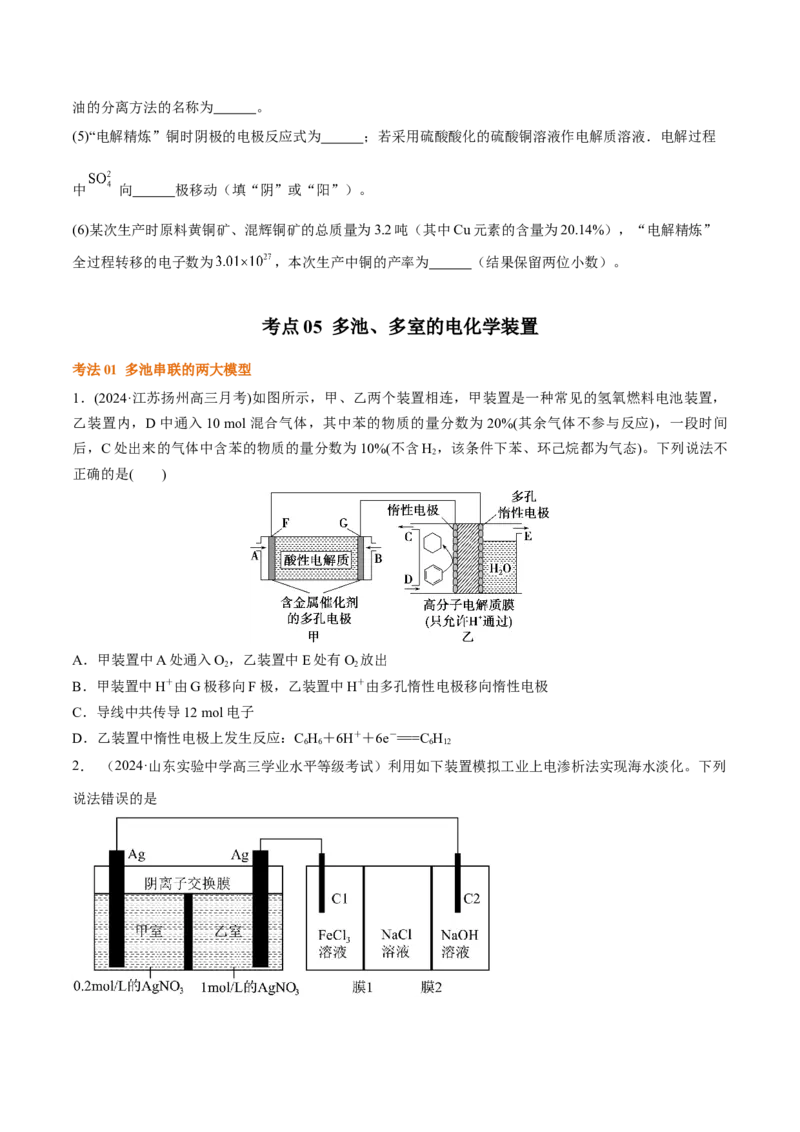
1.(2024·江苏扬州高三月考)如图所示,甲、乙两个装置相连,甲装置是一种常见的氢氧燃料电池装置,
乙装置内,D中通入10 mol混合气体,其中苯的物质的量分数为20%(其余气体不参与反应),一段时间
后,C处出来的气体中含苯的物质的量分数为10%(不含H ,该条件下苯、环己烷都为气态)。下列说法不
2
正确的是( )
A.甲装置中A处通入O,乙装置中E处有O 放出
2 2
B.甲装置中H+由G极移向F极,乙装置中H+由多孔惰性电极移向惰性电极
C.导线中共传导12 mol电子
D.乙装置中惰性电极上发生反应:C H+6H++6e-===C H
6 6 6 12
2. (2024·山东实验中学高三学业水平等级考试)利用如下装置模拟工业上电渗析法实现海水淡化。下列
说法错误的是A.乙室的Ag电极电势高于甲室
B.Cl电极的反应为
C.膜1为阳离子交换膜、膜2为阴离子交换膜
D.当乙室Ag电极的质量增加 时,理论上NaCl溶液减少
3. 利用浓差电池制备高铁电池的重要材料NaFeO,反应原理如图所示。下列说法错误的是( )
2 4
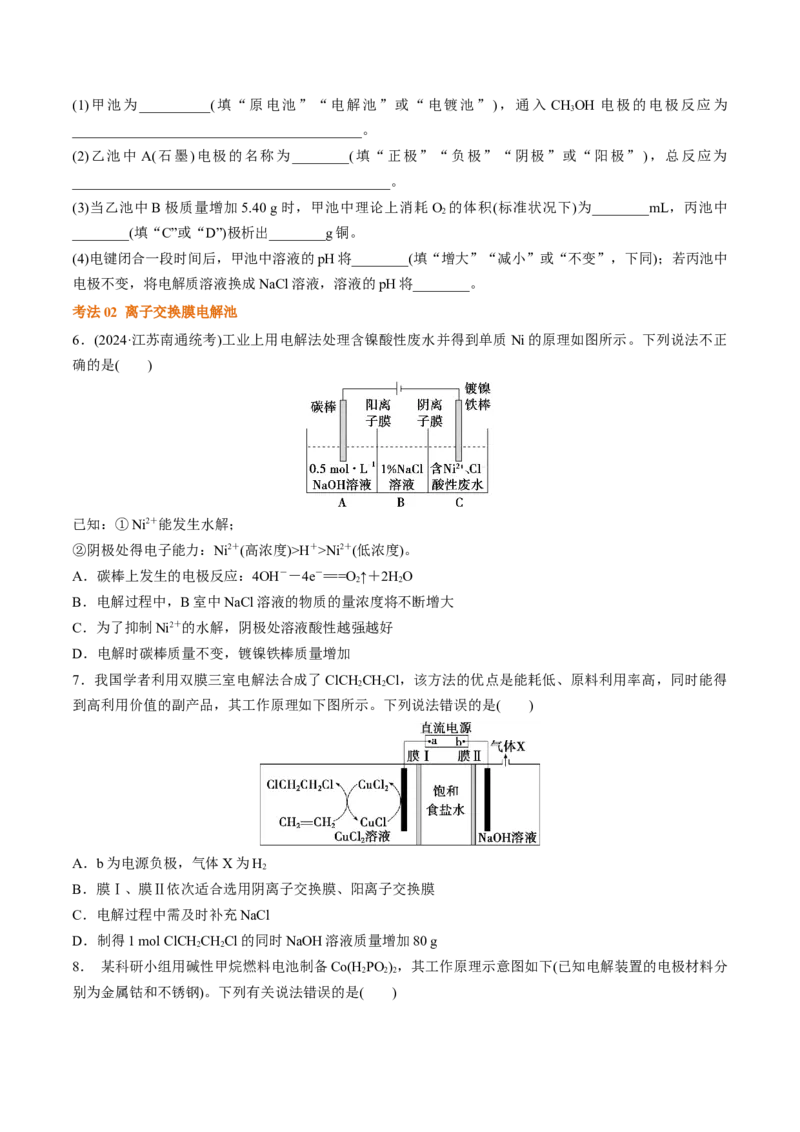
A.aH+>Ni2+(低浓度)。
A.碳棒上发生的电极反应:4OH--4e-===O ↑+2HO
2 2
B.电解过程中,B室中NaCl溶液的物质的量浓度将不断增大
C.为了抑制Ni2+的水解,阴极处溶液酸性越强越好
D.电解时碳棒质量不变,镀镍铁棒质量增加
7.我国学者利用双膜三室电解法合成了ClCH CHCl,该方法的优点是能耗低、原料利用率高,同时能得
2 2
到高利用价值的副产品,其工作原理如下图所示。下列说法错误的是( )
A.b为电源负极,气体X为H
2
B.膜Ⅰ、膜Ⅱ依次适合选用阴离子交换膜、阳离子交换膜
C.电解过程中需及时补充NaCl
D.制得1 mol ClCHCHCl的同时NaOH溶液质量增加80 g
2 2
8. 某科研小组用碱性甲烷燃料电池制备Co(HPO ) ,其工作原理示意图如下(已知电解装置的电极材料分
2 2 2
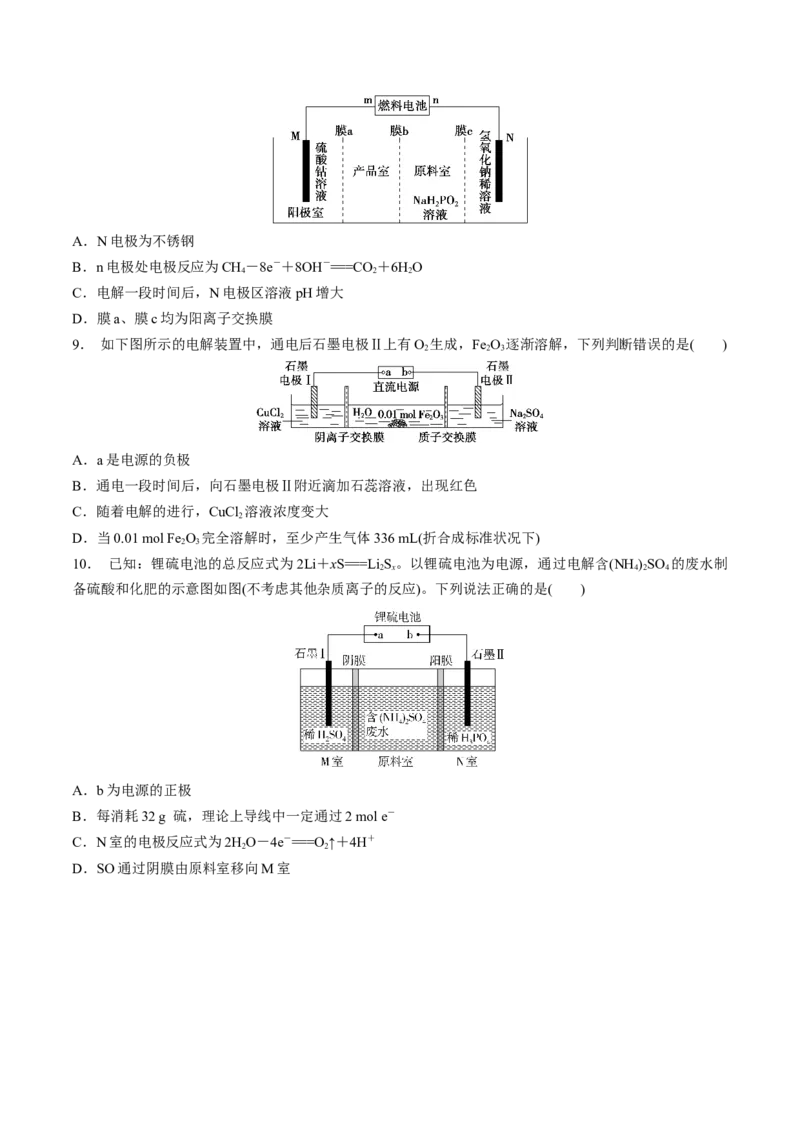
别为金属钴和不锈钢)。下列有关说法错误的是( )A.N电极为不锈钢
B.n电极处电极反应为CH-8e-+8OH-===CO +6HO
4 2 2
C.电解一段时间后,N电极区溶液pH增大
D.膜a、膜c均为阳离子交换膜
9. 如下图所示的电解装置中,通电后石墨电极Ⅱ上有O 生成,Fe O 逐渐溶解,下列判断错误的是( )
2 2 3
A.a是电源的负极
B.通电一段时间后,向石墨电极Ⅱ附近滴加石蕊溶液,出现红色
C.随着电解的进行,CuCl 溶液浓度变大
2
D.当0.01 mol Fe O 完全溶解时,至少产生气体336 mL(折合成标准状况下)
2 3
10. 已知:锂硫电池的总反应式为2Li+xS===Li S。以锂硫电池为电源,通过电解含(NH )SO 的废水制
2 x 4 2 4
备硫酸和化肥的示意图如图(不考虑其他杂质离子的反应)。下列说法正确的是( )
A.b为电源的正极
B.每消耗32 g 硫,理论上导线中一定通过2 mol e-
C.N室的电极反应式为2HO-4e-===O ↑+4H+
2 2
D.SO通过阴膜由原料室移向M室