文档内容
解密 06 化学反应与热能
考点热度 ★★★★★
【考纲导向】
1.了解化学能与热能的相互转化。了解吸热反应、放热反应、反应热等概念。
2.了解热化学方程式的含义,能正确书写热化学方程式。
3.了解焓变(ΔH)的含义。
4.理解盖斯定律,并能运用盖斯定律进行有关反应焓变的简单计算。
5.了解能源是人类生存和社会发展的重要基础。了解化学在解决能源危机中的重要作用。
【命题分析】
高考对本专题的考查点主要是运用盖斯定律进行ΔH的计算,而且考查频率较高;利用键能进行ΔH的计
算及化学反应中的能量变化的有关知识同样会涉及。预计2023年高考对本专题的考查仍会以综合题中的某
一设问为主,也不排除以选择题的形式对盖斯定律的应用及 ΔH的大小比较进行考查。
核心考点一 化学反应与能量变化图象
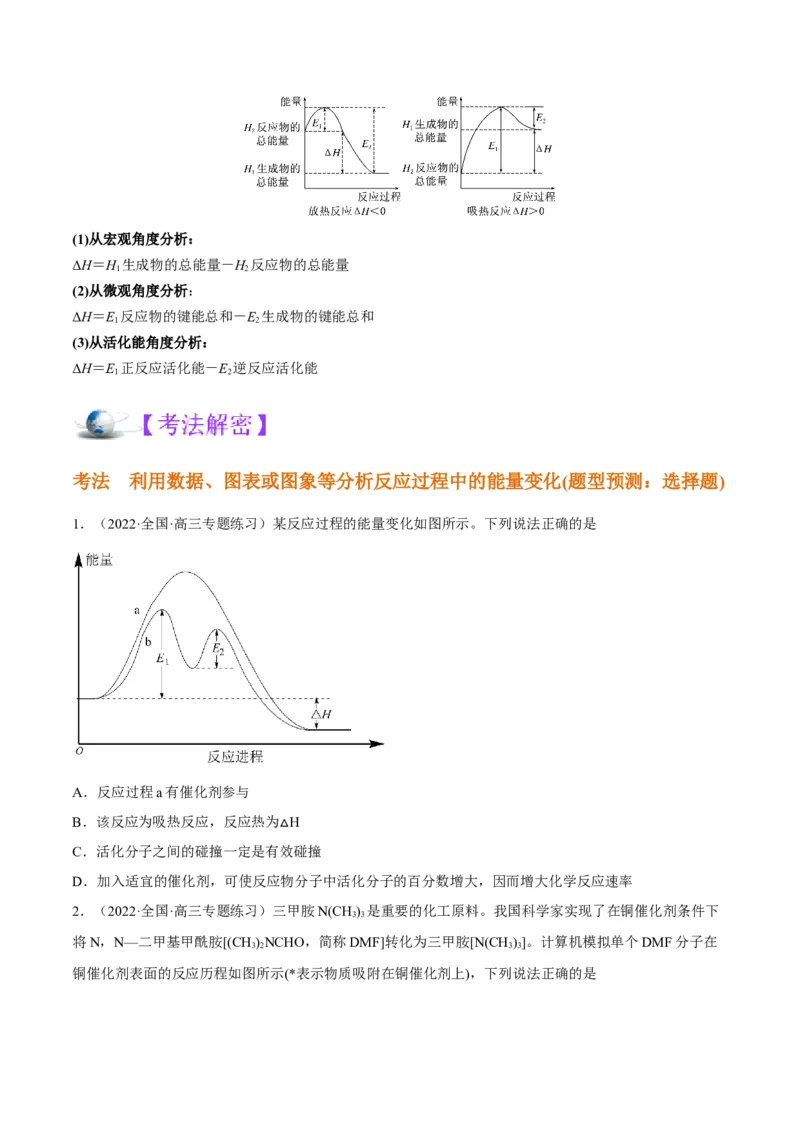
1.产生化学反应热效应的原因(1)从宏观角度分析:
ΔH=H 生成物的总能量-H 反应物的总能量
1 2
(2)从微观角度分析:
ΔH=E 反应物的键能总和-E 生成物的键能总和
1 2
(3)从活化能角度分析:
ΔH=E 正反应活化能-E 逆反应活化能
1 2
考法 利用数据、图表或图象等分析反应过程中的能量变化(题型预测:选择题)
1.(2022·全国·高三专题练习)某反应过程的能量变化如图所示。下列说法正确的是
A.反应过程a有催化剂参与
B.该反应为吸热反应,反应热为 H
C.活化分子之间的碰撞一定是有△效碰撞
D.加入适宜的催化剂,可使反应物分子中活化分子的百分数增大,因而增大化学反应速率
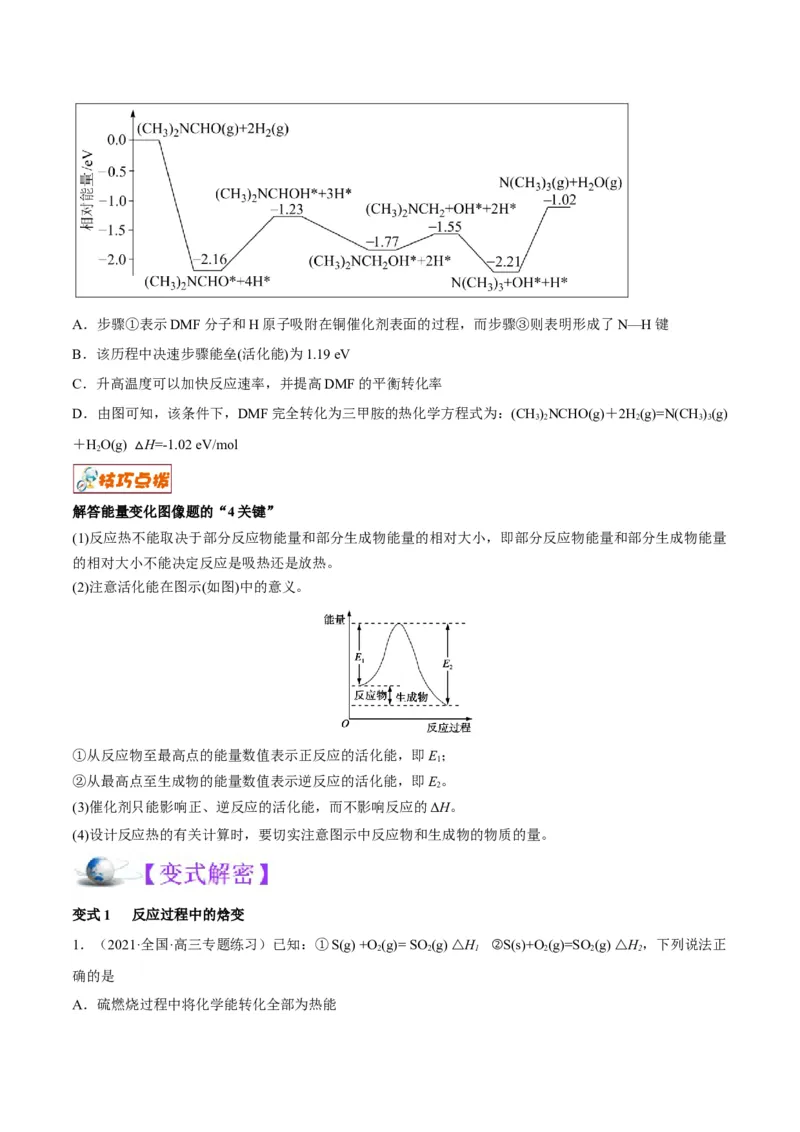
2.(2022·全国·高三专题练习)三甲胺N(CH ) 是重要的化工原料。我国科学家实现了在铜催化剂条件下
3 3
将N,N—二甲基甲酰胺[(CH )NCHO,简称DMF]转化为三甲胺[N(CH )]。计算机模拟单个DMF分子在
3 2 3 3
铜催化剂表面的反应历程如图所示(*表示物质吸附在铜催化剂上),下列说法正确的是A.步骤①表示DMF分子和H原子吸附在铜催化剂表面的过程,而步骤③则表明形成了N—H键
B.该历程中决速步骤能垒(活化能)为1.19 eV
C.升高温度可以加快反应速率,并提高DMF的平衡转化率
D.由图可知,该条件下,DMF完全转化为三甲胺的热化学方程式为:(CH)NCHO(g)+2H(g)=N(CH )(g)
3 2 2 3 3
+HO(g) H=-1.02 eV/mol
2
△
解答能量变化图像题的“4关键”
(1)反应热不能取决于部分反应物能量和部分生成物能量的相对大小,即部分反应物能量和部分生成物能量
的相对大小不能决定反应是吸热还是放热。
(2)注意活化能在图示(如图)中的意义。
①从反应物至最高点的能量数值表示正反应的活化能,即E;
1
②从最高点至生成物的能量数值表示逆反应的活化能,即E。
2
(3)催化剂只能影响正、逆反应的活化能,而不影响反应的ΔH。
(4)设计反应热的有关计算时,要切实注意图示中反应物和生成物的物质的量。
变式1 反应过程中的焓变
1.(2021·全国·高三专题练习)已知:①S(g) +O (g)= SO (g) △H ②S(s)+O (g)=SO(g) △H,下列说法正
2 2 1 2 2 2
确的是
A.硫燃烧过程中将化学能转化全部为热能B.相同条件下,1 mol S(s) 比l mol S(g) 燃烧更剧烈
C.两个过程的能量变化可用下图表示, H< H<0
1 2
△ △
D.两个反应中反应物的总键能都比生成物的总键能小
变式2 反应过程中能量变化图像
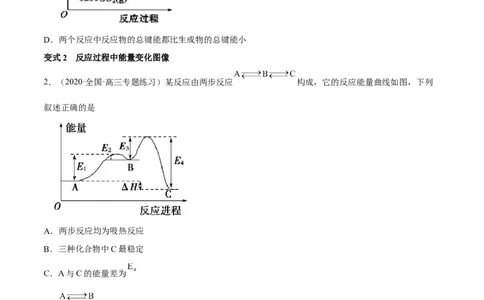
2.(2020·全国·高三专题练习)某反应由两步反应 构成,它的反应能量曲线如图,下列
叙述正确的是
A.两步反应均为吸热反应
B.三种化合物中C最稳定
C.A与C的能量差为
D. 反应,反应条件一定需要加热
变式3 反应能量变化与键能关系
3.(2022·黑龙江·哈尔滨三中高三期中)合成氨工业中氢气可由天然气和水反应制备,其主要反应为:
。已知下列键能数据:
化学键 C-H H-O C=O H-H键能/ 414 464 803 436
则该反应的反应热△H为A.-162kJ/mol B.+162kJ/mol C.+965kJ/mol D.+1470kJ/mol
变式4 反应历程与能量变化
4.(2021·浙江·模拟预测)2A(g) B(g) ΔH(ΔH <0); 2A(g) B(l) ΔH;下列能量变化示意图正
1 1 2
确的是
A. B.
C. D.
变式5 能量变化与活化能
5.(2021·浙江·高三专题练习)N(g)+3H(g) 2NH (g)反应过程中的能量变化如图所示。下列说法中错误
2 2 3
的是 ⇌
A.该反应的活化能为E B.该反应的ΔH=E-E
1 1 2
C.该反应为放热反应 D.图中表示温度T>T
1 2
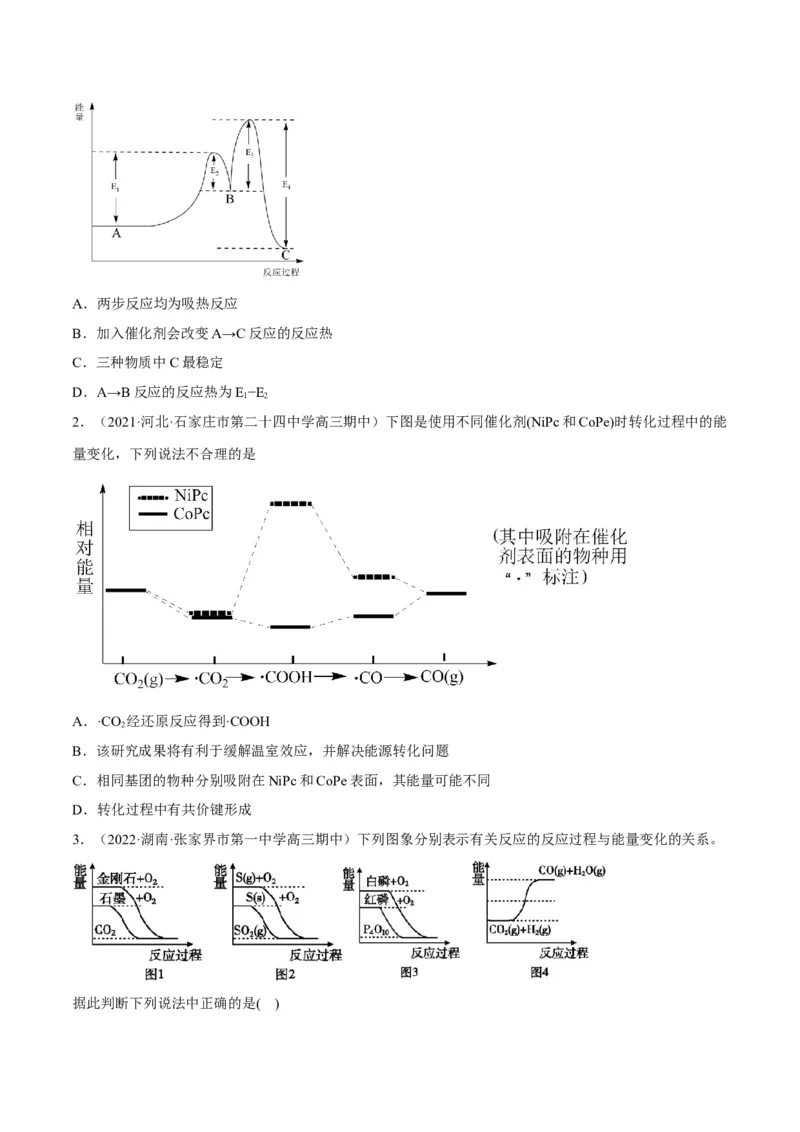
1.(2022·湖南·攸县第三中学高三阶段练习)某反应由两步反应A→B→C构成,它的反应过程中能量变
化曲线如图所示。下列说法正确的是A.两步反应均为吸热反应
B.加入催化剂会改变A→C反应的反应热
C.三种物质中C最稳定
D.A→B反应的反应热为E−E
1 2
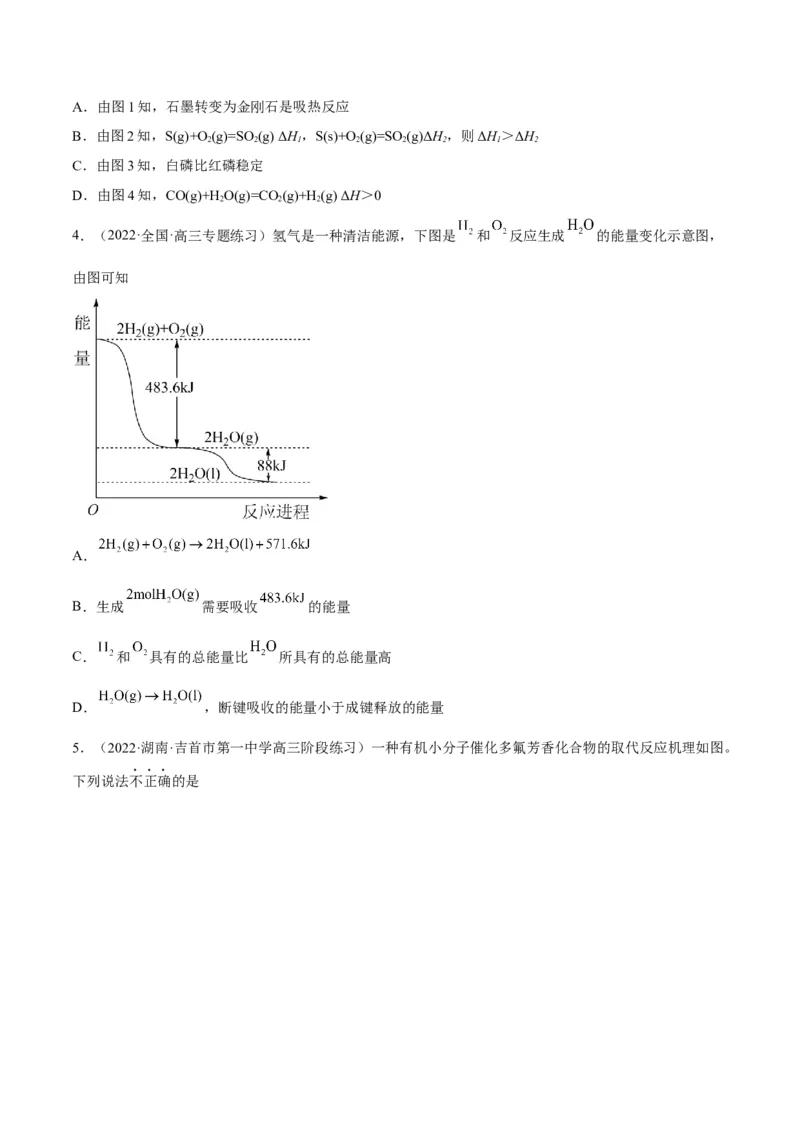
2.(2021·河北·石家庄市第二十四中学高三期中)下图是使用不同催化剂(NiPc和CoPe)时转化过程中的能
量变化,下列说法不合理的是
A.·CO 经还原反应得到·COOH
2
B.该研究成果将有利于缓解温室效应,并解决能源转化问题
C.相同基团的物种分别吸附在NiPc和CoPe表面,其能量可能不同
D.转化过程中有共价键形成
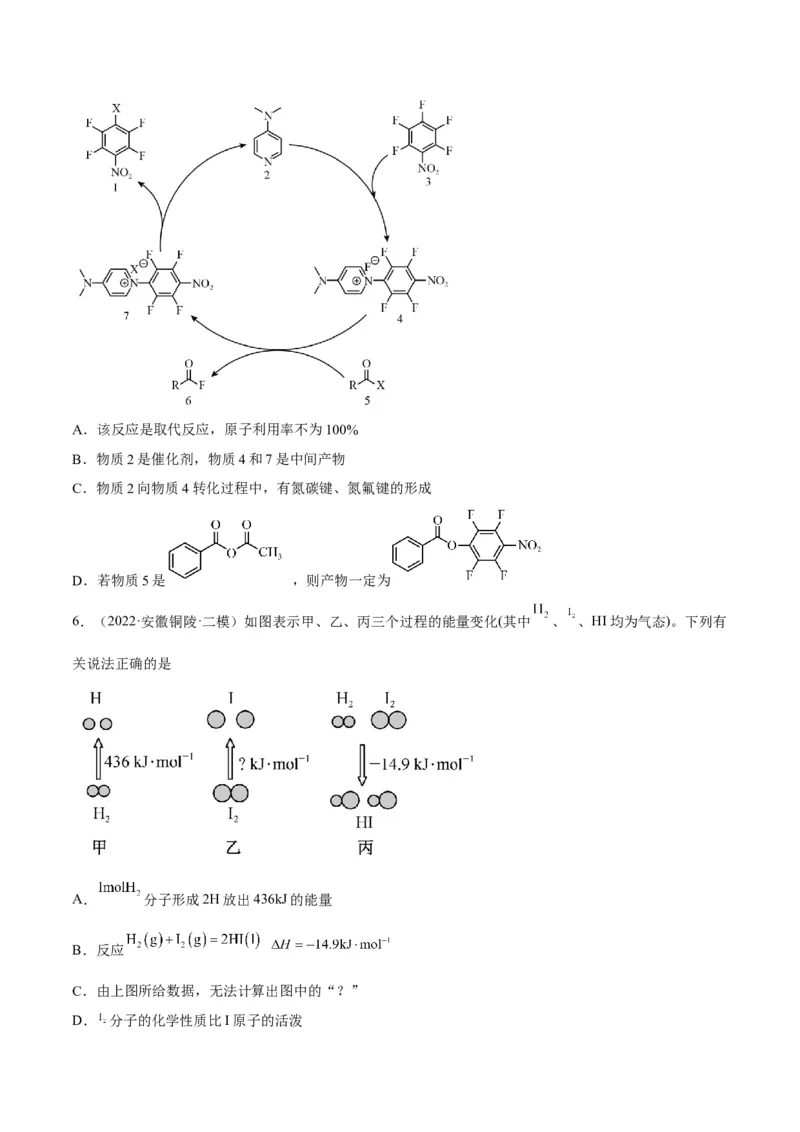
3.(2022·湖南·张家界市第一中学高三期中)下列图象分别表示有关反应的反应过程与能量变化的关系。
据此判断下列说法中正确的是( )A.由图1知,石墨转变为金刚石是吸热反应
B.由图2知,S(g)+O(g)=SO(g) ΔH,S(s)+O (g)=SO(g)ΔH,则ΔH>ΔH
2 2 1 2 2 2 1 2
C.由图3知,白磷比红磷稳定
D.由图4知,CO(g)+HO(g)=CO(g)+H(g) ΔH>0
2 2 2
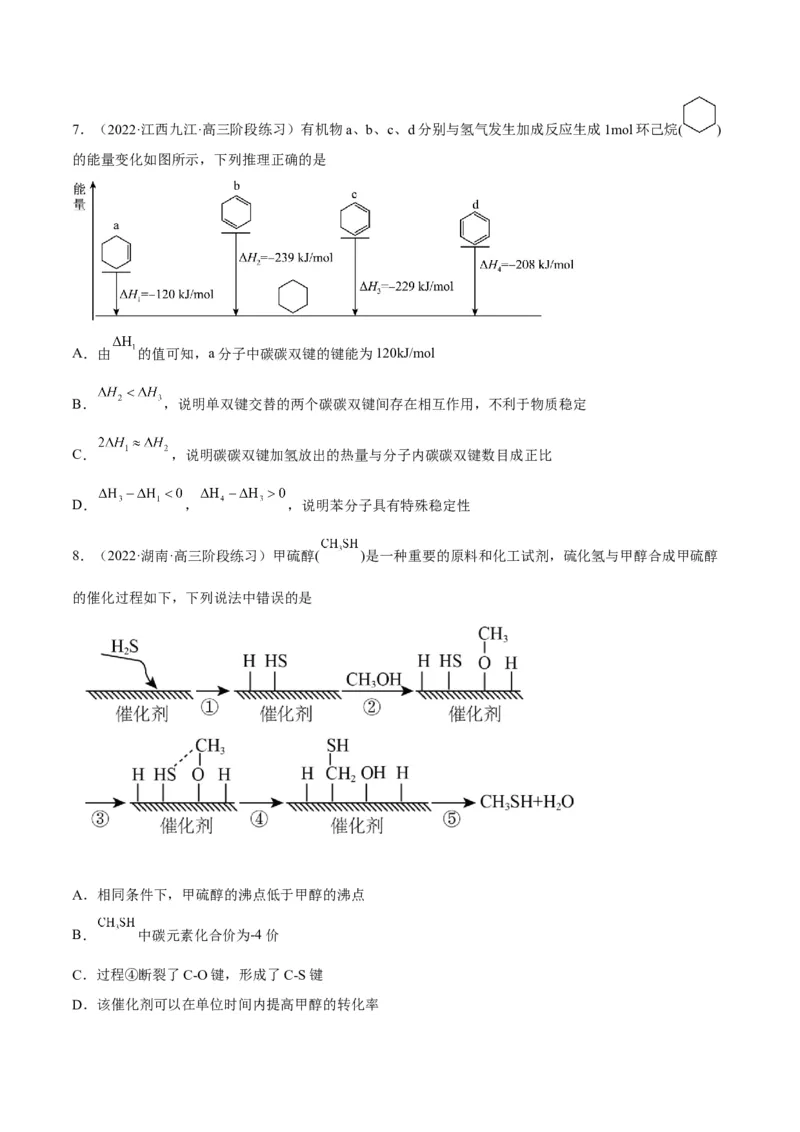
4.(2022·全国·高三专题练习)氢气是一种清洁能源,下图是 和 反应生成 的能量变化示意图,
由图可知
A.
B.生成 需要吸收 的能量
C. 和 具有的总能量比 所具有的总能量高
D. ,断键吸收的能量小于成键释放的能量
5.(2022·湖南·吉首市第一中学高三阶段练习)一种有机小分子催化多氟芳香化合物的取代反应机理如图。
下列说法不正确的是A.该反应是取代反应,原子利用率不为100%
B.物质2是催化剂,物质4和7是中间产物
C.物质2向物质4转化过程中,有氮碳键、氮氟键的形成
D.若物质5是 ,则产物一定为
6.(2022·安徽铜陵·二模)如图表示甲、乙、丙三个过程的能量变化(其中 、 、HI均为气态)。下列有
关说法正确的是
A. 分子形成2H放出436kJ的能量
B.反应
C.由上图所给数据,无法计算出图中的“?”
D. 分子的化学性质比I原子的活泼7.(2022·江西九江·高三阶段练习)有机物a、b、c、d分别与氢气发生加成反应生成1mol环己烷( )
的能量变化如图所示,下列推理正确的是
A.由 的值可知,a分子中碳碳双键的键能为120kJ/mol
B. ,说明单双键交替的两个碳碳双键间存在相互作用,不利于物质稳定
C. ,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
D. , ,说明苯分子具有特殊稳定性
8.(2022·湖南·高三阶段练习)甲硫醇( )是一种重要的原料和化工试剂,硫化氢与甲醇合成甲硫醇
的催化过程如下,下列说法中错误的是
A.相同条件下,甲硫醇的沸点低于甲醇的沸点
B. 中碳元素化合价为-4价
C.过程④断裂了C-O键,形成了C-S键
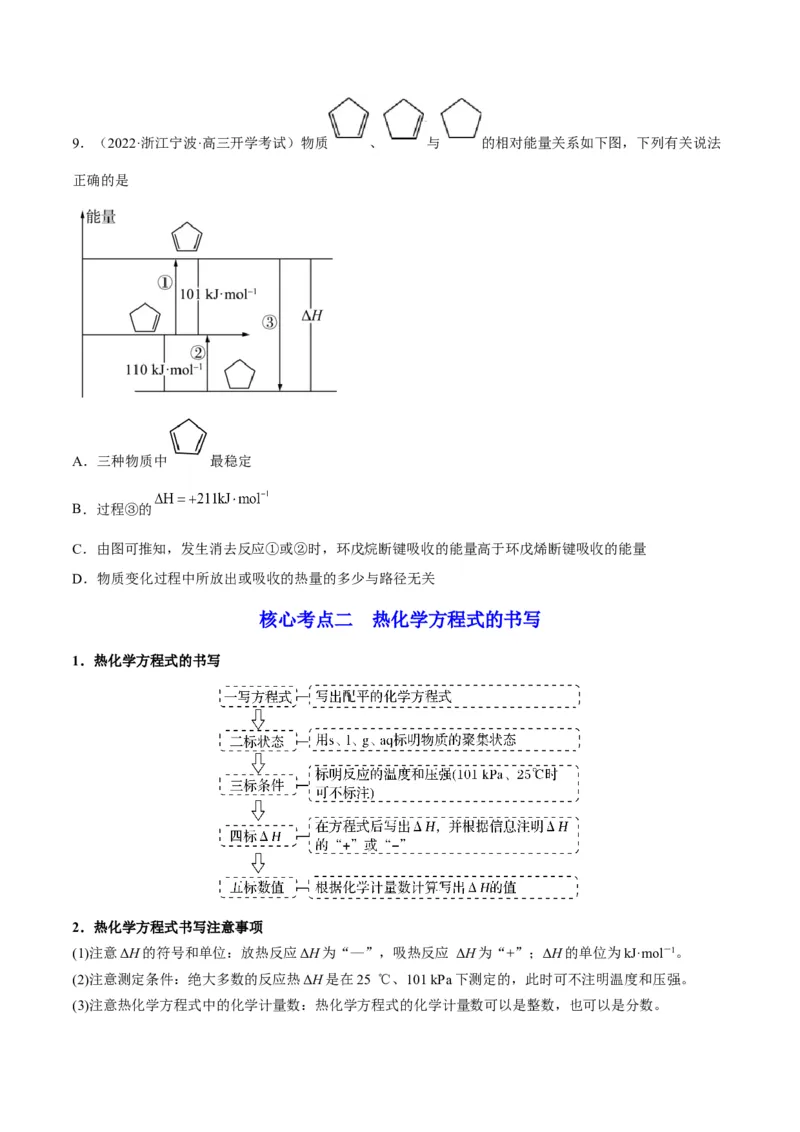
D.该催化剂可以在单位时间内提高甲醇的转化率9.(2022·浙江宁波·高三开学考试)物质 、 与 的相对能量关系如下图,下列有关说法
正确的是
A.三种物质中 最稳定
B.过程③的
C.由图可推知,发生消去反应①或②时,环戊烷断键吸收的能量高于环戊烯断键吸收的能量
D.物质变化过程中所放出或吸收的热量的多少与路径无关
核心考点二 热化学方程式的书写
1.热化学方程式的书写
2.热化学方程式书写注意事项
(1)注意ΔH的符号和单位:放热反应ΔH为“—”,吸热反应 ΔH为“+”;ΔH的单位为kJ·mol-1。
(2)注意测定条件:绝大多数的反应热ΔH是在25 ℃、101 kPa下测定的,此时可不注明温度和压强。
(3)注意热化学方程式中的化学计量数:热化学方程式的化学计量数可以是整数,也可以是分数。(4)注意物质的聚集状态:气体用“g”,液体用“1”,固体用“s”,溶液用“aq”。热化学方程式中不
用“↑”和“↓”。
(5)注意ΔH的数值与符号:如果化学计量数加倍,则ΔH也要加倍。逆反应的反应热与正反应的反应热数
值相等,但符号相反。
(6)对于具有同素异形体的物质,除了要注明聚集状态外,还要注明物质的名称。
如:①S(单斜,s)+O(g)═══SO (g) ΔH=-297.16 kJ·mol-1
2 2
②S(正交,s)+O(g)═══SO (g) ΔH=-296.83 kJ·mol-1
2 2 2
③S(单斜,s)═══S(正交,s) ΔH=-0.33 kJ·mol-1
3
(7)两个概念:①燃烧热:指1mol可燃物,C→CO(g),H(g)→HO(l)
2 2 2
②中和热:指生成1molHO(l)
2
3.利用盖斯定律书写热化学方程式
(1)盖斯定律是指化学反应不管是一步完成还是分几步完成,其反应热是相同的,即化学反应的反应热只与
反应体系的始态和终态有关,而与反应的途径无关。
(2)在具体的应用过程中,采用以下五个步骤就能快速、准确地解决问题。
具体步骤:
第一步:写,书写待求的反应方程式。
第二步:看,看待求的反应方程式中的反应物和生成物在已知方程式中的位置,如果位置相同,即都是反
应物或都是生成物,则用加法,即加ΔH;如果位置相反,则用减法,即减ΔH。
第三步:调,根据待求方程式中的反应物和生成物的系数,观察同一物质前的系数是否一致,若不一致,
则在相应的物质前乘或除以一定数字,将其系数调整与待求的方程式中的反应物和生成物的系数一致。
第四步:查,有时往往会出现一些干扰的方程式,我们最好检验上述分析的正确与否。
第五步:和,将已知方程式变形后的ΔH相加,计算得出新的ΔH的值。
4.盖斯定律应用
(1)当热化学方程式乘、除以某一个数时,ΔH也应相应地乘、除以某一个数;方程式进行加减运算时,ΔH
也同样要进行加减运算,且要带“+”“-”符号。
(2)将一个热化学方程式颠倒书写时,ΔH的符号也随之改变,但数值不变。
(3)同一物质的三态变化(固、液、气),状态由固→ 液→气变化时,会吸热;反之会放热。
(4)利用状态,迅速比较反应热的大小(若反应为放热反应)
①当反应物状态相同,生成物状态不同时,生成固体放热最多,生成气体放热最少。
②当反应物状态不同,生成物状态相同时,固体反应放热最少,气体反应放热最多。
③在比较反应热(ΔH)的大小时,应带符号比较。对于放热反应,放出的热量越多,ΔH反而越小。
考法 热化学方程式书写或正误判断及盖斯定律的运用(题型预测:选择题)1.下列关于热化学方程式的说法正确的是
A.若 的燃烧热为 ,则热化学方程式为
B.若1mol 和0.5mol 完全反应放热98.3kJ,则热化学方程式为
C.若 ,则稀硫酸与稀 反应的热化学方程式为
D.若31g白磷的能量比31g红磷多b kJ,则白磷转化为红磷的热化学方程式为
2.氢卤酸的能量关系如图所示,下列说法错误的是
A.已知HF气体溶于水放热,则HF的 H>0
1
B.相同条件下,HCl的 H
2
比HBr的大Δ
C.相同条件下,HCl的ΔH
3
+ H
4
比HI的大
D. H= H
1
+ H
2
+ H
3
+ HΔ4 + HΔ5 + H
6
Δ Δ Δ Δ Δ Δ Δ
热化学方程式书写与正误判断易出现的5种常见错误
(1)“+”“-”漏写或使用不正确。如放热反应未标“-”。
(2)单位与热量Q单位混淆。ΔH的单位为“kJ·mol-1(或kJ/ mol)”,易错写成“kJ”。
(3)物质的状态标注不正确。s、l、 g和aq分别表示固态、液态、气态和水溶液。
(4)ΔH的数值不正确。即ΔH的数值必须与方程式中的化学计量数相对应。
(5)对概念的理解不正确。如燃烧热是指1 mol可燃物,且生成CO(g)、HO(l)、SO (g)等;中和热是指1
2 2 2mol H+和1 mol OH-生成1 mol H O(l)。
2
变式1 热化学方程式的书写
1.回答问题
(1) 反应的 则 的燃烧热是_______。
(2)葡萄糖的燃烧热是 ,则表示葡萄糖燃烧热的热化学方程式为_______。
(3)氢气的燃烧热为 ,则电解水的热化学方程式为_______。
(4)已知中和反应的中和热为 。则 和盐酸反应表示中和热的热化学方程式为_______。
(5) 乙硼烷(分子式 )在氧气中燃烧,生成固态三氧化二硼和液态水,放出 的热量,则其
热化学方程式为_______。
变式2 热化学方程式的正误判断
2.下列热化学方程式正确的是
A.甲烷的燃烧热为ΔH = -890.3 kJ/mol,则甲烷燃烧的热化学方程式可表示为: CH(g) + 2O(g) = CO (g)
4 2 2
+ 2H O(g) ΔH = -890.3 kJ/mol
2
B.500 ℃、30 MPa下,将0.5 mol N 和1.5 mol H 置于密闭容器中充分反应生成NH (g),放热19.3 kJ,其
2 2 3
热化学方程式为N(g)+3H(g) 2NH (g) ΔH=-38.6 kJ/mol
2 2 3
C.已知H+(aq) + OH-(aq) = H O(l) ΔH=-57.3 kJ/mol,则稀HSO 溶液和稀Ba(OH) 溶液反应的反应热
2 2 4 2
ΔH=2×(-57.3) kJ/mol
D.25 ℃、101 KPa下,1 g H 燃烧生成液态水放出142.9 kJ热量,其热化学方程式为H(g)+ O(g) =
2 2 2
HO(l) ΔH =-285.8 kJ/mol
2
变式3 焓变的判断与比较
3.已知几种离子反应的热化学方程式如下
①
②③
④
下列有关判断正确的是
A. , B.
C. D.
变式4 盖斯定律的简单运用
4.2022北京冬奥会采用氢气作为火炬燃料,选择氢能汽车作为赛事交通服务用车,充分体现了绿色奥运
的理念。已知:
下列说法不正确的是
A.氢气既可以通过燃烧反应提供热能,也可以设计成燃料电池提供电能
B. 的过程中, ,
C.断裂2mol 和1mol 中化学键所需能量大于断裂2mol 中化学键所需能量
D.化学反应的 ,只与反应体系的始态和终态有关,与反应途径无关
变式5 盖斯定律的综合运用
5.根据图中各物质间的能量循环图,下列说法错误的是
A. H= H+ H+ H+ H+ H+ H
1 2 3 5 6 7 8
B.△H 3 >△0, △H 7 <△0, H△8 <0△ △
△ △ △C. H+ H> H+ H
2 3 4 8
D.△将图中△的“△Cl”改△为“Br”,则溴的 H
3
大于氯的 H
3
△ △
1.今有如下三个热化学方程式:
(1)H (g)+1/2O (g)=HO(g) ΔH=a kJ·mol-1
2 2 2 1
(2)H (g)+1/2O (g)=HO(l) ΔH=b kJ·mol-1
2 2 2 2
(3)2H (g)+O(g)=2HO(l) ΔH=c kJ·mol-1
2 2 2 3
下列关于它们的叙述正确的是
A.它们都是吸热反应 B.a、b和c均为负值
C.a=b D.2b=c>0
2.下列关于反应热的说法正确的是
A.a. ;b. ,若a、b反应放热,则
B.已知 ,则甲烷的燃烧热为
C. ,则常温下 比 更稳定
D. ,恒温恒压下达平衡后加入X,上述反应 增大
3.下列对热化学方程式的解读或书写正确的是
A.已知 ,则石墨比金刚石稳定
B.已知① ;② ,则
C.已知甲烷燃烧热为 ,则甲烷燃烧的热化学方程式可以表示为
D.已知中和热 ,则1mol硫酸和足量稀NaOH溶液反应的反应热就是中和热
4.下列依据热化学方程式得出的结论正确的是A.在 、 时, 完全燃烧生成液态水,放出 热量,则表示氢气燃烧热的热化学方程
式为:
B. 的燃烧热是 ,则
C.在稀溶液中: ,若将含 的浓硫酸与含
的溶液混合,放出的热量大于
D.已知 石墨, 金刚石, ,则金刚石比石墨稳定
5.北京奥运会“祥云”奥运火炬所用环保型燃料为丙烷( ),悉尼奥运会所用火炬燃料为65%丁烷(
)和 丙烷。
已知: 。
丙烷: 。
正丁烷: 。
异丁烷: 。
下列有关说法正确的是
A.常温下,正丁烷的燃烧热为
B.相同质量的丙烷和正丁烷分别完全燃烧,前者需要的氧气少产生的热量也多
C.常温下, 的燃烧热为
D.人类利用的能源都是通过化学反应获得的
6.已知:H(g)+F (g)→2HF(g)+270 kJ,下列说法正确的是
2 2
A.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出热量小于270 kJ
B.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量
C.在相同条件下,1mol氢气与1mol氟气的键能总和大于2mol氟化氢气体的键能
D.2L氟化氢气体分解成1L氢气与1L氟气吸收270 kJ的热量7.下列有关反应热的描述正确的是
①化学反应过程中一定有能量变化
②反应热是1mol物质参加反应时的能量变化
③ΔH的大小与热化学方程式中的化学计量数成正比
④放热反应在常温下就一定能进行⑤化学反应中放出的热才是反应热
A.①③ B.②④ C.①②③ D.④⑤
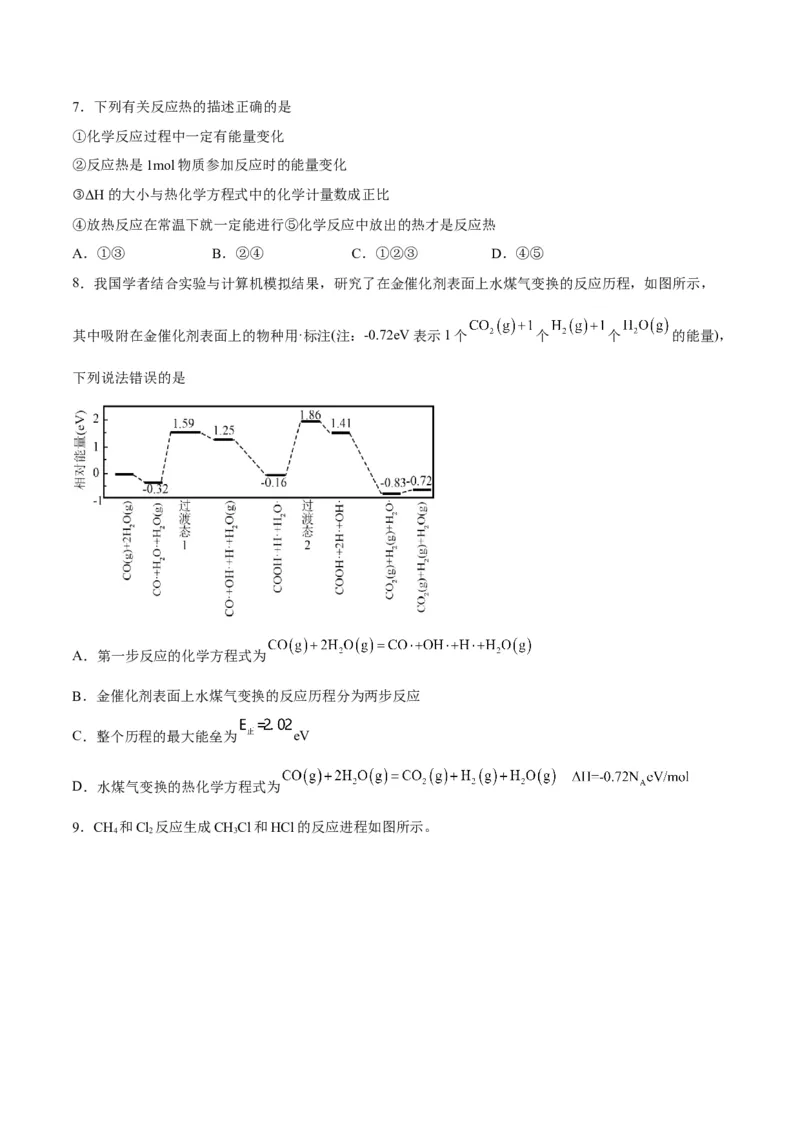
8.我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,
其中吸附在金催化剂表面上的物种用·标注(注:-0.72eV表示1个 个 个 的能量),
下列说法错误的是
A.第一步反应的化学方程式为
B.金催化剂表面上水煤气变换的反应历程分为两步反应
C.整个历程的最大能垒为 eV
D.水煤气变换的热化学方程式为
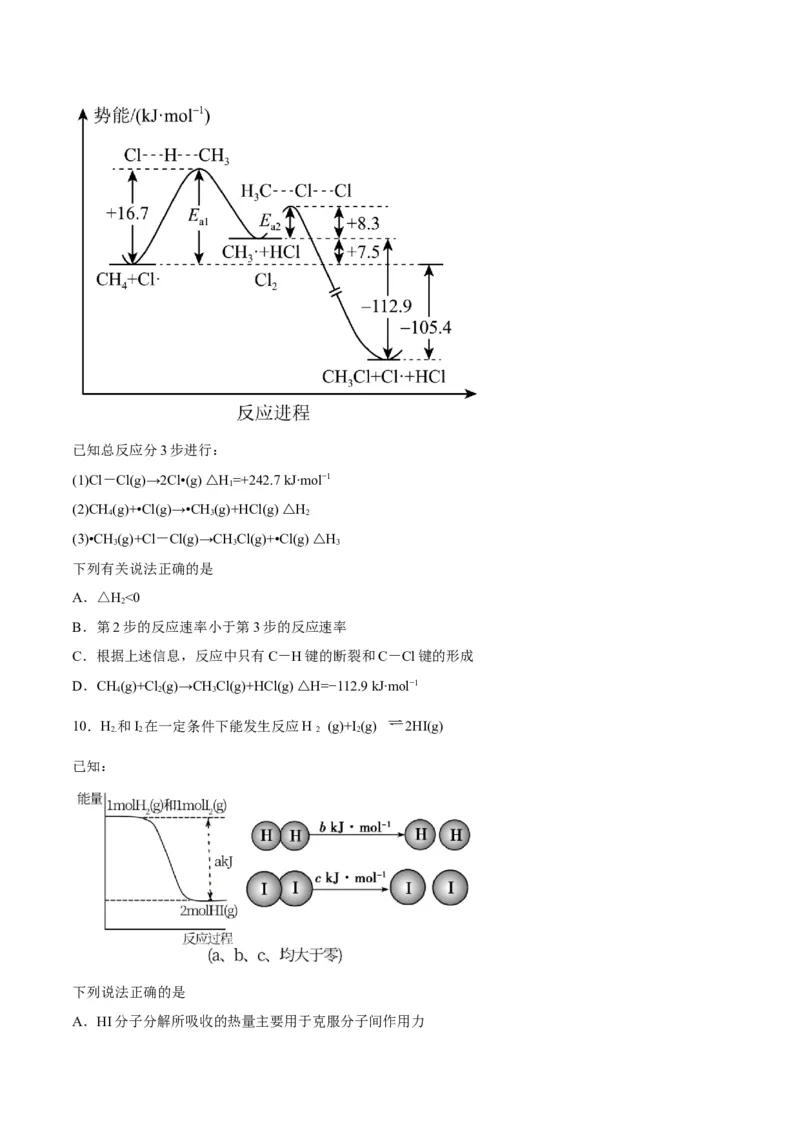
9.CH 和Cl 反应生成CHCl和HCl的反应进程如图所示。
4 2 3已知总反应分3步进行:
(1)Cl-Cl(g)→2Cl•(g) △H =+242.7 kJ∙mol−1
1
(2)CH (g)+•Cl(g)→•CH (g)+HCl(g) △H
4 3 2
(3)•CH (g)+Cl-Cl(g)→CH Cl(g)+•Cl(g) △H
3 3 3
下列有关说法正确的是
A.△H<0
2
B.第2步的反应速率小于第3步的反应速率
C.根据上述信息,反应中只有C-H键的断裂和C-Cl键的形成
D.CH(g)+Cl (g)→CH Cl(g)+HCl(g) △H=−112.9 kJ∙mol−1
4 2 3
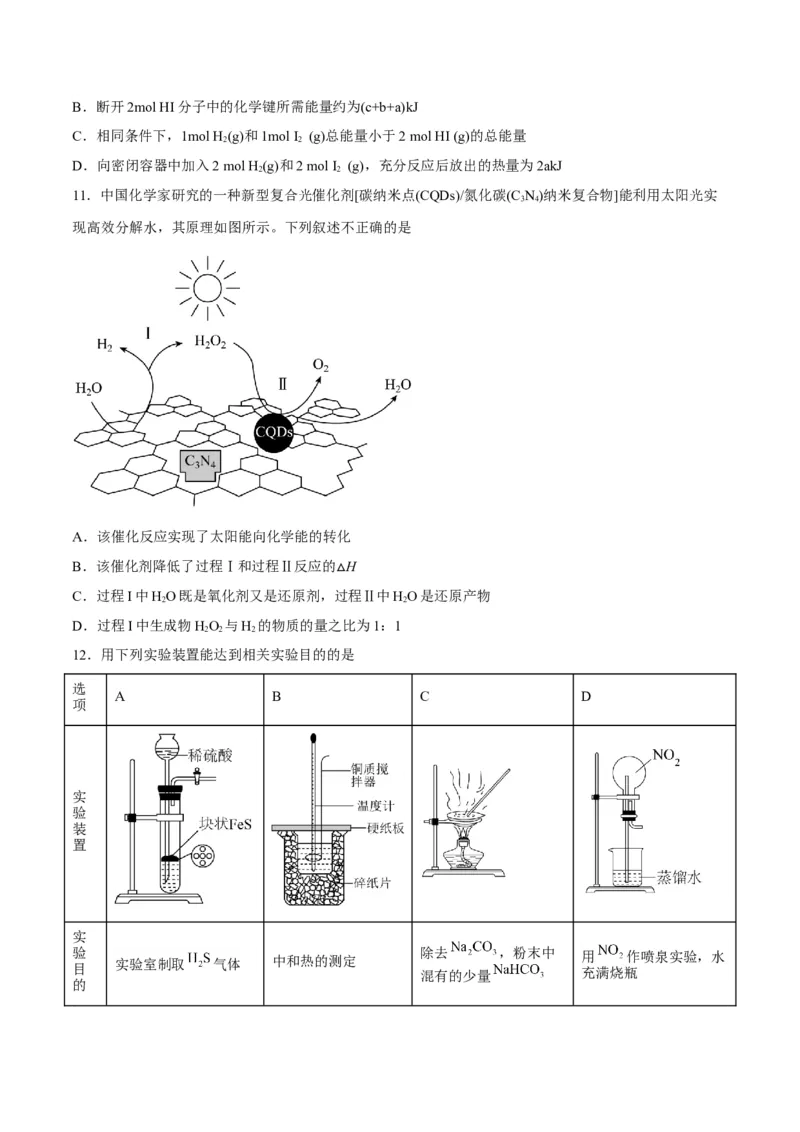
10.H 和I 在一定条件下能发生反应H (g)+I (g) 2HI(g)
2. 2 2 2
已知:
下列说法正确的是
A.HI分子分解所吸收的热量主要用于克服分子间作用力B.断开2mol HI分子中的化学键所需能量约为(c+b+a)kJ
C.相同条件下,1mol H(g)和1mol I (g)总能量小于2 mol HI (g)的总能量
2 2
D.向密闭容器中加入2 mol H (g)和2 mol I (g),充分反应后放出的热量为2akJ
2 2
11.中国化学家研究的一种新型复合光催化剂[碳纳米点(CQDs)/氮化碳(C N)纳米复合物]能利用太阳光实
3 4
现高效分解水,其原理如图所示。下列叙述不正确的是
A.该催化反应实现了太阳能向化学能的转化
B.该催化剂降低了过程Ⅰ和过程Ⅱ反应的 H
C.过程I中H
2
O既是氧化剂又是还原剂,过△程Ⅱ中H
2
O是还原产物
D.过程I中生成物HO 与H 的物质的量之比为1:1
2 2 2
12.用下列实验装置能达到相关实验目的的是
选
A B C D
项
实
验
装
置
实
验 除去 ,粉末中 用 作喷泉实验,水
实验室制取 气体 中和热的测定
目 混有的少量 充满烧瓶
的A.A B.B C.C D.D
13.下列说法中正确的是
A.若 2NO (g) NO(g) ∆H =-56.9kJ·mol-1 ,则 置于密闭容器中充分反应放出的热量为
2 2 4
56.9kJ
B.已知甲烷、一氧化碳、氢气的燃烧热分别是890.3 kJ/mol、283 kJ/mol、285.8 kJ/mol。则:CH(g)
4
+CO (g)=2CO(g)+2H(g) △H=+247.3 kJ/mol
2 2
C.在稀溶液中,强酸与强碱反应的中和热为ΔH=-57.3kJ·mol-1,若将含有0.5mol H SO 的浓硫酸和含有
2 4
1molNaOH的溶液混合,放出的热量等于57.3kJ
D.H(g)的燃烧热是285.8kJ·mol-1,则2HO(g)=2H (g)+O(g) ∆H =+571.6kJ·mol-1
2 2 2 2
核心考点三 反应热的计算与比较
1.反应热计算的四种方法
(1)从宏观角度计算 ΔH=H(生成物的总能量)-H(反应物的总能量)
1 2
(2)从微观角度计算 ΔH=E(反应物的键能总和)-E(生成物的键能总和)
1 2
(3)从活化能角度计算 ΔH=E(正反应的活化能)-E(逆反应的活化能)
1 2
(4)根据盖斯定律计算
①计算步骤
②计算方法2.规避两个易失分点
(1)旧化学键的断裂和新化学键的形成是同时进行的,缺少任何一个过程都不是化学变化。
(2)常见物质中的化学键数目
①CO(C===O):2;②CH(C—H):4;
2 4
③P(P—P):6; ④SiO(Si—O):4;
4 2
⑤石墨:1.5; ⑥金刚石:2;
⑦S(S—S):8; ⑧Si:2
8
3.反应热的大小比较方法
(1)利用盖斯定律比较。
(2)同一反应的生成物状态不同时,如A(g)+B(g)===C(g) ΔH,A(g)+B(g)===C(l) ΔH,则ΔH>ΔH。
1 2 1 2
(3)同一反应的同一反应物状态不同时,如 A(s)+B(g)===C(g) ΔH ,A(g)+B(g)===C(g) ΔH ,则
1 2
ΔH>ΔH。
1 2
总之,比较反应热的大小时要注意:
①反应中各物质的聚集状态;
②ΔH有正、负之分,比较时要连同“+”、“-”一起比较,类似数学中的正、负数大小的比较;
③若只比较放出或吸收热量的多少,则只比较数值的大小,不考虑正、负号。
考法 反应热的计算与比较(题型预测:选择题)
1.(2022·浙江·嘉兴一中高三期中)已知胆矾晶体相关的焓变如下:下列有关判断正确的是
A. B.
C. D.
2.(2022·黑龙江·牡丹江市第三高级中学高三阶段练习)下列各组热化学方程式中, 的是
①
②
③
④
A.①②③ B.②④ C.②③④ D.②③
1.利用盖斯定律计算ΔH的方法和步骤
2.比较反应热大小的四个注意要点
(1)反应物和生成物的状态:
物质的气、液、固三态的变化与反应热的关系。
(2)ΔH的符号:比较反应热的大小时,不要只比较ΔH数值的大小,还要考虑其符号。(3)参加反应物质的量:当反应物和生成物的状态相同时,参加反应物质的量越多,放热反应的 ΔH越小,
吸热反应的ΔH越大。
(4)反应的程度:参加反应物质的量和状态相同时,反应的程度越大,热量变化越大
变式1 从宏观角度计算
1.(2022·广东·蕉岭县蕉岭中学高三阶段练习)已知:2CO(g)+O(g)=2CO (g) ΔH=-566kJ/mol
2 2
2NaO(s)+2CO(g)=2Na CO(s)+O(g) ΔH=-452kJ/mol
2 2 2 2 3 2
下列说法正确的是
A.28克CO完全燃烧,放出热量为283J
B.NaO(s)+CO(g)=Na CO(s)+ O(g) ΔH=+226kJ/mol
2 2 2 2 3 2
C.CO(g)与NaO(s)反应放出509kJ热量时,电子转移数为1.204×1024
2 2
D.CO的燃烧热为283kJ/mol
变式2 从微观角度计算
2.(2022·重庆南开中学高三阶段练习)乙烯( )是石油化工产业的核心,作为一种可燃物,乙烯有着
热值高、产物清洁的优势。在25℃、 的条件下,乙烯的燃烧热为 。
已知:①部分化学键的键能如下表所示
化学键 C=C C-H O=O C=O H-O
612 414 498 x 464
键能
②3.6g水蒸气液化会放出8kJ热量,则x的值为A.809 B.1041 C.676 D.829
变式3 从活化能角度计算
3.(2020·甘肃·武威十八中高三期末)某反应由两步反应A→B→C构成,它的反应能量曲线如图(E 、
1
E、E、E 表示活化能).下列有关叙述正确的是( )
2 3 4
A.三种化合物中B最稳定 B.A→B为吸热反应,B→C为放热反应
C.加入催化剂会改变反应的焓变 D.整个反应的 H=E ﹣E
1 2
△变式4 根据盖斯定律计算
4.(2022·江苏·连云港市厉庄高级中学高三阶段练习)已知下列热化学方程式:
;
,由此可知 的 ,其中 的值是
A. B.
C. D.
变式5 反应热的大小比较方法
5.(2022·湖南·雅礼中学高三阶段练习)已知:① ;
② ;
③ ;
④ ;
⑤ 。
下列关于上述反应焓变的判断不正确的是
A. B.
C. D.
1.(2022·浙江·高三阶段练习)航天员呼吸产生的 通过反应
,再电解水可实现 的循环利用。热力学中规定由最稳定单质生成1mol某物质的焓变称为该物质的
标准摩尔生成焓( ),最稳定单质的标准生成焓规定为0.已知上述反应式中:
; ; ;。则 的数值为
A. B. C. D.
2.(2022·浙江·高三阶段练习)根据图中的各物质间的能量循环图,下列说法正确的是
A. H= H+ H+ H+ H+ H+ H+ H
1 2 3 4 5 6 7 8
B.△H 5 <△0, △H 7 >△0, H△8 <0△ △ △
C.△Br(g)的 H△6 小于Cl(△g)的 H
6
D. H
5
+ H△6 + H
7
+ H
8
< △H
2
3.(△2021△·河南△·义马△市高级△中学高三阶段练习)用一氧化碳还原氮氧化物,可防止氮氧化物污染。已知:
ⅰ.
ⅱ.
ⅲ.
则 完全燃烧所放出的热量为
A. B. C. D.
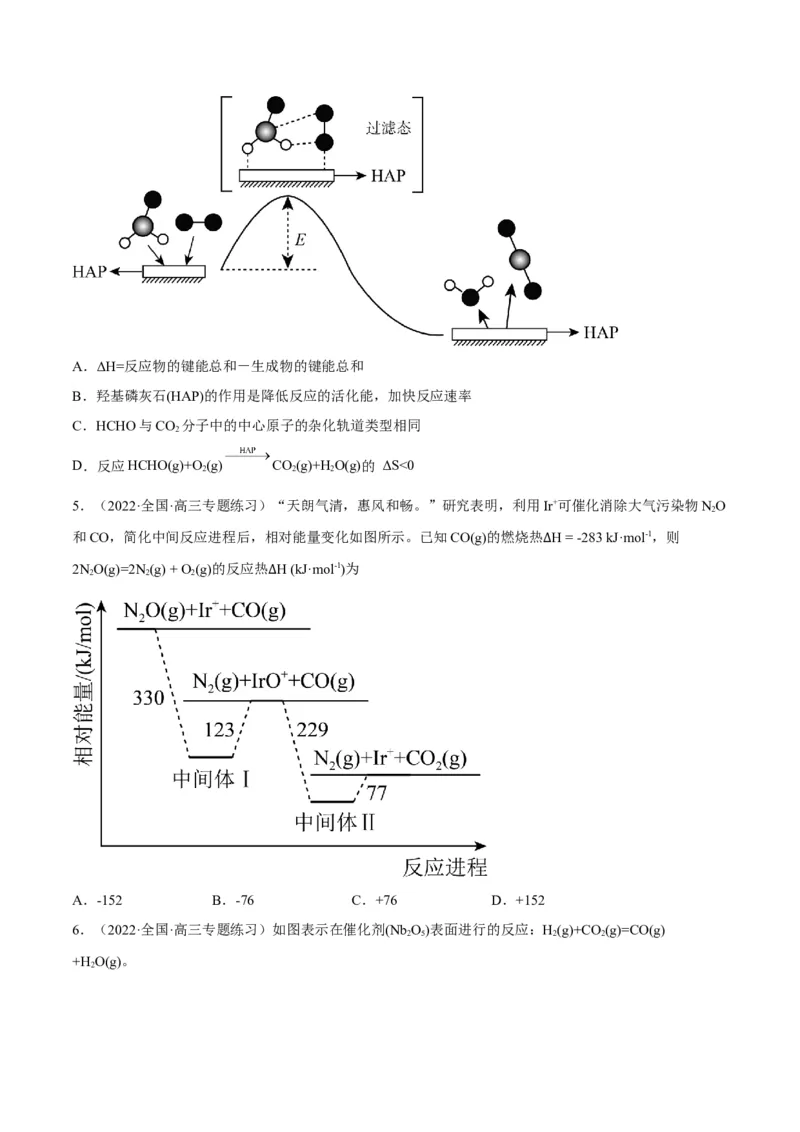
4.(2022·江苏南京·高三期中)HCHO(g)与O(g)在催化剂Ca₅(PO₄)₃(OH) (简写为HAP)表面催化生成
2
CO(g)和HO(g)的历程示意图如下。已知该反应在较高温度下不能自发进行。下列说法不正确的是
2 2A.ΔH=反应物的键能总和-生成物的键能总和
B.羟基磷灰石(HAP)的作用是降低反应的活化能,加快反应速率
C.HCHO与CO 分子中的中心原子的杂化轨道类型相同
2
D.反应HCHO(g)+O(g) CO(g)+HO(g)的 ΔS<0
2 2 2
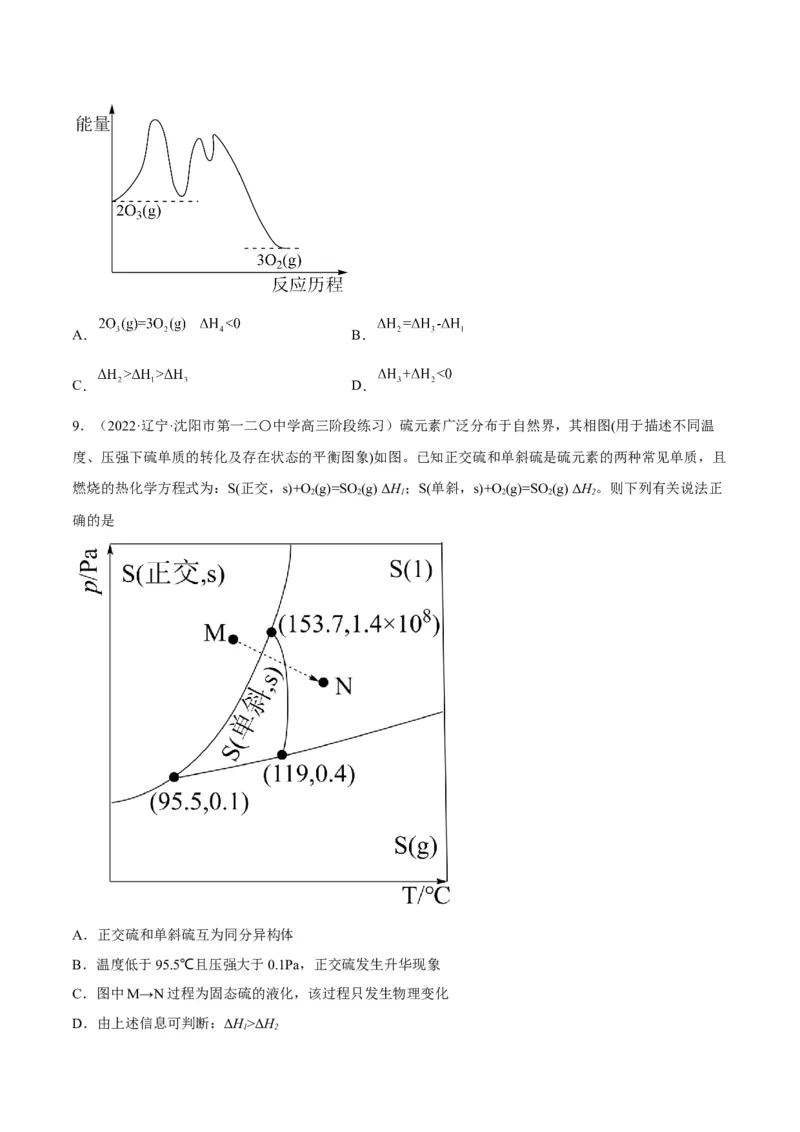
5.(2022·全国·高三专题练习)“天朗气清,惠风和畅。”研究表明,利用Ir+可催化消除大气污染物NO
2
和CO,简化中间反应进程后,相对能量变化如图所示。已知CO(g)的燃烧热 H = -283 kJ·mol-1,则
2NO(g)=2N (g) + O(g)的反应热 H (kJ·mol-1)为 ∆
2 2 2
∆
A.-152 B.-76 C.+76 D.+152
6.(2022·全国·高三专题练习)如图表示在催化剂(Nb O)表面进行的反应:H(g)+CO (g)=CO(g)
2 5 2 2
+H O(g)。
2已知下列反应:
①2H(g)+O(g)=2HO(g) ∆H
2 2 2 1
②C(s)+ O(g)=CO(g) ∆H
2 2
③C(s)+O (g)=CO (g) ∆H
2 2 3
下列说法不正确的是
A.∆H<∆H
2 3
B.图中的能量转化方式主要为太阳能转化为化学能
C.反应2CO(g)+O(g)=2CO (g) 的 ∆H=2(∆H −∆H )
2 2 3 2
D.反应H(g)+CO (g)=CO(g)+HO(g)的∆H=∆H −∆H + ∆H
2 2 2 2 3 1
7.(2022·全国·高三专题练习)下列各组热化学方程式中, H> H 的是
1 2
∆ ∆
①C(s)+O(g)=CO (g) H C(s)+ O(g)=CO(g) H
2 2 1 2 2
∆ ∆
②S(s)+O (g)=SO(g) H S(g)+O(g)=SO(g) H
2 2 1 2 2 2
∆ ∆
③H(g)+ O(g)=HO(l) H 2H(g)+O(g)=2HO(l) H
2 2 2 1 2 2 2 2
∆ ∆
④CaCO(s)=CaO(s)+CO (g) H CaO(s)+H O(l)=Ca(OH) (s) H
3 2 1 2 2 2
A.① B.④∆ C.②③④ ∆ D.①②③
8.(2022·浙江·高三阶段练习)氮氧化物破坏臭氧层反应机理如下:
i
ii
iii 其能量与反应历程的关系如图所示。下列判断不正确的是A. B.
C. D.
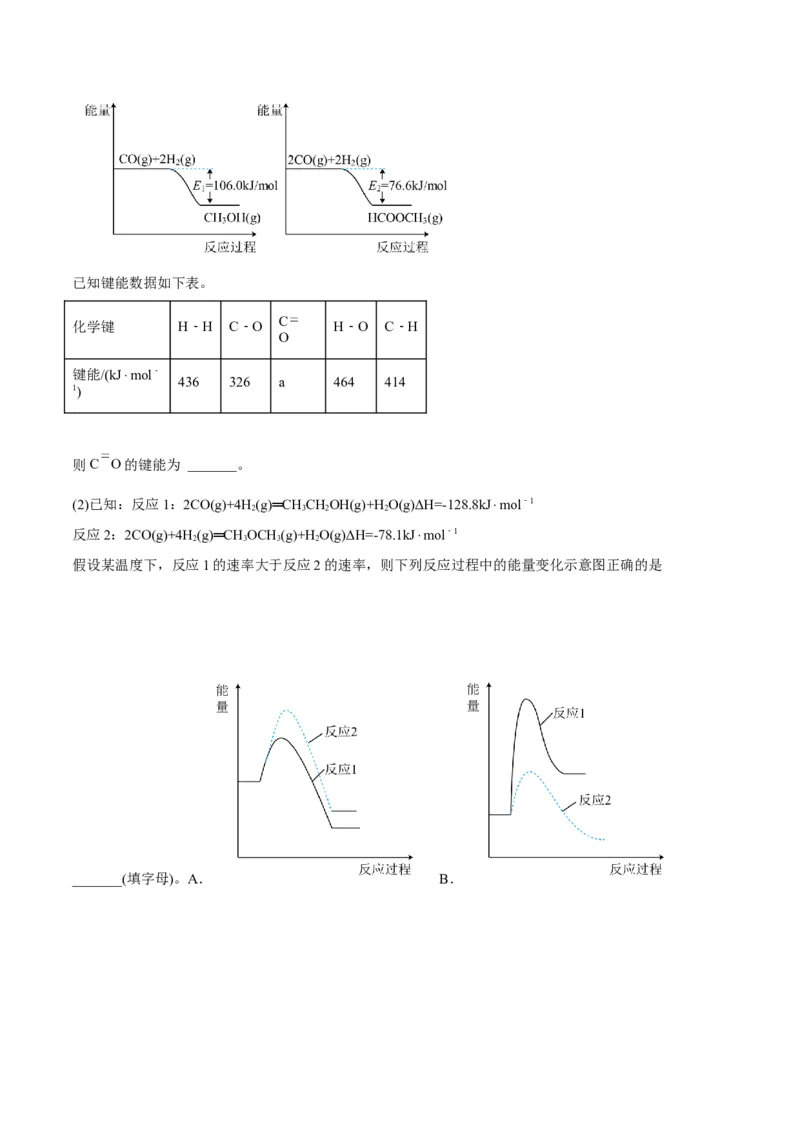
9.(2022·辽宁·沈阳市第一二〇中学高三阶段练习)硫元素广泛分布于自然界,其相图(用于描述不同温
度、压强下硫单质的转化及存在状态的平衡图象)如图。已知正交硫和单斜硫是硫元素的两种常见单质,且
燃烧的热化学方程式为:S(正交,s)+O(g)=SO(g) ΔH;S(单斜,s)+O(g)=SO(g) ΔH。则下列有关说法正
2 2 1 2 2 2
确的是
A.正交硫和单斜硫互为同分异构体
B.温度低于95.5℃且压强大于0.1Pa,正交硫发生升华现象
C.图中M→N过程为固态硫的液化,该过程只发生物理变化
D.由上述信息可判断:ΔH>ΔH
1 210.(2022·全国·高三专题练习)下图是不饱和烃加氢时能量变化示意图(E代表反应物具有的总能量),具
体数据如下:
反应
(1)如果 与 以物质的量 反应,其主要产物是X。
(2)如果 与 的醇溶液共热后,主要产物是Y,另一副产物是Z。
下列推断正确的是A.不饱和烃加氢的反应的 B.Y是
C.X是 D.
【考点拓展】能源、气候、绿色发展
拓展一 能量与碳中和融合
1.(2022·河南高三阶段练习)CO、CO 的回收和综合利用有利于实现“碳中和”。
2
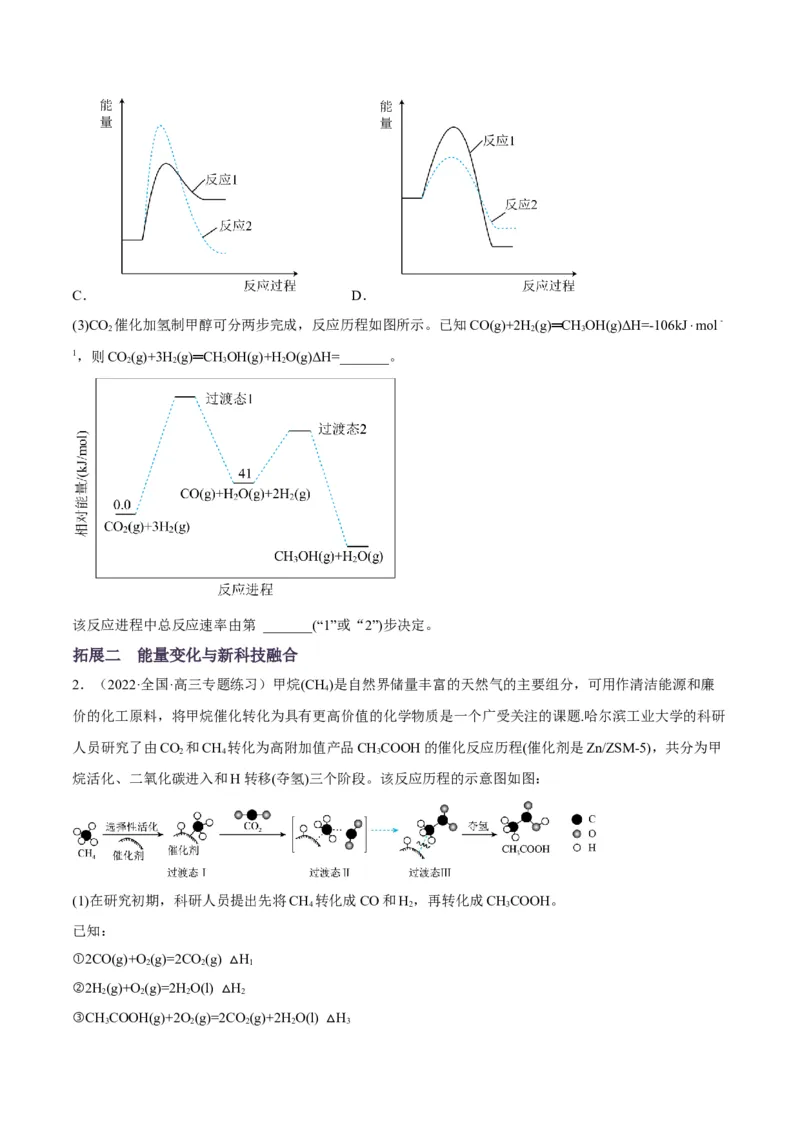
(1)CO和H 可以合成简单有机物,已知CO、H 合成CHOH、HCOOCH 的能量变化如图所示,计算
2 2 3 3
2CHOH(g) HCOOCH (g)+2H(g)ΔH=_______。
3 3 2已知键能数据如下表。
C
化学键 H﹣H C﹣O H﹣O C﹣H
O
键能/(kJ⋅mol﹣
436 326 a 464 414
1)
则C O的键能为 _______。
(2)已知:反应1:2CO(g)+4H(g)═CH CHOH(g)+H O(g)ΔH=-128.8kJ⋅mol﹣1
2 3 2 2
反应2:2CO(g)+4H(g)═CH OCH (g)+HO(g)ΔH=-78.1kJ⋅mol﹣1
2 3 3 2
假设某温度下,反应1的速率大于反应2的速率,则下列反应过程中的能量变化示意图正确的是
_______(填字母)。A. B.C. D.
(3)CO 催化加氢制甲醇可分两步完成,反应历程如图所示。已知CO(g)+2H(g)═CH OH(g)ΔH=-106kJ⋅mol﹣
2 2 3
1,则CO(g)+3H(g)═CH OH(g)+H O(g)ΔH=_______。
2 2 3 2
该反应进程中总反应速率由第 _______(“1”或“2”)步决定。
拓展二 能量变化与新科技融合
2.(2022·全国·高三专题练习)甲烷(CH)是自然界储量丰富的天然气的主要组分,可用作清洁能源和廉
4
价的化工原料,将甲烷催化转化为具有更高价值的化学物质是一个广受关注的课题.哈尔滨工业大学的科研
人员研究了由CO 和CH 转化为高附加值产品CHCOOH的催化反应历程(催化剂是Zn/ZSM-5),共分为甲
2 4 3
烷活化、二氧化碳进入和H转移(夺氢)三个阶段。该反应历程的示意图如图:
(1)在研究初期,科研人员提出先将CH 转化成CO和H,再转化成CHCOOH。
4 2 3
已知:
①2CO(g)+O(g)=2CO (g) H
2 2 1
②2H
2
(g)+O
2
(g)=2H
2
O(l) △H
2
③CH
3
COOH(g)+2O
2
(g)=2△CO
2
(g)+2H
2
O(l) H
3
△则混合气体CO和H 转化成CHCOOH(g)的热化学方程式为____。
2 3
(2)催化剂Zn/ZSM-5有以下四种形态:Z1(Zn2+/ZSM-5)、Z2([ZnOZn]2+/ZSM-5)、Z3(Zn2+,[ZnOZn]2+/
ZSM-5)、Z4([bi-ZnOZn]2+Zn2+/ZSM-5)。
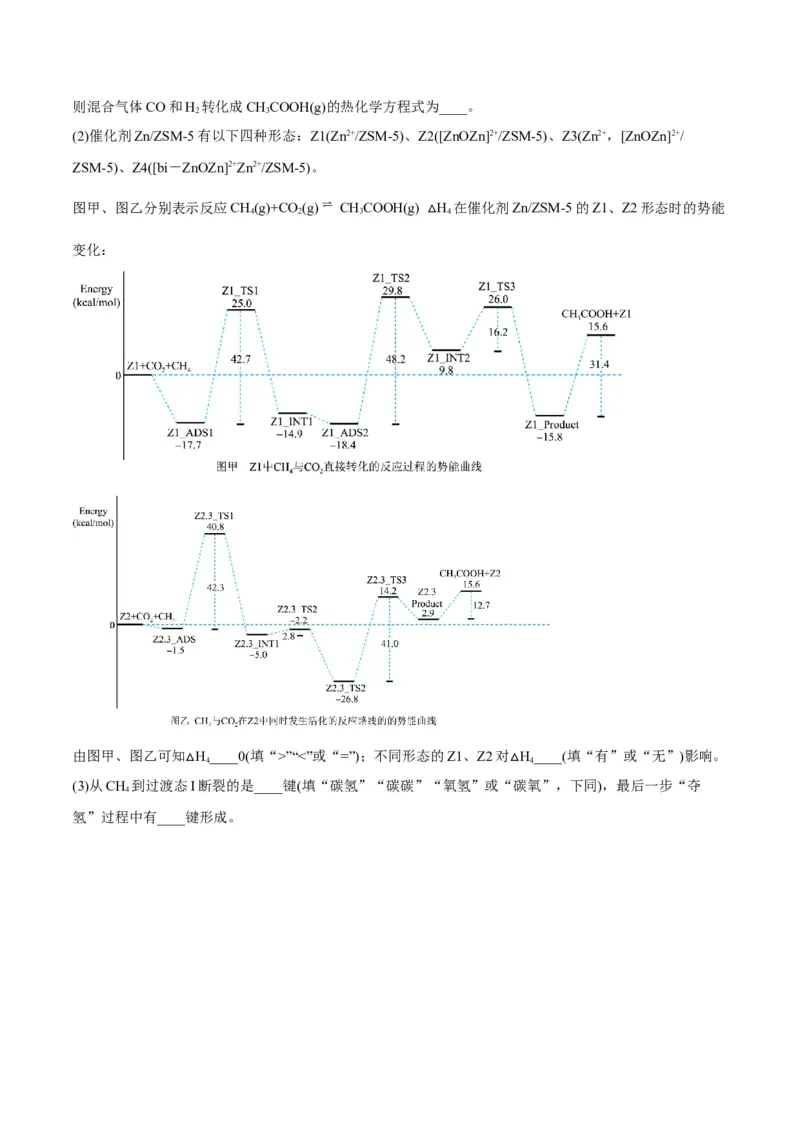
图甲、图乙分别表示反应CH(g)+CO (g) CHCOOH(g) H 在催化剂Zn/ZSM-5的Z1、Z2形态时的势能
4 2 3 4
△
变化:
由图甲、图乙可知 H____0(填“>”“<”或“=”);不同形态的Z1、Z2对 H____(填“有”或“无”)影响。
4 4
(3)从CH
4
到过渡态△I断裂的是____键(填“碳氢”“碳碳”“氧氢”或“△碳氧”,下同),最后一步“夺
氢”过程中有____键形成。