文档内容
解密 13 物质结构与性质
一、选择题
1.(2021·河西区·天津市新华中学高三模拟)从结构角度分析,下列说法错误的是( )
A.I+的立体构型为V形,中心原子的杂化方式为sp3
3
B.ZnCO 中,阴离子立体构型为平面三角形,C原子的杂化方式为sp2
3
C.因 分子间存在氢键,所以 中其沸点最高
D.因金属性K>Na>Mg,所以熔点:KCl>NaCl>MgCl
2
2.(2021·河南宜阳一中检测)下列说法正确的是( )
A.AB (n≥2,且n为整数)型分子中,若中心原子没有孤对电子,则AB 为空间对称结构,属于非极
n n
性分子
B.水很稳定是因为水中含有大量的氢键
C.HO、NH 、CH 分子中的O、N、C分别形成2个、3个、4个键,故O、N、C分别采取sp1、
2 3 4
sp2、sp3杂化
D.配合物[Cu(H O) ]SO 中,中心离子是Cu 2+,配体是SO 2-,配位数是1
2 4 4 4
3.(2021·潍坊市·山东诸城第一中学高三月考)亚铁氰化钾属于欧盟批准使用的食品添加剂,受热易分
解: 3K [Fe(CN) ] 12KCN+Fe C+2(CN) ↑+N ↑+C,下列关于该反应说法错误的是( )
4 6 3 2 2
A.已知 Fe C 晶胞中每个碳原子被 6 个铁原子包围,则铁的配位数是 2
3
B.配合物K[Fe(CN) ]中配位原子是碳原子
4 6
C.(CN) 分子中σ键和π键数目比为 3:4
2
D.Fe2+的最高能层电子排布为 3d6
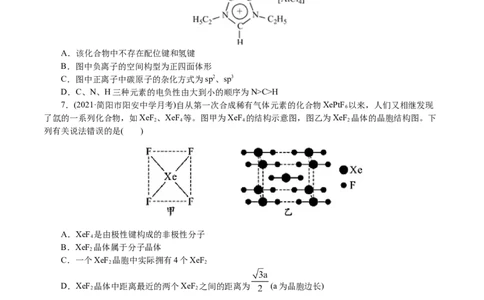
4.(2021·湖北高三零模)在碱性溶液中, 可以与缩二脲形成紫色配离子,其结构如图所示。
下列说法错误的是( )
A.该配离子与水分子形成氢键的原子只有N和O
B.该配离子中铜离子的配位数是4
C.基态Cu原子的价电子排布式是3d104s1
D.该配离子中非金属元素的电负性大小顺序为O>N>C>H
5.(2021·河南高三月考)下列关于N、B所形成化合物的结构和性质的叙述正确的是( )
A.NH -BH 中N和B的杂化方式不同
3 3
B.熔点:NB(原子晶体)>C N(原子晶体)
3 4
C. 含大π键,形成的大π键的电子由N、B提供
D.NH 的沸点明显高于NH 的原因是NH 分子间形成的氢键更强
2 4 3 2 4
5.(2021·威远中学校月考)下列各项叙述中,正确的是
A.镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态B.价电子排布为5s25p1的元素位于第五周期第ⅠA族,是s区元素
C.由图 知酸性:HPO >HClO,因为HPO 中非羟基氧原子数大于次氯酸中非羟基氧原
3 4 3 4
子数
D.元素周期表中s区、d区和ds区的元素都是金属元素
6.(2021·荆州市教育科学研究院期末)离子液体是一种由离子组成的液体,在低温下也能以液态存在,
是一种很有研究价值的溶剂。研究显示最常见的离子液体主要由如图所示正离子和负离子组成,图中正离
子有令人惊奇的稳定性,它的电子在其环外结构中高度离域。下列说法不正确的是
A.该化合物中不存在配位键和氢键
B.图中负离子的空间构型为正四面体形
C.图中正离子中碳原子的杂化方式为sp2、sp3
D.C、N、H三种元素的电负性由大到小的顺序为N>C>H
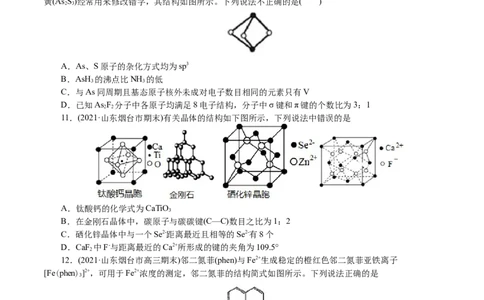
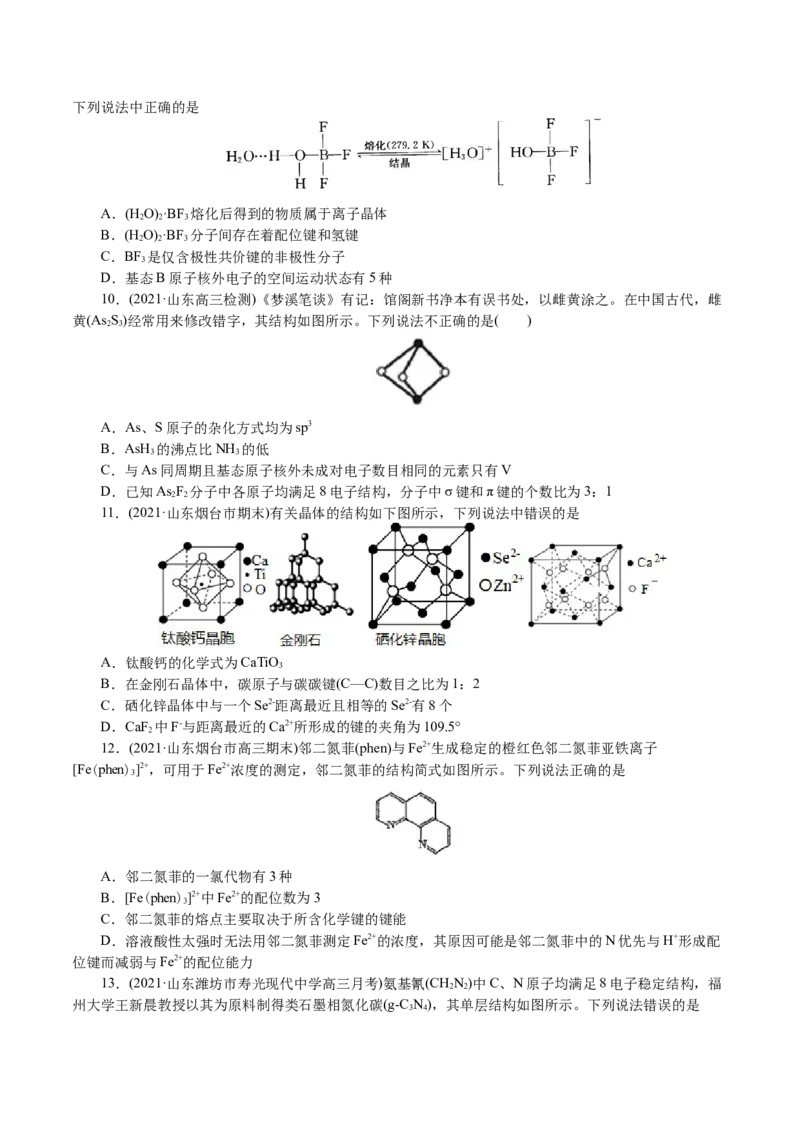
7.(2021·简阳市阳安中学月考)自从第一次合成稀有气体元素的化合物XePtF 以来,人们又相继发现
6
了氙的一系列化合物,如XeF 、XeF 等。图甲为XeF 的结构示意图,图乙为XeF 晶体的晶胞结构图。下
2 4 4 2
列有关说法错误的是( )
A.XeF 是由极性键构成的非极性分子
4
B.XeF 晶体属于分子晶体
2
C.一个XeF 晶胞中实际拥有4个XeF
2 2
D.XeF 晶体中距离最近的两个XeF 之间的距离为 (a为晶胞边长)
2 2
8.(2021·山西吕梁市期末)元素X的基态原子的2p能级有4个电子;元素Y的M层电子运动状态与X
的价电子运动状态相同;元素Z位于第四周期,其基态原子的2价阳离子M层轨道全部排满电子。下列推
断正确的是
A.Y是S元素,基态原子最外层电子排布图为
B.离子晶体ZX、ZY的熔点:ZX>ZY
C.在Y的氢化物HY分子中,Y原子轨道的杂化类型是sp2
2
D.Y与X可形成YX 2-,立体构型为四面体
3
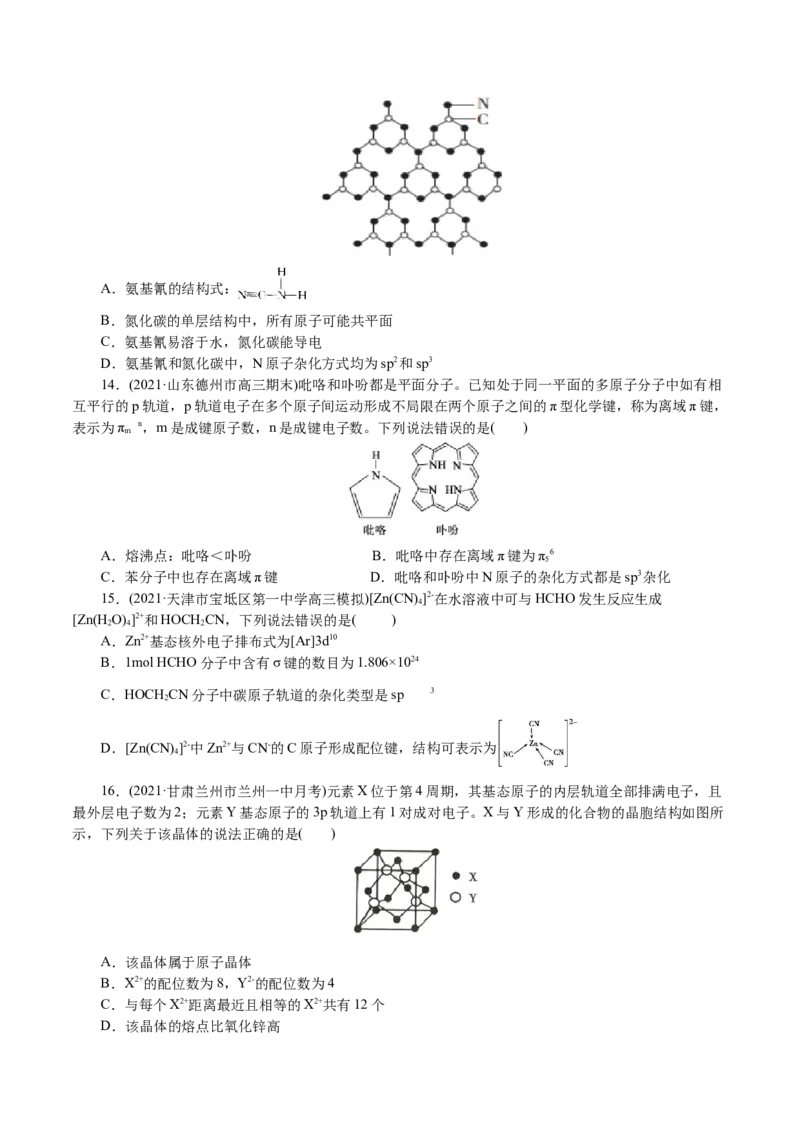
9.(2021·山东泰安市模拟)BF 与一定量的水形成(HO)·BF,一定条件下(HO)·BF 可发生如图转化,
3 2 2 3 2 2 3下列说法中正确的是
A.(HO)·BF 熔化后得到的物质属于离子晶体
2 2 3
B.(HO)·BF 分子间存在着配位键和氢键
2 2 3
C.BF 是仅含极性共价键的非极性分子
3
D.基态B原子核外电子的空间运动状态有5种
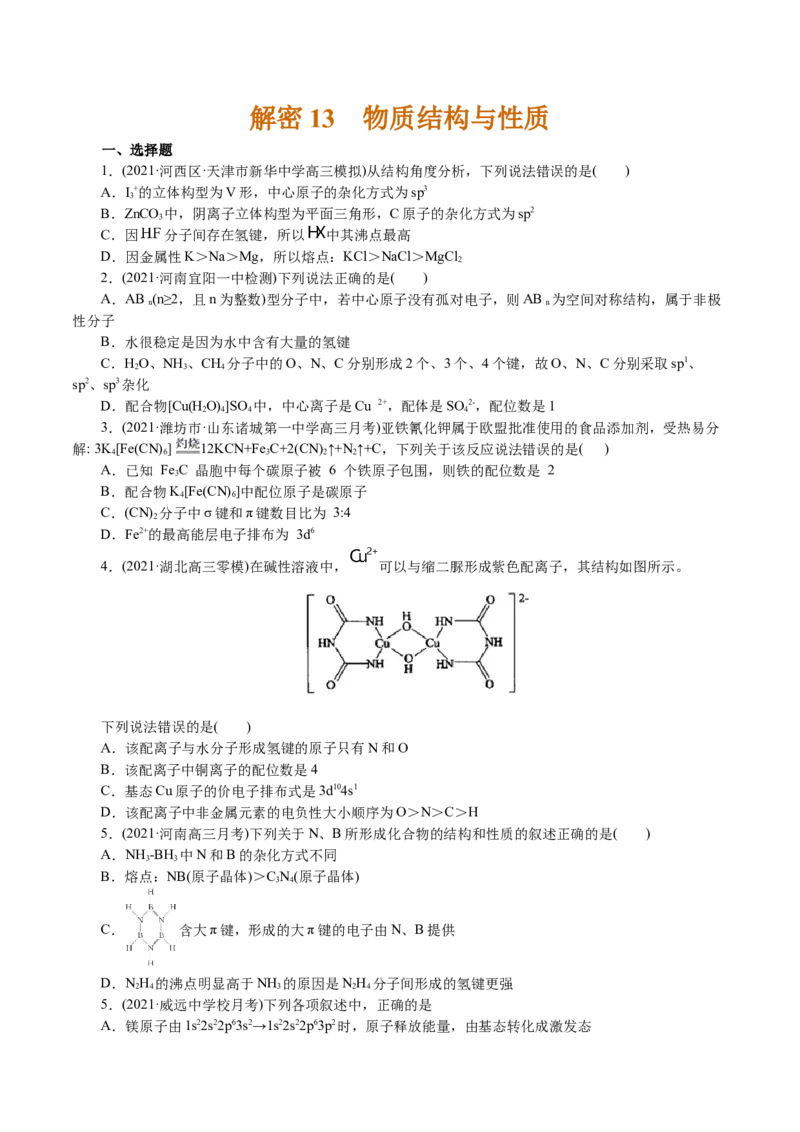
10.(2021·山东高三检测)《梦溪笔谈》有记:馆阁新书净本有误书处,以雌黄涂之。在中国古代,雌
黄(As S)经常用来修改错字,其结构如图所示。下列说法不正确的是( )
2 3
A.As、S原子的杂化方式均为sp3
B.AsH 的沸点比NH 的低
3 3
C.与As同周期且基态原子核外未成对电子数目相同的元素只有V
D.已知As F 分子中各原子均满足8电子结构,分子中σ键和π键的个数比为3:1
2 2
11.(2021·山东烟台市期末)有关晶体的结构如下图所示,下列说法中错误的是
A.钛酸钙的化学式为CaTiO
3
B.在金刚石晶体中,碳原子与碳碳键(C—C)数目之比为1:2
C.硒化锌晶体中与一个Se2-距离最近且相等的Se2-有8个
D.CaF 中F-与距离最近的Ca2+所形成的键的夹角为109.5°
2
12.(2021·山东烟台市高三期末)邻二氮菲(phen)与Fe2+生成稳定的橙红色邻二氮菲亚铁离子
[Fe(phen)]2+,可用于Fe2+浓度的测定,邻二氮菲的结构简式如图所示。下列说法正确的是
3
A.邻二氮菲的一氯代物有3种
B.[Fe(phen)]2+中Fe2+的配位数为3
3
C.邻二氮菲的熔点主要取决于所含化学键的键能
D.溶液酸性太强时无法用邻二氮菲测定Fe2+的浓度,其原因可能是邻二氮菲中的N优先与H+形成配
位键而减弱与Fe2+的配位能力
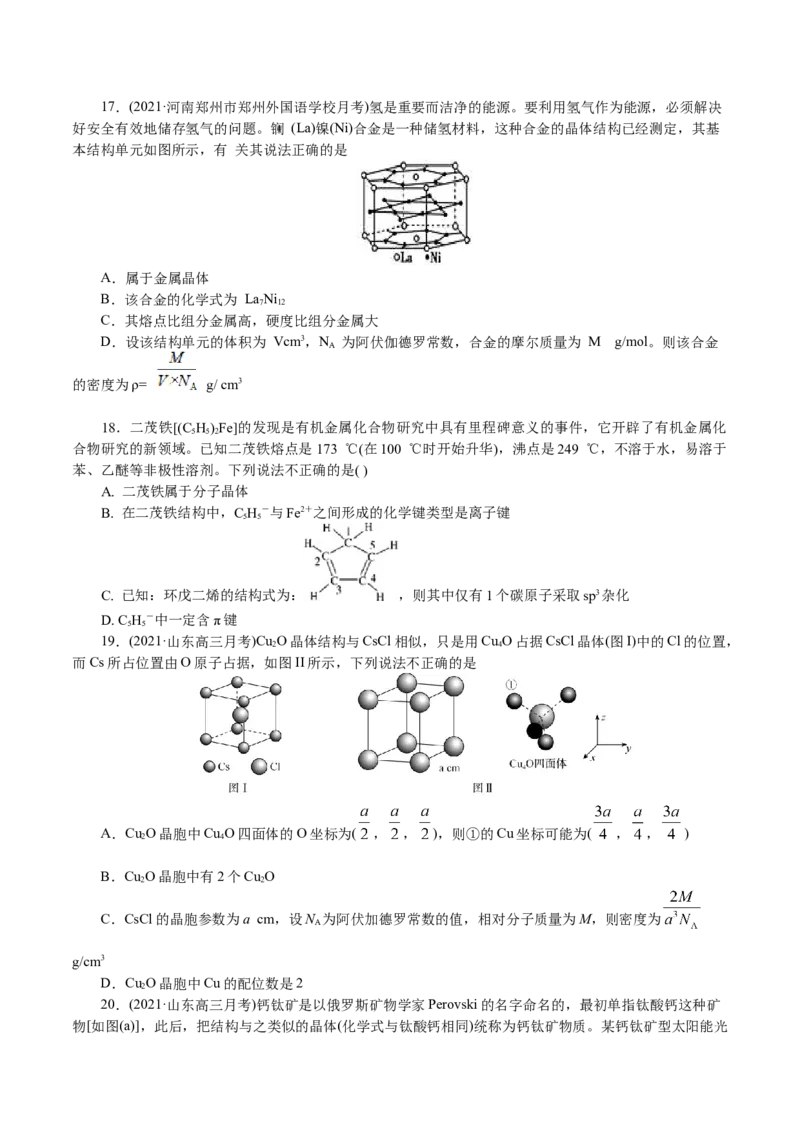
13.(2021·山东潍坊市寿光现代中学高三月考)氨基氰(CHN)中C、N原子均满足8电子稳定结构,福
2 2
州大学王新晨教授以其为原料制得类石墨相氮化碳(g-C N),其单层结构如图所示。下列说法错误的是
3 4A.氨基氰的结构式:
B.氮化碳的单层结构中,所有原子可能共平面
C.氨基氰易溶于水,氮化碳能导电
D.氨基氰和氮化碳中,N原子杂化方式均为sp2和sp3
14.(2021·山东德州市高三期末)吡咯和卟吩都是平面分子。已知处于同一平面的多原子分子中如有相
互平行的p轨道,p轨道电子在多个原子间运动形成不局限在两个原子之间的π型化学键,称为离域π键,
表示为π n,m是成键原子数,n是成键电子数。下列说法错误的是( )
m
A.熔沸点:吡咯<卟吩 B.吡咯中存在离域π键为π 6
5
C.苯分子中也存在离域π键 D.吡咯和卟吩中N原子的杂化方式都是sp3杂化
15.(2021·天津市宝坻区第一中学高三模拟)[Zn(CN) ]2-在水溶液中可与HCHO发生反应生成
4
[Zn(HO) ]2+和HOCH CN,下列说法错误的是( )
2 4 2
A.Zn2+基态核外电子排布式为[Ar]3d10
B.1mol HCHO分子中含有σ键的数目为1.806×1024
C.HOCH CN分子中碳原子轨道的杂化类型是sp 3
2
D.[Zn(CN) ]2-中Zn2+与CN-的C原子形成配位键,结构可表示为
4
16.(2021·甘肃兰州市兰州一中月考)元素X位于第4周期,其基态原子的内层轨道全部排满电子,且
最外层电子数为2;元素Y基态原子的3p轨道上有1对成对电子。X与Y形成的化合物的晶胞结构如图所
示,下列关于该晶体的说法正确的是( )
A.该晶体属于原子晶体
B.X2+的配位数为8,Y2-的配位数为4
C.与每个X2+距离最近且相等的X2+共有12个
D.该晶体的熔点比氧化锌高17.(2021·河南郑州市郑州外国语学校月考)氢是重要而洁净的能源。要利用氢气作为能源,必须解决
好安全有效地储存氢气的问题。镧 (La)镍(Ni)合金是一种储氢材料,这种合金的晶体结构已经测定,其基
本结构单元如图所示,有 关其说法正确的是
A.属于金属晶体
B.该合金的化学式为 LaNi
7 12
C.其熔点比组分金属高,硬度比组分金属大
D.设该结构单元的体积为 Vcm3,N 为阿伏伽德罗常数,合金的摩尔质量为 M g/mol。则该合金
A
的密度为ρ= g/ cm3
18.二茂铁[(C H)Fe]的发现是有机金属化合物研究中具有里程碑意义的事件,它开辟了有机金属化
5 5 2
合物研究的新领域。已知二茂铁熔点是173 ℃(在100 ℃时开始升华),沸点是249 ℃,不溶于水,易溶于
苯、乙醚等非极性溶剂。下列说法不正确的是( )
A. 二茂铁属于分子晶体
B. 在二茂铁结构中,C H-与Fe2+之间形成的化学键类型是离子键
5 5
C. 已知:环戊二烯的结构式为: ,则其中仅有1个碳原子采取sp3杂化
D. C H-中一定含π键
5 5
19.(2021·山东高三月考)Cu O晶体结构与CsCl相似,只是用Cu O占据CsCl晶体(图I)中的Cl的位置,
2 4
而Cs所占位置由O原子占据,如图II所示,下列说法不正确的是
A.Cu O晶胞中Cu O四面体的O坐标为( , , ),则①的Cu坐标可能为( , , )
2 4
B.Cu O晶胞中有2个Cu O
2 2
C.CsCl的晶胞参数为a cm,设N 为阿伏加德罗常数的值,相对分子质量为M,则密度为
A
g/cm3
D.Cu O晶胞中Cu的配位数是2
2
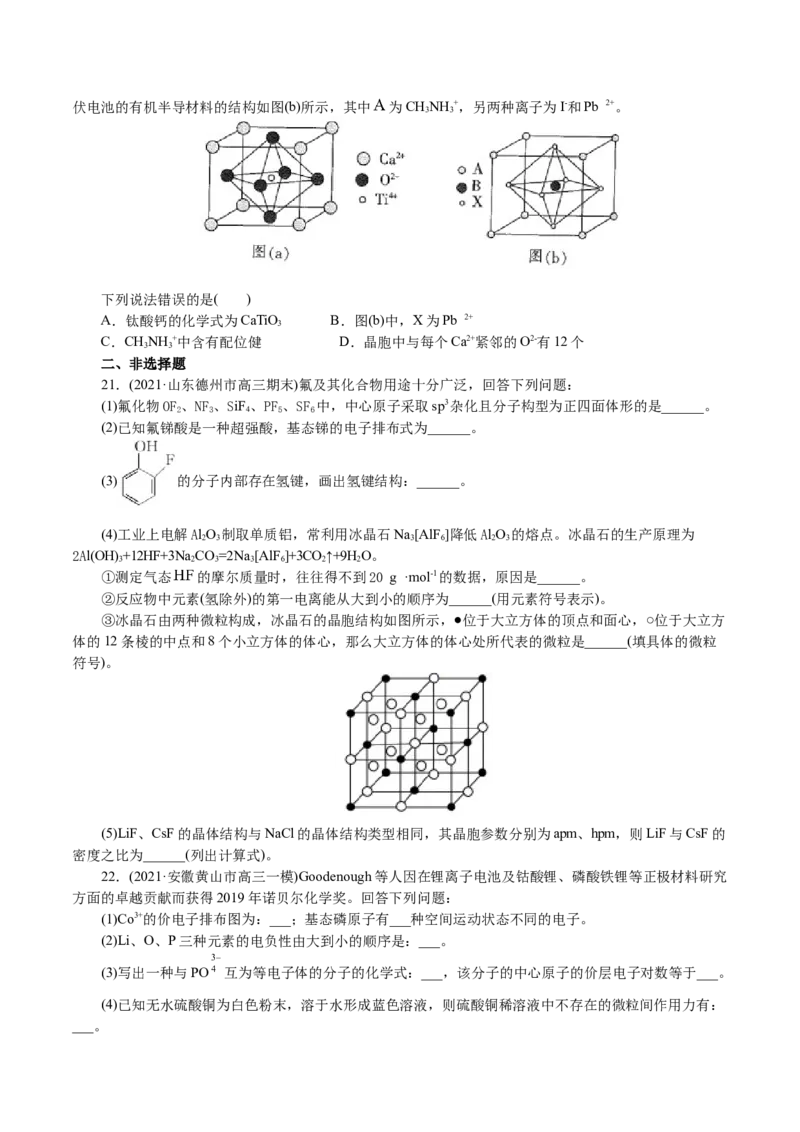
20.(2021·山东高三月考)钙钛矿是以俄罗斯矿物学家Perovski的名字命名的,最初单指钛酸钙这种矿
物[如图(a)],此后,把结构与之类似的晶体(化学式与钛酸钙相同)统称为钙钛矿物质。某钙钛矿型太阳能光伏电池的有机半导材料的结构如图(b)所示,其中 为CHNH +,另两种离子为I-和Pb 2+。
3 3
下列说法错误的是( )
A.钛酸钙的化学式为CaTiO B.图(b)中,X为Pb 2+
3
C.CHNH +中含有配位健 D.晶胞中与每个Ca2+紧邻的O2-有12个
3 3
二、非选择题
21.(2021·山东德州市高三期末)氟及其化合物用途十分广泛,回答下列问题:
(1)氟化物OF、NF、SiF、PF、SF 中,中心原子采取sp3杂化且分子构型为正四面体形的是______。
2 3 4 5 6
(2)已知氟锑酸是一种超强酸,基态锑的电子排布式为______。
(3) 的分子内部存在氢键,画出氢键结构:______。
(4)工业上电解AlO 制取单质铝,常利用冰晶石Na[AlF]降低AlO 的熔点。冰晶石的生产原理为
2 3 3 6 2 3
2Al(OH) +12HF+3NaCO=2Na[AlF]+3CO ↑+9H O。
3 2 3 3 6 2 2
①测定气态 的摩尔质量时,往往得不到20 g ·mol-1的数据,原因是______。
②反应物中元素(氢除外)的第一电离能从大到小的顺序为______(用元素符号表示)。
③冰晶石由两种微粒构成,冰晶石的晶胞结构如图所示,●位于大立方体的顶点和面心,○位于大立方
体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处所代表的微粒是______(填具体的微粒
符号)。
(5)LiF、CsF的晶体结构与NaCl的晶体结构类型相同,其晶胞参数分别为apm、hpm,则LiF与CsF的
密度之比为______(列出计算式)。
22.(2021·安徽黄山市高三一模)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究
方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)Co3+的价电子排布图为:___;基态磷原子有___种空间运动状态不同的电子。
(2)Li、O、P三种元素的电负性由大到小的顺序是:___。
(3)写出一种与PO 互为等电子体的分子的化学式:___,该分子的中心原子的价层电子对数等于___。
(4)已知无水硫酸铜为白色粉末,溶于水形成蓝色溶液,则硫酸铜稀溶液中不存在的微粒间作用力有:
___。A.配位键 B.金属键 C.离子键 D.共价键 E.氢键 F.范德华力
(5)N和P是同主族元素,但是NH 分子中的键角大于PH 分子中的键角,原因是:___。
3 3
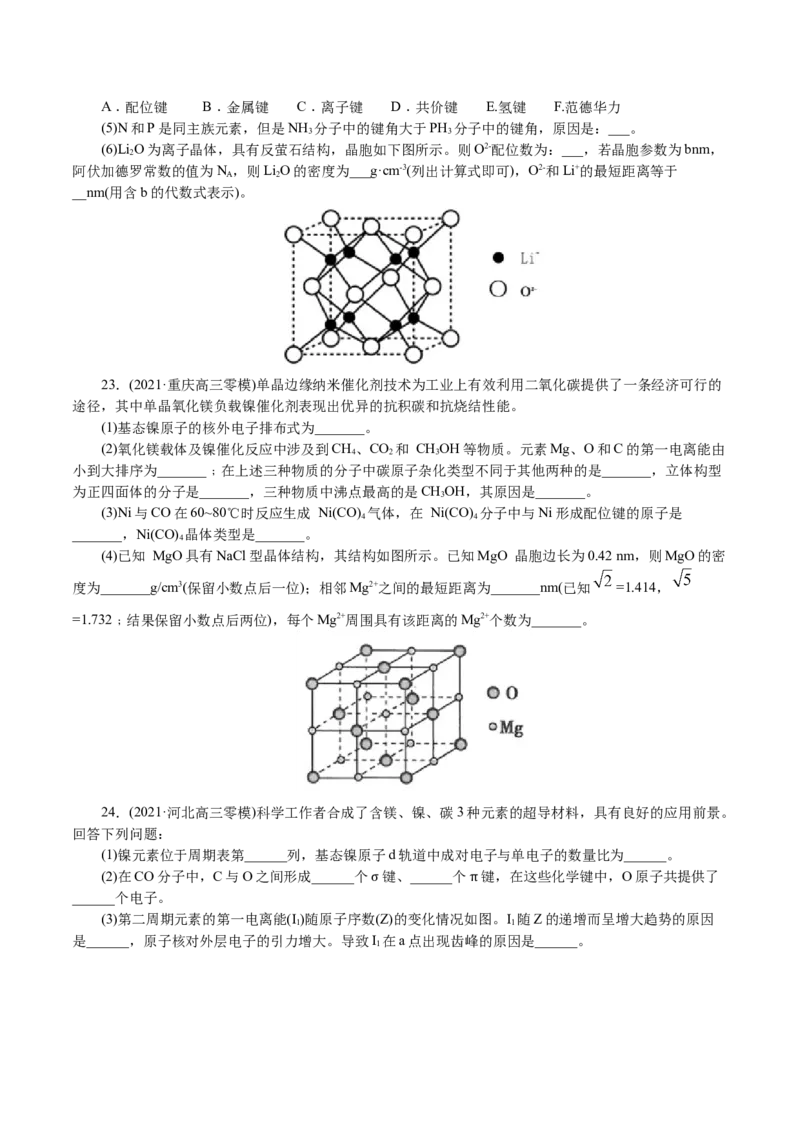
(6)Li O为离子晶体,具有反萤石结构,晶胞如下图所示。则O2-配位数为:___,若晶胞参数为bnm,
2
阿伏加德罗常数的值为N ,则LiO的密度为___g·cm-3(列出计算式即可),O2-和Li+的最短距离等于
A 2
__nm(用含b的代数式表示)。
23.(2021·重庆高三零模)单晶边缘纳米催化剂技术为工业上有效利用二氧化碳提供了一条经济可行的
途径,其中单晶氧化镁负载镍催化剂表现出优异的抗积碳和抗烧结性能。
(1)基态镍原子的核外电子排布式为_______。
(2)氧化镁载体及镍催化反应中涉及到CH、CO 和 CHOH等物质。元素Mg、O和C的第一电离能由
4 2 3
小到大排序为_______﹔在上述三种物质的分子中碳原子杂化类型不同于其他两种的是_______,立体构型
为正四面体的分子是_______,三种物质中沸点最高的是CHOH,其原因是_______。
3
(3)Ni与CO在60~80℃时反应生成 Ni(CO) 气体,在 Ni(CO) 分子中与Ni形成配位键的原子是
4 4
_______,Ni(CO) 晶体类型是_______。
4
(4)已知 MgO具有NaCl型晶体结构,其结构如图所示。已知MgО 晶胞边长为0.42 nm,则MgO的密
度为_______g/cm3(保留小数点后一位);相邻Mg2+之间的最短距离为_______nm(已知 =1.414,
=1.732﹔结果保留小数点后两位),每个Mg2+周围具有该距离的Mg2+个数为_______。
24.(2021·河北高三零模)科学工作者合成了含镁、镍、碳3种元素的超导材料,具有良好的应用前景。
回答下列问题:
(1)镍元素位于周期表第______列,基态镍原子d轨道中成对电子与单电子的数量比为______。
(2)在CO分子中,C与O之间形成______个 键、______个 键,在这些化学键中,O原子共提供了
______个电子。
σ π
(3)第二周期元素的第一电离能(I)随原子序数(Z)的变化情况如图。I 随Z的递增而呈增大趋势的原因
1 1
是______,原子核对外层电子的引力增大。导致I 在a点出现齿峰的原因是______。
1(4)下列分子或离子与CO 具有相同类型化学键和立体构型的是______(填标号)。
2
A.SO B.OCN- C.HF - D.NO +
2 2 2
(5)过渡金属与O形成羰基配合物时,每个CO分子向中心原子提供2个电子,最终使中心原子的电子
总数与同周期的稀有气体原子相同,称为有效原子序数规则。根据此规则推断,镍与CO形成的羰基配合
物N i (CO) 中,x =______。
x
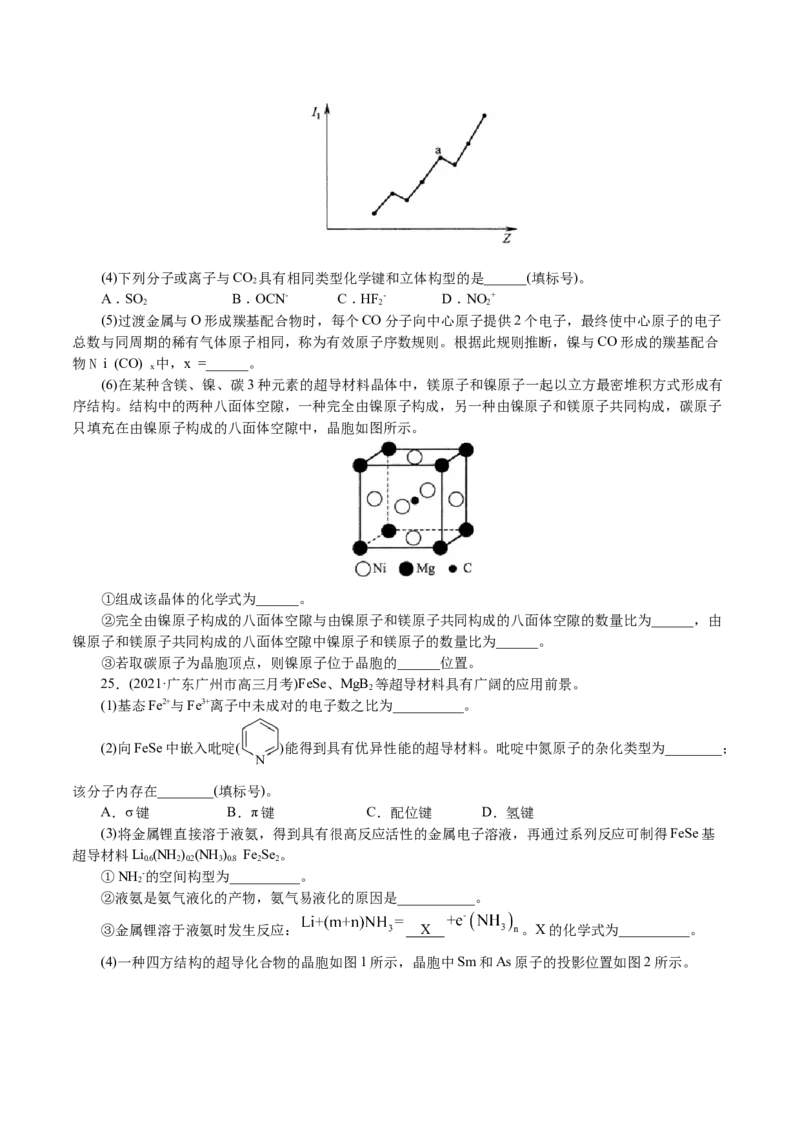
(6)在某种含镁、镍、碳3种元素的超导材料晶体中,镁原子和镍原子一起以立方最密堆积方式形成有
序结构。结构中的两种八面体空隙,一种完全由镍原子构成,另一种由镍原子和镁原子共同构成,碳原子
只填充在由镍原子构成的八面体空隙中,晶胞如图所示。
①组成该晶体的化学式为______。
②完全由镍原子构成的八面体空隙与由镍原子和镁原子共同构成的八面体空隙的数量比为______,由
镍原子和镁原子共同构成的八面体空隙中镍原子和镁原子的数量比为______。
③若取碳原子为晶胞顶点,则镍原子位于晶胞的______位置。
25.(2021·广东广州市高三月考)FeSe、MgB 等超导材料具有广阔的应用前景。
2
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为__________。
(2)向FeSe中嵌入吡啶( )能得到具有优异性能的超导材料。吡啶中氮原子的杂化类型为________;
该分子内存在________(填标号)。
A.σ键 B.π键 C.配位键 D.氢键
(3)将金属锂直接溶于液氨,得到具有很高反应活性的金属电子溶液,再通过系列反应可制得FeSe基
超导材料Li (NH ) (NH ) FeSe。
0.6 2 0.2 3 0.8 2 2
①NH -的空间构型为__________。
2
②液氨是氨气液化的产物,氨气易液化的原因是___________。
③金属锂溶于液氨时发生反应: X 。X的化学式为__________。
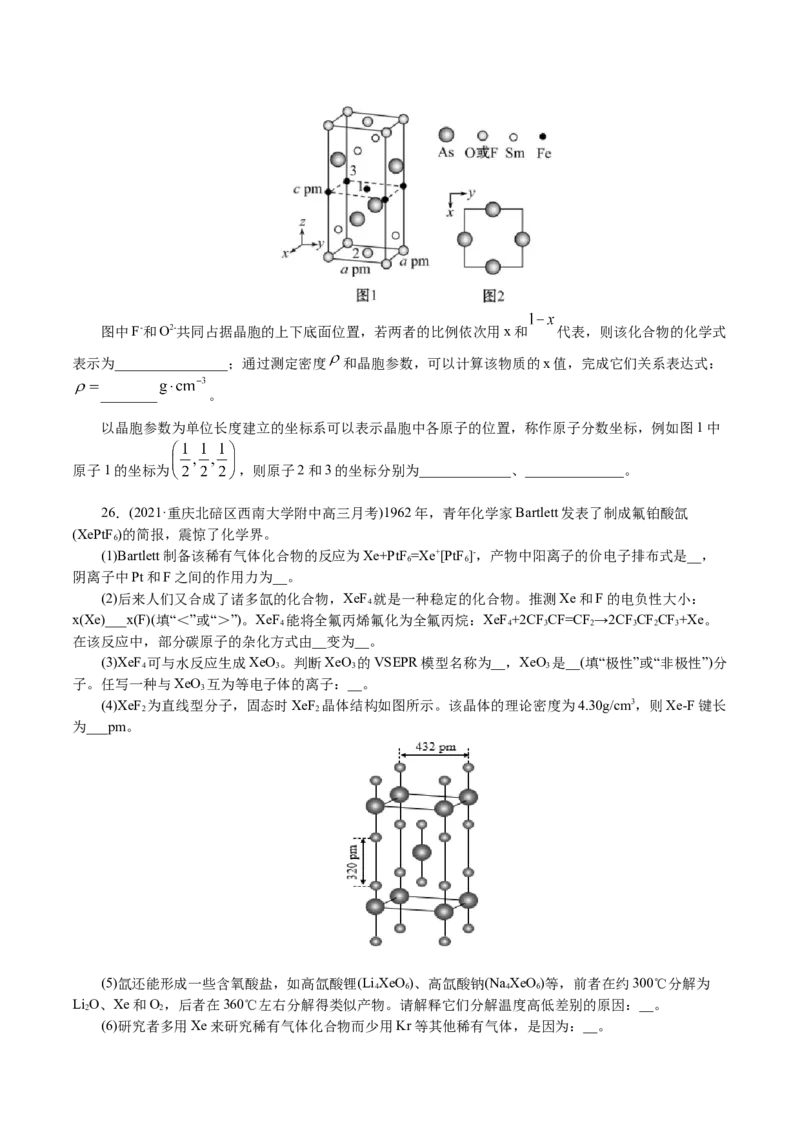
(4)一种四方结构的超导化合物的晶胞如图1所示,晶胞中Sm和As原子的投影位置如图2所示。图中F-和O2-共同占据晶胞的上下底面位置,若两者的比例依次用x和 代表,则该化合物的化学式
表示为________________;通过测定密度 和晶胞参数,可以计算该物质的x值,完成它们关系表达式:
________ 。
以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中
原子1的坐标为 ,则原子2和3的坐标分别为_____________、______________。
26.(2021·重庆北碚区西南大学附中高三月考)1962年,青年化学家Bartlett发表了制成氟铂酸氙
(XePtF )的简报,震惊了化学界。
6
(1)Bartlett制备该稀有气体化合物的反应为Xe+PtF =Xe+[PtF]-,产物中阳离子的价电子排布式是__,
6 6
阴离子中Pt和F之间的作用力为__。
(2)后来人们又合成了诸多氙的化合物,XeF 就是一种稳定的化合物。推测Xe和F的电负性大小:
4
x(Xe)___x(F)(填“<”或“>”)。XeF 能将全氟丙烯氟化为全氟丙烷:XeF +2CF CF=CF →2CFCFCF+Xe。
4 4 3 2 3 2 3
在该反应中,部分碳原子的杂化方式由__变为__。
(3)XeF 可与水反应生成XeO 。判断XeO 的VSEPR模型名称为__,XeO 是__(填“极性”或“非极性”)分
4 3 3 3
子。任写一种与XeO 互为等电子体的离子:__。
3
(4)XeF 为直线型分子,固态时XeF 晶体结构如图所示。该晶体的理论密度为4.30g/cm3,则Xe-F键长
2 2
为___pm。
(5)氙还能形成一些含氧酸盐,如高氙酸锂(Li XeO )、高氙酸钠(Na XeO )等,前者在约300℃分解为
4 6 4 6
LiO、Xe和O,后者在360℃左右分解得类似产物。请解释它们分解温度高低差别的原因:__。
2 2
(6)研究者多用Xe来研究稀有气体化合物而少用Kr等其他稀有气体,是因为:__。