文档内容
贵州新高考协作体 2023 届高三上学期入学质量监测
理科综合(化学)
可能用到的相对原子质量:H-1 O-16 Cl-35.5 K-39 Cr-52 Fe-56 Cu-64
一、选择题:本题共7小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求
的。
7.化学与生活密切相关,下列叙述不正确的是( )
A.葡萄酒中加入少量 可以起到杀菌和抗氧化作用
B.日常生活中,常用小苏打做食用碱
C.由于 易溶于水,可用于冷藏物品
D.漂白粉可以用来漂白棉、麻和纸张
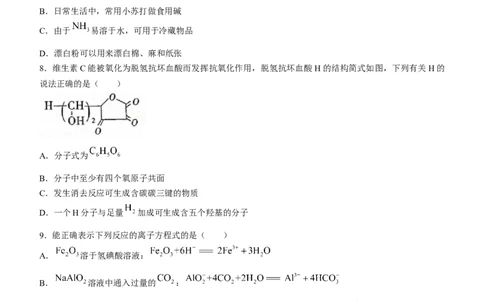
8.维生素C能被氧化为脱氢抗坏血酸而发挥抗氧化作用,脱氢抗坏血酸H的结构简式如图,下列有关H的
说法正确的是( )
A.分子式为
B.分子中至少有四个氧原子共面
C.发生消去反应可生成含碳碳三键的物质
D.一个H分子与足量 加成可生成含五个羟基的分子
9.能正确表示下列反应的离子方程式的是( )
A. 溶于氢碘酸溶液:
B. 溶液中通入过量的 :
C. 溶液与过量 溶液混合:
D.铝片放入NaOH溶液中:
10.某实验小组用铜和 溶液来制备 溶液,同时获得电能,装置如图所示,其中M、N为电解质,
下列说法正确的是( )A.电极A为铜
B.a为阴离子交换膜,电解质N为
C.理论上每生成1molN时会消耗1molM
D.当B电极质量减少6.4克,则N溶液质量增加6.4克
11. 为阿伏加德罗常数的值,下列说法正确的是( )
A.0℃101kPa下,11.2L 中原子的数目为2
B.25℃pH=13的NaOH溶液中, 的数目为0.1
C.2molNO和1mol 在密闭容器中充分反应后,分子数目为2
D.Na与 反应生成1mol 和 混合物,共转移电子的数目为2
12.w、x、y、z是原子序数依次增大的短周期主族元素,其最外层电子数之和为21。w与y最外层电子数相
同,z最外层电子数与w的核外电子数相等。下列说法正确的是( )
A.y单质与x的氢化物可能发生置换反应 B.原子半径不可能:
C.最高价含氧酸的酸性: D.w的氢化物不可能存在非极性共价键
13.下列各项实验操作得出的现象及结论均正确的是( )
实验操作 现象 结论
A 将乙烯和甲烷分别通入酸性 前者褪色,后者无
可用酸性 溶液除
明显变化
溶液 去甲烷中含的乙烯
B 室温下,向 NaOH 溶液中加入酸 HA为强酸
溶液
HA,充分反应后测其溶液的pH
C 相 同 温 度 下 , 分 别 检 测 pH前者小于后者
溶液的水解程度:
和 溶 1mol/L>0.1mol/L。
液的pH
D 用洁净的试管取少量的待测液,先 加入稀盐酸无现
原待测液中含有
加入稀盐酸,再加入 溶液 象,加入 溶
液有白色沉淀
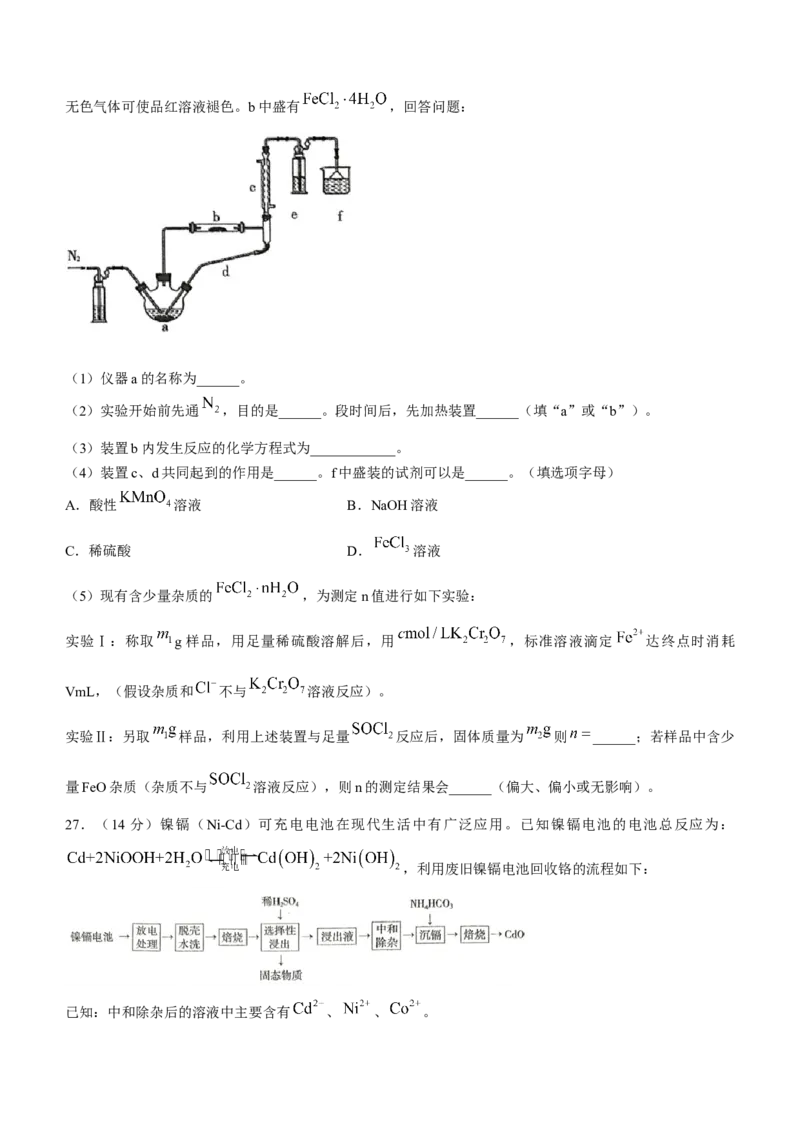
26.(14分)实验室利用 和亚硫酰氯( )制备无水 的装置如图所示(加热及夹
持装置略)。已知 沸点为76℃,遇水剧烈反应,液面上会产生白雾,并有刺激性气味的气体逸出,该无色气体可使品红溶液褪色。b中盛有 ,回答问题:
(1)仪器a的名称为______。
(2)实验开始前先通 ,目的是______。段时间后,先加热装置______(填“a”或“b”)。
(3)装置b内发生反应的化学方程式为____________。
(4)装置c、d共同起到的作用是______。f中盛装的试剂可以是______。(填选项字母)
A.酸性 溶液 B.NaOH溶液
C.稀硫酸 D. 溶液
(5)现有含少量杂质的 ,为测定n值进行如下实验:
实验Ⅰ:称取 g样品,用足量稀硫酸溶解后,用 ,标准溶液滴定 达终点时消耗
VmL,(假设杂质和 不与 溶液反应)。
实验Ⅱ:另取 样品,利用上述装置与足量 反应后,固体质量为 则 ______;若样品中含少
量FeO杂质(杂质不与 溶液反应),则n的测定结果会______(偏大、偏小或无影响)。
27.(14 分)镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知镍镉电池的电池总反应为:
,利用废旧镍镉电池回收铬的流程如下:
已知:中和除杂后的溶液中主要含有 、 、 。回答下列问题:
(1)NiOOH中,Ni的化合价为:______。
(2)写出“焙烧”过程中含镍物质变化的化学反应方程式:______。
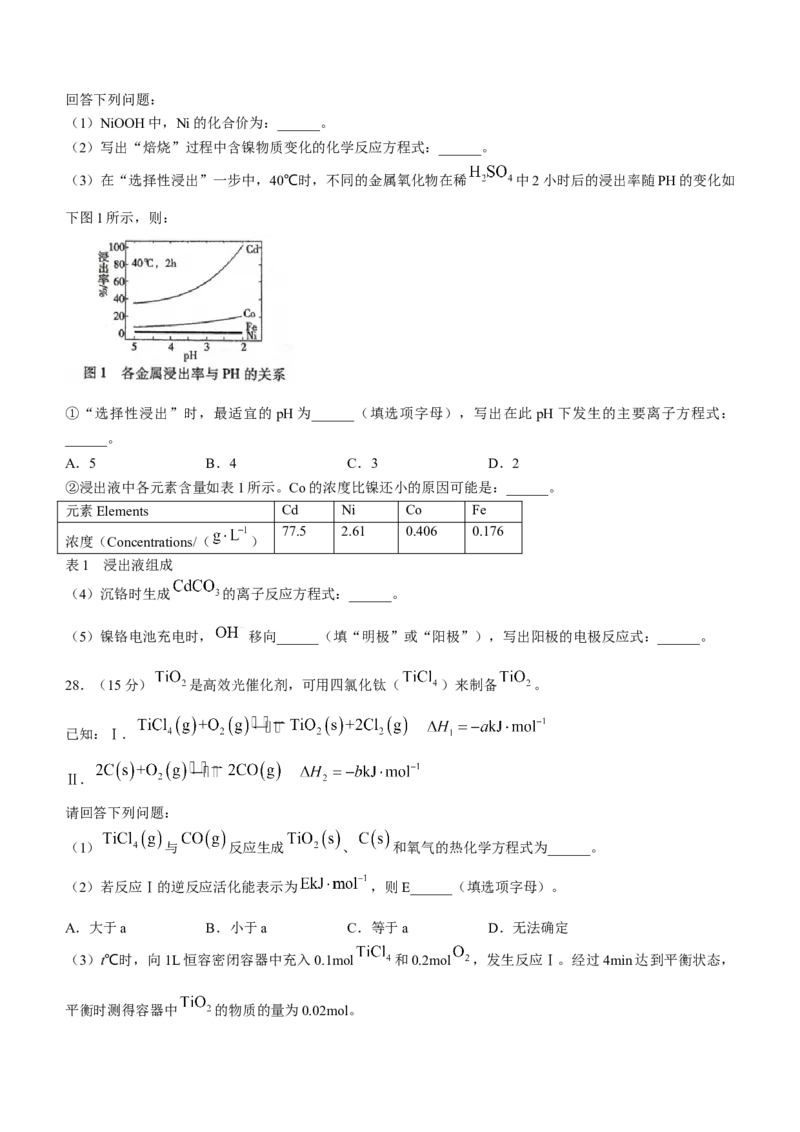
(3)在“选择性浸出”一步中,40℃时,不同的金属氧化物在稀 中2小时后的浸出率随PH的变化如
下图1所示,则:
①“选择性浸出”时,最适宜的pH为______(填选项字母),写出在此 pH下发生的主要离子方程式:
______。
A.5 B.4 C.3 D.2
②浸出液中各元素含量如表1所示。Co的浓度比镍还小的原因可能是:______。
元素Elements Cd Ni Co Fe
77.5 2.61 0.406 0.176
浓度(Concentrations/( )
表1 浸出液组成
(4)沉铬时生成 的离子反应方程式:______。
(5)镍铬电池充电时, 移向______(填“明极”或“阳极”),写出阳极的电极反应式:______。
28.(15分) 是高效光催化剂,可用四氯化钛( )来制备 。
已知:Ⅰ.
Ⅱ.
请回答下列问题:
(1) 与 反应生成 、 和氧气的热化学方程式为______。
(2)若反应Ⅰ的逆反应活化能表示为 ,则E______(填选项字母)。
A.大于a B.小于a C.等于a D.无法确定
(3)t℃时,向1L恒容密闭容器中充入0.1mol 和0.2mol ,发生反应Ⅰ。经过4min达到平衡状态,
平衡时测得容器中 的物质的量为0.02mol。①0~4min内 的反应速率 ______。
② 的平衡转化率 ______。
③下列措施即可加快反应速率,又能增大 平衡转化率的是______(填选项字母)。
A.缩小容器容积 B.加入催化剂
C.分离出部分 D.增大 浓度
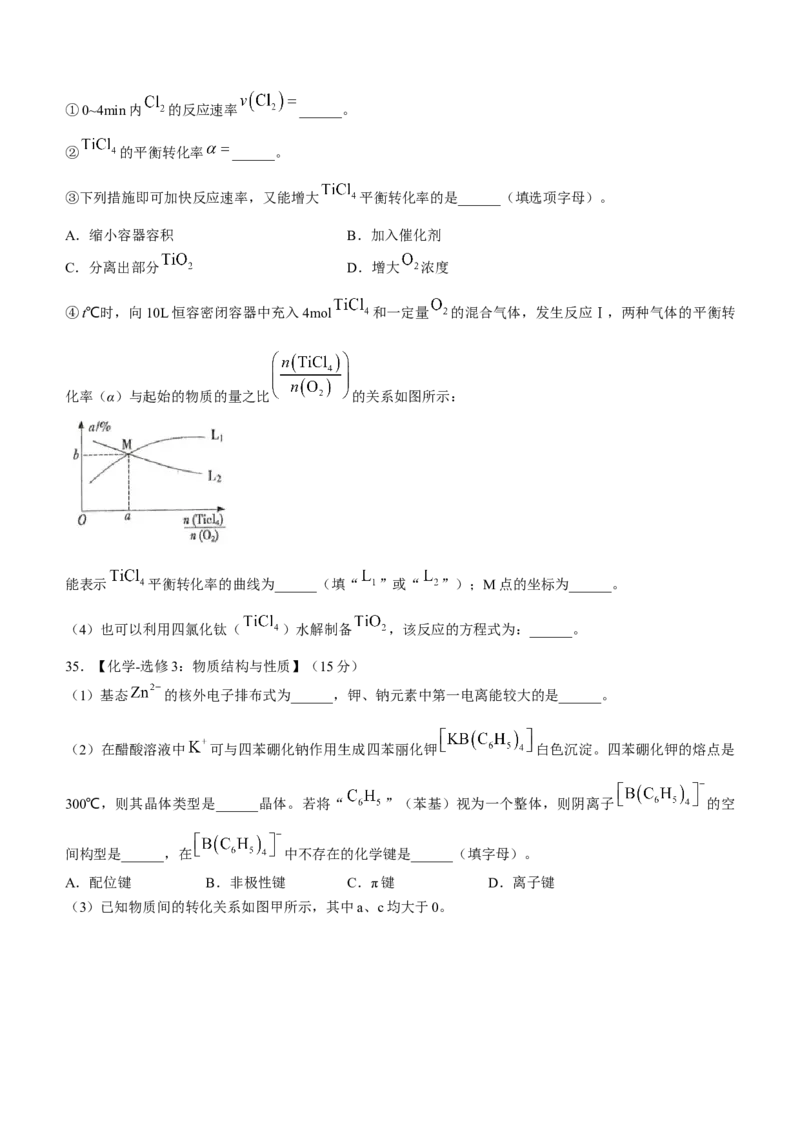
④t℃时,向10L恒容密闭容器中充入4mol 和一定量 的混合气体,发生反应Ⅰ,两种气体的平衡转
化率(α)与起始的物质的量之比 的关系如图所示:
能表示 平衡转化率的曲线为______(填“ ”或“ ”);M点的坐标为______。
(4)也可以利用四氯化钛( )水解制备 ,该反应的方程式为:______。
35.【化学-选修3:物质结构与性质】(15分)
(1)基态 的核外电子排布式为______,钾、钠元素中第一电离能较大的是______。
(2)在醋酸溶液中 可与四苯硼化钠作用生成四苯丽化钾 白色沉淀。四苯硼化钾的熔点是
300℃,则其晶体类型是______晶体。若将“ ”(苯基)视为一个整体,则阴离子 的空
间构型是______,在 中不存在的化学键是______(填字母)。
A.配位键 B.非极性键 C.π键 D.离子键
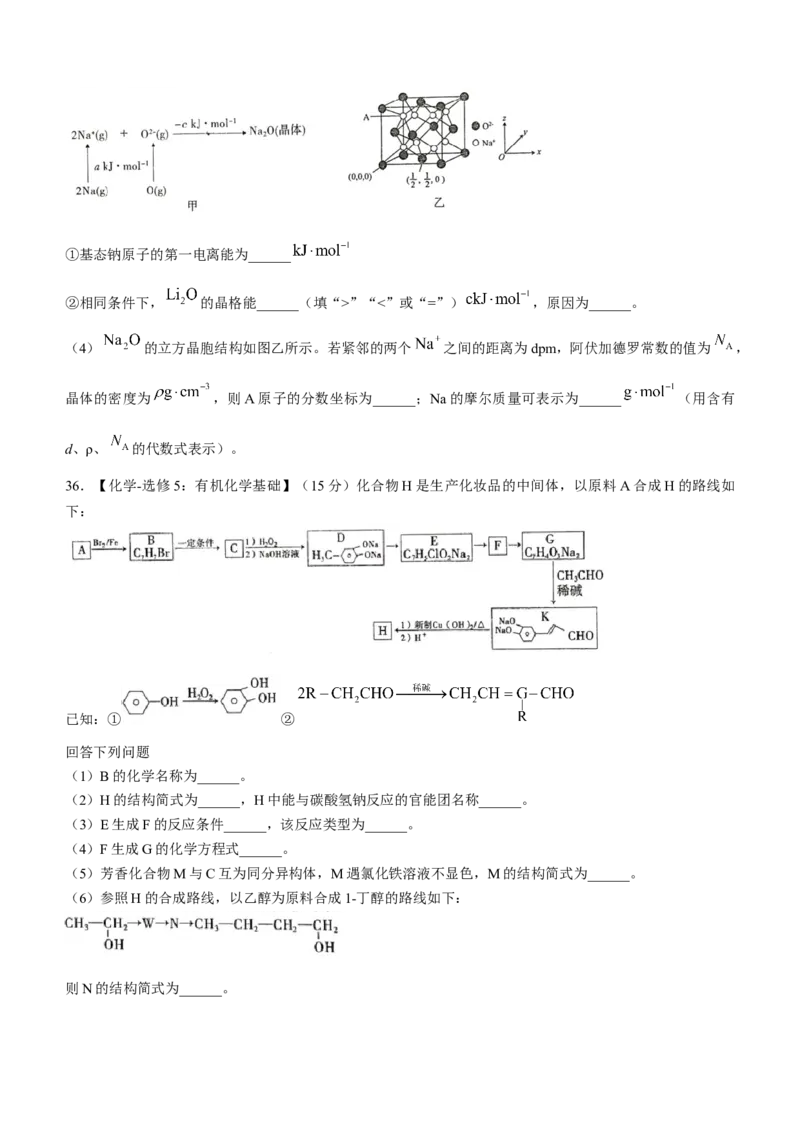
(3)已知物质间的转化关系如图甲所示,其中a、c均大于0。①基态钠原子的第一电离能为______
②相同条件下, 的晶格能______(填“>”“<”或“=”) ,原因为______。
(4) 的立方晶胞结构如图乙所示。若紧邻的两个 之间的距离为dpm,阿伏加德罗常数的值为 ,
晶体的密度为 ,则A原子的分数坐标为______;Na的摩尔质量可表示为______ (用含有
d、ρ、 的代数式表示)。
36.【化学-选修5:有机化学基础】(15分)化合物H是生产化妆品的中间体,以原料A合成H的路线如
下:
已知:① ②
回答下列问题
(1)B的化学名称为______。
(2)H的结构简式为______,H中能与碳酸氢钠反应的官能团名称______。
(3)E生成F的反应条件______,该反应类型为______。
(4)F生成G的化学方程式______。
(5)芳香化合物M与C互为同分异构体,M遇氯化铁溶液不显色,M的结构简式为______。
(6)参照H的合成路线,以乙醇为原料合成1-丁醇的路线如下:
则N的结构简式为______。贵州新高考协作体 2023 届上学期入学质量监测
化学参考答案
7 8 9 10 11 12 13
C C D B D A D
26.(1)三颈烧瓶(或三口烧瓶)(1分)
(2)排除装置内空气,防止产品被氧气氧化 a(1分)
(3)
(4)冷凝回流 BD
(5) 偏小
27.(1)+3(1分) (2)
(3)①D
②原料中镍的含量比钴多,故钴的浸出率虽然高于镍的浸出率,但浸出液中浓度仍然比镍低。
(4)
(5)阳极(1分)
28.(1)
(2)A(3)① ②20% ③D
(3)①. ②.20% ③.D ④.
(4) 或
35.(1) (1分) 钠(Na)(1分)
(2)分子(1分) 正四面体(2分) D(1分)(3) (2分) >(1分) 和 均为离子晶体, 的半径大于 的半径,故
的晶格能小于 的晶格能(2分)
(4) (2分) (2分)
36.(除标注外,每空2分,共15分)
(1)对溴甲苯(或4-溴甲苯)
(2) 羧基(1分)
(3)NaOH/水、加热 取代反应或水解反应
(4)
(5)
(6)