文档内容
题型 20 物质结构与性质基础
目录
.....................................................................................................................................1
【考向一】原子核外电子的排布......................................................................................................................1
【考向二】元素的电离能、电负性及微粒半径的大小比较..........................................................................4
【考向三】“两大理论”与微粒构型..............................................................................................................6
【考向四】分子性质与微粒作用....................................................................................................................10
【考向五】成键方式、晶体类型的判断........................................................................................................12
【考向六】晶体化学式及粒子数确定............................................................................................................15
【考向七】原子分数坐标分析方法................................................................................................................18
【考向八】有关晶胞参数的计算....................................................................................................................22
【考向九】解释原因类简答题........................................................................................................................27
...................................................................................................................................31
【考向一】原子核外电子的排布
【典例1】短周期元素R基态原子最外层的p能级上有2个未成对电子。下列关于基态R原子的描述正确
的是
A.基态R原子核外电子的电子云轮廓图有两种:球形和哑铃形
B.基态R原子的价层电子排布式为ns2np2(n=2或3)
C.基态R原子的原子轨道总数为9
D.基态R原子的轨道表示式为
【答案】A
【分析】由“短周期元素R基态原子最外层的p能级上有2个未成对电子”可知,可能有两种情况:p能
级上只有2个电子,R为第ⅣA族元素,C或Si;p能级上有4个电子,R为第ⅥA族元素,O或S,由此
可知:【解析】A.基态R原子核外电子的电子云轮廓图有两种:球形和哑铃形,A正确;
B.基态R原子的价层电子排布式还可能为ns2np4,B错误;
C.R元素一共有4种可能,C错误;
D.R元素还有可能为C,D错误;
故选A。
1.能层、能级、原子轨道数及最多容纳电子数
能层 一 二 三 四 五 …
符号 K L M N O …
能级 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s … …
包含原子轨道数 1 1 3 1 3 5 1 3 5 7 1 … …
2 2 6 2 6 10 2 6 10 14 2 … …
最多容纳电子数
2 8 18 32 … 2n2
2.常见原子轨道电子云轮廓图
原子轨道 电子云轮廓图形状 轨道个数
s 球形 1
p 哑铃(或纺锤)形 3(p,p,p)
x y z
3.基态原子的核外电子排布
(1)原子核外电子排布的“三规律”
能量最低原理 原子核外电子总是优先占有能量最低的原子轨道
泡利原理 每个原子轨道里,最多只能容纳2个自旋状态相反的电子
当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占
洪特规则
据一个轨道,而且自旋状态相同
(2)基态原子核外电子排布的四种表示方法
表示方法 举例
电子排布式 Cr:1s22s22p63s23p63d54s1
简化电子排布式 Cu:[Ar]3d104s1
价电子排布式 Fe:3d64s2
电子排布图(或轨道表示式)
【易错点】原子轨道处于全空、半充满、全充满状态更稳定。 Cr、Cu 的电子排布式分别为
1s22s22p63s23p63d54s1、1s22s22p63s23p63d104s1,而非1s22s22p63s23p63d44s2、1s22s22p63s23p63d94s2。
【变式1-1】通常情况下,原子核外p、d能级等原子轨道上电子排布为“全空”“半充满”“全充满”的时候更加稳定,称为洪特规则的特例。下列事实能作为这个规则的证据的是
①某种激发态碳原子的电子排布式是1s22s12p3而不是1s22s22p2
②基态Cu原子的电子排布式是[Ar]3d104s1而不是[Ar]3d94s2
③基态He原子的电子排布式为1s2,基态H原子的电子排布式为1s1
④Fe2+容易失电子转变为Fe3+,表现出较强的还原性
A.①②④ B.②④ C.③④ D.①②③
【答案】B
【解析】①1s22s22p2为基态,能量最低,激发态碳(C)原子电子排布式为1s22s12p3,与洪特规则的特例无关,
故错误;
②基态铜(Cu)原子的电子排布式为[Ar]3d104s1而不是[Ar]3d94s2,[Ar]3d104s1中d轨道处于全满,为稳定结
构,故正确;
③He的s轨道为全满状态,而H的s轨道为半满状态,故错误;
④亚铁离子的3d轨道排布为3d6,失去一个电子后,变为3d5后为半满状态,较稳定,所以 Fe2+容易失去
26
电子转变为稳定的 Fe3+,故正确;
26
故选B。
【变式1-2】(2023上·北京西城·高三北京育才学校校考期中)我国科研团队对嫦娥五号月壤的研究发现,
月壤中存在一种含“水”矿物下列化学用语或图示表达不正确的是
A. 的电子式: B.基态 的价电子排布式:
C. 的 模型: D.基态S原子的价层电子的轨道表示式:
【答案】B
【分析】A.简单阳离子的电子式就是离子符号,复杂离子的电子式要有中括号,NaOH的电子式没有错,
A正确;
B.基态Fe2+的价电子排布式为3d6, B错误;
C.HO的中心原子的价层电子对数为4,2个孤电子对,C正确;
2
D.基态S原子的价电子排布式为3S23P4,价层电子的轨道表示式正确 ,D正确;
故选B。
【考向二】元素的电离能、电负性及微粒半径的大小比较
【典例2】(2024上·山东·高三统考期末)利用α粒子(即氦核 )轰击不同原子,获得人工放射性元素
和 ,合成反应如下: ; 。其中元素Y、Z的基态原子核外未成对电子数之比为1:3.下列说法正确的是
A.基态原子第一电离能:YB;Mg>Al;
N>O;P>S。
(3)应用
①判断元素金属性的强弱
电离能越小,金属越容易失去电子,金属性越强;反之越弱。
②判断元素的化合价
如果某元素的I
n+1
≫I
n
,则该元素的常见化合价为+n。
2.元素电负性的递变性
(1)规律
同周期主族元素从左到右,电负性依次增大;同主族元素自上而下,电负性依次减小。
(2)应用3.微粒半径的比较(以短周期为例)
(1)相同电性微粒半径大小的比较
①原子半径:左下角的钠最大
②阳离子半径:左下角的钠离子最大
③阴离子半径:左下角的磷离子最大
(2)不同电性微粒半径大小的比较
①同周期:阴离子半径>阳离子半径,如Na+<Cl-
②同元素:电子数越多,微粒半径越大,如Fe2+>Fe3+
③同结构:质子数越多,离子半径越小,如Na+<O2-
【变式2-1】(2024上·北京·高三统考期末)砷化镓( )太阳能电池大量应用于我国超低轨通遥一体卫
星星座。下列说法正确的是
A.原子半径: B.电子层数:
C.电负性: D.单质还原性:
【答案】C
【解析】A.原子半径同周期主族元素自左向右逐渐减小,原子半径: ,A错误;
B. 都是第四周期元素,电子层数相同,B错误;
C.电负性同周期主族元素自左向右逐渐增大,电负性: ,C正确;
D.单质还原性同周期主族元素自左向右逐渐减小,单质还原性: ,D错误;
故选C。
【变式2-2】(2024上·辽宁·高三校联考期末)某离子液体的阴离子结构如图所示,其中X、Y、Z、R、Q
是原子序数依次增大的短周期非金属元素,其中X原子的最外层电子中未成对电子数目与成对电子数目相
同。下列说法正确的是A.电负性:Z>R>Q
B.简单离子半径:Q>Z>Y
C.五种元素形成的简单氢化物中沸点最高的是Z
D.同周期主族元素中只有一种元素的第一电离能大于Z
【答案】C
【分析】X、Y、Z、R、Q是原子序数依次增大的短周期非金属元素,其中X原子的最外层电子中未成对
电子数目与成对电子数目相同,可知X元素为C元素,结合Z元素的成键情况,可推断Z元素为O元素,
则Y元素为N元素,结合R形成一个共价键可推断R元素为F元素,结合Q元素形成六个共价键推断Q
元素为S元素;
【解析】A.同周期从左到右,金属性减弱,非金属性变强,元素的电负性变强;同主族由上而下,金属
性增强,非金属性逐渐减弱,元素电负性减弱;电负性:F>O>S,A错误;
B.电子层数越多半径越大,电子层数相同时,核电荷数越大,半径越小;简单离子半径:S2->N3->O2-,B
错误;
C.五种元素形成的简单氢化物中沸点最高的是氧元素形成的水,水常温下为液态,其它均为气体,C正
确;
D.同一周期随着原子序数变大,第一电离能变大,N的2p轨道为半充满稳定状态,第一电离能大于同周
期相邻元素,同周期主族元素中N、F的第一电离能大于O,D错误;
故选C。
【考向三】“两大理论”与微粒构型
【典例3】(2024上·辽宁朝阳·高三统考期末)价层电子对互斥理论可以预测某些微粒的空间结构。下列
说法正确的是
A. 和 的键角相同
B. 和 均为非极性分子
C. 和 的空间结构均为平面三角形
D. 和 的VSEPR模型均为四面体形
【答案】D
【解析】A. 空间结构为直线形,键角为180°, 空间结构为V形,键角为104.5°,A项错误;B. 分子中磷原子有一对孤对电子,空间结构为三角锥形,故 为极性分子,B项错误;
C. 的中心原子N的价层电子对数为3+ =3,空间结构为平面三角形, 的中心原子N
的价层电子对数为2+ =3,空间结构为V形,C项错误;
D. 和 的中心原子N的价层电子对数均为4,VSEPR模型均为四面体形,D项正确;
故选D。
1.共价键
(1)
(2)σ键和π键的判定
①
②ss、sp、杂化轨道之间一定形成σ键;pp可以形成σ键,也可以形成π键(优先形成σ键,其余只能
形成π键)。
2.与分子结构有关的两种理论
(1)杂化轨道理论
①基本观点:杂化轨道成键满足原子轨道最大重叠原理;杂化轨道形成的共价键更加牢固。
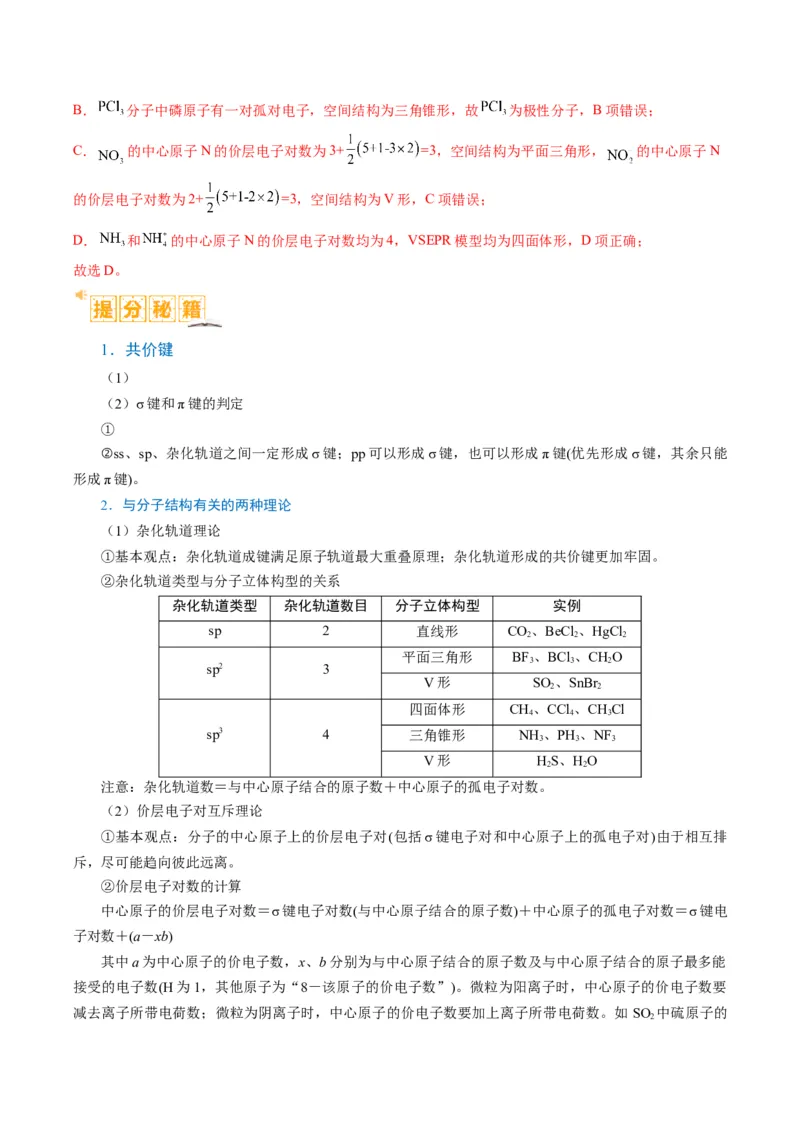
②杂化轨道类型与分子立体构型的关系
杂化轨道类型 杂化轨道数目 分子立体构型 实例
sp 2 直线形 CO、BeCl 、HgCl
2 2 2
平面三角形 BF、BCl 、CHO
3 3 2
sp2 3
V形 SO 、SnBr
2 2
四面体形 CH、CCl 、CHCl
4 4 3
sp3 4 三角锥形 NH 、PH 、NF
3 3 3
V形 HS、HO
2 2
注意:杂化轨道数=与中心原子结合的原子数+中心原子的孤电子对数。
(2)价层电子对互斥理论
①基本观点:分子的中心原子上的价层电子对(包括σ键电子对和中心原子上的孤电子对)由于相互排
斥,尽可能趋向彼此远离。
②价层电子对数的计算
中心原子的价层电子对数=σ键电子对数(与中心原子结合的原子数)+中心原子的孤电子对数=σ键电
子对数+(a-xb)
其中a为中心原子的价电子数,x、b分别为与中心原子结合的原子数及与中心原子结合的原子最多能
接受的电子数(H为1,其他原子为“8-该原子的价电子数”)。微粒为阳离子时,中心原子的价电子数要
减去离子所带电荷数;微粒为阴离子时,中心原子的价电子数要加上离子所带电荷数。如 SO 中硫原子的
2孤电子对数为=1;HO+中氧原子的孤电子对数为=1;CO中碳原子的孤电子对数为=0。
3
【易错点】在计算孤电子对数时,出现0.5或1.5,则把小数进位为整数,即1或2。如NO 的中心原子N
2
的孤电子对数为=0.5≈1,则价层电子对数为3,故VSEPR模型为平面三角形,分子立体构型为V形。
③利用价层电子对互斥理论判断分子(或离子)立体构型
价层电子对数 孤电子对数 分子(或离子)立体构型 示例
2 0 CO、BeCl
2 2
3 0 BF、SO 、CO
3 3
3 1 SO
2
4 0 CH、NH、SO、CCl
4 4
4 1 NH 、PCl 、HO+
3 3 3
4 2 HO、HS
2 2
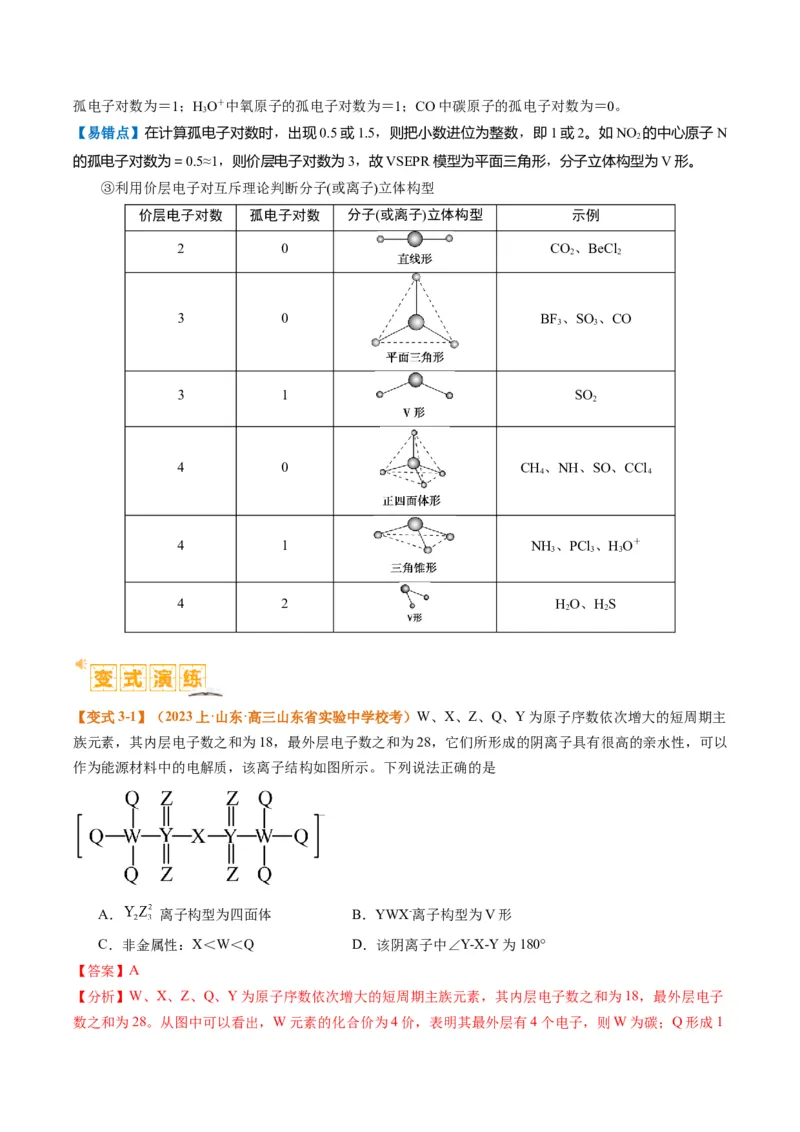
【变式3-1】(2023上·山东·高三山东省实验中学校考)W、X、Z、Q、Y为原子序数依次增大的短周期主
族元素,其内层电子数之和为18,最外层电子数之和为28,它们所形成的阴离子具有很高的亲水性,可以
作为能源材料中的电解质,该离子结构如图所示。下列说法正确的是
A. 离子构型为四面体 B.YWX-离子构型为V形
C.非金属性:X<W<Q D.该阴离子中∠Y-X-Y为180°
【答案】A
【分析】W、X、Z、Q、Y为原子序数依次增大的短周期主族元素,其内层电子数之和为18,最外层电子
数之和为28。从图中可以看出,W元素的化合价为4价,表明其最外层有4个电子,则W为碳;Q形成1个共价键,则Q应为氟;Y形成6个共价键,则最外层有6个电子,其为S;Z形成2个共价键,则Z为氧;
X形成2个共价键,又获得1个电子,所以X的最外层电子数为5,其为氮元素。从而得出W、X、Z、
Q、Y分别为C、N、O、F、S。
【解析】A. 离子的化学式为 ,其相当于 中的1个O原子被S替代,所以其构型与 相
似,为四面体结构,A正确;
B.YWX-离子为SCN-,其中心C原子的价层电子数为2,发生sp杂化,C原子的最外层无孤电子对,则
其构型为直线形,B不正确;
C.X、W、Q分别为N、C、F,它们的电子层数相同,为同周期元素,则非金属性:C<N<F,C不正确;
D.该阴离子中,S-N-S的中心N原子最外层存在孤电子对,对成键电子有排斥作用,所以∠S-N-S小于
180°,D不正确;
故选A。
【变式3-2】(2023上·河北邯郸·高三磁县第一中学校考)下列化学用语的表述正确的是
A. 杂化轨道模型: B.铍原子最外层电子的电子云图:
C.氨气分子的空间填充模型: D.质量数为127的碘原子:
【答案】A
【解析】A. 杂化轨道有1个s轨道和2个p轨道杂化形成,每个 杂化轨道含有 轨道成分,含有
轨道成分,A正确;
B.铍原子最外层电子位于 轨道,电子云图为球形,B错误;
C.氨气分子的空间构型为三角锥形,C错误;
D.质量数为127的碘原子: ,D错误;
故选A。
【考向四】分子性质与微粒作用
【典例4】(2024·广西·统考模拟预测)下列有关物质结构与性质的说法错误的是
A. 易溶于 ,可从 和 都是非极性分子的角度解释
B.对羟基苯甲酸存在分子内氢键,是其沸点比邻羟基苯甲酸的高的主要原因
C. 溶于氨水,是由于 与 反应生成了可溶性配合物D.熔融 能导电,是由于熔融状态下产生了自由移动的 和
【答案】B
【解析】A.单质碘和四氯化碳都是非极性分子,根据相似相溶的原理, 易溶于 ,A正确;
B.分子间氢键可以增大其熔沸点,则对羟基苯甲酸存在分子间氢键,是其沸点比邻羟基苯甲酸的高的主
要原因,B错误;
C.银离子可以和氨气形成配合物离子,导致氯化银可以溶解在氨水中,C正确;
D.氯化钠在熔融状态产生了自由移动的 和 ,从而可以导电,D正确;
故选B。
1.分子性质
(1)分子构型与分子极性的关系
(2)溶解性
“相似相溶”规律:非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂;若存在氢键,则
溶剂和溶质之间的氢键作用力越大,溶解性越好。
(3)无机含氧酸分子的酸性
无机含氧酸可写成(HO) RO ,如果成酸元素R相同,则n值越大,R的正电性越高,使R—O—H中O的
m n
电子向R偏移,在水分子的作用下越易电离出H+,酸性越强,如酸性:HClOOF B.酸性:CHCOOH>CH FCOOH
2 2 3 2
C.分子的极性:O>O D.基态原子未成对电子数:Mn>Cr
2 3
【答案】A
【解析】A.氧的电负性大于氯,ClO中键合电子对偏向氧;氟电负性强于氧,OF 中键合电子对偏向氟,
2 2
两对键合电子对排斥小,键角就小键角,所以键角ClO>OF ,故A正确;
2 2
B.F原子电负性大,吸电子能力强,所以极性CHCOOH<CHFCOOH,CHFCOOH更能电离出氢离子,
3 2 2
所以酸性:CHCOOH<CHFCOOH,故B错误;
3 2
C.O 是非极性分子,O 是极性分子,分子的极性:O<O,故C错误;
2 3 2 3
D.基态原子Mn原子价电子排布式为3d84s2,未成对电子数为2;基态原子Cr原子价电子排布式为
3d54s1,未成对电子数为6,基态原子未成对电子数Mn<Cr,故D错误。
答案选A。
【变式4-2】(2023上·北京西城·高三统考期末)下列事实不能用氢键解释的是
A.密度: B.沸点:
C.稳定性: D.溶解性(水中):
【答案】C
【解析】A.水分子间存在氢键,氢键具有方向性,导致水结冰时存在较大空隙,密度比液态水小,A不
符题意;
B.水分子间可形成氢键,硫化氢分子间不能形成氢键,所以沸点: ,B不符题意;
C.原子半径: ,键长: ,键能: ,所以稳定性: ,与氢键无
关,C符合题意;
D.氨分子与水分子间可形成氢键,增大溶解性;甲烷分子与水分子间不能形成氢键,所以溶解性(水中):
,D不符题意;
答案选C。【考向五】成键方式、晶体类型的判断
【典例5】(2023上·北京·高三北京一七一中校考)用 表示阿伏加德罗常数.下列说法正确的是
A.标准状况下,22.4L乙炔中 键数为 , 键数为
B.质量相同的 和 所含的分子数相同
C.同温同压下,相同体积的 和 所含的原子数相同
D.12g金刚石中C―C键数为
【答案】A
【解析】A.标准状况下,22.4L乙炔的物质的量为1mol,CH CH中 键数为3, 键数为2,则1mol乙
炔中 键数为 , 键数为 ,故A正确;
B.质量相同的HO和DO(重水)的物质的量之比为20:18,分子数之比为20:18,不相同,故B错误;
2 2
C.同温同压下,相同体积的 和 物质的量相等,所含的原子数不相同,故C错误;
D.12g碳是1mol,形成金刚石时一个碳形成4个共价键,而每个共价键同属于两个碳,所以12g金刚石
中含有碳碳键数为2N ,故D错误;
A
故选A。
1.σ键、π键的判断
(1)由轨道重叠方式判断:“头碰头”重叠为σ键,“肩并肩”重叠为π键
(2)由共用电子对数判断:单键为σ键;双键或三键,其中一个为σ键,其余为π键
(3)由成键轨道类型判断:s轨道形成的共价键全部是σ键;杂化轨道形成的共价键全部为σ键
配合物中σ键的算法 配位键是一种特殊的共价键
1mol Ni(CO) 中含___molσ键 4个CO中含有4个σ键,外加4个配位键,也属于σ键,总共8个σ键
4
2.晶体类别的判断方法
(1)依据构成晶体的微粒和微粒间作用力判断
由阴、阳离子形成离子键构成的晶体为离子晶体;由原子形成的共价键构成的晶体为原子晶体;由分子
依靠分子间作用力形成的晶体为分子晶体;由金属阳离子、自由电子以金属键形成的晶体为金属晶体
(2)依据物质的分类判断
①活泼金属氧化物和过氧化物(如KO、NaO 等),强碱(如NaOH、KOH等),绝大多数的盐是离子晶体
2 2 2
②部分非金属单质、所有非金属氢化物、部分非金属氧化物、几乎所有的酸、绝大多数有机物的晶体是
分子晶体
③常见的单质类原子晶体有金刚石、晶体硅、晶体硼等,常见的化合物类原子晶体有 SiC、SiO、AlN、
2BP、CaAs等
④金属单质、合金是金属晶体
(3)依据晶体的熔点判断
不同类型晶体熔点大小的一般规律:原子晶体>离子晶体>分子晶体。金属晶体的熔点差别很大,如钨、
铂等熔点很高,铯等熔点很低
(4)依据导电性判断
①离子晶体溶于水及熔融状态时均能导电
②原子晶体一般为非导体
③分子晶体为非导体,但分子晶体中的电解质(主要是酸和强极性非金属氢化物)溶于水时,分子内的化
学键断裂形成自由移动的离子,也能导电
④金属晶体是电的良导体
(5)依据硬度和机械性能判断
一般情况下,硬度:原子晶体>离子晶体>分子晶体。金属晶体多数硬度大,但也有较小的,且具有延展
性
【变式5-1】(2023上·北京·高三北京市第一六一中学校考)下列化学用语或图示表达不正确的是
A. 的空间结构模型:
B.HO的VSEPR模型
2
C.二氧化碳的电子式:
D.p-pπ键电子云轮廓图
【答案】A
【解析】A.在 中,中心P原子的价层电子对数为4,发生sp3杂化,则其空间构型为正四面体,空间
结构模型为 ,A不正确;
B.HO的中心O原子的价层电子对数为4,发生sp3杂化,则其VSEPR模型为四面体,即为 ,B正
2
确;
C.二氧化碳分子中,C原子与每个O原子形成2对共用电子,其电子式为 ,C正确;
D.p-pπ键是两个p轨道肩并肩重叠,其电子云轮廓图为 ,D正确;
故选A。
【变式5-2】(2023上·湖南长沙·高三统考)下列有关晶体结构说法正确的是A.在NaCl晶胞中,与 最邻近且等距离的 有6个
B.在干冰晶体中,每个晶胞拥有6个 分子
C. 晶胞中 的配位数为4
D.该气态团簇分子的化学式为
【答案】D
【解析】A.根据NaCl晶胞可知,与 最邻近且等距离的 位于各棱心,共计12个,A错误;
B.根据干冰晶胞可知,CO 位于顶点和面心,利用均摊法,每个晶胞拥有CO 的个数: ,B
2 2
错误;
C.取任意面心 为中心,与其距离最近且相等的 由8个,配位数为8,C错误;
D.气态团簇分子不用于晶胞,气态团簇分子中含有4个E原子和4个F原子,则分子式 ,D正确;
答案选D。
【考向六】晶体化学式及粒子数确定
【典例6】(2024上·辽宁锦州·高三统考期末)一种由Mn、Se组成的化合物立方晶胞结构如图所示。已知
化合物的摩尔质量为 ,晶胞参数为anm,阿伏加德罗常数的值为 。下列说法错误的是
A.该化合物的化学式可表示为MnSe B.与Se原子距离最近的Se原子有12个
C.Mn、Se原子的最近距离是 D.晶胞密度为
【答案】C【解析】A.根据均摊原则,晶胞中Se原子数为 、Mn原子数为4,该化合物的化学式可表
示为MnSe,故A正确;
B.根据图示,与Se原子距离最近的Se原子有12个,故B正确;
C.Mn、Se原子的最近距离为体对角线的 ,距离 ,故C错误;
D.每个晶胞中含有4个Se、4个Mn,所以晶胞密度为 ,故D正确;
选C。
1.晶胞中微粒数目的计算方法——均摊法
(1)原则:晶胞中任意位置上的一个原子如果是被n个晶胞所共有,那么,每个晶胞对这个原子分得的份
额就是
(2)方法:
①长方体(正方体)晶胞中不同位置的粒子数的计算
a.处于顶点上的粒子,同时为8个晶胞所共有,每个粒子有属于该晶胞
b.处于棱边上的粒子,同时为4个晶胞所共有,每个粒子有属于该晶胞
c.处于晶面上的粒子,同时为2个晶胞所共有,每个粒子有属于该晶胞
d.处于晶胞内部的粒子,则完全属于该晶胞
②非长方体晶胞中粒子视具体情况而定
三棱柱
六棱柱
石墨晶胞每一层内碳原子排成六边形,其顶点(1个
平面型
碳原子)被三个六边形共有,每个六边形占
2.熟记几种常见的晶胞结构及晶胞含有的粒子数目晶体 NaCl CsCl ZnS CaF 金刚石
2
晶体结构
4个Na 4个Ca2
1个Cs+, 4个S2-,
粒子数目 +, +, 8个C
1个Cl- 4个Zn2+
4个Cl- 8个F-
晶体 简单立方 体心立方 面心立方 氮化硼 干冰
晶体结构
粒子数目 1个原子 2个原子 4个原子 4个B,4个N 4个CO
2
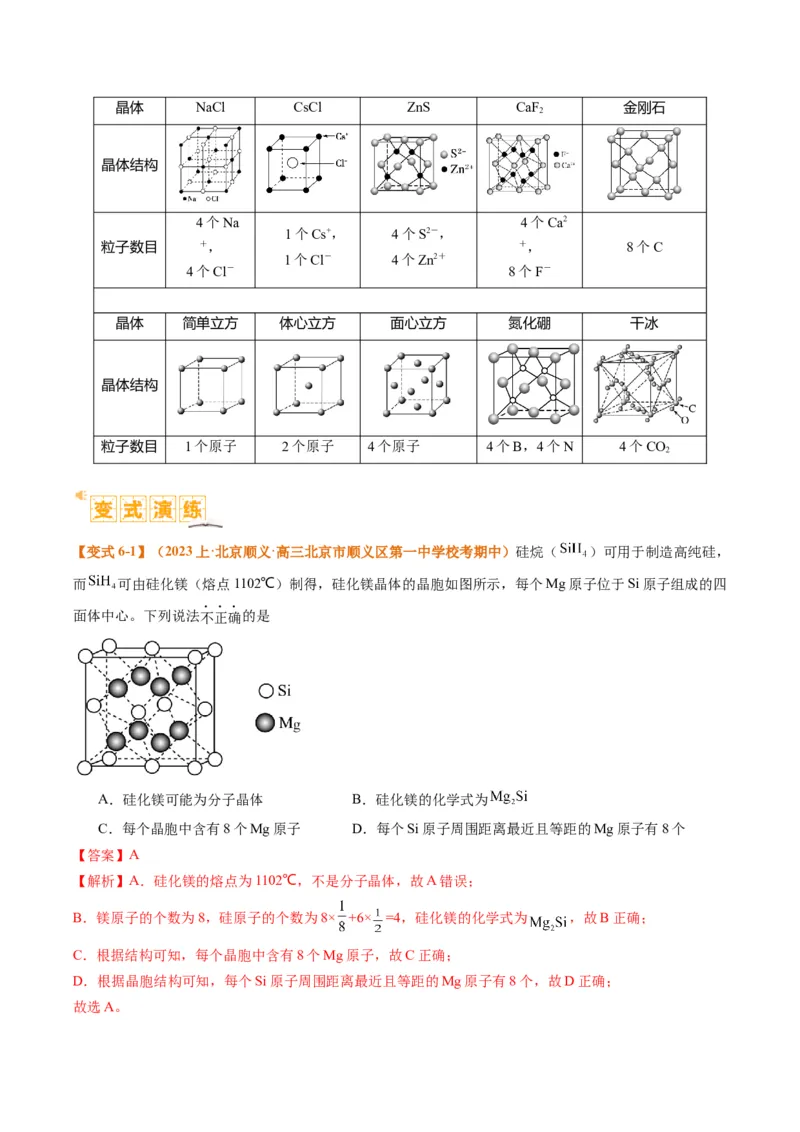
【变式6-1】(2023上·北京顺义·高三北京市顺义区第一中学校考期中)硅烷( )可用于制造高纯硅,
而 可由硅化镁(熔点1102℃)制得,硅化镁晶体的晶胞如图所示,每个Mg原子位于Si原子组成的四
面体中心。下列说法不正确的是
A.硅化镁可能为分子晶体 B.硅化镁的化学式为
C.每个晶胞中含有8个Mg原子 D.每个Si原子周围距离最近且等距的Mg原子有8个
【答案】A
【解析】A.硅化镁的熔点为1102℃,不是分子晶体,故A错误;
B.镁原子的个数为8,硅原子的个数为8× +6× =4,硅化镁的化学式为 ,故B正确;
C.根据结构可知,每个晶胞中含有8个Mg原子,故C正确;
D.根据晶胞结构可知,每个Si原子周围距离最近且等距的Mg原子有8个,故D正确;
故选A。【变式6-2】(2023上·山东·高三校联考)钙钛矿具有独特的晶体结构,广泛应用于传感器、固体电阻器等
诸多领域。图1、2均为钙钛矿型化合物,其中图1中另两种离子为 、 ,图2中另两种离子为 和
。
下列说法错误的是
A.钛酸钙的化学式为 B.图2中,Y为
C. 中含有配位键 D.晶胞中与每个 紧邻的 有12个
【答案】B
【解析】A.根据均摊原则,晶胞中Ca2+数为 、A离子数为 、B离子数为1,根据化合价
代数和等于0,A是O2-、B是Ti4+,钛酸钙的化学式为 ,故A正确;
B.根据均摊原则,图2中, 数为 、X离子数为1、Y离子数 ,根据化合价代数和
等于0,Y为 、X为 ,故B错误;
C.N原子能形成3个共价键, 中有1个N-H键为配位键,故C正确;
D.根据图示,图1中与每个 紧邻的 有12个,故D正确;
选B。
【考向七】原子分数坐标分析方法
【典例7】(2023上·黑龙江·高三牡丹江一中校考期末)砷化镉晶胞结构如图,图1中“①”和“②”位
是“真空”,晶胞参数为apm,建立如图2,①号位的坐标为( , , )。已知:砷化镉的摩尔质量为
Mg·mol-1,N 为阿伏加德罗常数的值,下列说法错误的是
AA.砷化镉中Cd与As原子个数比为3:2
B.两个Cd原子间最短距离为0.5a pm
C.③号位原子坐标参数为( ,1, )
D.该晶胞的密度为N (a×10—10)3g·cm-3
A
【答案】D
【解析】A.由晶胞结构可知,晶胞中位于体内的镉原子个数为6,位于顶点和面心的砷原子的个数为8×
+6× =4,则镉与砷原子个数比为3:2,故A正确;
B.由晶胞结构可知,两个镉原子间最短距离为边长的 ,则最短距离为apm× =0.5apm,故B正确;
C.由位于体对角线 处①号位的坐标为( , , )可知,晶胞的边长为1,则位于位于右侧面的面心上
的③号位原子坐标参数为( ,1, ),故C正确;
D.由晶胞结构可知,晶胞中位于体内的镉原子个数为6,位于顶点和面心的砷原子的个数为8× +6×
=4,设晶体的密度为dg/cm3,由晶胞的质量公式可得: =(10—10 a)3d,解得d= ,故D错误;
故选D。
1.原子分数坐标参数
(1)含义:以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子分数坐标
(2)原子分数坐标的确定方法
①依据已知原子的坐标确定坐标系取向
②一般以坐标轴所在正方体的棱长为1个单位
③从原子所在位置分别向x、y、z轴作垂线,所得坐标轴上的截距即为该原子的分数坐标
(3)示例
晶胞中原子坐标
A(0,0,0), B(0,1,0), C(1,1,0), D(1,0,0),E(0,0,1), F(0,1,1), G(1,1,1), H(1,0,1),
体心:(,,), 上面心:(,,1), 下面心:(,,0),
z 左面心:(,0,),右面心:(,1,), 前面心:(1,,),
E
F 后面心:(0,,)
H G
2.典型晶胞结构模型的原子分数坐标
A
B y
(1)简单立方体模型粒子坐标
D C
x 粒子坐标
若1(0,0,0),2(0,1,0),则确定3的原子分数坐标为(1,
1,0),7为(1,1,1)
(2)体心晶胞结构模型的原子坐标和投影图
粒子坐标
若1(0,0,0),3(1,1,0),5(0,0,1),则6的原子分数坐
标为(0,1,1),7为(1,1,1),9为(,,)
(3)面心立方晶胞结构模型的原子坐标和投影图
粒子坐标
若1(0,0,0),13(,,0),12(1,,),则15的原子分数坐标
为(,1,),11为(,,1)
(4)金刚石晶胞结构模型的原子坐标和投影图
粒子坐标
若a原子为坐标原点,晶胞边长的单位为1,则原子1、2、
3、4的坐标分别为(,,)、(,,)、(,,)、(,,)
【变式7-1】(2023上·河南濮阳·高三濮阳一高校考期中)硒化锌是一种重要的半导体材料,其晶胞结构如图甲所示。已知晶胞参数为q nm,乙图为晶胞的俯视图,a点的原子分数坐标为 。
下列说法正确的是
A.晶胞中硒原子的配位数为12
B.晶胞中d点的原子分数坐标为
C.相邻两个Zn原子的最短距离为 nm
D.Zn和Se在元素周期表中分别位于d区与p区
【答案】B
【解析】A.该晶胞中Zn原子的配位数是4,则ZnSe晶胞中Se原子的配位数也是4,A错误;
B.该晶胞中a点坐标为 ,b点坐标为 ,则a原子位于坐标原点,b原子在坐标轴正方向空
间内,由图乙可知d原子也在坐标轴正方向空间内,且到x轴、y轴、z轴的距离分别为 ,即d原
子的坐标为 ,B正确;
C.面对角线的两个Zn原子距离最短,为 ,C错误;
D.Zn的价层电子排布式为 ,位于ds区,Se的价层电子排布式为 ,位于p区,D错误;
故选B。
【变式7-2】(2024上·黑龙江齐齐哈尔·高三齐齐哈尔市第八中学校校考)一种铜的溴化物晶胞结构如图所
示。下列说法正确的是A.该化合物的化学式为CuBr
2
B.铜原子的配位数为12
C.与每个Br紧邻的Br有6个
D.由图中P点和Q点原子的分数坐标,可确定R点原子的分数坐标为( , , )
【答案】D
【解析】A.该晶胞中,溴原子位于8个顶点和6个面心,共有 个,铜原子位于晶胞内部,
共有4个,故该化合物的化学式为 ,故A错误;
B.1个铜原子连接4个溴原子,则铜原子的配位数是4,故B错误;
C.溴原子位于晶胞的顶点和面心,与干冰结构类似,所以与每个Br紧邻的Br有12个,故C错误;
D.R点原子在x、y、z三个坐标轴中的坐标均为 ,故坐标参数为( ),故D正确;
故答案选D。
【考向八】有关晶胞参数的计算
【典例8】科学家合成了一种高温超导材料,其晶胞结构如图所示,该立方晶胞参数为 。阿伏加德罗
常数的值为 。下列说法错误的是
A.晶体最简化学式为
B.晶体中与 最近且距离相等的 有6个
C.晶胞中B和C原子构成的多面体有14个面
D.晶体的密度为
【答案】B
【解析】A.晶胞中K位于顶点,每个晶胞中含K原子 个,Ca位于体心,每个晶胞中含Ca原子1
个,B和C位于面心,每个晶胞中含B原子和C原子各 个,则晶体最简化学式为 ,A正确;
B.晶体中与 位于顶点, 位于体心,则晶体中与 最近且距离相等的 有8个,B错误;
C.晶胞中B和C原子构成的多面体,有6个面位于晶胞的六个面上,上半部分和下半部分还各有4个面,
故该多面体共有14个面,C正确;
D. 的摩尔质量为217g/mol,一个晶胞的质量为 ,体积为 ,故晶体的密度为
,D正确;
故选B。
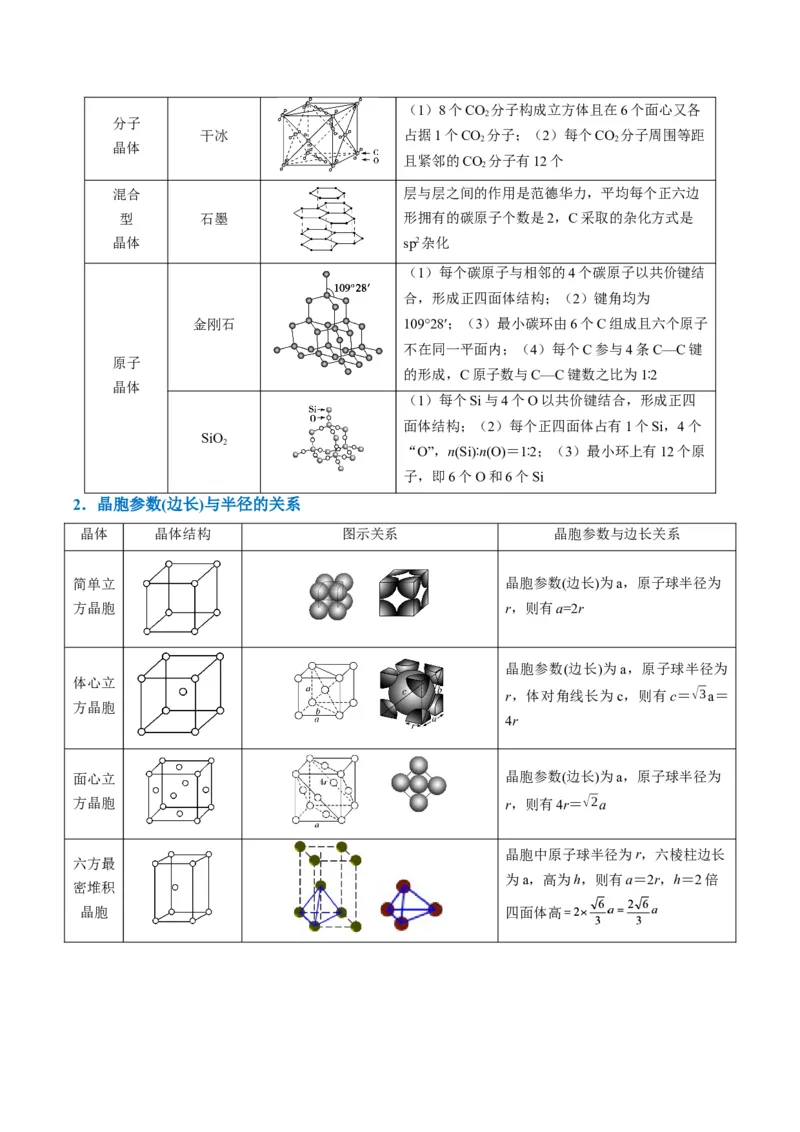
1.典型晶体模型
晶体 晶体结构 晶体详解
(1)每个Na+(Cl-)周围等距且紧邻的Cl-(Na+)
NaCl
有6个,每个Na+周围等距且紧邻的Na+有12
型
个;(2)每个晶胞中含4个Na+和4个Cl-
(1)每个Cs+周围等距且紧邻的Cl-有8个,每
离子
个Cs+(Cl-)周围等距且紧邻的Cs+(Cl-)有6个;
晶体
CsCl型
(2)如图为8个晶胞,每个晶胞中含1个Cs+、1
个Cl-
在晶体中,每个F-吸引4个Ca2+,每个Ca2+吸引
CaF 型
2
8个F-,Ca2+的配位数为8,F-的配位数为4
简单立方堆
典型代表为Po,空间利用率为52%,配位数为6
积
体心立方堆 典型代表为Na、K、Fe,空间利用率为68%,配
积 位数为8
金属
晶体
六方最密堆 典型代表为Mg、Zn、Ti,空间利用率为74%,配
积 位数为12
面心立方 典型代表为Cu、Ag、Au,空间利用率为74%,
最密堆积 配位数为12(1)8个CO 分子构成立方体且在6个面心又各
2
分子
干冰 占据1个CO 分子;(2)每个CO 分子周围等距
2 2
晶体
且紧邻的CO 分子有12个
2
混合 层与层之间的作用是范德华力,平均每个正六边
型 石墨 形拥有的碳原子个数是2,C采取的杂化方式是
晶体 sp2杂化
(1)每个碳原子与相邻的4个碳原子以共价键结
合,形成正四面体结构;(2)键角均为
金刚石 109°28′;(3)最小碳环由6个C组成且六个原子
不在同一平面内;(4)每个C参与4条C—C键
原子
的形成,C原子数与C—C键数之比为1∶2
晶体
(1)每个Si与4个O以共价键结合,形成正四
面体结构;(2)每个正四面体占有1个Si,4个
SiO
2
“O”,n(Si)∶n(O)=1∶2;(3)最小环上有12个原
子,即6个O和6个Si
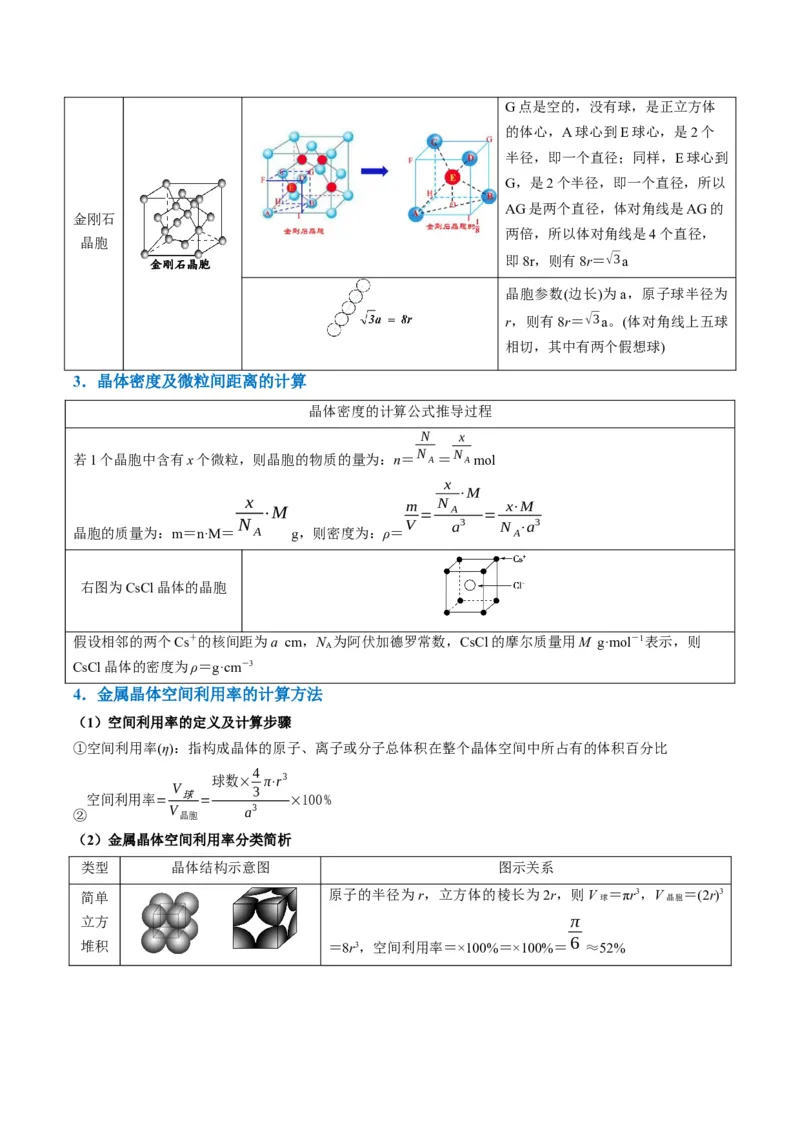
2.晶胞参数(边长)与半径的关系
晶体 晶体结构 图示关系 晶胞参数与边长关系
简单立 晶胞参数(边长)为a,原子球半径为
方晶胞 r,则有a=2r
晶胞参数(边长)为a,原子球半径为
体心立
r,体对角线长为c,则有c=√3a=
方晶胞
4r
面心立 晶胞参数(边长)为a,原子球半径为
方晶胞 r,则有4r=√2a
晶胞中原子球半径为r,六棱柱边长
六方最
为a,高为h,则有a=2r,h=2倍
密堆积
晶胞 四面体高G点是空的,没有球,是正立方体
的体心,A球心到E球心,是2个
半径,即一个直径;同样,E球心到
G,是2个半径,即一个直径,所以
AG是两个直径,体对角线是AG的
金刚石
两倍,所以体对角线是4个直径,
晶胞
金刚石晶胞
即8r,则有8r=√3a
晶胞参数(边长)为a,原子球半径为
r,则有8r=√3a。(体对角线上五球
相切,其中有两个假想球)
3.晶体密度及微粒间距离的计算
晶体密度的计算公式推导过程
N x
N N
若1个晶胞中含有x个微粒,则晶胞的物质的量为:n= A= Amol
x
⋅M
x
⋅M
m
=
N
A
=
x⋅M
N V a3 N ⋅a3
晶胞的质量为:m=n·M= A g,则密度为:ρ= A
右图为CsCl晶体的晶胞
假设相邻的两个Cs+的核间距为a cm,N 为阿伏加德罗常数,CsCl的摩尔质量用M g·mol-1表示,则
A
CsCl晶体的密度为ρ=g·cm-3
4.金属晶体空间利用率的计算方法
(1)空间利用率的定义及计算步骤
①空间利用率(η):指构成晶体的原子、离子或分子总体积在整个晶体空间中所占有的体积百分比
4
球数× π⋅r3
V 3
空间利用率= 球 = ×100%
②
V
晶胞
a3
(2)金属晶体空间利用率分类简析
类型 晶体结构示意图 图示关系
简单 原子的半径为r,立方体的棱长为2r,则V 球 =πr3,V 晶胞 =(2r)3
立方 π
堆积 =8r3,空间利用率=×100%=×100%= 6 ≈52%原子的半径为r,体对角线c为4r,面对角线b为a,由(4r)2=a2
体心
+b2得a=r。1个晶胞中有2个原子,故空间利用率=×100%=
立方
√3π
晶胞
8
×100%=×100%= ≈68%
原子的半径为 r,面对角线为 4r,a=2r,V =a3=(2r)3=
面心 晶胞
立方
16r3,1个晶胞中有4个原子,则空间利用率=×100%=×100%
最密 √2π
堆积 6
= ≈74%
原子的半径为r,底面为菱形(棱长为2r,其中一个角为60°),则
六方
底面面积S=2r×r=2r2,h=r,V
晶胞
=S×2h=2r2×2×r=8r3,1个
最密 √2π
堆积 晶胞中有 2个原子,则空间利用率=×100%=×100%= 6
≈74%
设原子半径为R,由于原子在晶胞体对角线方向上相切(相邻两
金刚 个碳原子之间的距离为晶胞体对角线的四分之一),可以计算出
石型 晶胞参数:a=b=c=R,α=β=γ=90°。每个晶胞中包含八个原
堆积 金刚石晶胞 子。
η=×100%=×100%≈34.01%
【变式8-1】(2023上·贵州贵阳·高三贵阳一中校考)钙钛矿电池是第三代非硅薄膜太阳能电池的代表,具
有较高的能量转化效率。如图是一种边长为 的钙钛矿的正方体晶胞结构,其中 原子占据正方体中
心,O原子位于每条棱的中点。其中以原子1为原点,原子2的坐标为 。下列有关说法错误的是
A.原子3的坐标为 B. 原子与 原子最近距离为
C.距离 原子最近的O原子有6个 D.该晶胞密度约为
【答案】B【解析】A.原子1为原点,原子2的坐标为 ,则原子3的坐标为 ,A正确;
B. 原子与 原子最近距离为体对角线的一半,晶胞边长为 ,体对角线的一半为 ,B错误;
C.如图,以顶点 原子为中心,与该晶胞及周围晶胞距离最近的O原子有6个,围成正八面体,C正确;
D.该晶胞中含有1个 ,1个Ti,3个O, 摩尔质量为136g/mol,晶胞边长为 ,可得该晶胞
密度约为 ,D正确;
故选B。
【变式8-2】(2024上·黑龙江哈尔滨·高三哈尔滨三中校考期末)已知Mg、Al、O三种元素组成尖晶石型
晶体结构,其晶胞由4个A型小晶格和4个B型小晶格构成,其中 和 都在小晶格内部, 部分
在小晶格内部,部分在小晶格顶点(如图),下列分析错误的是
A.该晶体为离子晶体
B.该物质的化学式为
C.晶胞中,距离 等距且最近的 数为12
D. 与 之间最近的距离是
【答案】D
【解析】A.从题干信息可知,构成晶体的微粒为 、 、 ,则该晶体为离子晶体,A正确;
B.在晶胞结构中, 位于晶胞顶角、面心及A型小晶格体心,共 个, 位于晶胞
B型小晶格体内,共 个, 位于晶胞A型小晶格及B型小晶格体内,共 ,在晶胞
中 、 、 个数比为8:16:32=1:2:4,化学式为 ,B正确;
C.在B型小晶格内与 等距且最近的 有3个,在晶体中,每个 参与形成4个B型小晶格,
故距离 等距且最近的 数为12,C正确;
D.在A型小晶格或B型小晶格内, 与 之间最近的距离是体对角线的 ,故
,D错误;答案选D。
【考向九】解释原因类简答题
【典例9】(2023·全国·高三专题练习)钛酸钙具有特殊的物理、化学性质,钛酸钙结构材料是当前材料科
学研究领域的热点之一,回答下列问题。
(1)钛在元素周期表中的位置是 。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的则用- 表示,
称为电子的自旋磁量子数。对于基态钛原子,其价电子自旋磁量子数的代数和为 。从结构角度解
释TiCl 中Ti还原性较强的原因 。
3
(3)离子半径Ca2+>Ti4+,理由是 。
【答案】(1)第四周期第ⅣB族
(2) +1或-1 +3价Ti外围电子为3d1,失去一个电子后,3d能级处于全空稳定状态
(3)Ca2+和Ti4+电子层结构相同,核电荷数Ti>Ca,导致离子半径Ca2+大于Ti4+
【分析】Ti核电荷数为22,位于周期表的第四周期第ⅣB族 ,价电子排布式为3d24s2,
价电子排布图为 。
【解析】(1)Ti原子核电荷数为22,钛位于周期表的第四周期第ⅣB族;
(2)Ti价电子排布式为3d24s2价电子排布图为 3d2是分占2个d轨道、
自旋方向相同的2个电子,4s轨道填了自旋方向相反的2个电子,则其价电子自旋磁量子数的代数和为
或 ;+3价Ti外围电子为3d1,失去一个电子后,3d能级处于全空稳定状态,因此
TiCl 中Ti(Ⅲ)还原性较强;
3
(3)Ca2+和Ti4+核外均为18电子,电子层结构相同,核电荷数Ti>Ca,导致离子半径Ca2+大于Ti4+ ;
1.晶体熔、沸点的比较
(1)不同类型晶体熔、沸点的比较
①不同类型晶体的熔、沸点高低的一般规律:共价晶体>离子晶体>分子晶体
②金属晶体的熔、沸点差别很大,如:钨、铂等熔、沸点很高,汞、铯等熔、沸点很低
(2)同种晶体类型熔、沸点的比较——比较晶体内微粒之间相互作用力的大小
①共价晶体:看共价键的强弱,取决于键长,即:成键原子半径大小规律:原子半径越小 键长越短 键能越大 熔沸点越高
如熔点:金刚石>碳化硅>晶体硅
②离子晶体:看离子键的强弱,取决于阴、阳离子半径大小和所带电荷数
规律:衡量离子晶体稳定性的物理量是晶格能。晶格能越大,形成的离子晶体越稳定,熔点越高,硬度越
大。一般地说,阴、阳离子的电荷数越多,离子半径越小,晶格能越大,离子间的作用力就越强,离子晶
体的熔、沸点就越高,如熔点:MgO>NaCl>CsCl
③分子晶体:看分子间作用力 (一般先氢键后范德华力最后分子的极性)
a.分子间作用力越大,物质的熔、沸点越高;具有分子间氢键的分子晶体熔、沸点反常得高,
如沸点:HO>HTe>HSe>HS
2 2 2 2
b.组成和结构相似的分子晶体,相对分子质量越大,熔、沸点越高,如沸点:SnH >GeH >SiH>CH
4 4 4 4
c.组成和结构不相似的物质(相对分子质量接近),分子的极性越大,其熔、沸点越高,如沸点:CO>N
2
d.在同分异构体中,一般支链越多,熔、沸点越低,如沸点:正戊烷>异戊烷>新戊烷
④金属晶体:看金属键的强弱,取决于金属阳离子半径和所带电荷数
规律:金属离子的半径越小,离子的电荷数越多,其金属键越强,金属的熔、沸点就越高
如熔、沸点:Na<Mg<Al
【变式9-1】(2023上·上海浦东新·高三上海市洋泾中学校考)关于化学键和分子间作用力的理论是关于物
质结构的基本理论。
(1)N、P、As 电负性由大到小的顺序为 。
(2)用“>”或“<”填空:
第一电离能 离子半径 熔点 酸性
O2- Na
Si S NaCl Si HSO HClO
2 4 4
+
(3)MgCl 在工业上应用广泛,可由 MgO 制备。MgO 的熔点比 BaO 的熔点 (填“高” 或
2
“低”)。
(4)HCHO 分子的立体构型为 形,它与 H 加成后,加成产物的熔、沸点比 CH 的熔、沸点
2 4
高,其主要原因是 (须指明加成产物是何物质) 。
(5)已知 HO 分子的结构如图所示:HO 分子不是直线形的,两个氢原子犹如在半展开的书的两面上,
2 2 2 2
两个氧原子在书脊位置上,书页夹角为 93o52′,而两个O—H 键与O—O 键的夹角均为96o52′。
①HO 分子是含有 键和 键的 (填“极性”或“非极性”)分子。
2 2
②H O 难溶于 CS,简要说明理由: 。
2 2 2
【答案】(1)N>P>S(2) < > < <
(3)高
(4) 平面三角 加成产物 CHOH 分子之间能形成氢键
3
(5) 极性 非极性 极性 HO 为极性分子,而 CS 为非极性溶剂,根据“相似相溶”
2 2 2
规律,HO 难溶于 CS
2 2 2
【解析】(1)N、P、As同主族自上而下电负性逐渐增大,所以电负性由大到小的顺序为N>P>S,答案:
N>P>S;
(2)第一电离能Si 。NaCl为离子晶体,Si为共价晶体,所以熔点NaCl;<;<;
2 4 4
(3)MgO 、 BaO 均为离子晶体, 半径小于 ,MgO离子键强,熔点高。答案:高;
(4)HCHO中心碳原子形成3个σ键,中心碳原子无孤电子对,所以HCHO 分子的立体构型为平面三角
形。HCHO它与 H 加成生成乙醇。乙醇的熔、沸点比 CH 的熔、沸点高,其主要原因是加成产物
2 4
CHOH 分子之间能形成氢键,答案:平面三角;加成产物 CHOH 分子之间能形成氢键;
3 3
(5)①HO 分子含有的H-O键为极性键, O-O键为非极性键,正负电荷中心不重合,为极性分子。答
2 2
案:极性;非极性;极性;
②分子的溶解性可根据“相似相溶”规律解释,HO 为极性分子,而 CS 为非极性溶剂,根据“相似相
2 2 2
溶”规律,HO 难溶于 CS。
2 2 2
【变式9-2】(2023上·上海杨浦·高三复旦附中校考)NH 、HO 以及分子 PH 的空间结构和相应的键角
3 2 3
如下图所示。
(1)PH 中P的杂化类型是 ,HO 的键角小于 NH ,分析原因 。
3 2 3
(2)HO、PH 、KH按熔点由高到低的顺序排列为 。
2 3
(3) 的分子内部存在氢键,画出含氢键的分子结构: ,形成分子内氢键一般会使
得熔点 。(填“升高”或“降低”)
【答案】(1) sp3 NH 含有1个孤电子对,而HO含有2个孤电子对,HO中的孤电子对对成键
3 2 2
电子对的排斥作用较大
(2)KH>H O>PH
2 3(3) 较低
【解析】(1)由结构可知PH 中P的价层电子对数为4,P采用sp3杂化;
3
NH 含有1个孤电子对,而HO含有2个孤电子对,HO中的孤电子对对成键电子对的排斥作用较大,因
3 2 2
此HO 的键角小于 NH ;
2 3
(2)KH为离子晶体,HO、PH 均为分子晶体,HO分子间存在氢键,因此熔点:KH>H O>PH ;
2 3 2 2 3
(3) 的分子内部F原子与羟基H之间存在氢键,可表示为: ;形成分子内氢键使得分
子间作用力减弱,一般会使得熔点降低。
1.(2023·福建卷)某含锰着色剂的化学式为 ,Y、X、Q、Z为原子序数依次增大的短周期元
素,其中 具有正四面体空间结构, 结构如图所示。下列说法正确的是
A.键角: B.简单氢化物沸点:
C.第一电离能: D.最高价氧化物对应的水化物酸性:
【答案】C
【分析】由题意,Y、X、Q、Z为原子序数依次增大的短周期元素,其中 具有正四面体空间结构,可
知 为 ,故Y为H,X为N;同时分析 结构,可知Q正常情况应该成两根键,Q为ⅥA的元
素,同时Z也成5根键,Z为ⅤA的元素,故Q为O,Z为P。
【解析】A. 和 都是sp3杂化,但是 中有一对孤电子对,孤电子对对成键电子对的排斥作用
更大,在一个 是三角锥形结构,而 是正四面体结构,故键角: < ,A错误;
B.X、Q、Z分别为N、O、P,沸点顺序为 ,正确顺序为Q>X>Z,B错误;C.同主族元素从上到下第一电离能减小,同周期从左到右第一电离能有增大的趋势,故第一电离能:N>
O>Mn,C正确;
D.Z的最高价氧化物对应的水化物为 ,X最高价氧化物对应的水化物为 ,前者为中强酸而后者
为强酸,D错误;
故选C。
2.(2023·重庆卷)“嫦娥石”是中国首次在月球上发现的新矿物,其主要由 和 (钇,原
子序数比 大13)组成,下列说法正确的是
A.Y位于元素周期表的第ⅢB族
B.基态 原子的核外电子填充在6个轨道中
C.5种元素中,第一电离能最小的是
D.5种元素中,电负性最大的是
【答案】A
【解析】A.钇原子序数比 大13,为39号元素,为元素周期表的第五周期第ⅢB族,A正确;
B.钙为20号元素,原子核外电子排布为1s22s22p63s23p64s2,基态 原子的核外电子填充在10个轨道中,
B错误;
C.同一主族随原子序数变大,原子半径变大,第一电离能变小;同一周期随着原子序数变大,第一电离
能变大,5种元素中,钙第一电离能比铁小,C错误;
D.同周期从左到右,金属性减弱,非金属性变强,元素的电负性变强;同主族由上而下,金属性增强,
非金属性逐渐减弱,元素电负性减弱;5种元素中,电负性最大的是O,D错误;
故选A。
3.(2023·江苏卷)元素C、Si、Ge位于周期表中ⅣA族。下列说法正确的是
A.原子半径: B.第一电离能:
C.碳单质、晶体硅、SiC均为共价晶体 D.可在周期表中元素Si附近寻找新半导体材料
【答案】D
【解析】A.同主族元素原子半径从上往下原子半径增大,故原子半径: ,A错误;
B.同周期主族元素,从上往下原子半径增大,更易失电子,第一电离能: ,B错误;
C.晶体硅、SiC均为共价晶体,碳单质中金刚石为共价晶体,而石墨为混合晶体,C 为分子晶体,C错
60
误;
D.周期表中元素Si附近存在许多准金属,可在其周围寻找半导体材料,D正确。
故选D。
4.(2023·海南卷)下列有关元素单质或化合物的叙述正确的是
A. 分子呈正四面体,键角为
B.NaCl焰色试验为黄色,与Cl电子跃迁有关
C.Cu基态原子核外电子排布符合构造原理D. 是由极性键构成的极性分子
【答案】D
【解析】A. 分子呈正四面体,磷原子在正四面体的四个顶点处,键角为 ,A错误;
B.NaCl焰色试验为黄色,与Na电子跃迁有关,B错误;
C.Cu基态原子核外电子排布不符合构造原理,考虑了半满规则和全满规则,价电子排布式为3d104s1,这
样能量更低更稳定,C错误;
D. 的构型是V形,因此是由极性键构成的极性分子,D正确;
故选D。
5.(2023·广东卷)化合物 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有
Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周期,E
在地壳中含量最多。下列说法正确的是
A.元素电负性: B.氢化物沸点:
C.第一电离能: D. 和 的空间结构均为三角锥形
【答案】A
【分析】E在地壳中含量最多为氧元素,X的基态原子价层电子排布式为 ,所以 , ,X为
镁或者 ,X为锂,Y的基态原子价层p轨道半充满所以可能为氮或磷,Y和M同族所以为氮或磷,根
据X与M同周期、 化合价之和为零,可确定Z为氢元素、M为磷元素、X为镁元素、E为氧元
素、Y氮元素。
【解析】A.元素电负性:氧大于氮大于氢,A正确;
B.磷化氢、氨气、水固体均是分子晶体,氨气、水固体中都存在氢键沸点高,磷化氢没有氢键沸点低,
所以氢化物沸点:冰大于氨大于磷化氢,B错误;
C.同周期第一电离能自左向右总趋势逐渐增大,当出现第ⅡA族和第ⅤA族时比左右两侧元素电离能都
要大,所以氮大于氧大于镁 ,C错误;
D. 价层电子对为 ,有一对孤电子对,空间结构为三角锥形, 价层电子对为 ,没有
孤电子对, 空间结构为平面三角形,D错误;
故选A。
6.(2023·重庆卷) 和 均可发生水解反应,其中 的水解机理示意图如下:
下列说法正确的是
A. 和 均为极性分子 B. 和 中的 均为 杂化C. 和 的水解反应机理相同 D. 和 均能与 形成氢键
【答案】D
【解析】A. 中中心原子N周围的价层电子对数为:3+ =4,故空间构型为三角锥形,其分子
中正、负电荷中心不重合,为极性分子,而 中中心原子周围的价层电子对数为:4+ =4,是
正四面体形结构,为非极性分子,A错误;
B. 和 中中心原子N周围的价层电子对数均为:3+ =4,故二者 均为 杂化,B错误;
C.由题干NCl 反应历程图可知,NCl 水解时首先HO中的H原子与NCl 上的孤电子对结合,O与Cl结
3 3 2 3
合形成HClO,而SiCl 上无孤电子对,故SiCl 的水解反应机理与之不相同,C错误;
4 4
D. 和 分子中均存在N-H键和孤电子对,故均能与 形成氢键,D正确;
故答案为:D。
7.(2023·河北卷)锆 是重要的战略金属,可从其氧化物中提取。下图是某种锆的氧化物晶体的立方
晶胞, 为阿伏加德罗常数的值。下列说法错误的是
A.该氧化物的化学式为
B.该氧化物的密度为
C. 原子之间的最短距离为
D.若坐标取向不变,将p点 原子平移至原点,则q点 原子位于晶胞 面的面心
【答案】B
【解析】A.根据“均摊法”,晶胞中含4个Zr、 个O,则立方氧化锆的化学式为
ZrO,选项A正确;
2B.结合A分析可知,晶体密度为 ,选项B错误;
C. 原子之间的最短距离为面对角线的一般,即 ,选项C正确;
D.根据晶胞的位置可知,若坐标取向不变,将p点 原子平移至原点,则垂直向下,q点 原子位于晶
胞 面的面心,选项D正确;
答案选B。
8.(2023·河北卷)物质的结构决定其性质。下列实例与解释不相符的是
选项 实例 解释
A 用 替代 填充探空气球更安全 的电子构型稳定,不易得失电子
B 与 形成配合物 中的B有空轨道接受 中N的孤电子对
C 碱金属中 的熔点最高 碱金属中 的价电子数最少,金属键最强
D 不存在稳定的 分子 N原子价层只有4个原子轨道,不能形成5个 键
A.A B.B C.C D.D
【答案】C
【解析】A.氢气具有可燃性,使用氢气填充气球存在一定的安全隐患,而相比之下,氦气是一种惰性气体,
不易燃烧或爆炸,因此使用电子构型稳定,不易得失电子的氦气填充气球更加安全可靠,故A正确;
B.三氟化硼分子中硼原子具有空轨道,能与氨分子中具有孤对电子的氮原子形成配位键,所以三氟化硼
能与氨分子形成配合物 ,故B正确;
C.碱金属元素的价电子数相等,都为1,锂离子的离子半径在碱金属中最小,形成的金属键最强,所以碱
金属中锂的熔点最高,故C错误;
D.氮原子价层只有4个原子轨道,3个不成对电子,由共价键的饱和性可知,氮原子不能形成5个氮氟键,
所以不存在稳定的五氟化氮分子,故D正确;
故选C。
9.(2023·重庆卷)配合物[MA L]的分子结构以及分子在晶胞中的位置如图所示,下列说法错误的是
2 2
A.中心原子的配位数是4 B.晶胞中配合物分子的数目为2
C.晶体中相邻分子间存在范德华力 D.该晶体属于混合型晶体【答案】D
【解析】A.由题干配合物[MA L]的分子结构示意图可知,中心原子M周围形成了4个配位键,故中心原
2 2
子M的配位数是4,A正确;
B.由题干图示晶胞结构可知,晶胞中配合物分子的数目为 =2,B正确;
C.由题干信息可知,该晶体为由分子组成的分子晶体,故晶体中相邻分子间存在范德华力,C正确;
D.由题干信息可知,该晶体为由分子组成的分子晶体,D错误;
故答案为:D。
10.(2023·浙江卷)氮的化合物种类繁多,应用广泛。
请回答:
(1)基态N原子的价层电子排布式是 。
(2)与碳氢化合物类似,N、H两元素之间也可以形成氮烷、氮烯。
①下列说法不正确的是 。
A.能量最低的激发态N原子的电子排布式:
B.化学键中离子键成分的百分数:
C.最简单的氮烯分子式:
D.氮烷中N原子的杂化方式都是
②氮和氢形成的无环氮多烯,设分子中氮原子数为n,双键数为m,其分子式通式为 。
③给出 的能力: (填“>”或“<”),理由是 。
(3)某含氮化合物晶胞如图,其化学式为 ,每个阴离子团的配位数(紧邻的阳离子数)为
。
【答案】(1)2s22p3
(2) A NH ( ,m为正整数) < 形成配位键后,由于Cu对电子
n n+2−2m
的吸引,使得电子云向铜偏移,进一步使氮氢键的极性变大,故其更易断裂
(3) CaCN 6
2【解析】(1)N核电荷数为7,核外有7个电子,基态N原子电子排布式为1s22s22p3,则基态N原子的价
层电子排布式是2s22p3;故答案为:2s22p3。
(2)①A.能量最低的激发态N原子应该是2p能级上一个电子跃迁到3s能级,其电子排布式:
,故A错误;B.钙的金属性比镁的金属性强,则化学键中离子键成分的百分数:
,故B正确;C.氮有三个价键,最简单的氮烯即含一个氮氮双键,另一个价键与氢结合,
则其分子式: ,故C正确;D.氮烷中N原子有一对孤对电子,有三个价键,则氮原子的杂化方式
都是 ,故D正确;综上所述,答案为:A。
②氮和氢形成的无环氮多烯,一个氮的氮烷为NH ,两个氮的氮烷为NH,三个氮的氮烷为NH,四个氮
3 2 4 3 5
的氮烷为NH,设分子中氮原子数为n,其氮烷分子式通式为NH ,根据又一个氮氮双键,则少2个氢
4 6 n n+2
原子,因此当双键数为m,其分子式通式为NH ( ,m为正整数);故答案为:NH ( ,
n n+2−2m n n+2−2m
m为正整数)。
③ 形成配位键后,由于Cu对电子的吸引,使得电子云向铜偏移,进一步使氮氢键的极性变大,
故其更易断裂,因此给出 的能力: < (填“>”或“<”);故答案为:<; 形成
配位键后,由于Cu对电子的吸引,使得电子云向铜偏移,进一步使氮氢键的极性变大,故其更易断裂。
(3)钙个数为 , 个数为 ,则其化学式为CaCN ;根据六方最密
2
堆积图 ,以上面的面心分析下面红色的有3个,同理上面也应该有3个,本体中分析得到
,以这个 进行分析,其俯视图为 ,因此距离最近的钙离子个数为
6,其配位数为6;故答案为:CaCN ;6。
2
1.下列说法或化学用语的使用正确的是
A.符号为M的能层最多容纳的电子数为32个
B.构造原理呈现的能级交错源于光谱学实验C.Se的价层电子排布为:3d104s24p4
D.Ni的简化电子排布式:[Ar]3d94s1
【答案】B
【解析】A.符号为M是第3层,第3层包含3s、3p、3d三个能级,最多容纳的电子数为18个,故A错
误;
B.以光谱学事实为基础,从氢开始,随核电荷数递增,新增电子填入能级的顺序称为构造原理,构造原
理呈现的能级交错源于光谱学实验,故B正确;
C.Se位于第4周期第VIA族,价层电子排布为:4s24p4,故C错误;
D.Ni是28号元素,简化电子排布式:[Ar]3d84s2,故D错误;
故答案为B。
2.(2023上·全国·高三校联考期末)工业上可用 处理水体中的氨氮(NH 、NH )生成 。下列说
3
法正确的是
A.原子半径:
B.电负性:
C. 属于分子晶体
D.第一电离能:
【答案】B
【解析】A.同一周期元素的原子半径随原子序数的递增而减小;同一族的元素从上到下,随电子层数增
多,原子半径增大。原子半径: ,故A错误;
B.同一周期,从左到右元素电负性递增,同一主族,自上而下元素电负性递减,电负性:
,故B正确;
C. 属于离子晶体,故C错误;
D.N原子最外层电子为半满,第一电离能大于O原子,故D错误;
故答案选B。
3.(2023上·山东·高三校联考)某种离子液体的结构如图所示,X、Y、Z、M、Q为原子序数依次增大的
短周期元素,Z的原子序数等于X、Y原子序数之和,Q为非金属性最强的元素。
下列说法正确的是
A.氧化物对应水化物的酸性:ZM>Z>X>Y
【答案】D
【分析】根据题意,X、Y、Z、M、Q为原子序数依次增大的短周期元素,Z的原子序数等于X、Y原子
序数之和,Q为非金属性最强的元素,结合图中信息可知,Q为F,Z为C,X为H,Y为B,M为N,据
此分析解题。
【解析】A.Z和M的氧化物均有多种,无法比较对应水化物的酸性,故A错误;
B.MQ 分子NF ,有4个价层电子对,其VSEPR模型为四面体,故B错误;
3 3
C.C和N不能与氢元素形成含非极性键的二元化合物,故C错误;
D.Q为F,Z为C,X为H,Y为B,M为N,电负性:F>N>C>B>H,故D正确;
故答案选D。
4.在“石蜡→液体石蜡→石蜡蒸气→裂化气”的变化过程中,被破坏的作用力依次是
A.范德华力、范德华力、范德华力 B.范德华力、范德华力、共价键
C.范德华力、共价键、共价键 D.共价键、共价键、共价键
【答案】B
【解析】石蜡→液体石蜡破坏范德华力,液体石蜡→石蜡蒸气破坏范德华力,石蜡蒸气→裂化气破坏共价
键,故B符合题意。
答案选B。
5.(2023上·重庆·高三重庆南开中学校考)设 为阿伏加德罗常数的值,下列说法正确的是
A.32g ( )中含有 个S―S键
B.标准状况下22.4L 中含 个成键电子对
C.足量浓硫酸与1mol Zn完全反应,转移电子数为
D.1mol晶体硅中有 个Si―Si键
【答案】C
【解析】A.32g 的物质的量为0.125mol, 的结构为 ,一个分子含有8个S―S键,
0.125mol含有 个S―S键,故A错误;
B.标准状况下水不是气体,22.4L 无法确定成键电子对,故B错误;
C.足量浓硫酸与1mol Zn完全反应,生成二氧化硫和硫酸锌,一个锌原子失去2个电子,1mol Zn转移电
子数为 ,故C正确;
D.一个硅和周围四个硅形成Si―Si键,但是只有2个Si―Si键属于这个硅原子,1mol晶体硅中有 个
Si―Si键,故D错误;
故选:C。
6.(2023上·江苏常州·高三江苏省前黄高级中学校考)下列有关铁及其化合物的说法正确的是A. 元素位于元素周期表的VIIIB族
B.绿矾中 核外有6个未成对电子
C. (赤血盐)是含有配位键的离子化合物
D.若 (黄血盐)受热分解产物之一的晶胞结构如图所示,则其化学式为
【答案】C
【解析】A.Fe是26号元素,位于周期表的第Ⅷ族,A项错误;
B. 价电子排布为 ,核外有4个未成对电子,B项错误;
C. (赤血盐)中 通过配位键与6个 结合为 , 是含有配位
键的离子化合物,C项正确;
D.若 (黄血盐)受热分解产物之一的晶胞结构如图所示,根据均摊原则,碳原子数为
、铁原子数为 ,则其化学式为 ,D项错误;
故选C。
7.(2024上·河北石家庄·高三石家庄二中校联考)稀磁半导体LiZnAs 的立方晶胞结构如下图所示,已
x y z
知N、Q两点对应的原子坐标分( , , )和( , ,0),阿伏加德罗常数的值为N ,下列说法错误的
A
是
A.该晶体的化学式为LiZnAs
B.该晶体中M点的原子坐标为( , , )
C.晶体的密度为 g/cm3D.晶胞x轴方向的投影图
【答案】D
【解析】A.根据均摊法计算:Li位于棱上和体心,其个数: ;As位于晶胞体内,其个数:
4;Zn位于顶角和面心,其个数: ,所以其化学式:LiZnAs,A正确;
B.M点对应原子为As,As原子在晶胞中八个小立方体的4个体心,参考N、Q两点坐标,其坐标为:(
, , ),B正确;
C.参考A选项,晶胞中含4个LiZnAs,晶胞质量: ,晶胞体积: ,晶胞
密度: ,C正确;
D.As原子在晶胞中八个小立方体的4个体心,其晶胞x轴方向的投影图: ,D错误;
答案选D。
8.(2024上·河北石家庄·高三石家庄外国语学校)采用了氮化镓元件的充电器体积小、质量轻,在发热量、
效率转换上相比普通充电器也有更大的优势,被称为“快充黑科技”,下图是氮化镓的三种晶体结构(N
A
表示阿伏加德罗常数的值)。下列有关说法错误的是
A.Ga、N均属于p区元素
B.图a晶体结构中含有6个Ga、6个N
C.图b晶体结构中若Ga和N的距离为xnm,则晶体的密度为
D.三种晶体结构中Ga原子的配位数之比为3∶2∶3
【答案】D
【解析】A. Ga、N的价电子分别是4s24p1、2s22p3、Ga、N均属于p区元素,故A正确;B. 图a晶体结构中 含有12× +2× +3=6个Ga、6× +4=6个N,故B正确;
C. 图b晶体结构中若Ga和N的距离为xnm,取晶胞的八分之一作为一个小立方体,小立方体的对角线
为2xnm,小立方体的边长为 nm,晶胞的边长为2 nm,则晶体的密度为ρ=
= ,故C正确;
D. a的晶胞为 ,Ga原子的配位数为4,三种晶体结构中Ga原子的配位数之比为
4∶4∶6=2∶2∶3,故D错误;
故选D。
9.已知一些物质的熔点数据如表:
物质 熔点/℃
NaCl 800.7
SiCl -68.8
4
GeCl -51.5
4
SnCl -34.1
4
Na与Si均为第三周期元素,NaCl熔点明显高于SiCl ,原因是 。分析同族元素的氯化物SiCl 、
4 4
GeCl 、SnCl 熔点变化趋势及其原因 。SiCl 的空间结构为 ,其中Si的轨道杂化形式为
4 4 4
。
【答案】 氯化钠为离子晶体,SiCl 为分子晶体 SiCl 、GeCl 、SnCl 均为分子晶体,其熔点依次
4 4 4 4
升高;分子晶体中,组成与结构相似的物质,相对分子质量越大,分子间作用力越大,物质的熔点越高
正四面体 sp3
【解析】一般情况下,不同类型晶体的熔点大小关系为共价晶体>离子晶体>分子晶体。钠与氯的电负性差
值较大,形成离子晶体;Si与Cl的电负性差值不大,形成分子晶体,故NaCl熔点明显高于SiCl 。SiCl 、
4 4
GeCl 、SnCl 均为分子晶体,且三者组成结构相似,相对分子质量越大,分子间作用力越大,物质的熔点
4 4越高,故其熔点依次升高。SiCl 中心原子Si没有孤电子对,只有4个共用电子对,故其空间构型为正四面
4
体,Si的轨道杂化形式为sp3杂化。