文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(浙江专用)
黄金卷04
(考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 Si 28 P 31 S 32 Cl
35.5 K 39 Ca 40 Mn 55 Fe 56 Cu 64 Zn 65 Br 80 Ag 108 Ba 137
第Ⅰ卷
一、单项选择题:共16题,每题3分,共48分。每题只有一个选项最符合题意。
1.下列物质含有非极性共价键且属于分子晶体的是( )
A.HO B.NaS C.CO D.NaO
2 2 2 2 2 2
2.下列化学用语表示正确的是
A.中子数为10的氧原子: 8O
18
B.1-丁醇的键线式:
C.CO2-的空间结构为三角锥形
3
D.某激发态碳原子的轨道表示式:
3.ClO 是一种新型的自来水消毒剂,下列说法不正确的是( )
2
A.ClO 属于非电解质 B.ClO 具有强氧化性
2 2
C.ClO 为直线形分子 D.电负性:O>Cl
2
4.下列说法不正确的是( )
A.食品中添加适量的SO 可起到漂白、防腐和抗氧化等作用
2
B.KAl(SO )·12H O具有强氧化性,可用作消毒剂
4 2 2
C.钛的合金与人体“相容性”好,可用于制造人造骨骼
D.NH 分子间存在较多的氢键,液氨常用作制冷剂
3
5.利用下列装置和试剂进行实验,能达到实验目的的是( )
A.观察钠的 C.检验CHCHBr与 D.铁片表面
B.制备氢氧化铁胶体 3 2
燃烧 NaOH乙醇溶液反应后的气 镀铜(夹持装置省略) 态产物
6.电极材料LiFePO 制备的反应为6FePO +3Li CO+C H O 9CO↑+6LiFePO +6H O,下列说法正
4 4 2 3 6 12 6 4 2
确的是( )
A.生成0.1 mol LiFePO ,转移的电子数为0.1N
4 A
B.还原产物为LiFePO 和CO
4
C.标准状况下,生成20.16L CO时,被还原的C H O 为0.1 mol
6 12 6
D.还原剂与氧化剂的物质的量之比为1∶6
7.氨对水体的污染情况越来越受人们的重视。用次氯酸钠可以脱除水中的NH ,其反应式为:
3
2NH +3NaClO=N +3NaCl+3HO。设N 为阿伏加德罗常数值,下列说法正确的是( )
3 2 2 A
A.33.6LNH 中所含的 键数目为4.5N
3 A
B.2L0.5mol/LNaClO溶液中含有的ClO-数目为N
A
C.若该反应生成27gHO时,转移的电子数为3N
2 A
D.该反应中氧化剂与还原剂物质的量之比为2:3
8.下列说法正确的是( )
A.淀粉和纤维素都属于高分子化合物,都能发生水解反应和酯化反应
B.蛋白质受某些因素影响,其空间结构发生变化 一级结构不变 ,引起其理化性质和生物活性的变
化,此时发生了蛋白质的盐析
C.苯酚与甲醛在碱作用下可得到网状结构的酚醛树脂,属于热塑性塑料
D.油脂在酸性条件下的水解可以得到高级脂肪酸盐,常用于生产肥皂
9.下列离子方程式书写正确的是( )
A.硝酸钡溶液中通入少量SO :Ba2++NO -+SO +HO=BaSO↓+NO+H+
2 3 2 2 4
B.用过量的碳酸钠溶液吸收氯气:CO2-+Cl =CO +ClO-+Cl-
3 2 2
C.氯乙酸乙酯在足量NaOH溶液中加热:ClCH COOC H+OH- ClCH COO-+C HOH
2 2 5 2 2 5
D.铝片投入过量的NaOH溶液中发生反应:2Al+2OH-+2H O=2Al(OH) -+3H ↑
2 4 2
10.对布洛芬分子进行如下图所示的修饰,可以减轻布洛芬的副作用。下列说法不正确的是( )已知: 的性质与 相似。
A.乙的分子式为C H ON
19 21 2
B.1mol乙最多能与6mol H 发生加成反应
2
C.甲和乙都能与氢氧化钠溶液发生反应
D.分子修饰后,在水中的溶解性明显下降
11.R、X、Y、Z、M五种短周期主族元素,原子序数依次增大。基态R原子每个能级上电子数相
等,基态X原子的价层电子排布为 ,Y与M同主族,Z是同周期元素中原子半径最大的元素,Z
核电荷数等于X、M原子的最外层电子数之和。下列说法不正确的是( )
A.电负性:Y>X>R
B.原子半径:Z>M>Y
C.氢化物的沸点:R<Y
D.Z与Y可形成两种常见的离子化合物,且晶体中的阴阳离子个数比均为1∶2
12.氨既是一种重要的化工产品,又是一种重要的化工原料。如图为合成氨以及氨氧化制硝酸的流程
示意图。下列说法不正确的是( )
A.合成塔内发生的反应中有非极性键的断裂和极性键的生成
B.氧化炉内发生的反应氧化剂与还原剂的物质的量之比为5∶4
C.使用 溶液吸收尾气中的氮氧化物, 和NO 是酸性氧化物
2
D.向吸收塔中通入O 的作用是氧化
2
13.海水原位直接电解制氢技术是利用海水侧和电解质侧的水蒸气压力差使海水自然蒸发,并以蒸汽
形式通过透气膜扩散到电解质侧重新液化,为电解提供淡水(工作时KOH溶液的浓度保持不变)。装置如图所示,下列叙述不正确的是( )
A.M电极反应式为4OH―-4e-=O↑+2HO
2 2
B.该技术避免了生成强氧化性的含氯粒子腐蚀电极
C.离子交换膜b为阳离子交换膜
D.当产生标准状况下33.6L H 时,有1.5mol H O(g)透过透气膜a
2 2
14.已知反应NO (g)+CO(g) NO(g)+CO(g)的能量变化如图所示,下列说法正确的是( )
2 2
A.该反应的ΔH=(E - E )kJ·mol−1
2 1
B.正反应活化能E 等于反应物的键能之和
1
C.由图可知升温对NO (g)+CO(g) NO(g)+CO(g)的逆反应速率影响更大
2 2
D.恒温条件下,缩小容器体积,平衡不移动,所以正逆反应速率均不变
15.25℃时,某小组做如下两组实验:
实验Ⅰ:分别往浓度均为0.10mol·L-1NaHCO 、NaCO 溶液中通入CO 至 ;
3 2 3 2
实验Ⅱ:在1.0L、0.10mol·L-1NaCO 溶液中加入0.010mol BaSO 固体,充分反应。
2 3 4
[已知:25℃,HCO 的电离常数 、 ; 、
2 3
。混合后溶液体积变化忽略不计]。下列说法不正确的是( )
A.0.10mol·L-1NaHCO 、NaCO 溶液中水的电离程度:NaCO>NaHCO
3 2 3 2 3 3B.实验Ⅰ结束后,NaCO、NaHCO 溶液中均有c(HCO -)>c(H CO)
2 3 3 3 2 3
C.实验Ⅱ的转化存在平衡常数:
D.实验Ⅱ中,改用饱和NaCO 溶液,NaCO 的平衡转化率减小
2 3 2 3
16.下列方案设计、现象和结论不正确的是( )
实验方案 现象 结论
试管中依次加入3mL乙醇2mL浓硫酸、2mL 饱和碳酸钠液面上出现
A 有酯类物质生成
乙酸及沸石后连接好装置并加热 有香味的无色油状液体
将SnCl 液体和CuSO 固体分别暴露在潮湿空 相同条件下水解程度:
B 4 4 只有前者会冒“白烟”
气中 SnCl>CuSO
4 4
溶液变浑浊且有刺激性 NaSO 既体现还原性又体
C 室温下,将NaSO 溶液和稀HSO 混合 2 2 3
2 2 3 2 4 气味的气体生成 现氧化性
向2 mL0.1mol·L-1 KCr O 溶液中加入5滴 c(H + ) 减 小 , 平 衡 向
D 2 2 7 溶液由橙色变黄色
溶液 c(CrO2-)减小的方向移动
2 7
第Ⅱ卷
二、非选择题:共5题,共52分。
17.(10分)铝是常见金属,其合金、化合物在生产生活中有重要应用。请回答:
(1)能量最低的激发态Al3+的核外电子排布式是 。
(2)铝能与H、C、N、F、Cl 等元素形成多种化合物
①下列说法不正确的是 。
A.NaAlH 中Al原子的杂化方式是sp2
4
B.化学键中离子键成分的百分数:AlF>AlBr
3 3
C.AlNH 分子中有6对共用电子对
6
D.NaAlF 中所有原子或离子满足8 电子稳定结构
6
②常温下 AlCl 在四氯化碳中的溶解度大于MgCl ,理由是 。
3 2
③三乙基铝是一种金属有机物,结构简式为Al(C H),可做高能火箭燃料,原因是 。
2 5 3
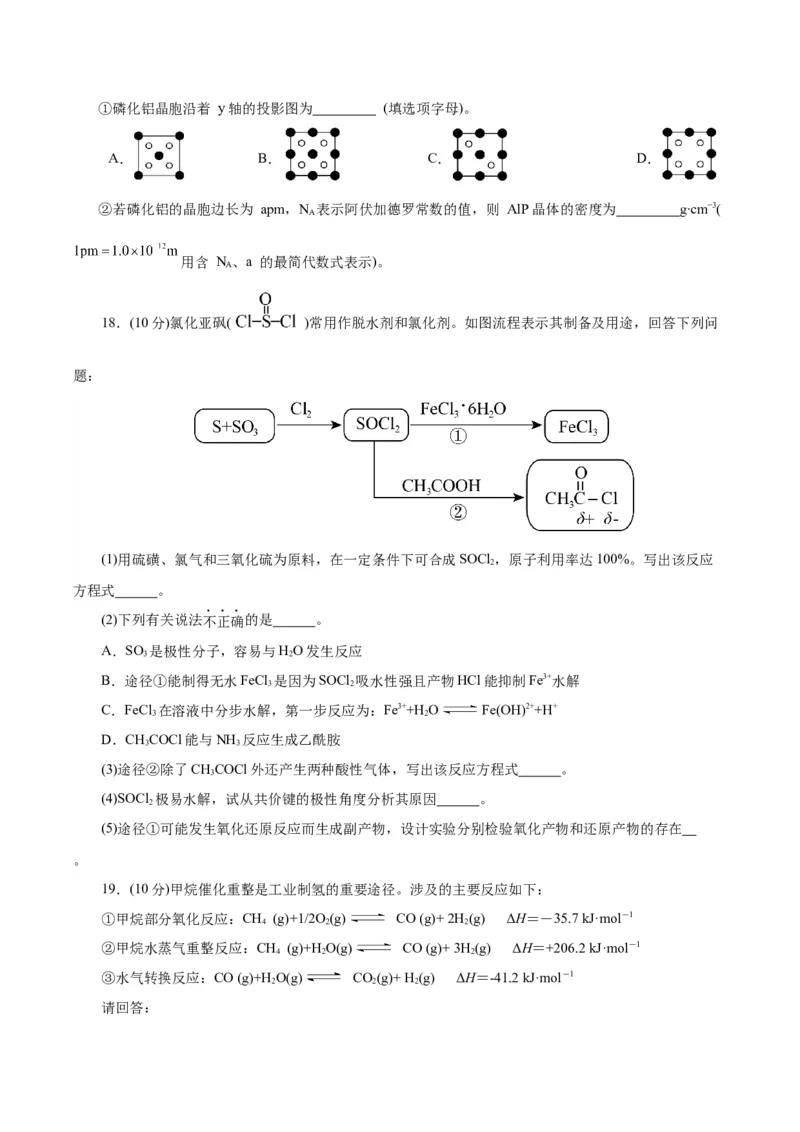
(3)AlP 晶胞结构如下图所示:①磷化铝晶胞沿着 y轴的投影图为 (填选项字母)。
A. B. C. D.
②若磷化铝的晶胞边长为 apm,N 表示阿伏加德罗常数的值,则 AlP晶体的密度为 g∙cm−3(
A
用含 N 、a 的最简代数式表示)。
A
18.(10分)氯化亚砜( )常用作脱水剂和氯化剂。如图流程表示其制备及用途,回答下列问
题:
(1)用硫磺、氯气和三氧化硫为原料,在一定条件下可合成SOCl ,原子利用率达100%。写出该反应
2
方程式 。
(2)下列有关说法不正确的是 。
A.SO 是极性分子,容易与HO发生反应
3 2
B.途径①能制得无水FeCl 是因为SOCl 吸水性强且产物HCl能抑制Fe3+水解
3 2
C.FeCl 在溶液中分步水解,第一步反应为:Fe3++H O Fe(OH)2++H+
3 2
D.CHCOCl能与NH 反应生成乙酰胺
3 3
(3)途径②除了CHCOCl外还产生两种酸性气体,写出该反应方程式 。
3
(4)SOCl 极易水解,试从共价键的极性角度分析其原因 。
2
(5)途径①可能发生氧化还原反应而生成副产物,设计实验分别检验氧化产物和还原产物的存在
。
19.(10分)甲烷催化重整是工业制氢的重要途径。涉及的主要反应如下:
①甲烷部分氧化反应:CH (g)+1/2O (g) CO (g)+ 2H (g) ΔH=-35.7 kJ·mol-1
4 2 2
②甲烷水蒸气重整反应:CH (g)+HO(g) CO (g)+ 3H (g) ΔH=+206.2 kJ·mol-1
4 2 2
③水气转换反应:CO (g)+H O(g) CO(g)+ H (g) ΔH=-41.2 kJ·mol-1
2 2 2
请回答:(1)甲烷水蒸气重整—水气变换耦合反应为CH (g)+2HO(g) CO (g)+ 4H (g),该反应的ΔH =
4 2 2 2
kJ·mol-1,该反应自发进行的条件是 。
(2)一定温度下,恒容反应器中注入初始浓度均为1mol·L-1的原料气CH (g)、O(g)、HO(g),充分反
4 2 2
应达到平衡状态,测得c [CH (g)]= c [CO(g)]=0.25mol·L-1、c [O (g)]=0.75mol·L-1。该条件下反应③的平衡
4 2 2
常数为 。
(3)下列说法正确的是_______。
A.通过控制氧气用量,有利于实现甲烷重整过程的热平衡
B.升高温度,水气变换反应速率降低,H 产率降低
2
C.恒压条件比恒容条件利于提高CH 平衡转化率
4
D.一定温度下,恒容反应器中c [CO(g)]:c [CO(g)]=1,说明反应达到平衡状态
2
(4)在进气量为 下,CH (g)、O(g)、HO(g)以恒定比例通入催化反应器,研究温度对反
4 2 2
应的影响。结果如图1所示。
①
①在图2中画出CH 转化率与温度关系示意图 。
4
②近年来发展了钯膜催化甲烷重整制氢技术,反应器中 选择性透过膜的机理如图3所示。说明该制
备技术的优点: 。
20.(10分)溴化亚铜可用作工业催化剂,是一种白色粉末,微溶于冷水,不溶于乙醇等有机溶剂,在
热水中或见光都会分解,在空气中会慢慢氧化成绿色粉末。制备CuBr的实验步骤如下:
(1)实验所用蒸馏水需经煮沸,煮沸目的是___________。步骤III中用“溶有SO ”蒸馏水洗涤的方法是
2___________。
(2)下列说法不正确的是___________。
A.实验过程中可加少量还原 粉防止CuBr被氧化
B.多孔玻璃泡可以增大气体与溶液的接触面积,起到充分反应目的
C.防止CuBr见光分解,步骤3过滤需避光进行
D.洗涤时,为防止 被氧化需用玻璃棒快速搅拌多次以加快洗涤速度
(3)判断反应已完成的简单方法___________。
(4)欲利用上述装置烧杯中的吸收液(经检测主要含NaSO 、NaHSO 等)制取较纯净的NaSO ·7H O晶
2 3 3 2 3 2
体。从下列选项中选择最佳操作并排序___________。
____→____→(⑥)→____→____→____→(⑦)
①蒸发浓缩至出现大量晶体②蒸发浓缩至出现晶膜,冷却结晶③乙醇洗涤2~3次④热水洗涤2~3次
⑤过滤⑥加入少量维生素C溶液(抗氧剂)⑦真空干燥⑧烧杯中加入100g20%的NaOH溶液⑨烧杯中通入
SO 至饱和
2
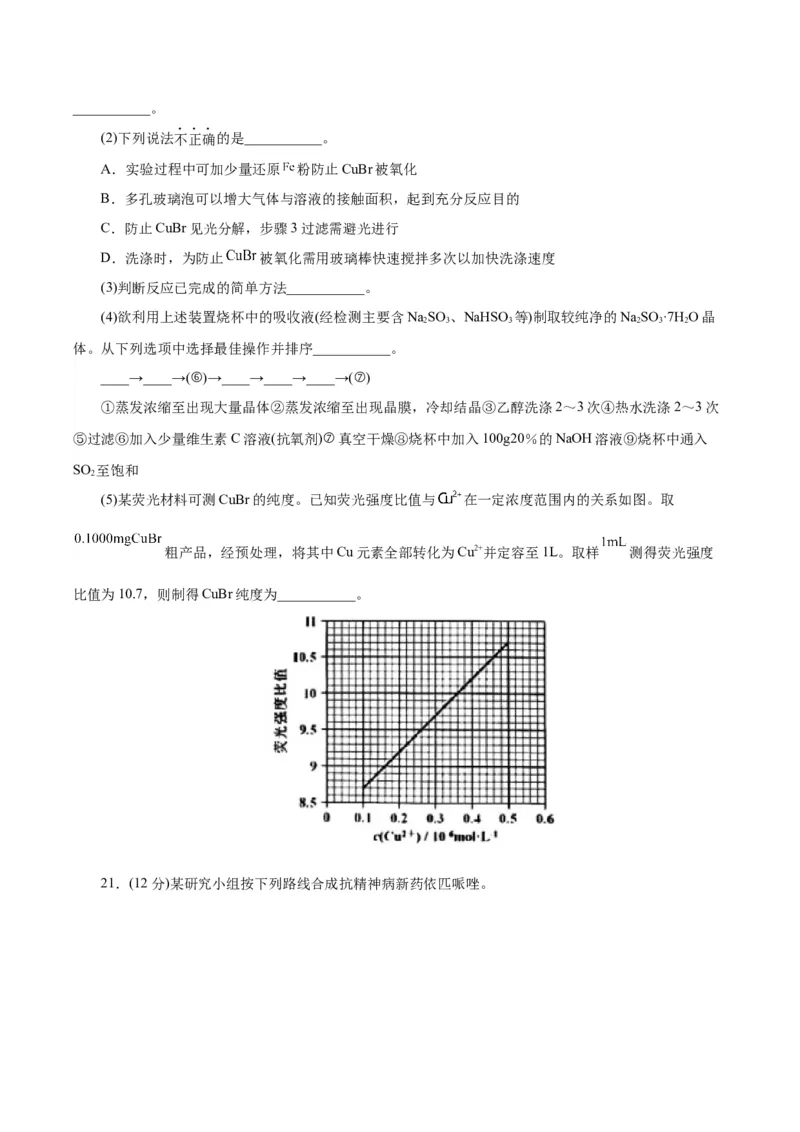
(5)某荧光材料可测CuBr的纯度。已知荧光强度比值与 在一定浓度范围内的关系如图。取
粗产品,经预处理,将其中Cu元素全部转化为Cu2+并定容至1L。取样 测得荧光强度
比值为10.7,则制得CuBr纯度为___________。
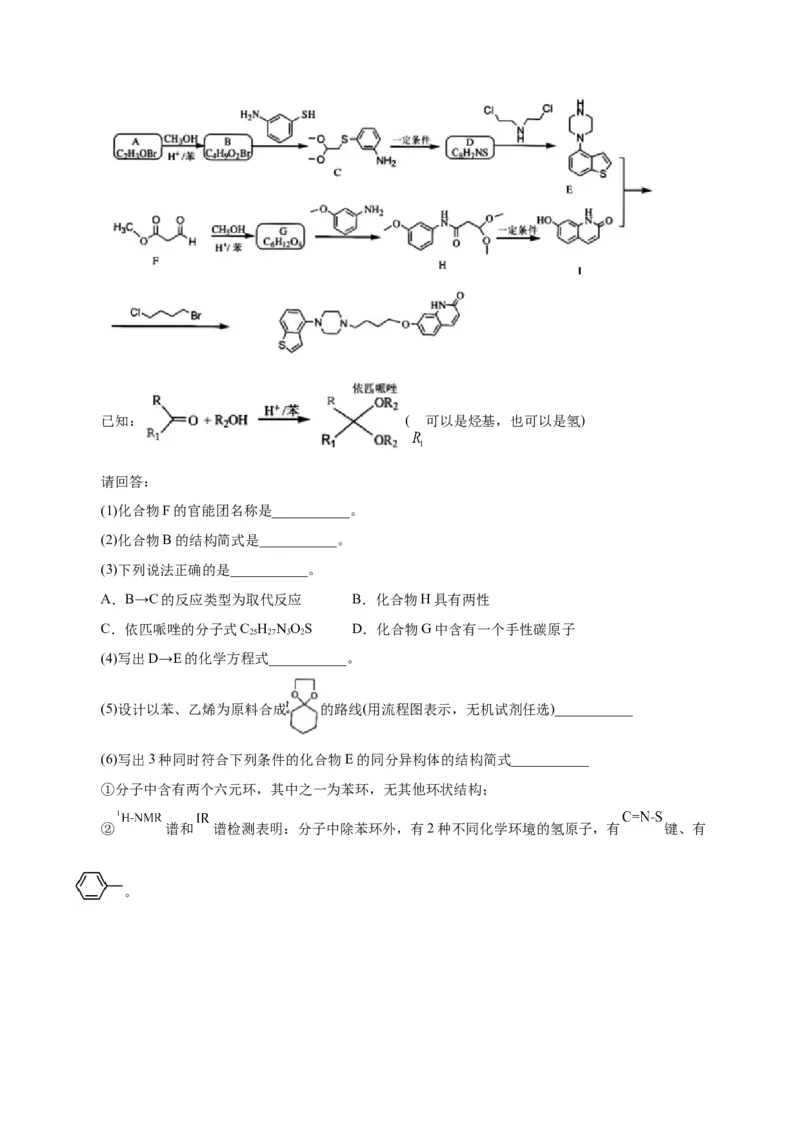
21.(12分)某研究小组按下列路线合成抗精神病新药依匹哌唑。已知: ( 可以是烃基,也可以是氢)
请回答:
(1)化合物F的官能团名称是___________。
(2)化合物B的结构简式是___________。
(3)下列说法正确的是___________。
A.B→C的反应类型为取代反应 B.化合物H具有两性
C.依匹哌唑的分子式C H NOS D.化合物G中含有一个手性碳原子
25 27 3 2
(4)写出D→E的化学方程式___________。
(5)设计以苯、乙烯为原料合成 的路线(用流程图表示,无机试剂任选)___________
(6)写出3种同时符合下列条件的化合物E的同分异构体的结构简式___________
①分子中含有两个六元环,其中之一为苯环,无其他环状结构;
② 谱和 谱检测表明:分子中除苯环外,有2种不同化学环境的氢原子,有 键、有
。