文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(辽宁专用)
黄金卷04
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64
第Ⅰ卷
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项符合题目要
求。
1.我国古代先民在生活、生产过程中积累了丰富的化学知识。下列有关说法中错误的是
A.《天工开物》中记载的琉璃石与水晶的成分相同,二者均为单晶硅
B.《吕氏春秋》中记载了有关青铜的性质,青铜的硬度比铜的硬度大
C.《本草纲目》中记载的有关乙醇和水的分离过程,应用了蒸馏操作
D.《本草经集注》中利用“火烧法”区分 和 ,应用了焰色试验
2.下列有关化学用语的表述中正确的是
A.质量数为34的 的结构示意图为
B.四氯化碳的电子式为
C. 甲基丁烷的球棍模型为
D.基态 的价电子排布图为
3.设 为阿伏加德罗常数的值。下列有关叙述正确的是
A.10 g 60%的乙酸水溶液中含有的氧原子总数为0.2
B.常温常压下,15g甲基碳正离子( )所含的电子数为8
C.0.5 mol的 和 混合物中,所含阴离子数为D.标准状况下,22.4 L 参加反应时,转移电子数为2
4.下列反应的离子方程式正确的是
A.向硫代硫酸钠溶液中滴入稀硝酸:
B.向苯酚钠溶液中通入少量二氧化碳:2 +CO +H O=2 +
2 2
C.氧化铜与氨水:
D.向次氯酸钠溶液中通入少量二氧化硫:
5.反应 。下列说法不正确的是
A.该反应在低温下能自发进行是由于 的影响
B.该反应的平衡常数
C.实际生产中选择高温是因为高温时Si的平衡转化率比低温时大
D.其他条件不变时,可通过缩小体积增大压强提高Si的转化率
6.类比推理是化学中常用的思维方法。下列推理正确的是
A.Na与 在加热条件下反应生成 ,故可推测Li与 在加热条件下反应生成
B. 可用作医疗X射线检查的内服药剂,俗称“钡餐”,故可推测 也用作“钡餐”
C.工业上采用电解熔融NaCl的方法冶炼金属钠,故工业上也可用电解熔融 的方法冶炼金属铝
D. 与 反应生成 ,故可推测 与 反应生成
7.下列说法正确的是
2
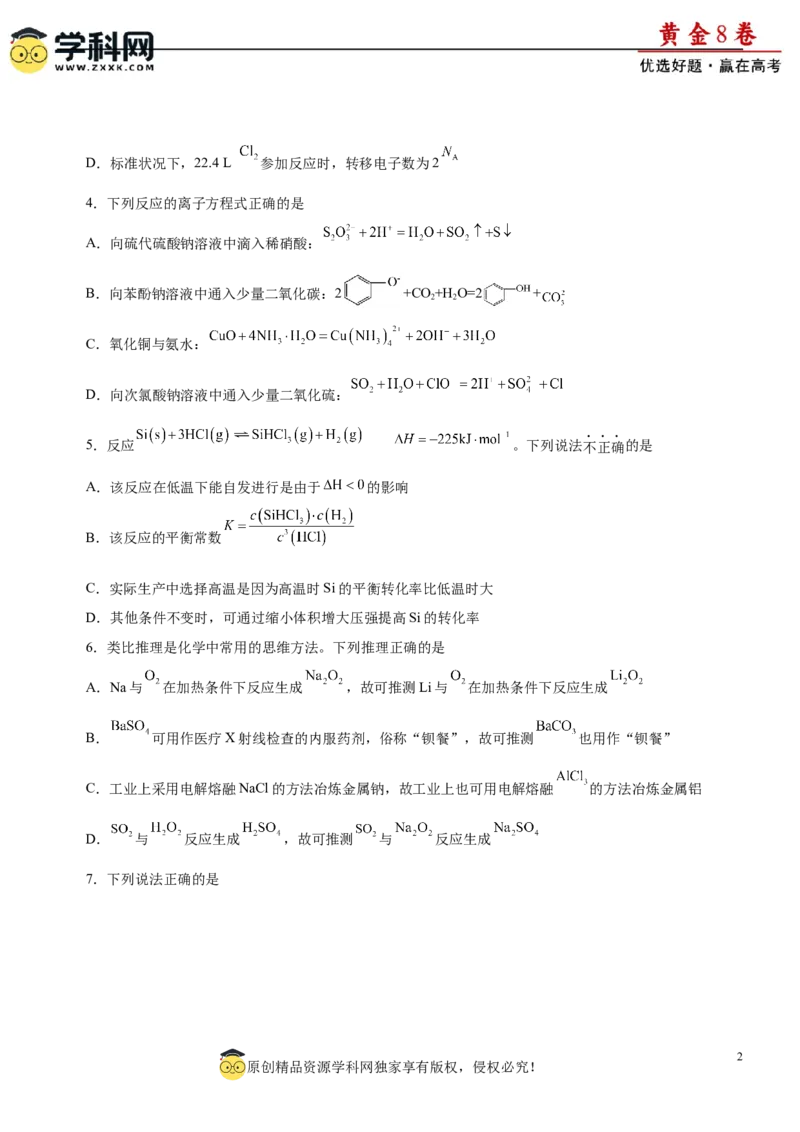
原创精品资源学科网独家享有版权,侵权必究!A.图①操作配制银氨溶液 B.图②装置可用于分离溴苯和苯
C.图③操作测定氯水的pH D.图④装置可用于比较Cl、S元素的非金属性
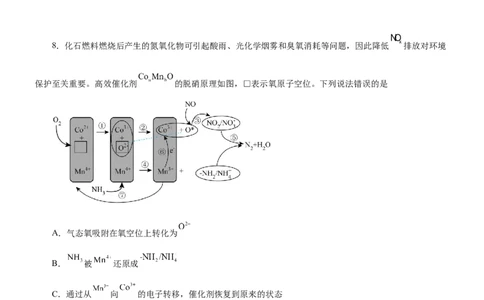
8.化石燃料燃烧后产生的氮氧化物可引起酸雨、光化学烟雾和臭氧消耗等问题,因此降低 排放对环境
保护至关重要。高效催化剂 的脱硝原理如图,□表示氧原子空位。下列说法错误的是
A.气态氧吸附在氧空位上转化为
B. 被 还原成
C.通过从 向 的电子转移,催化剂恢复到原来的状态
D.Co和 之间的协同效应在提高 催化剂的活性方面起着关键作用
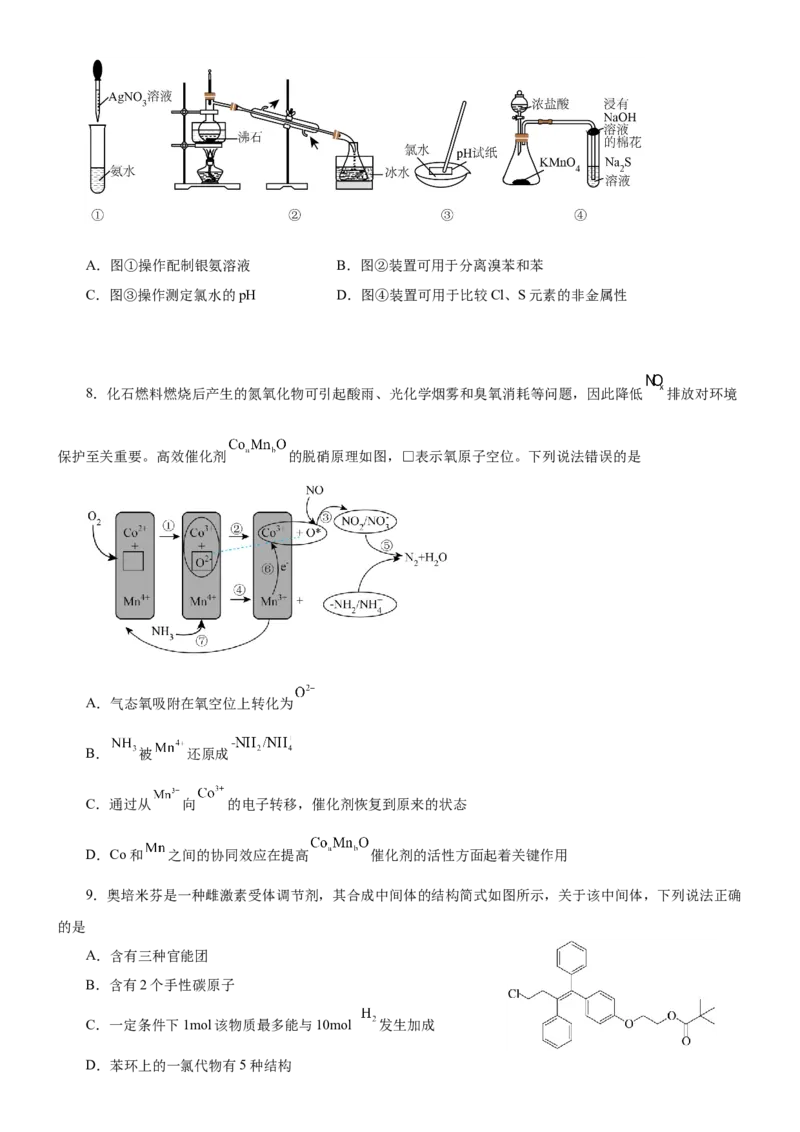
9.奥培米芬是一种雌激素受体调节剂,其合成中间体的结构简式如图所示,关于该中间体,下列说法正确
的是
A.含有三种官能团
B.含有2个手性碳原子
C.一定条件下1mol该物质最多能与10mol 发生加成
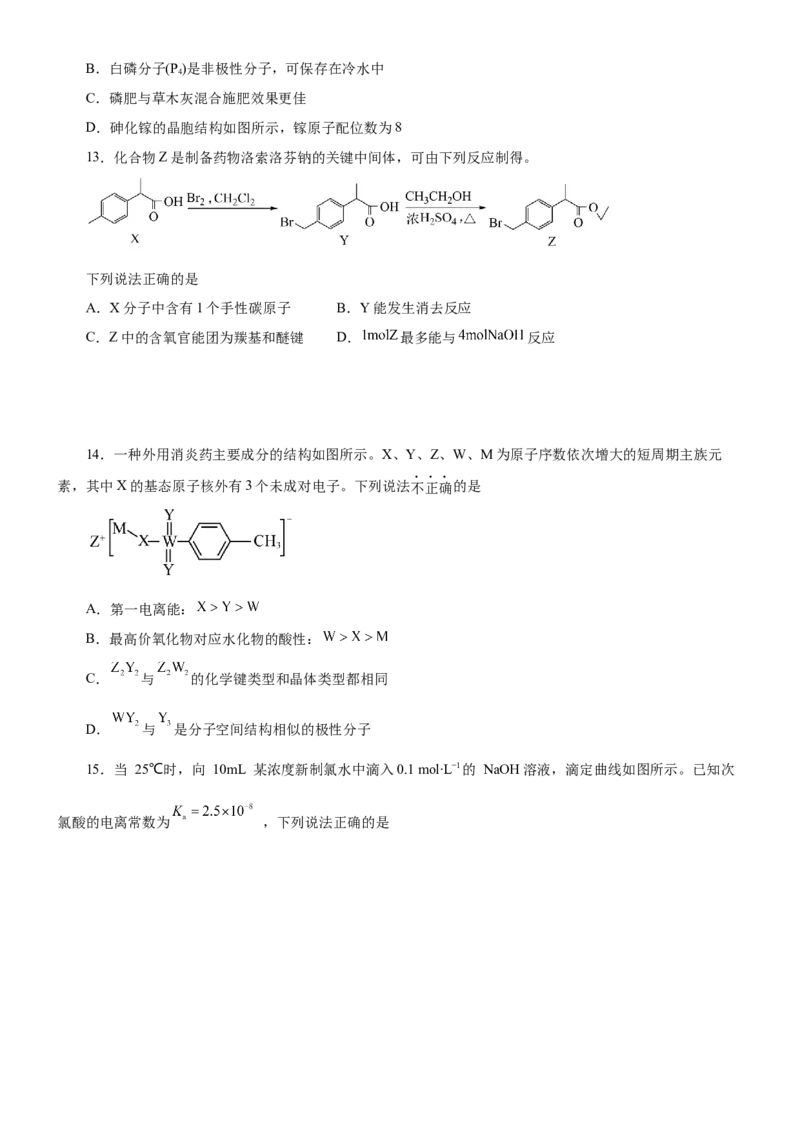
D.苯环上的一氯代物有5种结构10.某科研人员提出HCHO与O 在羟基磷灰石(HAP)表面催化氧化生成CO、HO的历程,该历程示意图
2 2 2
如下(图中只画出了HAP的部分结构)。
下列说法正确的是
A.HAP能降低HCHO与O 的反应的活化能,增大了平衡转化率
2
B.该历程中有非极性键的断裂,没有非极性键形成
C.HCHO分子中σ键与π键之比为2:1
D.根据图示信息,CO 分子中的氧原子全部来自O
2 2
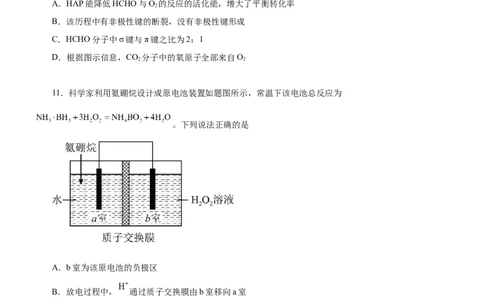
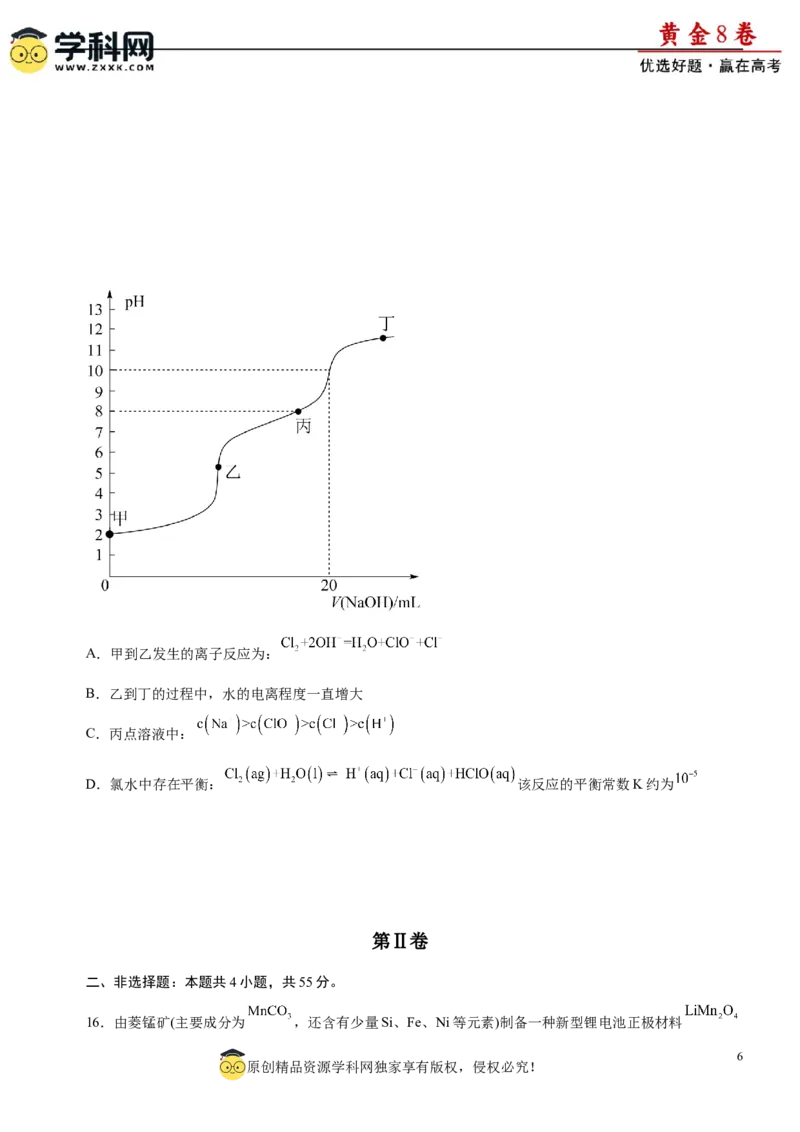
11.科学家利用氨硼烷设计成原电池装置如题图所示,常温下该电池总反应为
。下列说法正确的是
A.b室为该原电池的负极区
B.放电过程中, 通过质子交换膜由b室移向a室
C.a室的电极反应式为
D.其他条件不变时,向 溶液中加入适量 溶液能增大电流强度
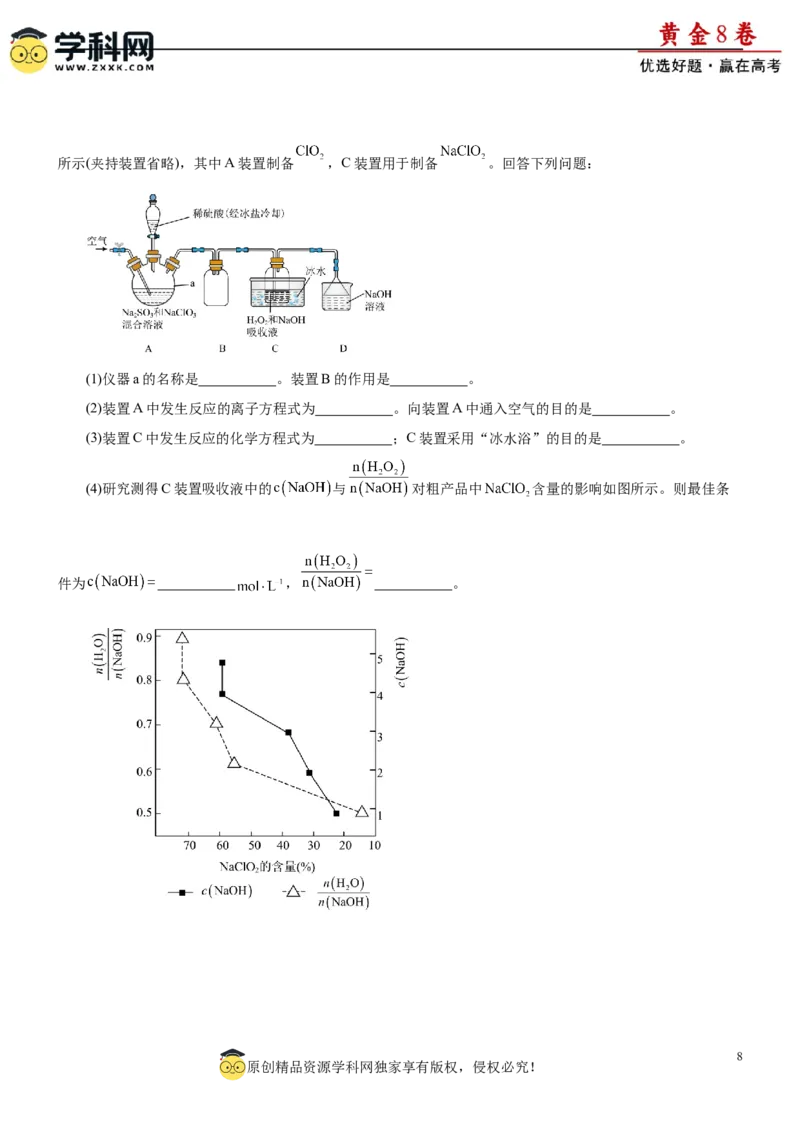
12.已知:氮、磷、砷元素广泛应用于生产生活中,NH 、NH、NO、NO 、HNO 等是氮的重要化合物,
3 2 4 2 3
白磷(P )易自燃,易溶于CS,Ca(HPO ) 是磷肥的有效成分;砷化镓是重要的半导体材料。下列有关说法正确
4 2 2 4 2
的是
A.NH、NO 、HNO 中N的杂化方式均为sp2
2 4 2 3
4
原创精品资源学科网独家享有版权,侵权必究!B.白磷分子(P )是非极性分子,可保存在冷水中
4
C.磷肥与草木灰混合施肥效果更佳
D.砷化镓的晶胞结构如图所示,镓原子配位数为8
13.化合物Z是制备药物洛索洛芬钠的关键中间体,可由下列反应制得。
下列说法正确的是
A.X分子中含有1个手性碳原子 B.Y能发生消去反应
C.Z中的含氧官能团为羰基和醚键 D. 最多能与 反应
14.一种外用消炎药主要成分的结构如图所示。X、Y、Z、W、M为原子序数依次增大的短周期主族元
素,其中X的基态原子核外有3个未成对电子。下列说法不正确的是
A.第一电离能:
B.最高价氧化物对应水化物的酸性:
C. 与 的化学键类型和晶体类型都相同
D. 与 是分子空间结构相似的极性分子
15.当 25℃时,向 10mL 某浓度新制氯水中滴入0.1 mol∙L−1的 NaOH溶液,滴定曲线如图所示。已知次
氯酸的电离常数为 ,下列说法正确的是A.甲到乙发生的离子反应为:
B.乙到丁的过程中,水的电离程度一直增大
C.丙点溶液中:
D.氯水中存在平衡: 该反应的平衡常数K约为
第Ⅱ卷
二、非选择题:本题共4小题,共55分。
16.由菱锰矿(主要成分为 ,还含有少量Si、Fe、Ni等元素)制备一种新型锂电池正极材料
6
原创精品资源学科网独家享有版权,侵权必究!的工艺流程如下:
已知:① , , ,
, 。
②当溶液中离子浓度小于 时,可视为沉淀完全。
③ 可溶于水。
(1)基态锰原子的核外电子排布式为 。
(2)加入少量 的目的是氧化 ,实际生产中不用 替代 的原因是 。
(3)溶矿反应完成后,先向反应后溶液中加入石灰乳至溶液 ,再加 进一步除去 。加石灰乳调
节溶液pH时,不直接将 沉淀完全为 的原因是 。
(4)若分离后的溶液中 ,要使 完全除尽,则需控制 的范围为 ;生产
中也可用 (填化学式)代替 除去 ,同时增加 产量。
(5)电解废液中可循环利用的物质是 (填化学式)
(6)煅烧时,生成 的化学方程式为 。
17.纯 遇热易发生分解,工业上通常制成 固体以便运输和储存。制备 的实验装置如图所示(夹持装置省略),其中A装置制备 ,C装置用于制备 。回答下列问题:
(1)仪器a的名称是 。装置B的作用是 。
(2)装置A中发生反应的离子方程式为 。向装置A中通入空气的目的是 。
(3)装置C中发生反应的化学方程式为 ;C装置采用“冰水浴”的目的是 。
(4)研究测得C装置吸收液中的 与 对粗产品中 含量的影响如图所示。则最佳条
件为 , 。
8
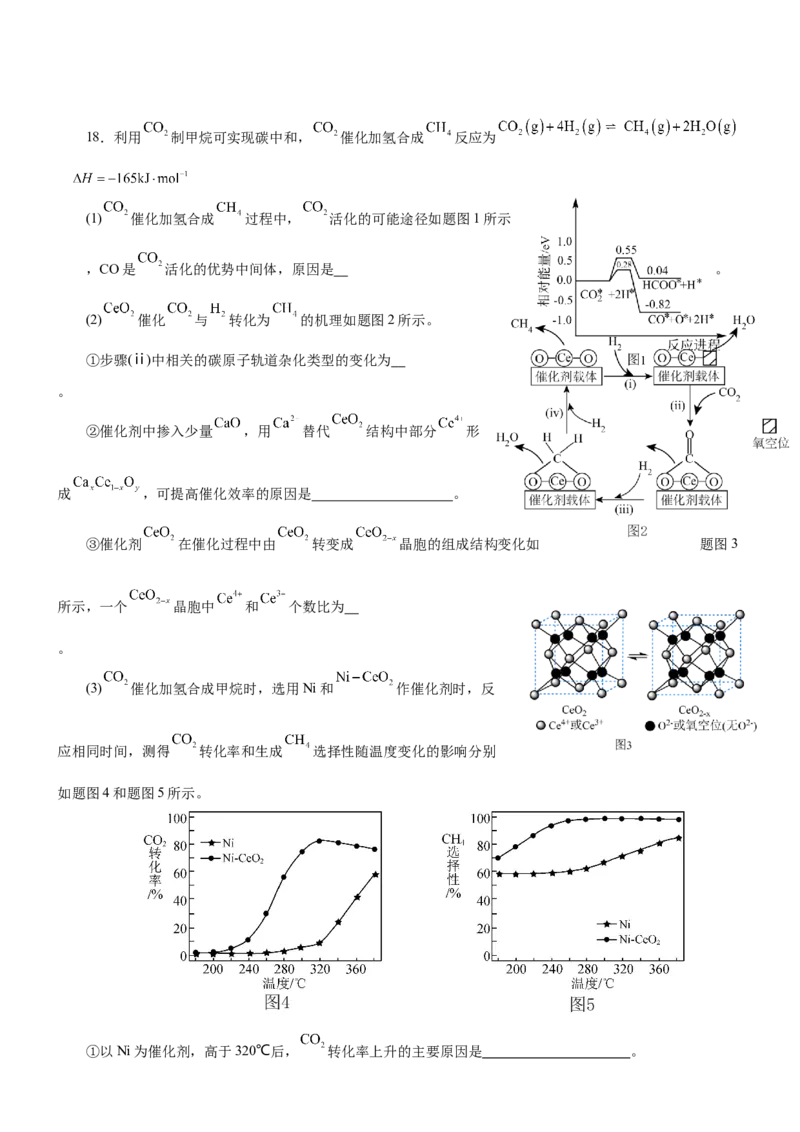
原创精品资源学科网独家享有版权,侵权必究!18.利用 制甲烷可实现碳中和, 催化加氢合成 反应为
(1) 催化加氢合成 过程中, 活化的可能途径如题图1所示
,CO是 活化的优势中间体,原因是 。
(2) 催化 与 转化为 的机理如题图2所示。
①步骤(ⅱ)中相关的碳原子轨道杂化类型的变化为
。
②催化剂中掺入少量 ,用 替代 结构中部分 形
成 ,可提高催化效率的原因是 。
③催化剂 在催化过程中由 转变成 晶胞的组成结构变化如 题图3
所示,一个 晶胞中 和 个数比为
。
(3) 催化加氢合成甲烷时,选用Ni和 作催化剂时,反
应相同时间,测得 转化率和生成 选择性随温度变化的影响分别
如题图4和题图5所示。
①以Ni为催化剂,高于320℃后, 转化率上升的主要原因是 。②以 为催化剂,高于320℃后, 转化率略有下降的可能原因是 。
19.化合物G可用于药用多肽的结构修饰,其人工合成路线如下:
(1)G分子中官能团名称 。
(2)A→B的反应类型为 ,E→F过程1)的反应类型为
(3)D中碳原子的杂化类型有 。
(4)写出C→D的化学方程式 。
(5)F的分子式为C H NO ,其结构简式为 。
12 17 2
(6)A的同分异构体中满足下列条件的有 种。
①遇FeCl 溶液呈紫色 ②能发生水解 ③苯环上含两个取代基,且不含其它环
3
写出其中核磁共振氢谱有6个峰,且峰面积之比为2:2:1:1:1:1的分子的结构简式 。
10
原创精品资源学科网独家享有版权,侵权必究!