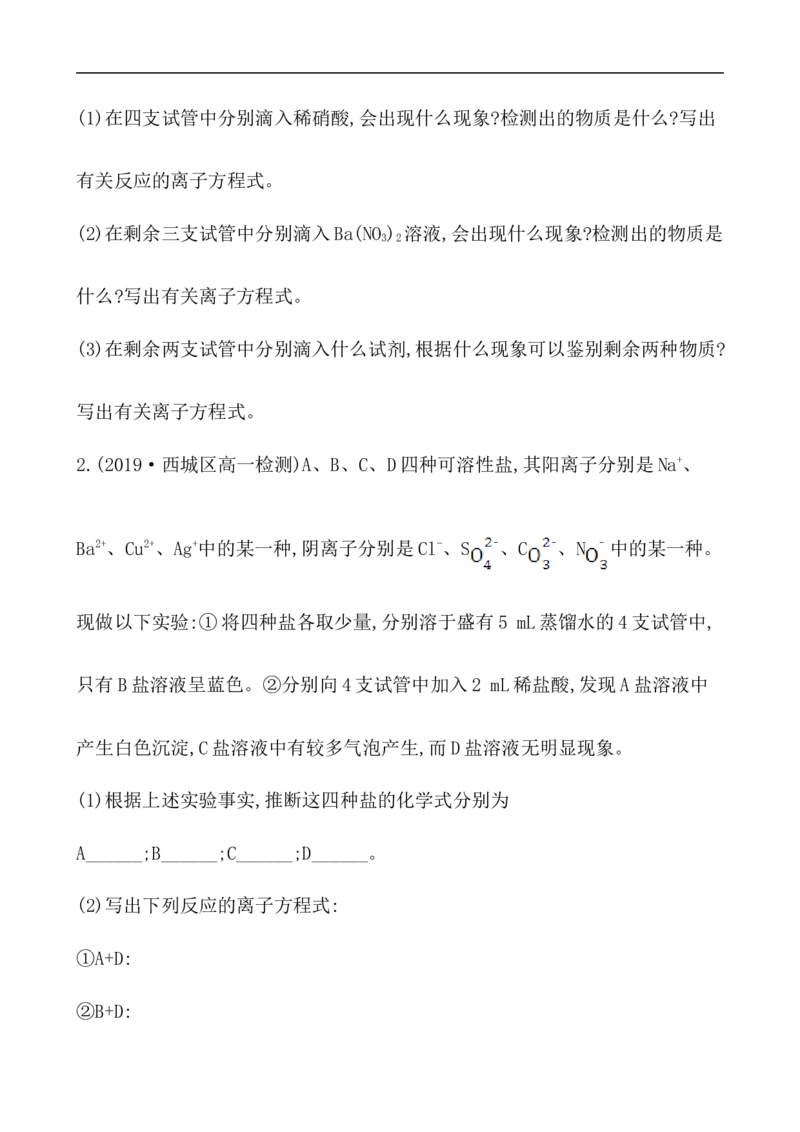文档内容
离 子 反 应
(30分钟 50分)
一、选择题(本题包括4小题,每小题5分,共20分)
1.离子方程式BaCO +2H+ CO ↑+H O+Ba2+中H+不能代表的物质是 ( )
3 2 2
①HCl ②H SO ③HNO
2 4 3
④NaHSO ⑤CH COOH
4 3
A.①③ B.①④⑤ C.②④⑤ D.①⑤
【补偿训练】
离子方程式C +2H+ CO ↑+H O表示 ( )
2 2
A.碳酸盐与盐酸之间的反应
B.一切碳酸盐与一切酸之间的反应
C.可溶性碳酸盐与强酸之间的反应
D.可溶性碳酸盐与一切酸之间的反应
2.化学中微粒之间因为发生反应而“水火不容”。下列各组离子能在溶液中大
量共存的是 ( )
A.Na+、Mg2+、Cl-、OH-B.H+、Ca2+、C 、N
C.Cu2+、K+、S 、N
D.Na+、HC 、OH-、Ca2+
3.(2019·武汉高一检测)下列反应的离子方程式中正确的是 ( )
A.铜片插入硝酸银溶液中:Cu+Ag+ Cu2++Ag
B.氢氧化钡溶液与稀硫酸混合:Ba2++OH-+H++S BaSO ↓+H O
4 2
C.石灰乳与Na CO 溶液混合:Ca2++C CaCO ↓
2 3 3
D.碳酸钙溶于稀盐酸中:CaCO +2H+ Ca2++H O+CO ↑
3 2 2
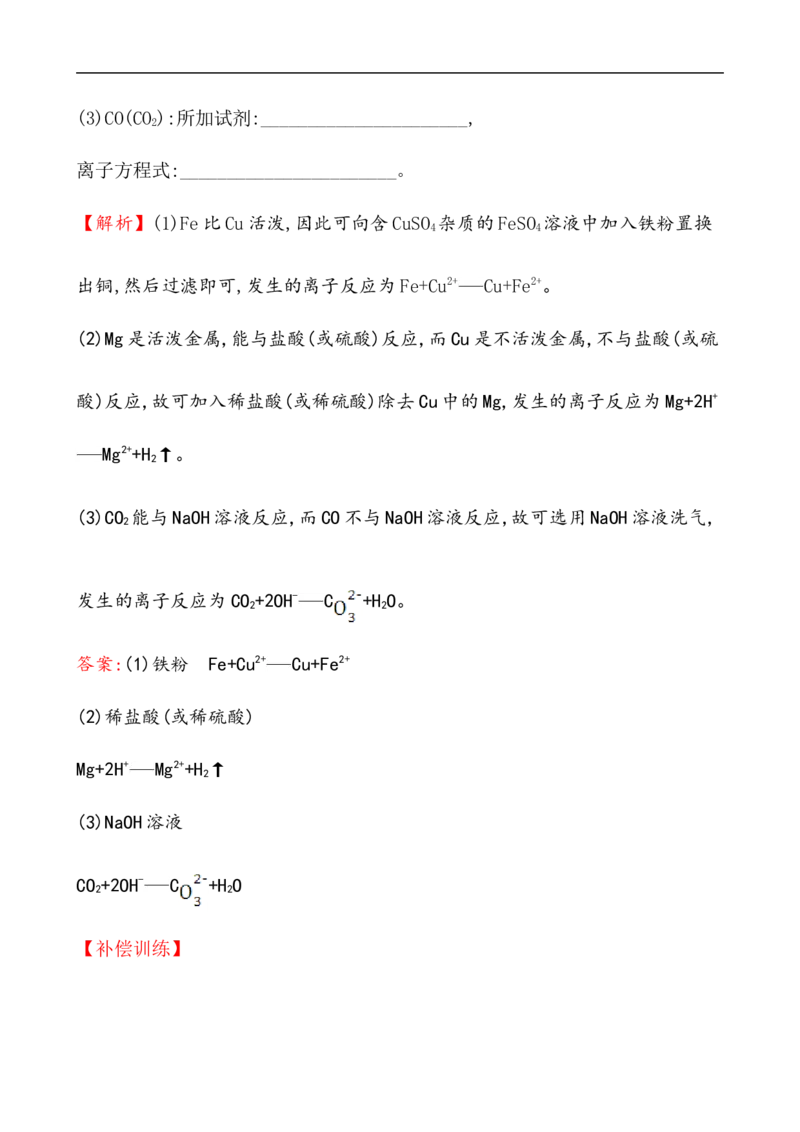
4.(2019·全国卷Ⅲ)离子交换法净化水过程如图所示。下列说法中错误的是
( )
A.经过阳离子交换树脂后,水中阳离子的总数不变B.水中的N 、S 、Cl-通过阴离子树脂后被除去
C.通过净化处理后,水的导电性降低
D.阴离子树脂填充段存在反应H++OH- H O
2
二、非选择题(本题包括1小题,共10分)
5.(2019·临沂高一检测)用一种试剂除去下列物质中的杂质(括号内物质为杂
质,所用试剂均为适量),写出所加的试剂及有关反应的离子方程式。
(1)FeSO 溶液(CuSO ):所加试剂:___________________,
4 4
离子方程式: ______________________。
(2)Cu(Mg):所加试剂:________,
离子方程式: _________________________。
(3)CO(CO ):所加试剂:______________________,
2
离子方程式:_______________________。
【补偿训练】
1.四个试剂瓶中分别盛装有NaNO 溶液、Na CO 溶液、Na SO 溶液和NaCl溶
3 2 3 2 4
液,就如何检验这四种溶液分别做如下探究。(已知:BaSO 和AgCl既不溶于水也
4
不溶于强酸)
探究过程:分别取四种溶液各1 mL于四支试管中,做下列实验。(1)在四支试管中分别滴入稀硝酸,会出现什么现象?检测出的物质是什么?写出
有关反应的离子方程式。
(2)在剩余三支试管中分别滴入Ba(NO ) 溶液,会出现什么现象?检测出的物质是
3 2
什么?写出有关离子方程式。
(3)在剩余两支试管中分别滴入什么试剂,根据什么现象可以鉴别剩余两种物质?
写出有关离子方程式。
2.(2019·西城区高一检测)A、B、C、D四种可溶性盐,其阳离子分别是Na+、
Ba2+、Cu2+、Ag+中的某一种,阴离子分别是Cl-、S 、C 、N 中的某一种。
现做以下实验:①将四种盐各取少量,分别溶于盛有5 mL蒸馏水的4支试管中,
只有B盐溶液呈蓝色。②分别向4支试管中加入2 mL稀盐酸,发现A盐溶液中
产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
(1)根据上述实验事实,推断这四种盐的化学式分别为
A______;B______;C______;D______。
(2)写出下列反应的离子方程式:
①A+D:
②B+D:③C+HCl→气体:
一、选择题(本题包括1小题,共5分)
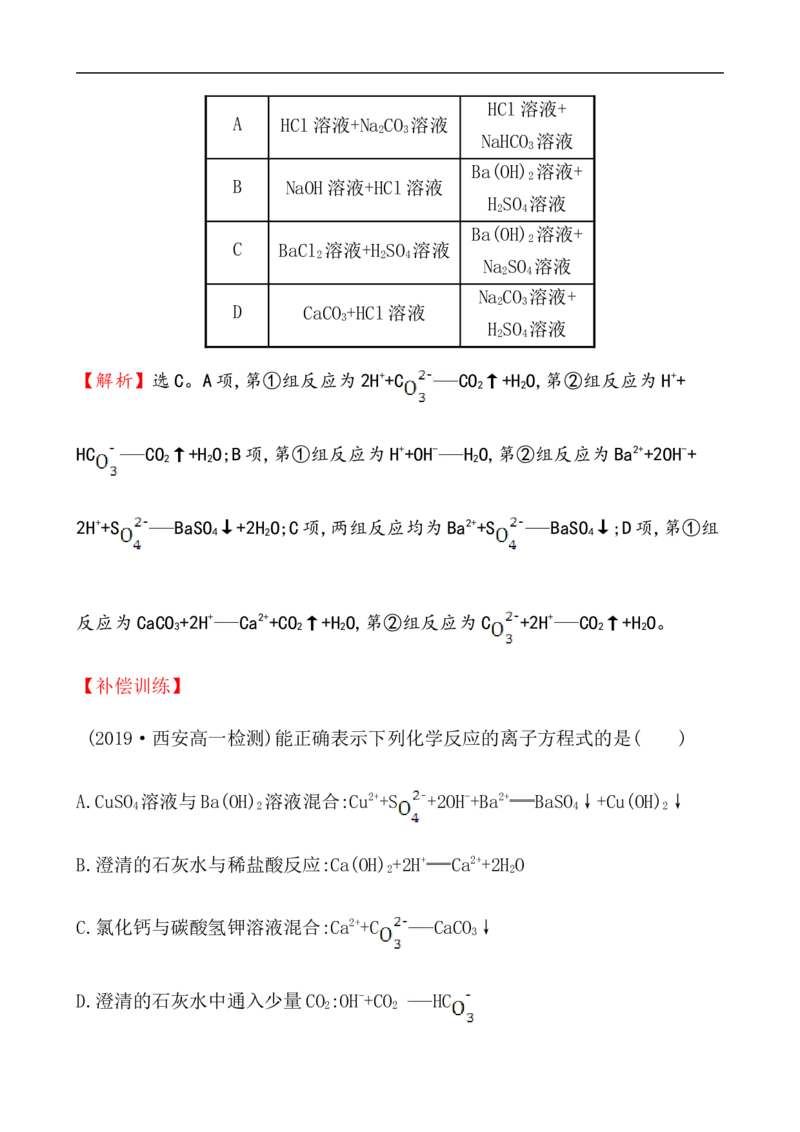
6.下列反应可以用同一离子方程式表示的是
( )
选项 ① ②
HCl溶液+
A HCl溶液+Na CO 溶液
2 3
NaHCO 溶液
3
Ba(OH) 溶液+
2
B NaOH溶液+HCl溶液
H SO 溶液
2 4
Ba(OH) 溶液+
2
C BaCl 溶液+H SO 溶液
2 2 4
Na SO 溶液
2 4
Na CO 溶液+
2 3
D CaCO +HCl溶液
3
H SO 溶液
2 4
【补偿训练】
(2019·西安高一检测)能正确表示下列化学反应的离子方程式的是( )
A.CuSO 溶液与Ba(OH) 溶液混合:Cu2++S +2OH-+Ba2+ BaSO ↓+Cu(OH) ↓
4 2 4 2
B.澄清的石灰水与稀盐酸反应:Ca(OH) +2H+ Ca2++2H O
2 2
C.氯化钙与碳酸氢钾溶液混合:Ca2++C CaCO ↓
3
D.澄清的石灰水中通入少量CO :OH-+CO HC
2 2
二、非选择题(本题包括1小题,共15分)7.2019年2月28日我国生态环境部在例行新闻发布会上表示,我国水污染防治
工作取得新的积极进展,水污染防治将建立健全流域生态环境综合管理体系。
某河道两旁建有甲、乙两化工厂,某兴趣小组的同学分别收集了两厂排放的污
水带回学校进行实验探究,工厂的师傅告诉同学们甲、乙厂排放的工业废水中
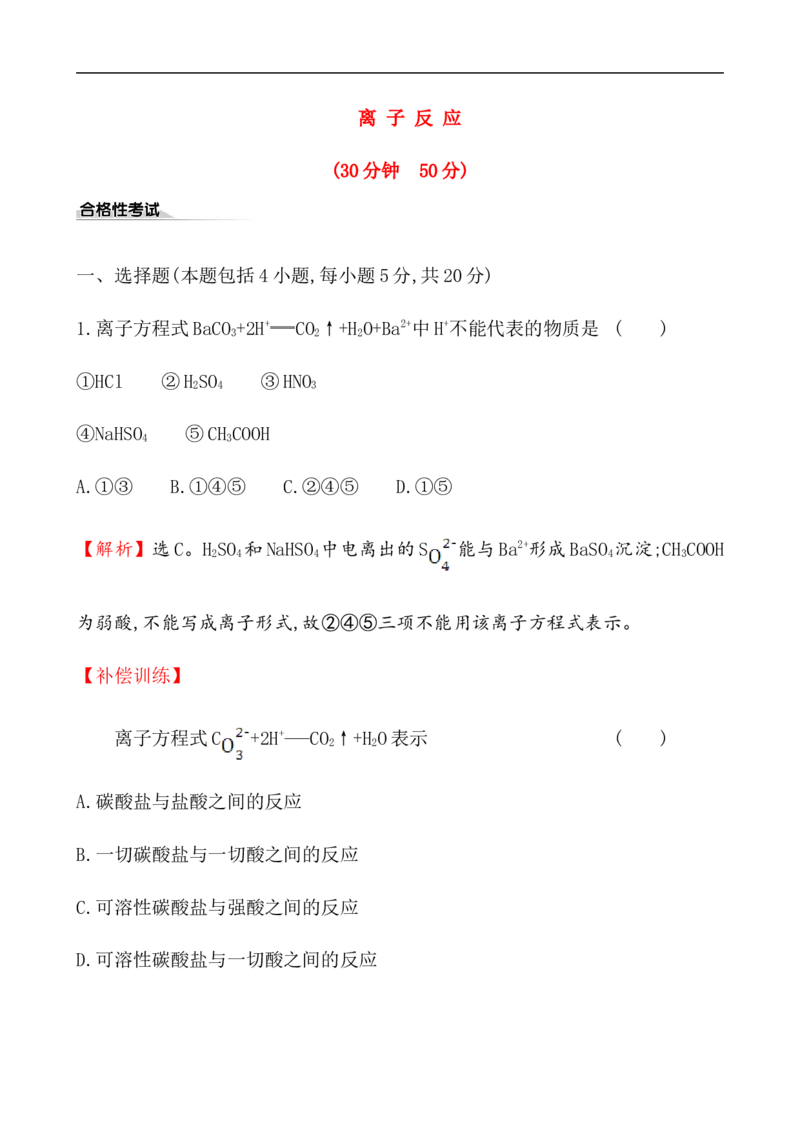
含有下列离子中的三种(各不相同)。
阳离子 K+、Ag+、Fe3+
阴离子 Cl-、OH-、N
(1)甲同学用pH计(一种测量溶液酸碱性的仪器)测量甲厂的废水明显呈碱性,然
后就判断了甲、乙两厂中所含有的离子。请你简述判断的理由。
(2)乙同学看到工厂师傅给出的离子后,认为可以在某工厂的废水中加入一种
金属,从而回收另一种金属。请你帮助乙同学在实验室中设计相应的实验,完成
此种金属的回收。并写出反应过程中的离子方程式。(3)丙同学认为将甲厂和乙厂的废水按适当的比例混合,可以使废水中的某些
离子完全转化为沉淀,写出甲、乙两厂废水混合过程中反应的离子方程式,并简
述经上述处理后废水的主要作用。
【补偿训练】
(2019·齐齐哈尔高一检测)“绿水青山就是金山银山”。蓝天白云、青山
绿水是人类赖以生存的环境,是社会长远发展的最大本钱。某地区只追求经济
发展而忽视环境保护,在一条小河边建有四座工厂:甲、乙、丙、丁(如图所示)
致使河中鱼、虾绝迹。经处理,它们所排出的废液里每座工厂只含有Na CO 、
2 3
FeCl 、Ca(OH) 、HCl中的一种。
3 2
某环保小组对河水监测时发现:
①甲处河水呈乳白色
②乙处河水呈红褐色
③丙处河水由浑浊变清
④丁处河水产生气泡,河水仍清(1)经分析,四座工厂排出的废液里分别含有什么污染物?
(2)在M处取出的河水中,含有哪些离子?离 子 反 应
(30分钟 50分)
一、选择题(本题包括4小题,每小题5分,共20分)
1.离子方程式BaCO +2H+ CO ↑+H O+Ba2+中H+不能代表的物质是 ( )
3 2 2
①HCl ②H SO ③HNO
2 4 3
④NaHSO ⑤CH COOH
4 3
A.①③ B.①④⑤ C.②④⑤ D.①⑤
【解析】选C。H SO 和NaHSO 中电离出的S 能与Ba2+形成BaSO 沉淀;CH COOH
2 4 4 4 3
为弱酸,不能写成离子形式,故②④⑤三项不能用该离子方程式表示。
【补偿训练】
离子方程式C +2H+ CO ↑+H O表示 ( )
2 2
A.碳酸盐与盐酸之间的反应
B.一切碳酸盐与一切酸之间的反应
C.可溶性碳酸盐与强酸之间的反应
D.可溶性碳酸盐与一切酸之间的反应【解析】选C。C 只代表可溶性的碳酸盐,从此点分析选项A和B都是不正确
的;H+只代表强酸而不是一切酸(如弱酸H S、HF、CH COOH等均不能用H+表示)。
2 3
2.化学中微粒之间因为发生反应而“水火不容”。下列各组离子能在溶液中大
量共存的是 ( )
A.Na+、Mg2+、Cl-、OH-
B.H+、Ca2+、C 、N
C.Cu2+、K+、S 、N
D.Na+、HC 、OH-、Ca2+
【解析】选C。溶液中的离子能否大量共存,关键是看离子间能否发生反应。A
项,Mg2++2OH- Mg(OH) ↓;B项, 2H++C H O+CO ↑,Ca2++C CaCO ↓;C
2 2 2 3
项,离子相互之间不会发生反应;D项,HC +OH- H O+C ,Ca2++C
2
CaCO ↓,另外Ca(OH) 为微溶。
3 2
3.(2019·武汉高一检测)下列反应的离子方程式中正确的是 ( )
A.铜片插入硝酸银溶液中:Cu+Ag+ Cu2++AgB.氢氧化钡溶液与稀硫酸混合:Ba2++OH-+H++S BaSO ↓+H O
4 2
C.石灰乳与Na CO 溶液混合:Ca2++C CaCO ↓
2 3 3
D.碳酸钙溶于稀盐酸中:CaCO +2H+ Ca2++H O+CO ↑
3 2 2
【解析】选D。A项中方程式两端电荷数不相等,应写成Cu+2Ag+ Cu2++2Ag;B
项违背约简原则,在方程式中绝对不能只约简部分物质前面的化学计量数,该反
应方程式只约简了OH-、H+及水的化学计量数,显然不正确,应为Ba2++2OH-+2H++
S BaSO ↓+2H O;C项中石灰乳应写化学式不能拆;D项正确。
4 2
4.(2019·全国卷Ⅲ)离子交换法净化水过程如图所示。下列说法中错误的是
( )
A.经过阳离子交换树脂后,水中阳离子的总数不变
B.水中的N 、S 、Cl-通过阴离子树脂后被除去
C.通过净化处理后,水的导电性降低D.阴离子树脂填充段存在反应H++OH- H O
2
【解析】选A。本题为信息题,注意从题目信息中提取有用信息。根据示意图,
水经过阳离子交换树脂后,Ca2+、Na+、 Mg2+均被H+交换,因为Ca2+、Mg2+是+2价
阳离子,H+是+1价阳离子,根据电荷守恒与Ca2+、Mg2+交换的H+数目应为Ca2+、
Mg2+总数的2倍,因此水中阳离子总数增加,A错误。根据示意图,N 、S 、
Cl-经过阴离子交换树脂后被OH-替换,B正确。水经过净化后溶液中离子浓度减
小,水的导电性降低,纯水几乎不导电,C正确。经过阳离子交换树脂后溶液中的
阳离子全部是H+,经过阴离子交换树脂后溶液中的阴离子被OH-替换,所以在阴
离子树脂填充段存在反应H++ OH- H O,D正确。
2
二、非选择题(本题包括1小题,共10分)
5.(2019·临沂高一检测)用一种试剂除去下列物质中的杂质(括号内物质为杂
质,所用试剂均为适量),写出所加的试剂及有关反应的离子方程式。
(1)FeSO 溶液(CuSO ):所加试剂:___________________,
4 4
离子方程式: ______________________。
(2)Cu(Mg):所加试剂:________,
离子方程式: _________________________。(3)CO(CO ):所加试剂:______________________,
2
离子方程式:_______________________。
【解析】(1)Fe比Cu活泼,因此可向含CuSO 杂质的FeSO 溶液中加入铁粉置换
4 4
出铜,然后过滤即可,发生的离子反应为Fe+Cu2+ Cu+Fe2+。
(2)Mg是活泼金属,能与盐酸(或硫酸)反应,而Cu是不活泼金属,不与盐酸(或硫
酸)反应,故可加入稀盐酸(或稀硫酸)除去Cu中的Mg,发生的离子反应为Mg+2H+
Mg2++H ↑。
2
(3)CO 能与NaOH溶液反应,而CO不与NaOH溶液反应,故可选用NaOH溶液洗气,
2
发生的离子反应为CO +2OH- C +H O。
2 2
答案:(1)铁粉 Fe+Cu2+ Cu+Fe2+
(2)稀盐酸(或稀硫酸)
Mg+2H+ Mg2++H ↑
2
(3)NaOH溶液
CO +2OH- C +H O
2 2
【补偿训练】1.四个试剂瓶中分别盛装有NaNO 溶液、Na CO 溶液、Na SO 溶液和NaCl溶
3 2 3 2 4
液,就如何检验这四种溶液分别做如下探究。(已知:BaSO 和AgCl既不溶于水也
4
不溶于强酸)
探究过程:分别取四种溶液各1 mL于四支试管中,做下列实验。
(1)在四支试管中分别滴入稀硝酸,会出现什么现象?检测出的物质是什么?写出
有关反应的离子方程式。
(2)在剩余三支试管中分别滴入Ba(NO ) 溶液,会出现什么现象?检测出的物质是
3 2
什么?写出有关离子方程式。
(3)在剩余两支试管中分别滴入什么试剂,根据什么现象可以鉴别剩余两种物质?
写出有关离子方程式。
【解析】此题中四种试剂的阳离子相同,实际是检验四种阴离子,Na CO 与酸反
2 3
应产生气体,Na SO 与可溶性钡盐反应生成白色沉淀,检验Cl-用AgNO 溶液。检
2 4 3
验时要注意顺序,Ag+与C 、S 、Cl-都能反应生成白色沉淀,Ba2+与C 、S
都能反应生成白色沉淀,所以应最先加入稀硝酸,然后加入Ba(NO ) 溶液,最
3 2
后加入AgNO 溶液。
3答案:(1)三支试管无明显现象,一支试管内有气泡产生;检测出的是Na CO 溶液,
2 3
离子方程式为2H++C H O+CO ↑。
2 2
(2)两支试管无明显现象,一支试管产生白色沉淀;检测出的是Na SO 溶液,离子
2 4
方程式为S +Ba2+ BaSO ↓。
4
(3)加入AgNO 溶液产生白色沉淀可检测出NaCl溶液,离子方程式为Ag++Cl-
3
AgCl↓。
2.(2019·西城区高一检测)A、B、C、D四种可溶性盐,其阳离子分别是Na+、
Ba2+、Cu2+、Ag+中的某一种,阴离子分别是Cl-、S 、C 、N 中的某一种。
现做以下实验:①将四种盐各取少量,分别溶于盛有5 mL蒸馏水的4支试管中,
只有B盐溶液呈蓝色。②分别向4支试管中加入2 mL稀盐酸,发现A盐溶液中
产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
(1)根据上述实验事实,推断这四种盐的化学式分别为
A______;B______;C______;D______。
(2)写出下列反应的离子方程式:
①A+D:②B+D:
③C+HCl→气体:
【解析】由于这四种盐均可溶,则Ba2+不可能与S 、C 组合,Cu2+不可能与C
组合,Ag+只能与N 组合。由实验①可知,B为铜盐(Cu2+在水溶液中呈蓝色)。
由实验②可知,A为AgNO (与盐酸反应生成AgCl白色沉淀),C为碳酸盐(C 与
3
盐酸反应生成CO 气体),只能是Na CO 。则剩余阳离子为Ba2+,它与Cl-形成
2 2 3
BaCl ,与盐酸不反应,即为D,而铜盐B一定是CuSO 。
2 4
答案:(1)AgNO CuSO Na CO BaCl
3 4 2 3 2
(2)①Ag++Cl- AgCl↓
②S +Ba2+ BaSO ↓
4
③C +2H+ CO ↑+H O
2 2
一、选择题(本题包括1小题,共5分)
6.下列反应可以用同一离子方程式表示的是
( )
选项 ① ②HCl溶液+
A HCl溶液+Na CO 溶液
2 3
NaHCO 溶液
3
Ba(OH) 溶液+
2
B NaOH溶液+HCl溶液
H SO 溶液
2 4
Ba(OH) 溶液+
2
C BaCl 溶液+H SO 溶液
2 2 4
Na SO 溶液
2 4
Na CO 溶液+
2 3
D CaCO +HCl溶液
3
H SO 溶液
2 4
【解析】选C。A项,第①组反应为2H++C CO ↑+H O,第②组反应为H++
2 2
HC CO ↑+H O;B项,第①组反应为H++OH- H O,第②组反应为Ba2++2OH-+
2 2 2
2H++S BaSO ↓+2H O;C项,两组反应均为Ba2++S BaSO ↓;D项,第①组
4 2 4
反应为CaCO +2H+ Ca2++CO ↑+H O,第②组反应为C +2H+ CO ↑+H O。
3 2 2 2 2
【补偿训练】
(2019·西安高一检测)能正确表示下列化学反应的离子方程式的是( )
A.CuSO 溶液与Ba(OH) 溶液混合:Cu2++S +2OH-+Ba2+ BaSO ↓+Cu(OH) ↓
4 2 4 2
B.澄清的石灰水与稀盐酸反应:Ca(OH) +2H+ Ca2++2H O
2 2
C.氯化钙与碳酸氢钾溶液混合:Ca2++C CaCO ↓
3
D.澄清的石灰水中通入少量CO :OH-+CO HC
2 2【解析】选A。B项,应为H++OH- H O;C项,不发生离子反应;D项,应为Ca2+
2
+CO +2OH- CaCO ↓+H O。
2 3 2
【易错提醒】(1)多离子间的反应防止出现遗漏。如Ba(OH) 溶液与CuSO 溶液
2 4
反应,若只写为Ba2++S BaSO ↓或Cu2++2OH- Cu(OH) ↓是错误的,应写为
4 2
Ba2++2OH-+Cu2++S BaSO ↓+Cu(OH) ↓。
4 2
(2)离子方程式的书写与反应物间的用量有关。澄清的石灰水中通入过量CO 反
2
应的离子方程式为OH-+CO HC ,通入少量CO 生成碳酸钙沉淀。
2 2
二、非选择题(本题包括1小题,共15分)
7.2019年2月28日我国生态环境部在例行新闻发布会上表示,我国水污染防治
工作取得新的积极进展,水污染防治将建立健全流域生态环境综合管理体系。
某河道两旁建有甲、乙两化工厂,某兴趣小组的同学分别收集了两厂排放的污
水带回学校进行实验探究,工厂的师傅告诉同学们甲、乙厂排放的工业废水中
含有下列离子中的三种(各不相同)。阳离子 K+、Ag+、Fe3+
阴离子 Cl-、OH-、N
(1)甲同学用pH计(一种测量溶液酸碱性的仪器)测量甲厂的废水明显呈碱性,然
后就判断了甲、乙两厂中所含有的离子。请你简述判断的理由。
提示:Ag+只能和N 共存,二者可存在于同一个工厂的废水中,而Ag+、Fe3+与OH-
不能大量共存,所以Fe3+只能和Ag+、N 存在于同一个工厂的废水中。由于甲
厂排放的废水显碱性,所以甲厂废水中含有OH-、Cl-、K+,而乙厂废水中含有
Fe3+、Ag+、N 。
(2)乙同学看到工厂师傅给出的离子后,认为可以在某工厂的废水中加入一种金
属,从而回收另一种金属。请你帮助乙同学在实验室中设计相应的实验,完成此
种金属的回收。并写出反应过程中的离子方程式。
提示:可以将Ag+转换成金属银,只要加入铁粉就可以置换出溶液中的Ag+,反应
的离子方程式是Fe+2Ag+ 2Ag+Fe2+。(3)丙同学认为将甲厂和乙厂的废水按适当的比例混合,可以使废水中的某些离
子完全转化为沉淀,写出甲、乙两厂废水混合过程中反应的离子方程式,并简述
经上述处理后废水的主要作用。
提示:根据两厂废水中含有的离子可知,混合后反应的离子方程式是Ag++Cl-
AgCl↓、Fe3++3OH- Fe(OH) ↓,这样反应后的废水中就只有K+和N ,这样
3
经过滤后的废水主要含KNO ,可以用作化肥,用来浇灌农田,也可以提取KNO 固
3 3
体作为工业原料。
【补偿训练】
(2019·齐齐哈尔高一检测)“绿水青山就是金山银山”。蓝天白云、青山
绿水是人类赖以生存的环境,是社会长远发展的最大本钱。某地区只追求经济
发展而忽视环境保护,在一条小河边建有四座工厂:甲、乙、丙、丁(如图所示)
致使河中鱼、虾绝迹。经处理,它们所排出的废液里每座工厂只含有Na CO 、
2 3
FeCl 、Ca(OH) 、HCl中的一种。
3 2某环保小组对河水监测时发现:
①甲处河水呈乳白色
②乙处河水呈红褐色
③丙处河水由浑浊变清
④丁处河水产生气泡,河水仍清
(1)经分析,四座工厂排出的废液里分别含有什么污染物?
(2)在M处取出的河水中,含有哪些离子?
【解析】(1)甲处河水呈乳白色的是熟石灰;乙处河水呈红褐色是因为熟石灰和
FeCl 反应生成氢氧化铁沉淀,因此乙厂废液中含FeCl ;丙处河水由浑浊变清,说
3 3
明丙厂废液为盐酸,盐酸溶解氢氧化铁使河水变清;丁处河水产生气泡,河水仍
清说明丁厂废液为碳酸钠,丁厂的碳酸钠和上游流下来的过量盐酸反应产生二
氧化碳气体。
(2)丁厂的碳酸钠和上游流下来的过量盐酸反应使C 消耗,M处于下游,含有
Na+、Cl-、Fe3+、Ca2+、H+。
答案:(1)甲:Ca(OH) ;乙:FeCl ;丙:HCl;丁:Na CO
2 3 2 3
(2)Na+、Cl-、Fe3+、Ca2+、H+