文档内容
课时素养评价 七
氧化还原反应的基本规律
(40分钟 70分)
一、选择题(本题包括10小题,每小题5分,共50分)
1.(2019·泰安高一检测) 下列物质中,按只有氧化性、只有还原性、既有氧化
性又有还原性的顺序排列的一组是 ( )
A.Al3+、K、Fe2+ B.Cl-、Al、H
2
C.NO 、Na+、Br D.O 、SO 、Fe
2 2 2 2
2.一定条件下,KClO 与I 发生下列反应:2KClO +I 2KIO +Cl ,下列推断正确
3 2 3 2 3 2
的是 ( )
A.该反应属于复分解反应
B.氧化性:I >KClO
2 3
C.还原性:KClO >I
3 2
D.还原剂为I ,氧化剂为KClO
2 3
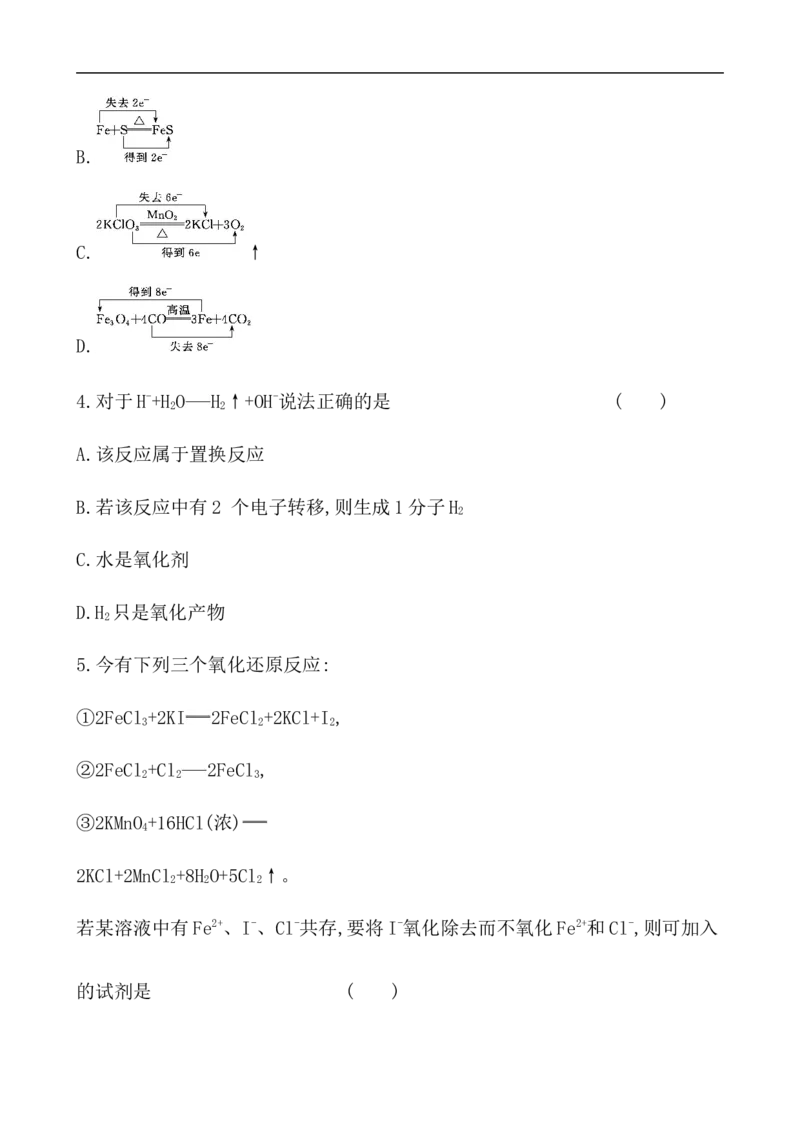
3.(2019·长春高一检测)下列电子转移表示正确的是 ( )
A.B.
C. ↑
D.
4.对于H-+H O H ↑+OH-说法正确的是 ( )
2 2
A.该反应属于置换反应
B.若该反应中有2 个电子转移,则生成1分子H
2
C.水是氧化剂
D.H 只是氧化产物
2
5.今有下列三个氧化还原反应:
①2FeCl +2KI 2FeCl +2KCl+I ,
3 2 2
②2FeCl +Cl 2FeCl ,
2 2 3
③2KMnO +16HCl(浓)
4
2KCl+2MnCl +8H O+5Cl ↑。
2 2 2
若某溶液中有Fe2+、I-、Cl-共存,要将I-氧化除去而不氧化Fe2+和Cl-,则可加入
的试剂是 ( )A.Cl B.KMnO
2 4
C.FeCl D.HCl
3
6.(2019·成都高一检测)用高铁酸钠(Na FeO )对河湖水消毒是城市饮水处理的
2 4
新技术。
一种生成Na FeO 的反应如下:Fe O +Na O (氧为-1价) Na FeO +Na O(未配平),
2 4 2 3 2 2 2 4 2
下列说法不正确的是 ( )
A.Na O 既是氧化剂又是还原剂
2 2
B.Fe O 在反应中失去电子
2 3
C.配平后为Fe O +3Na O 2Na FeO +Na O
2 3 2 2 2 4 2
D.Na FeO 能消毒杀菌是因其具有强氧化性
2 4
7.(2019·广州高一检测)已知氧化性:Br >Fe3+>I ,还原性:I->Fe2+>Br-,则下列反
2 2
应不能发生的是 ( )
A.Br +2I- 2Br-+I
2 2
B.Br +2Fe2+ 2Br-+2Fe3+
2
C.2Fe3++2I- 2Fe2++I
2D.2Fe3++2Br- 2Fe2++Br
2
8.将SO 气体与足量Fe (SO ) 溶液完全反应后,再加入K Cr O 溶液,发生如下两
2 2 4 3 2 2 7
个化学反应:
SO +2Fe3++2H O S +2Fe2++4H+
2 2
Cr +6Fe2++14H+
2
2Cr3++6Fe3++7H O
2
下列有关说法正确的是 ( )
A.还原性Cr3+>Fe2+>SO
2
B.氧化性Cr >S >Fe3+
2
C.Cr 能将Na SO 氧化成Na SO
2 2 3 2 4
D.两个反应中Fe (SO ) 均作还原剂
2 4 3
9.含有氧化剂X 的溶液与亚硫酸钠(Na SO )溶液恰好反应完全,已知Na SO 被
2 3 2 3
氧化为Na SO ,已知X 、Na SO 的个数比为1∶2,则还原产物中元素X的价态
2 4 2 3
是
( )A.+2 B.-2
C.+1 D.0
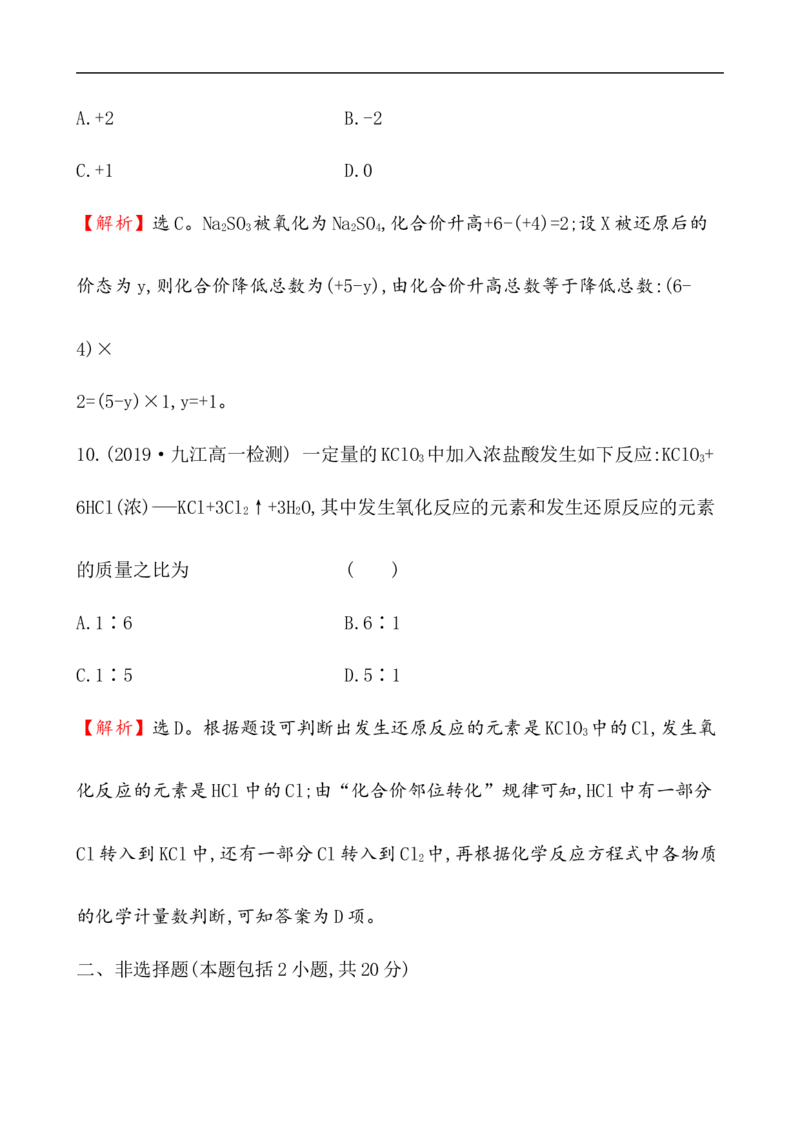
10.(2019·九江高一检测) 一定量的KClO 中加入浓盐酸发生如下反应:KClO +
3 3
6HCl(浓) KCl+3Cl ↑+3H O,其中发生氧化反应的元素和发生还原反应的元素
2 2
的质量之比为 ( )
A.1∶6 B.6∶1
C.1∶5 D.5∶1
二、非选择题(本题包括2小题,共20分)
11.(10分)某反应中反应物与生成物有:AsH 、H SO 、KBrO 、K SO 、H AsO 、H O
3 2 4 3 2 4 3 4 2
和一种未知物质X。
(1)已知KBrO 在反应中得到电子,则该反应的还原剂是__________________。
3
(2)已知2个KBrO 在反应中得到10个电子生成X,则X的化学式为___________。
3
(3)根据上述反应可推知________。
a.氧化性:KBrO >H AsO
3 3 4
b.氧化性:H AsO >KBrO
3 4 3
c.还原性:AsH >X
3d.还原性:X>AsH
3
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子
转移的方向和数目:
12.(10分)2019年5月12日是中国第11个全国防灾减灾日,中国地震局当天在
北京正式启动2019年防震减灾千场科普讲座,并推出第三届全国防震减灾科普
讲解大赛决赛。
地震后的消毒工作至关重要,各种含氯消毒剂得到了广泛应用。
请回答下列问题:
(1)漂白剂亚氯酸钠(NaClO )在常温与黑暗处可保存一年。亚氯酸不稳定可分解,
2
反应的离子方程式为HClO ClO ↑+H++Cl-+H O,试配平。
2 2 2
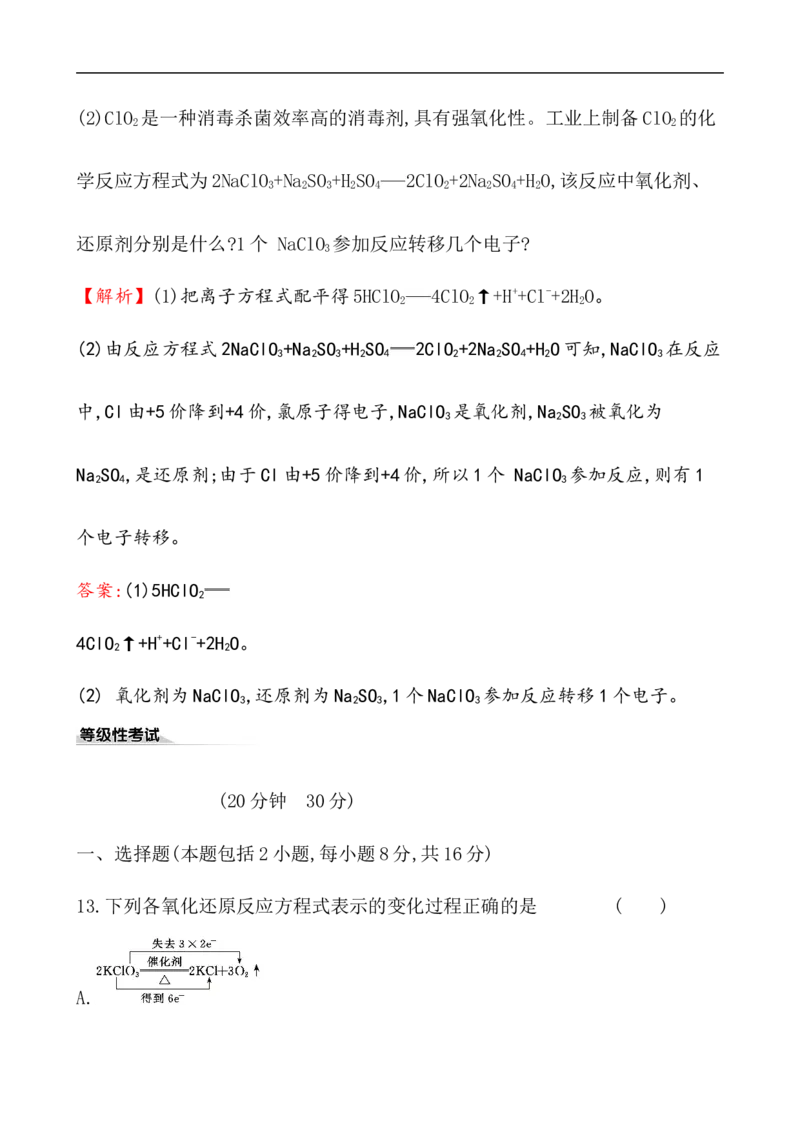
(2)ClO 是一种消毒杀菌效率高的消毒剂,具有强氧化性。工业上制备ClO 的化
2 2
学反应方程式为2NaClO +Na SO +H SO 2ClO +2Na SO +H O,该反应中氧化剂、
3 2 3 2 4 2 2 4 2
还原剂分别是什么?1个 NaClO 参加反应转移几个电子?
3(20分钟 30分)
一、选择题(本题包括2小题,每小题8分,共16分)
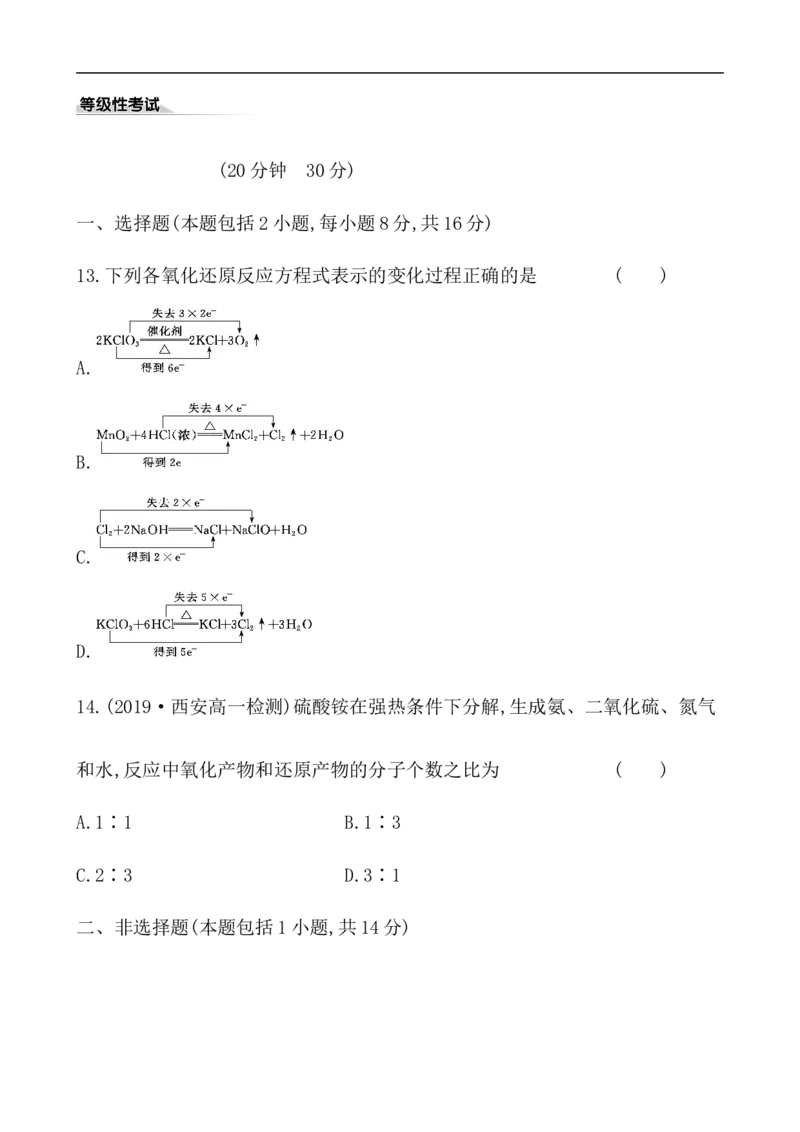
13.下列各氧化还原反应方程式表示的变化过程正确的是 ( )
A.
B.
C.
D.
14.(2019·西安高一检测)硫酸铵在强热条件下分解,生成氨、二氧化硫、氮气
和水,反应中氧化产物和还原产物的分子个数之比为 ( )
A.1∶1 B.1∶3
C.2∶3 D.3∶1
二、非选择题(本题包括1小题,共14分)15.(2019·西安高一检测)凡是养鱼的人都知道一种很不错的消毒剂,这就是被
称为当今第四代消毒产品的二氧化氯。其属于A1级别安全高效消毒剂之一,并
且可以在极低的浓度下对病菌有杀灭作用,功效显而易见。一起来看看它的使
用方法吧。
KClO 和浓盐酸在一定温度下反应生成黄绿色的易爆物二氧化氯。其变化可表述
3
为
(1)请完成该化学方程式并配平(未知物化学式和系数填入框内)。
(2)浓盐酸在反应中显示出来的性质是________(填序号)。
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
(3)产生1分子Cl ,转移的电子为________个。
2(4)ClO 具有很强的氧化性,因此常被用作消毒剂,其消毒效率(以单位质量得到
2
的电子数表示)是Cl 的________倍(保留小数点后两位)。
2课时素养评价 七
氧化还原反应的基本规律
(40分钟 70分)
一、选择题(本题包括10小题,每小题5分,共50分)
1.(2019·泰安高一检测) 下列物质中,按只有氧化性、只有还原性、既有氧化
性又有还原性的顺序排列的一组是 ( )
A.Al3+、K、Fe2+ B.Cl-、Al、H
2
C.NO 、Na+、Br D.O 、SO 、Fe
2 2 2 2
【解析】选A。Al3+处于最高价,只有氧化性;K的化合价只能升高,只有还原
性;Fe2+化合价既能升高也能降低,既有氧化性又有还原性,A正确;Cl-化合价只
能升高,只有还原性,B错误;NO 中氮元素化合价既能升高也能降低,既有氧化性
2
又有还原性,Na+化合价只能降低,只有氧化性,C错误;SO 既有氧化性又有还原性,
2
Fe化合价只能升高,只有还原性,D错误。
2.一定条件下,KClO 与I 发生下列反应:2KClO +I 2KIO +Cl ,下列推断正确
3 2 3 2 3 2
的是 ( )
A.该反应属于复分解反应B.氧化性:I >KClO
2 3
C.还原性:KClO >I
3 2
D.还原剂为I ,氧化剂为KClO
2 3
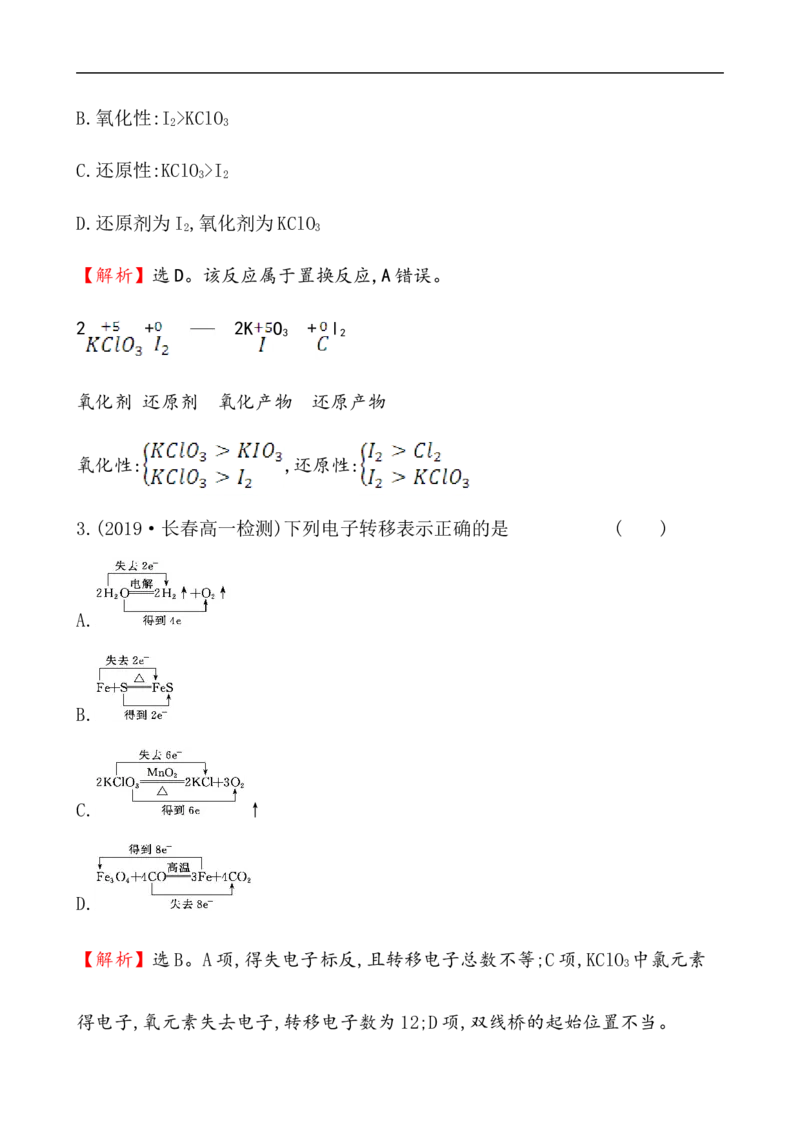
【解析】选D。该反应属于置换反应,A错误。
2 + 2K O + l
3 2
氧化剂 还原剂 氧化产物 还原产物
氧化性: ,还原性:
3.(2019·长春高一检测)下列电子转移表示正确的是 ( )
A.
B.
C. ↑
D.
【解析】选B。A项,得失电子标反,且转移电子总数不等;C项,KClO 中氯元素
3
得电子,氧元素失去电子,转移电子数为12;D项,双线桥的起始位置不当。4.对于H-+H O H ↑+OH-说法正确的是 ( )
2 2
A.该反应属于置换反应
B.若该反应中有2 个电子转移,则生成1分子H
2
C.水是氧化剂
D.H 只是氧化产物
2
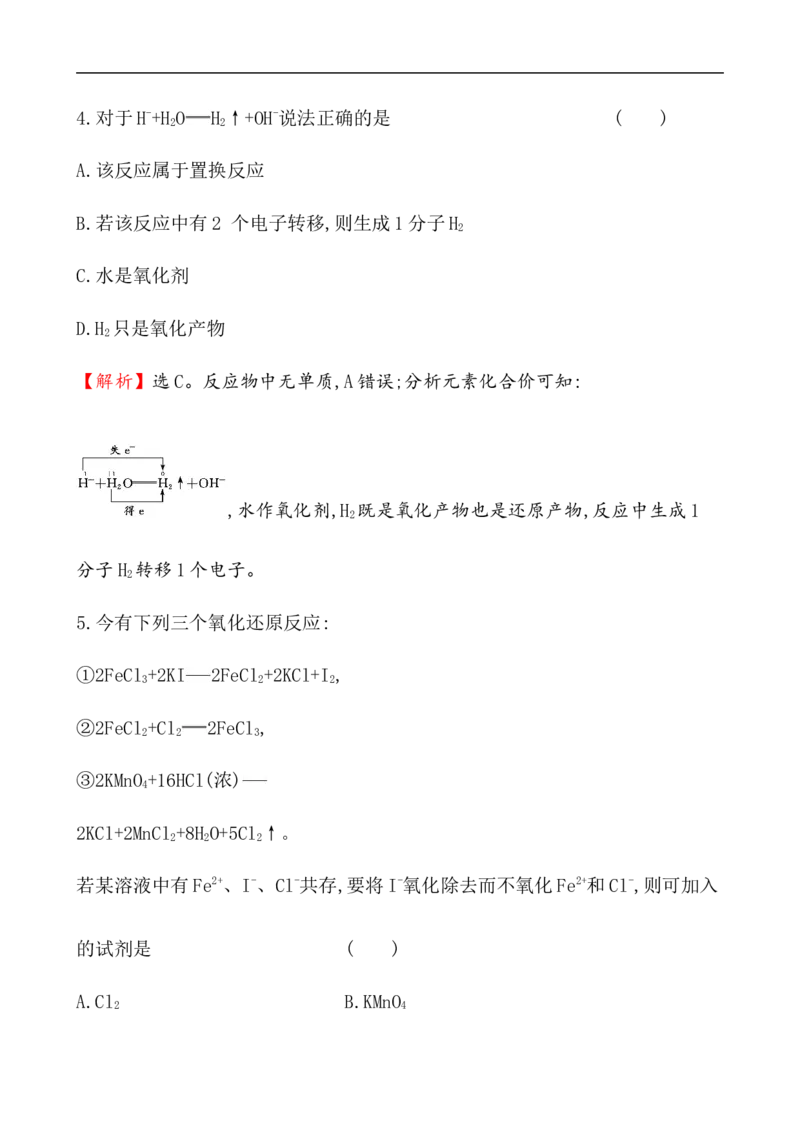
【解析】选C。反应物中无单质,A错误;分析元素化合价可知:
,水作氧化剂,H 既是氧化产物也是还原产物,反应中生成1
2
分子H 转移1个电子。
2
5.今有下列三个氧化还原反应:
①2FeCl +2KI 2FeCl +2KCl+I ,
3 2 2
②2FeCl +Cl 2FeCl ,
2 2 3
③2KMnO +16HCl(浓)
4
2KCl+2MnCl +8H O+5Cl ↑。
2 2 2
若某溶液中有Fe2+、I-、Cl-共存,要将I-氧化除去而不氧化Fe2+和Cl-,则可加入
的试剂是 ( )
A.Cl B.KMnO
2 4C.FeCl D.HCl
3
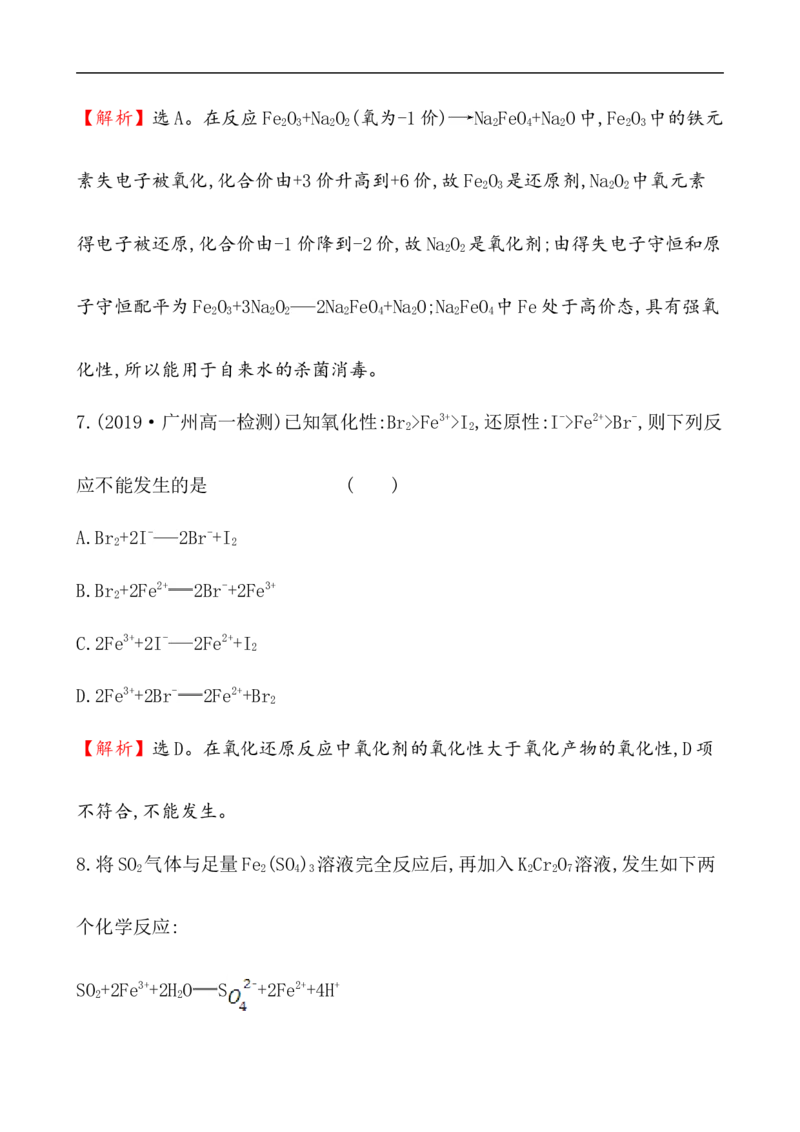
【解析】选C。由①知氧化性Fe3+>I ,还原性I->Fe2+;由②知氧化性Cl >Fe3+,还
2 2
原性Fe2+>Cl-;由③知氧化性Mn >Cl ,还原性Cl->Mn2+。由此推知氧化性强弱顺
2
序为KMnO >Cl >FeCl >I ,还原性强弱顺序为I->Fe2+>Cl->Mn2+。所以KMnO 可氧化
4 2 3 2 4
Cl-、Fe2+及I-,Cl 可氧化Fe2+及I-,FeCl 只氧化I-。
2 3
6.(2019·成都高一检测)用高铁酸钠(Na FeO )对河湖水消毒是城市饮水处理的
2 4
新技术。
一种生成Na FeO 的反应如下:Fe O +Na O (氧为-1价) Na FeO +Na O(未配平),
2 4 2 3 2 2 2 4 2
下列说法不正确的是 ( )
A.Na O 既是氧化剂又是还原剂
2 2
B.Fe O 在反应中失去电子
2 3
C.配平后为Fe O +3Na O 2Na FeO +Na O
2 3 2 2 2 4 2
D.Na FeO 能消毒杀菌是因其具有强氧化性
2 4【解析】选A。在反应Fe O +Na O (氧为-1价) Na FeO +Na O中,Fe O 中的铁元
2 3 2 2 2 4 2 2 3
素失电子被氧化,化合价由+3价升高到+6价,故Fe O 是还原剂,Na O 中氧元素
2 3 2 2
得电子被还原,化合价由-1价降到-2价,故Na O 是氧化剂;由得失电子守恒和原
2 2
子守恒配平为Fe O +3Na O 2Na FeO +Na O;Na FeO 中Fe处于高价态,具有强氧
2 3 2 2 2 4 2 2 4
化性,所以能用于自来水的杀菌消毒。
7.(2019·广州高一检测)已知氧化性:Br >Fe3+>I ,还原性:I->Fe2+>Br-,则下列反
2 2
应不能发生的是 ( )
A.Br +2I- 2Br-+I
2 2
B.Br +2Fe2+ 2Br-+2Fe3+
2
C.2Fe3++2I- 2Fe2++I
2
D.2Fe3++2Br- 2Fe2++Br
2
【解析】选D。在氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,D项
不符合,不能发生。
8.将SO 气体与足量Fe (SO ) 溶液完全反应后,再加入K Cr O 溶液,发生如下两
2 2 4 3 2 2 7
个化学反应:
SO +2Fe3++2H O S +2Fe2++4H+
2 2Cr +6Fe2++14H+
2
2Cr3++6Fe3++7H O
2
下列有关说法正确的是 ( )
A.还原性Cr3+>Fe2+>SO
2
B.氧化性Cr >S >Fe3+
2
C.Cr 能将Na SO 氧化成Na SO
2 2 3 2 4
D.两个反应中Fe (SO ) 均作还原剂
2 4 3
【解析】选C。由两个氧化还原反应得:氧化性强弱顺序为Cr >Fe3+>S ,
2
还原性强弱顺序为SO >Fe2+>Cr3+,所以A、B错误,Fe (SO ) 在第一个反应中作氧
2 2 4 3
化剂,第二个反应中是氧化产物。
9.含有氧化剂X 的溶液与亚硫酸钠(Na SO )溶液恰好反应完全,已知Na SO 被
2 3 2 3
氧化为Na SO ,已知X 、Na SO 的个数比为1∶2,则还原产物中元素X的价态
2 4 2 3
是
( )A.+2 B.-2
C.+1 D.0
【解析】选C。Na SO 被氧化为Na SO ,化合价升高+6-(+4)=2;设X被还原后的
2 3 2 4
价态为y,则化合价降低总数为(+5-y),由化合价升高总数等于降低总数:(6-
4)×
2=(5-y)×1,y=+1。
10.(2019·九江高一检测) 一定量的KClO 中加入浓盐酸发生如下反应:KClO +
3 3
6HCl(浓) KCl+3Cl ↑+3H O,其中发生氧化反应的元素和发生还原反应的元素
2 2
的质量之比为 ( )
A.1∶6 B.6∶1
C.1∶5 D.5∶1
【解析】选D。根据题设可判断出发生还原反应的元素是KClO 中的Cl,发生氧
3
化反应的元素是HCl中的Cl;由“化合价邻位转化”规律可知,HCl中有一部分
Cl转入到KCl中,还有一部分Cl转入到Cl 中,再根据化学反应方程式中各物质
2
的化学计量数判断,可知答案为D项。
二、非选择题(本题包括2小题,共20分)11.(10分)某反应中反应物与生成物有:AsH 、H SO 、KBrO 、K SO 、H AsO 、H O
3 2 4 3 2 4 3 4 2
和一种未知物质X。
(1)已知KBrO 在反应中得到电子,则该反应的还原剂是__________________。
3
(2)已知2个KBrO 在反应中得到10个电子生成X,则X的化学式为___________。
3
(3)根据上述反应可推知________。
a.氧化性:KBrO >H AsO
3 3 4
b.氧化性:H AsO >KBrO
3 4 3
c.还原性:AsH >X
3
d.还原性:X>AsH
3
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子
转移的方向和数目:
【解析】(1)KBrO 在反应中得到电子,则另外一种化合价变化的元素在反应中失
3
去电子被氧化,所给物质中砷元素化合价发生了变化,低价态的AsH 是还原剂。
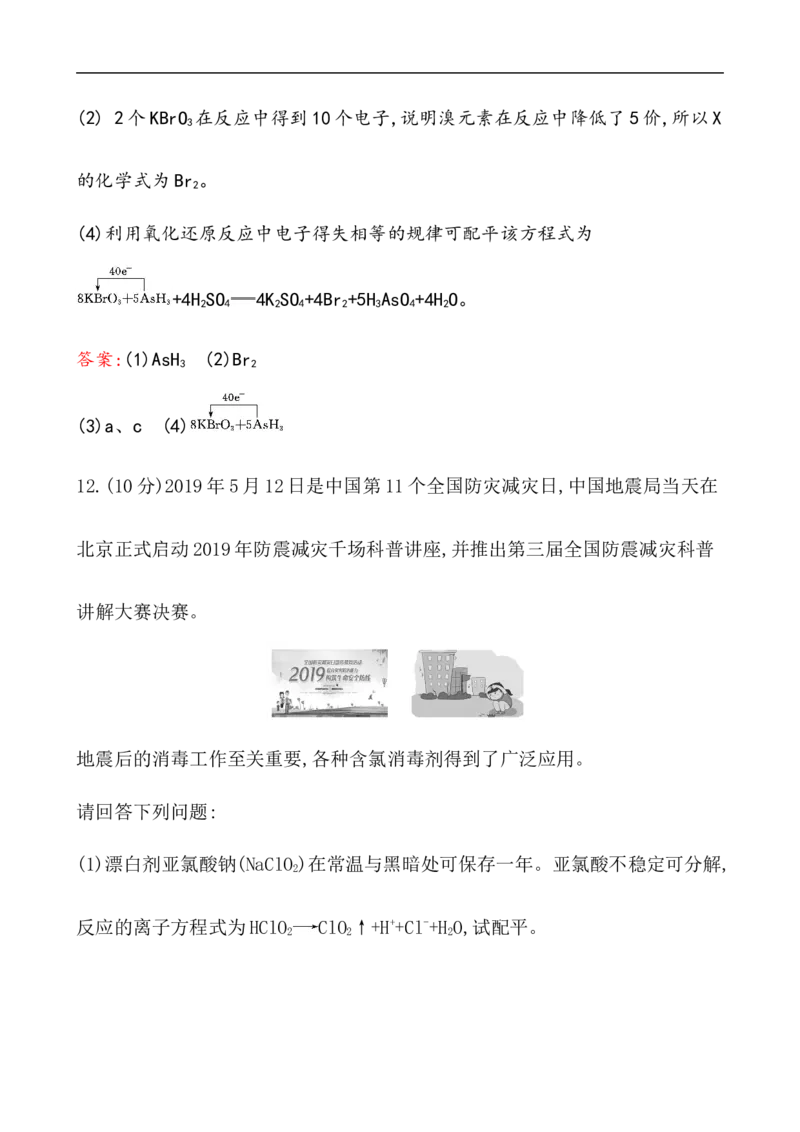
3(2) 2个KBrO 在反应中得到10个电子,说明溴元素在反应中降低了5价,所以X
3
的化学式为Br 。
2
(4)利用氧化还原反应中电子得失相等的规律可配平该方程式为
+4H SO 4K SO +4Br +5H AsO +4H O。
2 4 2 4 2 3 4 2
答案:(1)AsH (2)Br
3 2
(3)a、c (4)
12.(10分)2019年5月12日是中国第11个全国防灾减灾日,中国地震局当天在
北京正式启动2019年防震减灾千场科普讲座,并推出第三届全国防震减灾科普
讲解大赛决赛。
地震后的消毒工作至关重要,各种含氯消毒剂得到了广泛应用。
请回答下列问题:
(1)漂白剂亚氯酸钠(NaClO )在常温与黑暗处可保存一年。亚氯酸不稳定可分解,
2
反应的离子方程式为HClO ClO ↑+H++Cl-+H O,试配平。
2 2 2(2)ClO 是一种消毒杀菌效率高的消毒剂,具有强氧化性。工业上制备ClO 的化
2 2
学反应方程式为2NaClO +Na SO +H SO 2ClO +2Na SO +H O,该反应中氧化剂、
3 2 3 2 4 2 2 4 2
还原剂分别是什么?1个 NaClO 参加反应转移几个电子?
3
【解析】(1)把离子方程式配平得5HClO 4ClO ↑+H++Cl-+2H O。
2 2 2
(2)由反应方程式2NaClO +Na SO +H SO 2ClO +2Na SO +H O可知,NaClO 在反应
3 2 3 2 4 2 2 4 2 3
中,Cl由+5价降到+4价,氯原子得电子,NaClO 是氧化剂,Na SO 被氧化为
3 2 3
Na SO ,是还原剂;由于Cl由+5价降到+4价,所以1个 NaClO 参加反应,则有1
2 4 3
个电子转移。
答案:(1)5HClO
2
4ClO ↑+H++Cl-+2H O。
2 2
(2) 氧化剂为NaClO ,还原剂为Na SO ,1个NaClO 参加反应转移1个电子。
3 2 3 3
(20分钟 30分)
一、选择题(本题包括2小题,每小题8分,共16分)
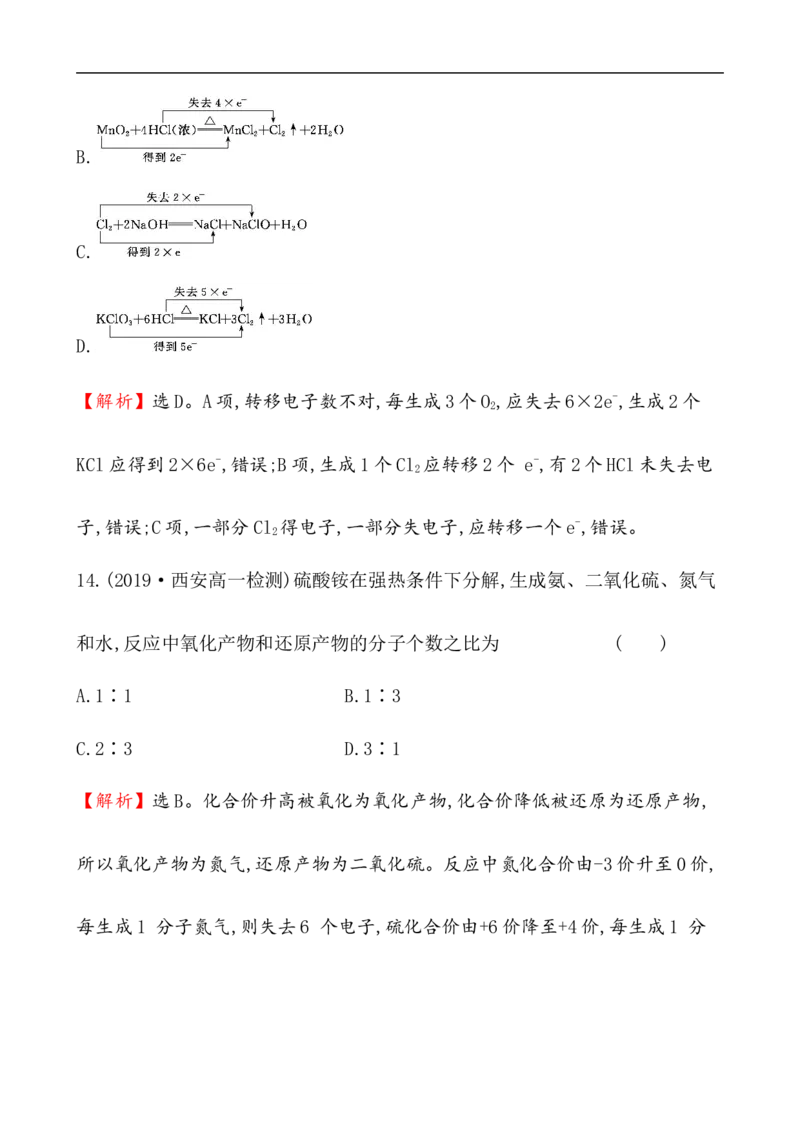
13.下列各氧化还原反应方程式表示的变化过程正确的是 ( )
A.B.
C.
D.
【解析】选D。A项,转移电子数不对,每生成3个O ,应失去6×2e-,生成2个
2
KCl应得到2×6e-,错误;B项,生成1个Cl 应转移2个 e-,有2个HCl未失去电
2
子,错误;C项,一部分Cl 得电子,一部分失电子,应转移一个e-,错误。
2
14.(2019·西安高一检测)硫酸铵在强热条件下分解,生成氨、二氧化硫、氮气
和水,反应中氧化产物和还原产物的分子个数之比为 ( )
A.1∶1 B.1∶3
C.2∶3 D.3∶1
【解析】选B。化合价升高被氧化为氧化产物,化合价降低被还原为还原产物,
所以氧化产物为氮气,还原产物为二氧化硫。反应中氮化合价由-3价升至0价,
每生成1 分子氮气,则失去6 个电子,硫化合价由+6价降至+4价,每生成1 分子二氧化硫,则得到2 个电子,由得失电子相等可知氮气与二氧化硫的分子个数
之比为1∶3。
二、非选择题(本题包括1小题,共14分)
15.(2019·西安高一检测)凡是养鱼的人都知道一种很不错的消毒剂,这就是被
称为当今第四代消毒产品的二氧化氯。其属于A1级别安全高效消毒剂之一,并
且可以在极低的浓度下对病菌有杀灭作用,功效显而易见。一起来看看它的使
用方法吧。
KClO 和浓盐酸在一定温度下反应生成黄绿色的易爆物二氧化氯。其变化可表述
3
为
(1)请完成该化学方程式并配平(未知物化学式和系数填入框内)。
(2)浓盐酸在反应中显示出来的性质是________(填序号)。
①只有还原性 ②还原性和酸性③只有氧化性 ④氧化性和酸性
(3)产生1分子Cl ,转移的电子为________个。
2
(4)ClO 具有很强的氧化性,因此常被用作消毒剂,其消毒效率(以单位质量得到
2
的电子数表示)是Cl 的________倍(保留小数点后两位)。
2
【解析】(1)氧化还原方程式的配平可从电子得失相等和原子守恒两个方面来
完成。注意不交叉规律的使用。
(2)反应中浓盐酸一部分转化成Cl 表现还原性,一部分转化成KCl表现酸性。
2
(4)设ClO 和Cl 的质量均为m,其消毒效率之比为( ×5)∶(
2 2
×2)=2.63。
答案:(1)2 4 2 2 1 2 H O
2
(2)② (3)2 (4)2.63