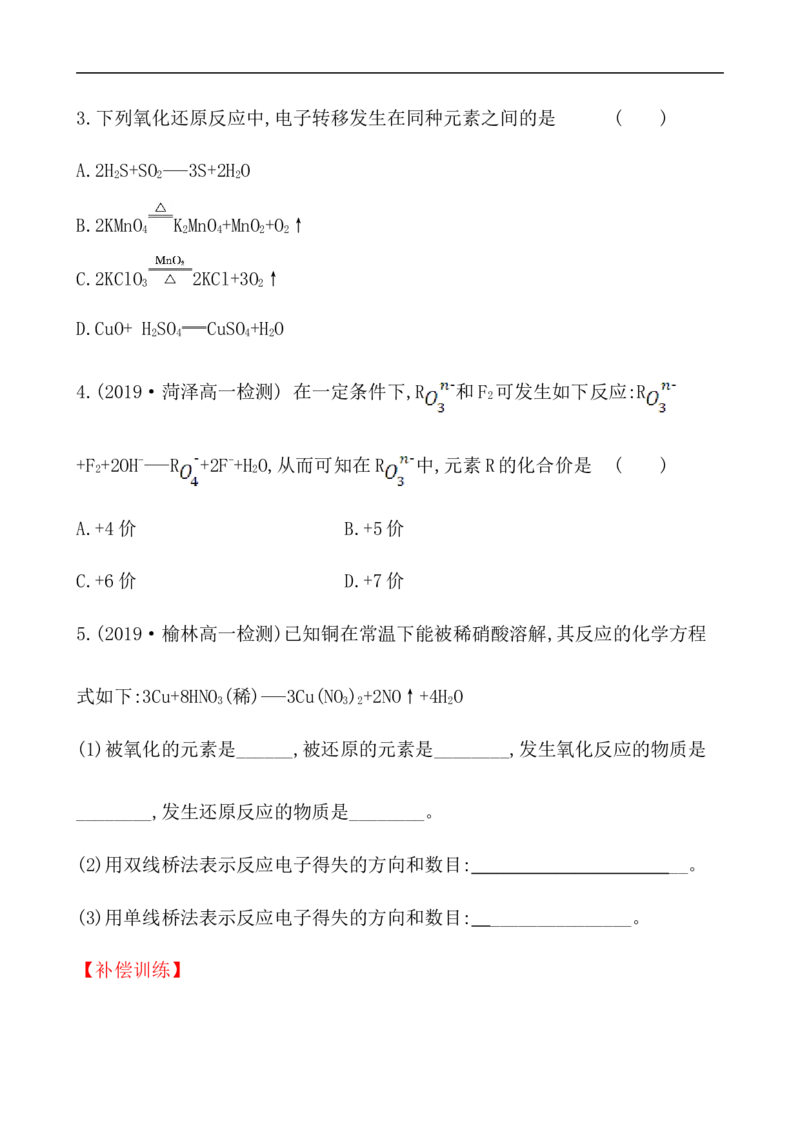文档内容
课堂检测·素养达标
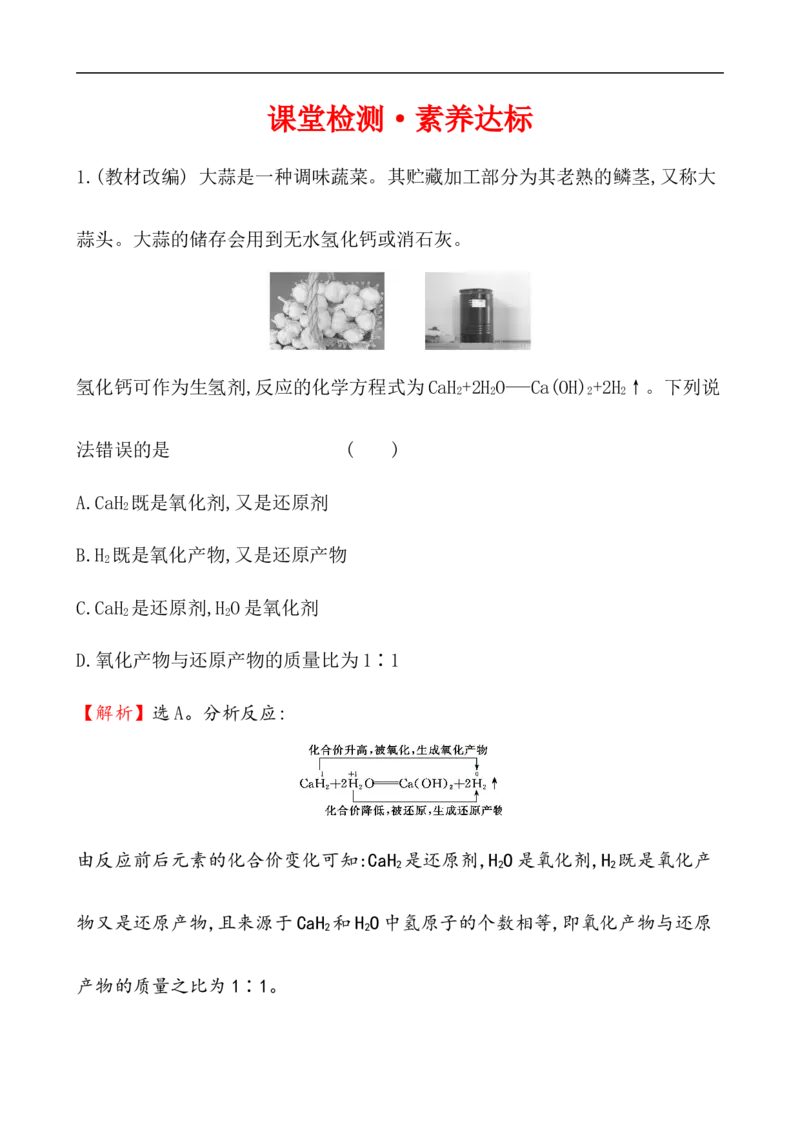
1.(教材改编) 大蒜是一种调味蔬菜。其贮藏加工部分为其老熟的鳞茎,又称大
蒜头。大蒜的储存会用到无水氢化钙或消石灰。
氢化钙可作为生氢剂,反应的化学方程式为CaH +2H O Ca(OH) +2H ↑。下列说
2 2 2 2
法错误的是 ( )
A.CaH 既是氧化剂,又是还原剂
2
B.H 既是氧化产物,又是还原产物
2
C.CaH 是还原剂,H O是氧化剂
2 2
D.氧化产物与还原产物的质量比为1∶1
2.(2019·济宁高一检测)在含有Cu(NO ) 、Mg(NO ) 、AgNO 的溶液中加入适量
3 2 3 2 3
锌粉,首先置换出的是 ( )
A.Mg B.Cu
C.Ag D.H
2
【互动探究】(1)最终不能置换出来的金属是______。
(2)上述反应中金属Zn起到什么作用?3.下列氧化还原反应中,电子转移发生在同种元素之间的是 ( )
A.2H S+SO 3S+2H O
2 2 2
B.2KMnO K MnO +MnO +O ↑
4 2 4 2 2
C.2KClO 2KCl+3O ↑
3 2
D.CuO+ H SO CuSO +H O
2 4 4 2
4.(2019·菏泽高一检测) 在一定条件下,R 和F 可发生如下反应:R
2
+F +2OH- R +2F-+H O,从而可知在R 中,元素R的化合价是 ( )
2 2
A.+4价 B.+5价
C.+6价 D.+7价
5.(2019·榆林高一检测)已知铜在常温下能被稀硝酸溶解,其反应的化学方程
式如下:3Cu+8HNO (稀) 3Cu(NO ) +2NO↑+4H O
3 3 2 2
(1)被氧化的元素是______,被还原的元素是________,发生氧化反应的物质是
________,发生还原反应的物质是________。
(2)用双线桥法表示反应电子得失的方向和数目: __。
(3)用单线桥法表示反应电子得失的方向和数目: _______________。
【补偿训练】某厂废水中含KCN,现用氯氧化法处理,发生如下反应(化合物中N化合价均
为-3价):
KCN+2KOH+Cl KOCN+2KCl+H O
2 2
(1)上述反应中被氧化的元素是________(用元素符号表示)。
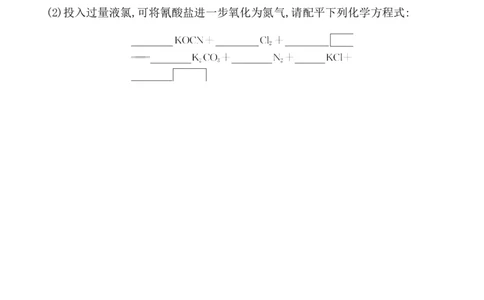
(2)投入过量液氯,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式:课堂检测·素养达标
1.(教材改编) 大蒜是一种调味蔬菜。其贮藏加工部分为其老熟的鳞茎,又称大
蒜头。大蒜的储存会用到无水氢化钙或消石灰。
氢化钙可作为生氢剂,反应的化学方程式为CaH +2H O Ca(OH) +2H ↑。下列说
2 2 2 2
法错误的是 ( )
A.CaH 既是氧化剂,又是还原剂
2
B.H 既是氧化产物,又是还原产物
2
C.CaH 是还原剂,H O是氧化剂
2 2
D.氧化产物与还原产物的质量比为1∶1
【解析】选A。分析反应:
由反应前后元素的化合价变化可知:CaH 是还原剂,H O是氧化剂,H 既是氧化产
2 2 2
物又是还原产物,且来源于CaH 和H O中氢原子的个数相等,即氧化产物与还原
2 2
产物的质量之比为1∶1。2.(2019·济宁高一检测)在含有Cu(NO ) 、Mg(NO ) 、AgNO 的溶液中加入适量
3 2 3 2 3
锌粉,首先置换出的是 ( )
A.Mg B.Cu
C.Ag D.H
2
【解析】选C。由金属活动性顺序可知,Cu2+、Mg2+、Ag+、H+的氧化性由强到弱
的顺序为Ag+>Cu2+>H+>Mg2+,故混合液与锌粉反应时,首先置换出Ag。
【互动探究】(1)最终不能置换出来的金属是______。
提示:Mg。由于Zn的还原性小于Mg,故Zn不能与Mg 2+反应。
(2)上述反应中金属Zn起到什么作用?
提示:金属Zn作还原剂。Zn的化合价升高作还原剂。
3.下列氧化还原反应中,电子转移发生在同种元素之间的是 ( )
A.2H S+SO 3S+2H O
2 2 2
B.2KMnO K MnO +MnO +O ↑
4 2 4 2 2
C.2KClO 2KCl+3O ↑
3 2
D.CuO+ H SO CuSO +H O
2 4 4 2
【解析】选A。2H S+SO 3S+2H O反应是在-2价硫和+4价硫之间的氧化还原
2 2 2
反应,A正确;2KMnO K MnO +MnO +O ↑反应是在锰元素和氧元素之间的氧化还
4 2 4 2 2原反应,B错误;2KClO 2KCl+3O ↑反应是在氯元素和氧元素之间的氧化还
3 2
原反应,C错误;CuO+ H SO CuSO +H O反应是非氧化还原反应,D错误。
2 4 4 2
4.(2019·菏泽高一检测) 在一定条件下,R 和F 可发生如下反应:R
2
+F +2OH- R +2F-+H O,从而可知在R 中,元素R的化合价是 ( )
2 2
A.+4价 B.+5价
C.+6价 D.+7价
【解析】选B。设元素R在R 中的化合价为x。根据氧化还原反应中,得失电
子守恒有(7-x)×1=[0-(-1)]×2,所以x=+5。
5.(2019·榆林高一检测)已知铜在常温下能被稀硝酸溶解,其反应的化学方程
式如下:3Cu+8HNO (稀) 3Cu(NO ) +2NO↑+4H O
3 3 2 2
(1)被氧化的元素是______,被还原的元素是________,发生氧化反应的物质是
________,发生还原反应的物质是________。
(2)用双线桥法表示反应电子得失的方向和数目: __。
(3)用单线桥法表示反应电子得失的方向和数目: _______________。
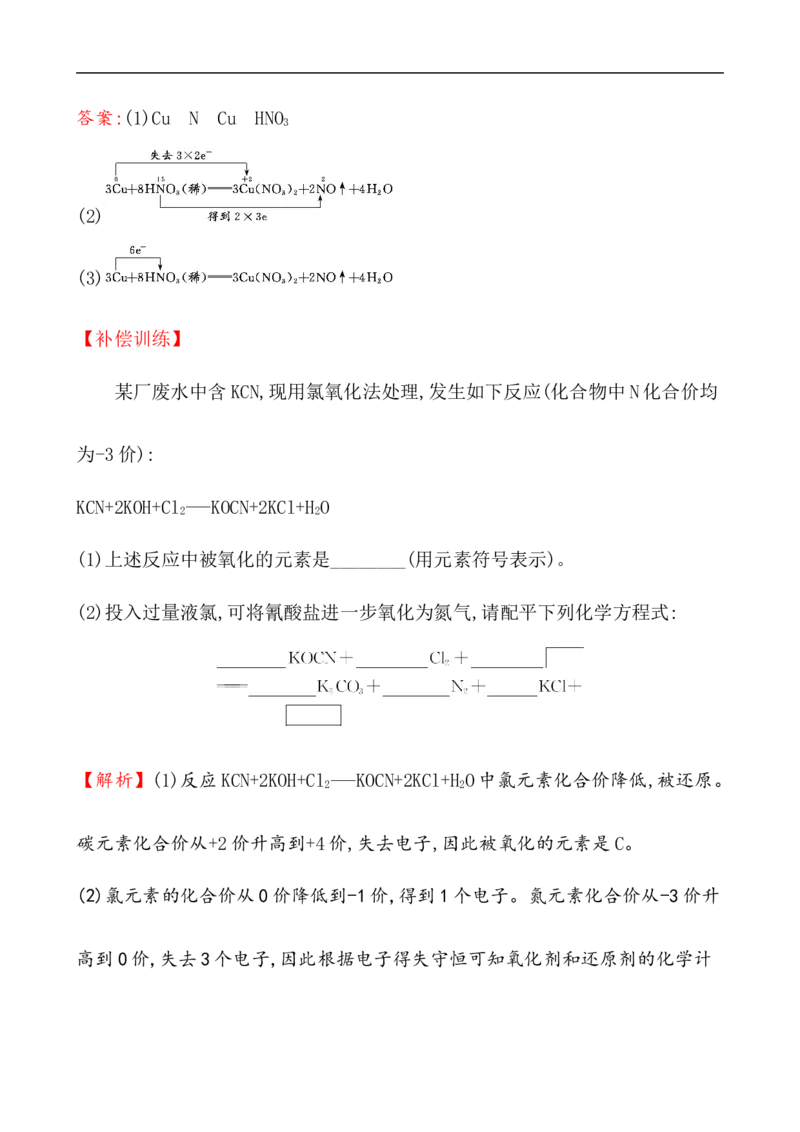
【解析】由方程式可知:铜元素化合价升高,从0价变为+2价,被氧化;氮元素化
合价降低,从+5价变为+2价,被还原;故Cu发生氧化反应,HNO 发生还原反应。
3答案:(1)Cu N Cu HNO
3
(2)
(3)
【补偿训练】
某厂废水中含KCN,现用氯氧化法处理,发生如下反应(化合物中N化合价均
为-3价):
KCN+2KOH+Cl KOCN+2KCl+H O
2 2
(1)上述反应中被氧化的元素是________(用元素符号表示)。
(2)投入过量液氯,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式:
【解析】(1)反应KCN+2KOH+Cl KOCN+2KCl+H O中氯元素化合价降低,被还原。
2 2
碳元素化合价从+2价升高到+4价,失去电子,因此被氧化的元素是C。
(2)氯元素的化合价从0价降低到-1价,得到1个电子。氮元素化合价从-3价升
高到0价,失去3个电子,因此根据电子得失守恒可知氧化剂和还原剂的化学计量数之比是3∶2,根据原子守恒可知还有水生成,因此反应的化学方程式为
2KOCN+3Cl +8KOH 2K CO +N +6KCl+4H O。
2 2 3 2 2
答案:(1)C
(2)2 3 8 KOH 2 1 6 4 H O
2