文档内容
课堂检测·素养达标
1.从煤油中取出钠块的正确操作是 ( )
A.用手指捏 B.用镊子夹
C.用纸槽取 D.用滴管吸
2.航空事故猛于虎,很多化学物品禁止携带: 爆炸物品、易燃易爆物品、剧毒
物品、放射性物品、腐蚀性物品、危险溶液及国家规定的其他禁运物品。装运
金属钠的包装箱应贴的标志是 ( )
3.钠与我们的生活息息相关,我们吃的食盐中就含有钠元素。下列关于钠的说
法不正确的是 ( )
A.金属钠和氧气反应,条件不同,产物不同
B.钠长期置于空气中,表面不能形成致密氧化膜
C.钠与水反应时,钠熔成小球在水面四处游动
D.由于钠比较活泼,所以它能从溶液中置换出金属活动性顺序表中钠后面的金
属4.钛和钛的合金大量用于航空工业,有“空间金属”之称;钛还可以用来制造潜
艇——钛潜艇,由于钛非常结实,能承受很高的压力,这种潜艇可以在深达4 500
米的深海中航行。金属钛可由反应TiCl +4Na 4NaCl+Ti制得。
4
对于反应,下列说法正确的是 ( )
A.该反应说明钠是强还原剂,可用于冶炼金属
B.该反应条件是TiCl 在熔融状态或水溶液中
4
C.Ti是氧化剂
D.TiCl 是还原剂
4
5.(2019·洛阳高一检测)金属钠是在1807年通过电解氢氧化钠制得的,这个原
理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制钠的
工业方法,其反应原理是2NaCl(熔融) 2Na+Cl ↑。回答下列有关单质钠的问
2
题:
(1)保存金属钠的正确方法是________。
A.放在棕色瓶中 B.放在细沙中C.放在水中 D.放在煤油中
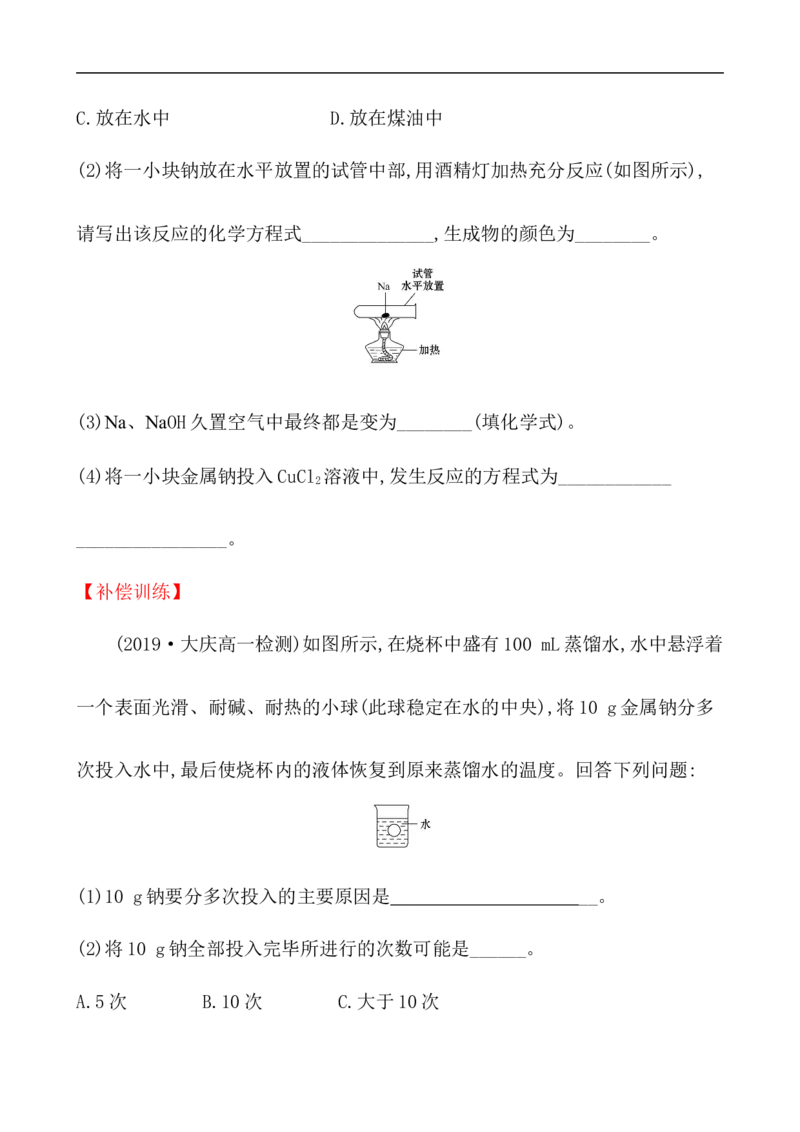
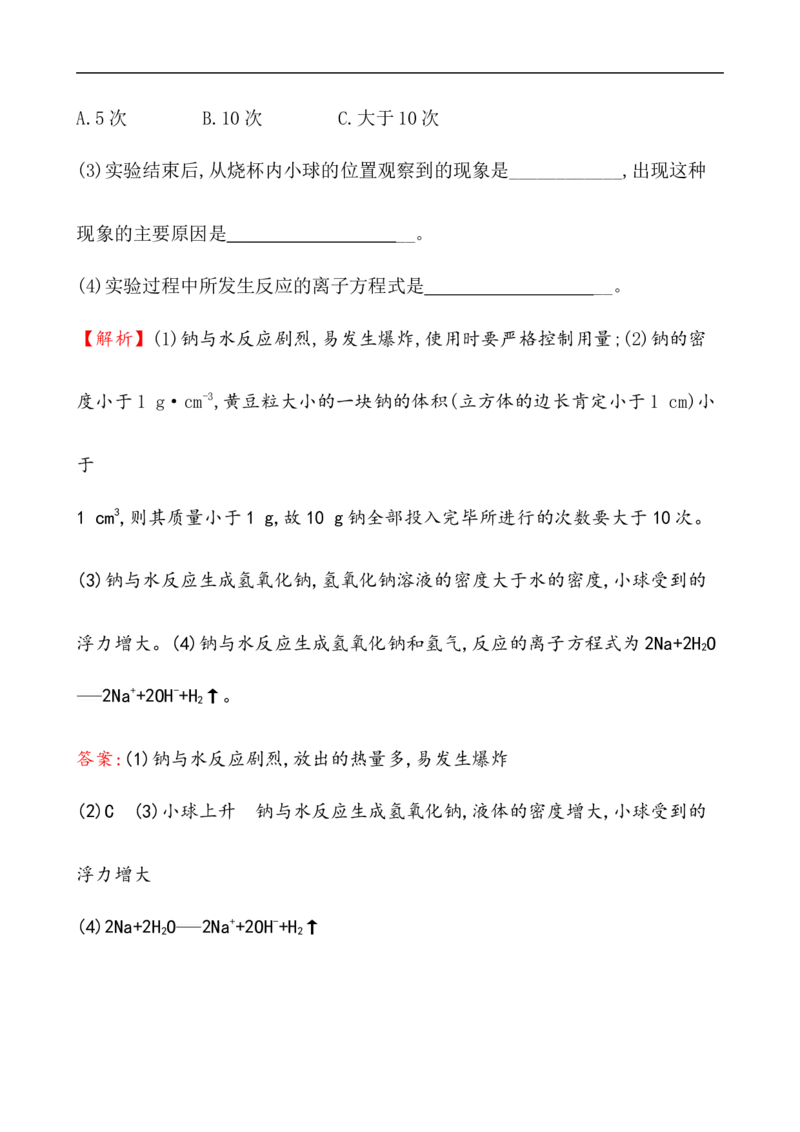
(2)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应(如图所示),
请写出该反应的化学方程式______________,生成物的颜色为________。
(3)Na、NaOH久置空气中最终都是变为________(填化学式)。
(4)将一小块金属钠投入CuCl 溶液中,发生反应的方程式为____________
2
________________。
【补偿训练】
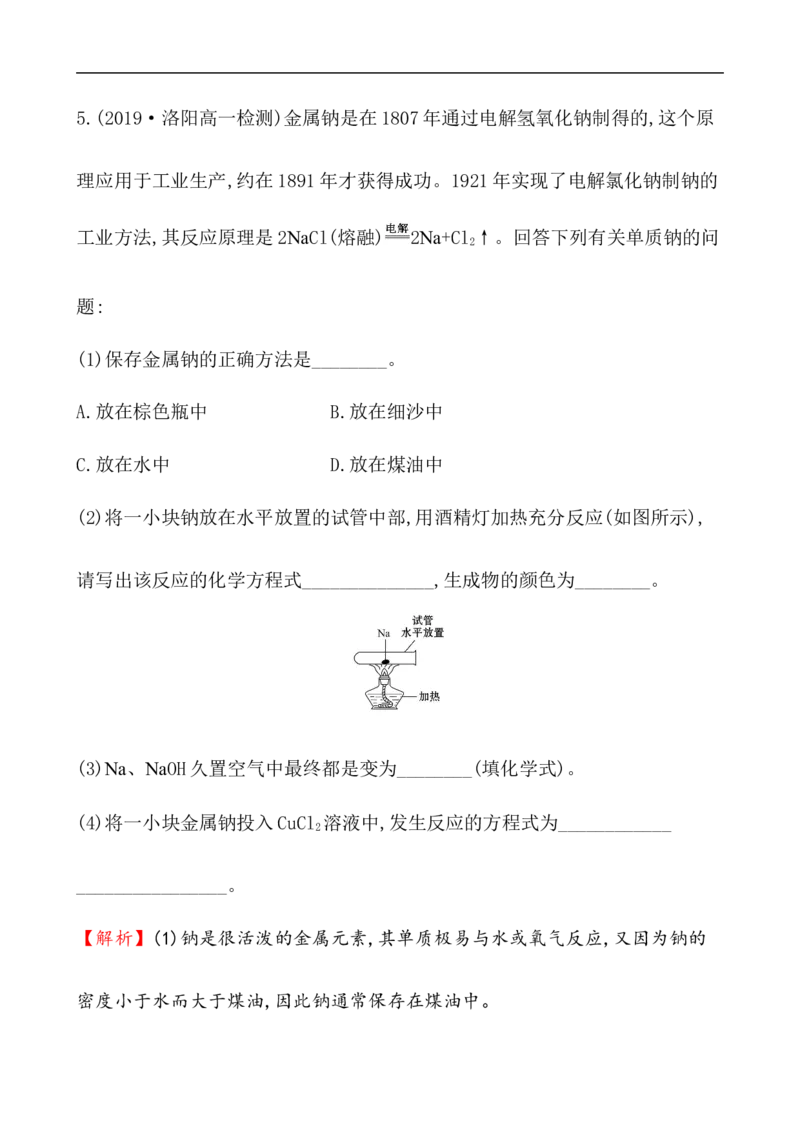
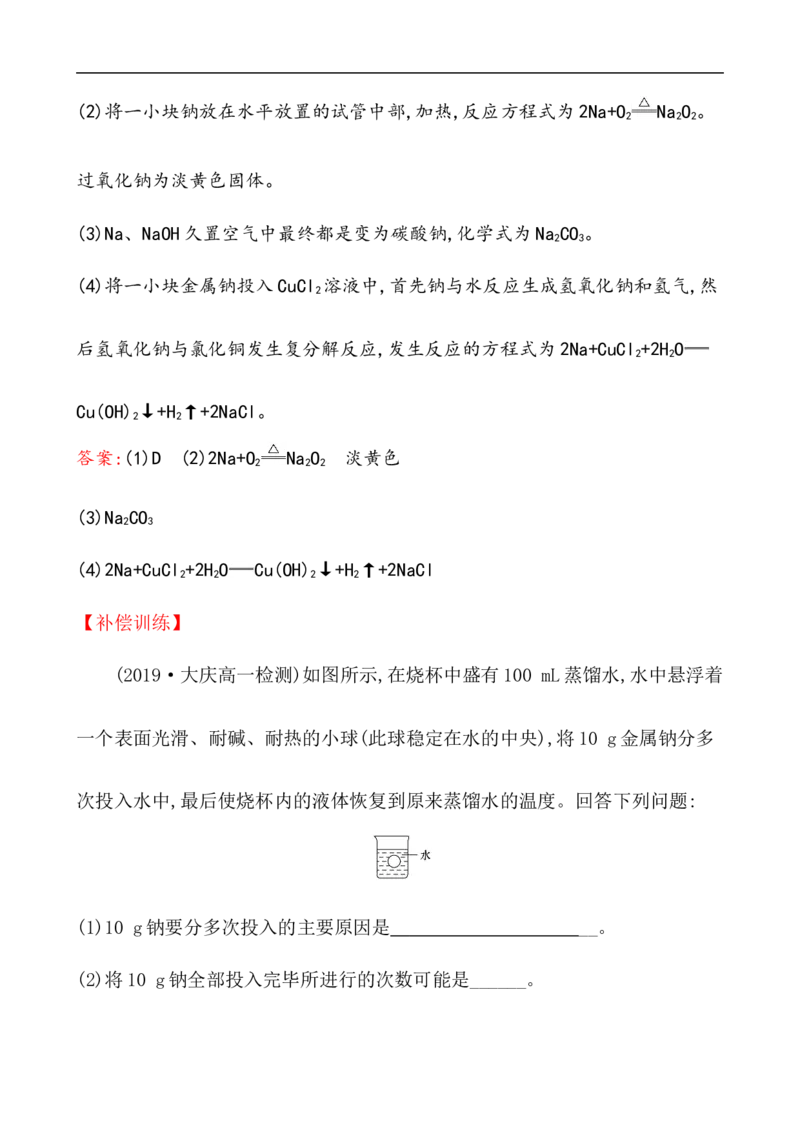
(2019·大庆高一检测)如图所示,在烧杯中盛有100 mL蒸馏水,水中悬浮着
一个表面光滑、耐碱、耐热的小球(此球稳定在水的中央),将10 g金属钠分多
次投入水中,最后使烧杯内的液体恢复到原来蒸馏水的温度。回答下列问题:
(1)10 g钠要分多次投入的主要原因是 __。
(2)将10 g钠全部投入完毕所进行的次数可能是______。
A.5次 B.10次 C.大于10次(3)实验结束后,从烧杯内小球的位置观察到的现象是____________,出现这种
现象的主要原因是 __。
(4)实验过程中所发生反应的离子方程式是 __。课堂检测·素养达标
1.从煤油中取出钠块的正确操作是 ( )
A.用手指捏 B.用镊子夹
C.用纸槽取 D.用滴管吸
【解析】选B。用镊子从煤油中夹取一小块钠。
2.航空事故猛于虎,很多化学物品禁止携带: 爆炸物品、易燃易爆物品、剧毒
物品、放射性物品、腐蚀性物品、危险溶液及国家规定的其他禁运物品。装运
金属钠的包装箱应贴的标志是 ( )
【解析】选C。金属钠投入水中发生剧烈反应,并有氢气生成,氢气易燃。
3.钠与我们的生活息息相关,我们吃的食盐中就含有钠元素。下列关于钠的说
法不正确的是 ( )
A.金属钠和氧气反应,条件不同,产物不同
B.钠长期置于空气中,表面不能形成致密氧化膜
C.钠与水反应时,钠熔成小球在水面四处游动D.由于钠比较活泼,所以它能从溶液中置换出金属活动性顺序表中钠后面的金
属
【解析】选D。钠不能从盐溶液中置换出金属。
4.钛和钛的合金大量用于航空工业,有“空间金属”之称;钛还可以用来制造潜
艇——钛潜艇,由于钛非常结实,能承受很高的压力,这种潜艇可以在深达4 500
米的深海中航行。金属钛可由反应TiCl +4Na 4NaCl+Ti制得。
4
对于反应,下列说法正确的是 ( )
A.该反应说明钠是强还原剂,可用于冶炼金属
B.该反应条件是TiCl 在熔融状态或水溶液中
4
C.Ti是氧化剂
D.TiCl 是还原剂
4
【解析】选A。由TiCl +4Na 4NaCl+Ti知,钠是强还原剂,可用于冶炼金属,A
4
项正确;钠性质非常活泼,能用于还原熔融状态TiCl 为Ti,但不能在水溶液中进
4
行,B项错误;该反应中,钛元素化合价降低,TiCl 是氧化剂,C、D项错误。
45.(2019·洛阳高一检测)金属钠是在1807年通过电解氢氧化钠制得的,这个原
理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制钠的
工业方法,其反应原理是2NaCl(熔融) 2Na+Cl ↑。回答下列有关单质钠的问
2
题:
(1)保存金属钠的正确方法是________。
A.放在棕色瓶中 B.放在细沙中
C.放在水中 D.放在煤油中
(2)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应(如图所示),
请写出该反应的化学方程式______________,生成物的颜色为________。
(3)Na、NaOH久置空气中最终都是变为________(填化学式)。
(4)将一小块金属钠投入CuCl 溶液中,发生反应的方程式为____________
2
________________。
【解析】(1)钠是很活泼的金属元素,其单质极易与水或氧气反应,又因为钠的
密度小于水而大于煤油,因此钠通常保存在煤油中。(2)将一小块钠放在水平放置的试管中部,加热,反应方程式为2Na+O Na O 。
2 2 2
过氧化钠为淡黄色固体。
(3)Na、NaOH久置空气中最终都是变为碳酸钠,化学式为Na CO 。
2 3
(4)将一小块金属钠投入CuCl 溶液中,首先钠与水反应生成氢氧化钠和氢气,然
2
后氢氧化钠与氯化铜发生复分解反应,发生反应的方程式为2Na+CuCl +2H O
2 2
Cu(OH) ↓+H ↑+2NaCl。
2 2
答案:(1)D (2)2Na+O Na O 淡黄色
2 2 2
(3)Na CO
2 3
(4)2Na+CuCl +2H O Cu(OH) ↓+H ↑+2NaCl
2 2 2 2
【补偿训练】
(2019·大庆高一检测)如图所示,在烧杯中盛有100 mL蒸馏水,水中悬浮着
一个表面光滑、耐碱、耐热的小球(此球稳定在水的中央),将10 g金属钠分多
次投入水中,最后使烧杯内的液体恢复到原来蒸馏水的温度。回答下列问题:
(1)10 g钠要分多次投入的主要原因是 __。
(2)将10 g钠全部投入完毕所进行的次数可能是______。A.5次 B.10次 C.大于10次
(3)实验结束后,从烧杯内小球的位置观察到的现象是____________,出现这种
现象的主要原因是 __。
(4)实验过程中所发生反应的离子方程式是 __。
【解析】(1)钠与水反应剧烈,易发生爆炸,使用时要严格控制用量;(2)钠的密
度小于1 g·cm-3,黄豆粒大小的一块钠的体积(立方体的边长肯定小于1 cm)小
于
1 cm3,则其质量小于1 g,故10 g钠全部投入完毕所进行的次数要大于10次。
(3)钠与水反应生成氢氧化钠,氢氧化钠溶液的密度大于水的密度,小球受到的
浮力增大。(4)钠与水反应生成氢氧化钠和氢气,反应的离子方程式为2Na+2H O
2
2Na++2OH-+H ↑。
2
答案:(1)钠与水反应剧烈,放出的热量多,易发生爆炸
(2)C (3)小球上升 钠与水反应生成氢氧化钠,液体的密度增大,小球受到的
浮力增大
(4)2Na+2H O 2Na++2OH-+H ↑
2 2