文档内容
课时素养评价 八
活泼的金属单质——钠
(30分钟 50分)
1.(2019·聊城高一检测)从生活常识角度考虑,试推断钠元素在自然界中存在
的主要形式是 ( )
A.Na B.NaCl
C.NaOH D.Na O
2
2.(2019·苏州高一检测)金属钠在氧气中燃烧,生成物是 ( )
A.氧化钠 B.过氧化钠
C.氢氧化钠 D.碳酸钠
3.(2019·北京平谷区高一检测)通过观察钠与水(含酚酞)的反应现象,不能得
出的结论是 ( )
A.钠的密度比水小
B.钠是活泼金属,与水反应后溶液呈碱性
C.钠有良好的延展性
D.钠的熔点低4.(2019·杭州高一检测)某学生将一小块钠投入滴有酚酞的水中,此实验能证
明钠下面4点性质中的 ( )
①钠的密度比水的小
②钠的熔点较低
③钠与水反应时放出热量
④钠与水反应后溶液呈碱性
A.①④ B.①②④
C.①③④ D.①②③④
5.(2019·南开区高一检测)人生是一幅大画布,你应该努力绘出绚丽多彩的画
面。实验现象也是绚丽多彩,让人流连忘返。向硫酸铜溶液中加入一小块金属
钠后,观察到的现象有 ( )
世纪金榜导学号
①钠浮于液面上
②熔化成小球
③发出嘶嘶的响声,放出气体
④钠周围蓝色沉淀部分变黑
⑤有蓝色沉淀产生⑥析出大量红色的铜
⑦小球在溶液中沉浮
⑧小球在液面上游动,逐渐变小,直至消失
A.①②③⑤⑧ B.①②③④⑤⑧
C.①②③⑤⑥⑧ D.①②③④⑤⑥⑦⑧
6.某同学将金属钠露置于空气中,观察到下列现象:银白色 变灰暗 变白色
出现液滴 白色晶体 白色粉末,根据钠及其化合物的性质分析,下列说法
正确的是 ( )
A.①发生了氧化还原反应
B.①钠表面变灰暗是因为生成了过氧化钠
C.③是碳酸钠吸收空气中的水蒸气形成了溶液
D.④⑤只发生物理变化
【补偿训练】
将2.3 g金属钠放入100 g水中,完全反应后溶液的质量分数为 ( )
A. ×100%
B. ×100%C. ×100%
D. ×100%
二、非选择题(本题包括1小题,共10分)
7.某化学实验小组拟用如图装置进行钠与氧气反应的实验。
(1)将一小块钠放在石棉网上加热,能观察到的实验现象有
__,
写出发生反应的化学方程式:
__。
(2)上述实验中还观察到有黑色固体物质生成,其原因可能为2Na+CO C+Na O
2 2 2
或4Na+3CO C+2Na CO ,这两个化学方程式的反应类型既属于基本反应类型中
2 2 3
的________反应,也属于________(填“氧化还原”或“非氧化还原”)反应。
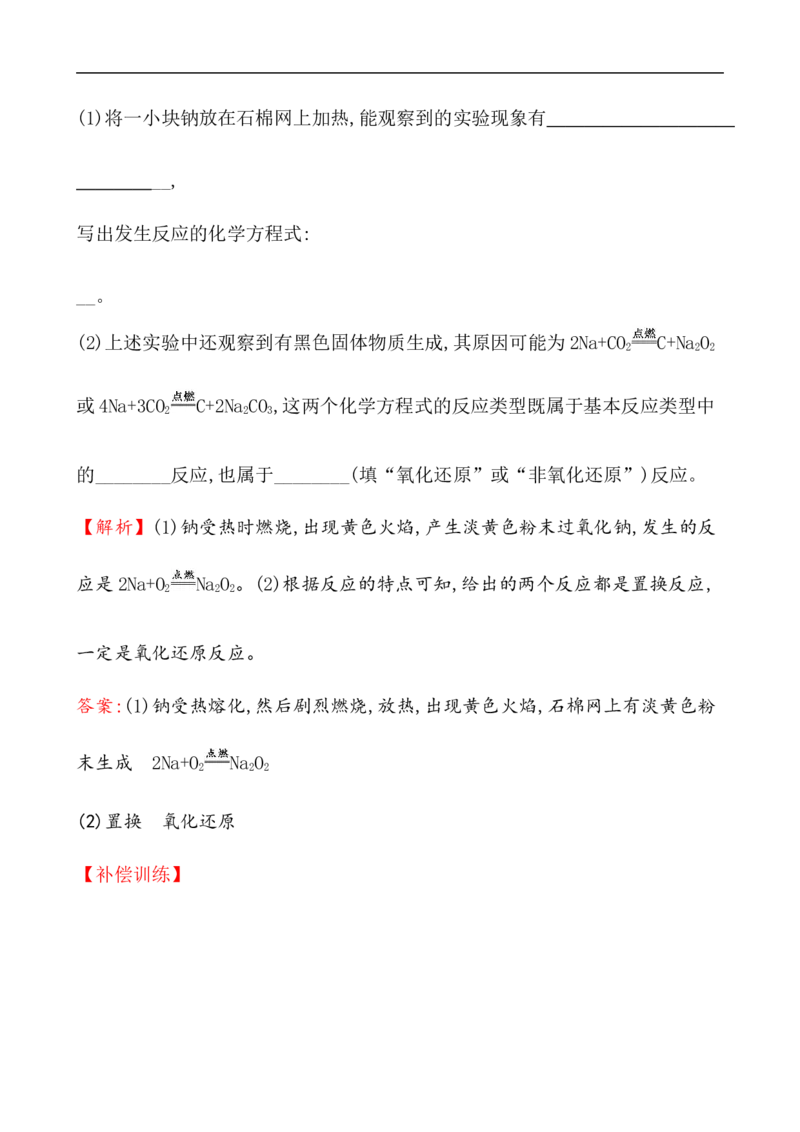
【补偿训练】某实验小组对中学课本中可生成氢气的反应进行了研究,总结出两个可以
生成H 的反应:①Zn+盐酸,②Na+水。为点燃上述两个反应生成的H ,他们设计
2 2
了图示装置。请回答下列问题:
(1)写出Na与H O反应的化学方程式: _________________________。
2
(2)实验小组在点燃用上述装置制得的H 时,①实验获得成功,②却失败了。他
2
们分析认为失败的原因是Na的用量太少,Na与H O的反应速率太快。于是他们
2
准备增加钠的用量,可老师说太危险,你认为产生危险的原因是______________。
(3)实验小组查阅钠、煤油、水的密度分别为0.97 g·cm-3、0.80 g·cm-3、
1.00 g·cm-3,并据此对实验进行改进。在改进后的实验中H 的生成速率减慢,
2
原因是 __。
一、选择题(本题包括1小题,共6分)
8.钠的化学性质非常活泼。下列关于金属钠的叙述错误的是 ( )A.金属钠可以保存在煤油中
B.钠元素只能以化合态形式存在于自然界中
C.实验室取用金属钠需要镊子、滤纸、小刀3种用品
D.钠元素在自然界中主要以NaCl的形式存在
【补偿训练】
在烧杯中加入水和苯(密度为0.88 g·cm-3,与水互不相溶,且不与钠反应)
各50 mL,将一小粒金属钠(密度为0.97 g·cm-3)投入烧杯中,观察到的现象可
能为 ( )
A.钠在水层中反应并四处游动
B.钠停留在苯层中不发生反应
C.钠在苯的液面上反应并四处游动
D.钠在苯与水的界面处反应并可能上浮下沉
二、非选择题(本题包括1小题,共10分)
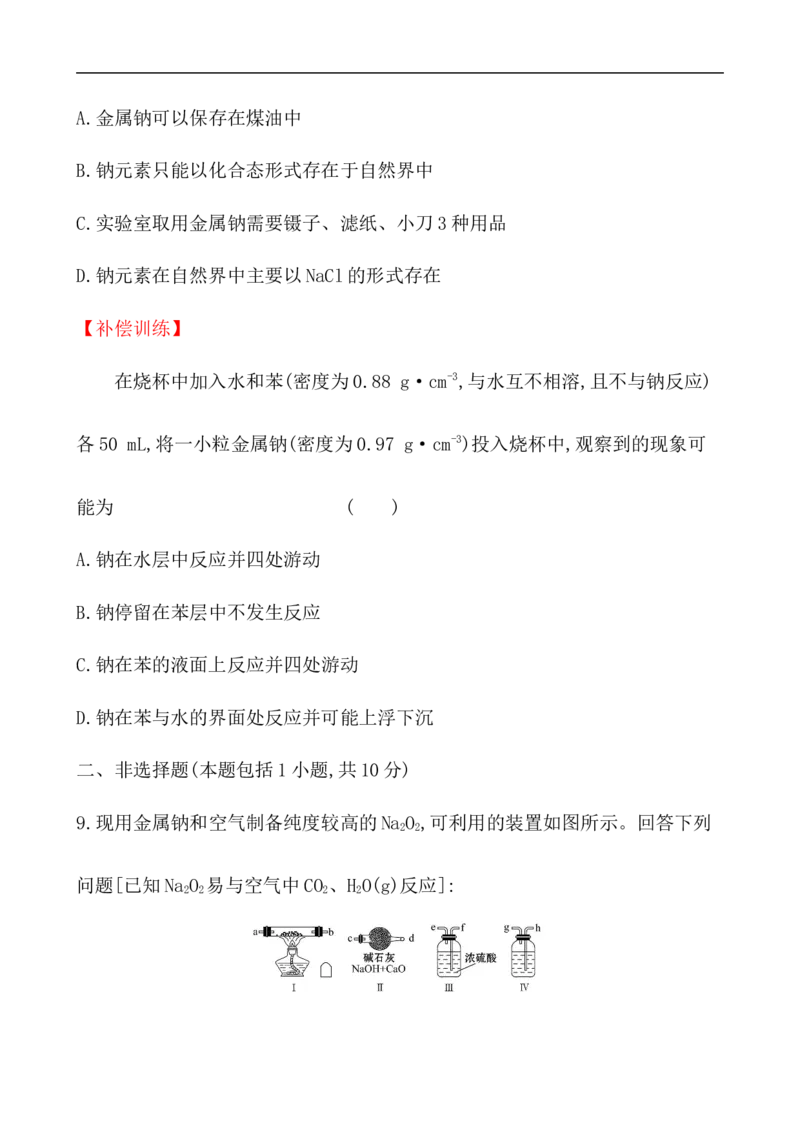
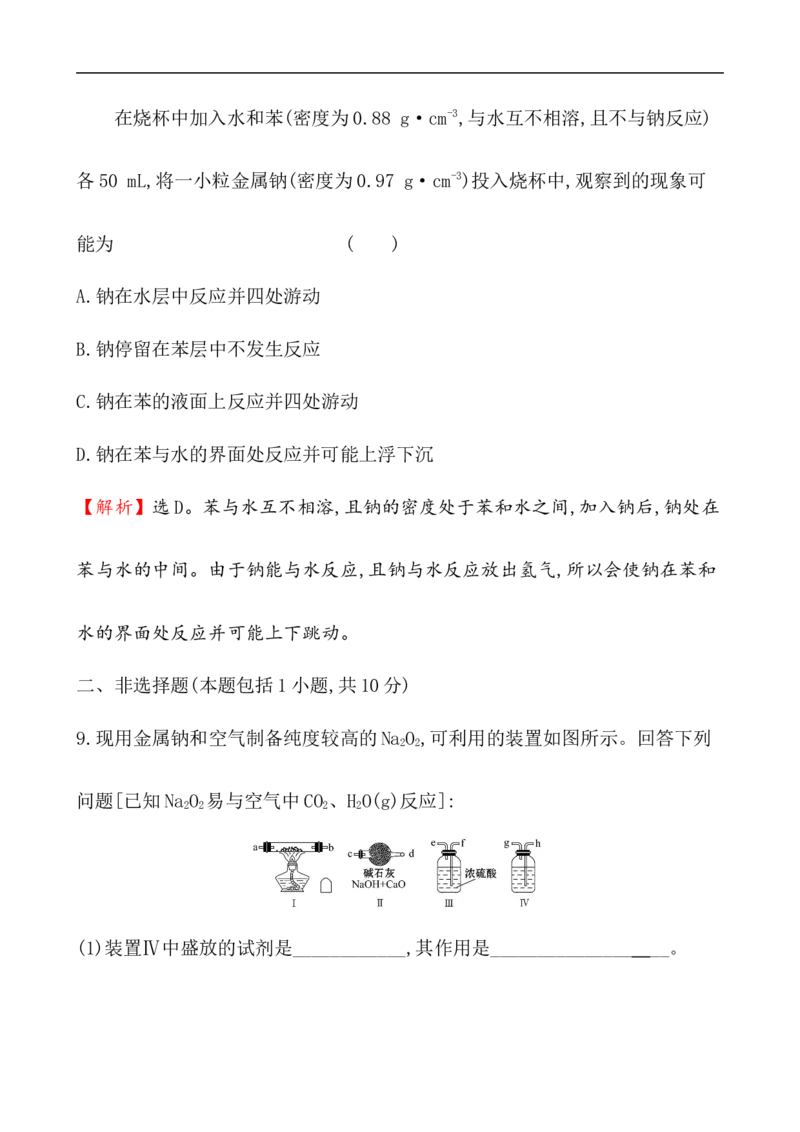
9.现用金属钠和空气制备纯度较高的Na O ,可利用的装置如图所示。回答下列
2 2
问题[已知Na O 易与空气中CO 、H O(g)反应]:
2 2 2 2(1)装置Ⅳ中盛放的试剂是____________,其作用是_______________ __。
(2)若规定气体的气流方向从左到右,则组合实验装置时各件仪器的正确连接顺
序为(按从左到右顺序写明仪器的编号Ⅰ、Ⅱ……)________________,各仪器
接口的标号字母(a、b……)顺序是空气进入________________,
________________接________,________接________,________接________。
(3)装置Ⅱ的作用是_____________________________。
(4)操作中通空气和加热的顺序为________________________________。课时素养评价 八
活泼的金属单质——钠
(30分钟 50分)
1.(2019·聊城高一检测)从生活常识角度考虑,试推断钠元素在自然界中存在
的主要形式是 ( )
A.Na B.NaCl
C.NaOH D.Na O
2
【解析】选B。Na能与空气中的氧气、水反应;NaOH能与空气中的CO 反
2
应;Na O能与空气中的CO 、水反应,所以都不能稳定存在。
2 2
2.(2019·苏州高一检测)金属钠在氧气中燃烧,生成物是 ( )
A.氧化钠 B.过氧化钠
C.氢氧化钠 D.碳酸钠
【解析】选B。金属钠在氧气中燃烧,生成淡黄色的Na O 。
2 2
3.(2019·北京平谷区高一检测)通过观察钠与水(含酚酞)的反应现象,不能得
出的结论是 ( )
A.钠的密度比水小B.钠是活泼金属,与水反应后溶液呈碱性
C.钠有良好的延展性
D.钠的熔点低
【解析】选C。A.钠浮在水面,密度比水小,A正确;B.滴有酚酞的溶液变红色,说
明钠性质活泼与水反应生成碱性物质,B正确;C.依据现象不能得出钠具有良好
的延展性,C错误;D.钠浮在水面,然后熔化成闪亮的小球,说明钠的密度比水小,
与水的反应是放热反应且钠熔点比较低,D正确。
4.(2019·杭州高一检测)某学生将一小块钠投入滴有酚酞的水中,此实验能证
明钠下面4点性质中的 ( )
①钠的密度比水的小
②钠的熔点较低
③钠与水反应时放出热量
④钠与水反应后溶液呈碱性
A.①④ B.①②④
C.①③④ D.①②③④【解析】选D。Na与水反应时,浮在水面上(密度比水小),熔化成闪亮的小球(反
应放热,钠熔点低),在水面四处游动(有气体生成),同时溶液使酚酞变红色(生
成碱性物质),体现了①②③④4点性质。
5.(2019·南开区高一检测)人生是一幅大画布,你应该努力绘出绚丽多彩的画
面。实验现象也是绚丽多彩,让人流连忘返。向硫酸铜溶液中加入一小块金属
钠后,观察到的现象有 ( )
世纪金榜导学号
①钠浮于液面上
②熔化成小球
③发出嘶嘶的响声,放出气体
④钠周围蓝色沉淀部分变黑
⑤有蓝色沉淀产生
⑥析出大量红色的铜
⑦小球在溶液中沉浮
⑧小球在液面上游动,逐渐变小,直至消失
A.①②③⑤⑧ B.①②③④⑤⑧
C.①②③⑤⑥⑧ D.①②③④⑤⑥⑦⑧【解析】选B。将钠块加入CuSO 溶液中时,反应的实质是钠先与水反应生成
4
NaOH和H ,NaOH再与CuSO 反应生成蓝色Cu(OH) 沉淀,反应放出的热量会导致
2 4 2
Cu(OH) 分解生成黑色的CuO,不会置换出单质Cu;因为钠的密度小于水,故反应
2
过程中钠浮于水面而不能在溶液中沉浮,⑥、⑦错误。
6.某同学将金属钠露置于空气中,观察到下列现象:银白色 变灰暗 变白色
出现液滴 白色晶体 白色粉末,根据钠及其化合物的性质分析,下列说法
正确的是 ( )
A.①发生了氧化还原反应
B.①钠表面变灰暗是因为生成了过氧化钠
C.③是碳酸钠吸收空气中的水蒸气形成了溶液
D.④⑤只发生物理变化
【解析】选A。钠露置在空气中由银白色变灰暗,是因为Na与O 反应生成了
2
Na O,Na O与H O反应生成白色固体NaOH,NaOH易潮解,吸收空气中的H O形成
2 2 2 2
NaOH溶液而出现液滴,同时吸收空气中的CO ,生成Na CO ·10H O,Na CO ·10H O
2 2 3 2 2 3 2
逐渐风化最后变为Na CO 固体,其中①发生了氧化还原反应,A项正确;Na只有在
2 3
加热或点燃时才能生成Na O ,B项错误;③是NaOH潮解,C项错误;④⑤中发生
2 2反应有2NaOH+CO Na CO +H O,Na CO +10H O Na CO ·10H O及Na CO ·10H O
2 2 3 2 2 3 2 2 3 2 2 3 2
Na CO +10H O,D项错误。
2 3 2
【补偿训练】
将2.3 g金属钠放入100 g水中,完全反应后溶液的质量分数为 ( )
A. ×100%
B. ×100%
C. ×100%
D. ×100%
【解析】选D。2.3 g Na与100 g水反应生成4 g NaOH和0.1 g H ,故溶液的
2
质量为(100+2.3-0.1) g,质量分数为 ×100%。
【易错警示】本题易忽视生成的氢气的质量。
二、非选择题(本题包括1小题,共10分)
7.某化学实验小组拟用如图装置进行钠与氧气反应的实验。(1)将一小块钠放在石棉网上加热,能观察到的实验现象有
__,
写出发生反应的化学方程式:
__。
(2)上述实验中还观察到有黑色固体物质生成,其原因可能为2Na+CO C+Na O
2 2 2
或4Na+3CO C+2Na CO ,这两个化学方程式的反应类型既属于基本反应类型中
2 2 3
的________反应,也属于________(填“氧化还原”或“非氧化还原”)反应。
【解析】(1)钠受热时燃烧,出现黄色火焰,产生淡黄色粉末过氧化钠,发生的反
应是2Na+O Na O 。(2)根据反应的特点可知,给出的两个反应都是置换反应,
2 2 2
一定是氧化还原反应。
答案:(1)钠受热熔化,然后剧烈燃烧,放热,出现黄色火焰,石棉网上有淡黄色粉
末生成 2Na+O Na O
2 2 2
(2)置换 氧化还原
【补偿训练】某实验小组对中学课本中可生成氢气的反应进行了研究,总结出两个可以
生成H 的反应:①Zn+盐酸,②Na+水。为点燃上述两个反应生成的H ,他们设计
2 2
了图示装置。请回答下列问题:
(1)写出Na与H O反应的化学方程式: _________________________。
2
(2)实验小组在点燃用上述装置制得的H 时,①实验获得成功,②却失败了。他
2
们分析认为失败的原因是Na的用量太少,Na与H O的反应速率太快。于是他们
2
准备增加钠的用量,可老师说太危险,你认为产生危险的原因是______________。
(3)实验小组查阅钠、煤油、水的密度分别为0.97 g·cm-3、0.80 g·cm-3、
1.00 g·cm-3,并据此对实验进行改进。在改进后的实验中H 的生成速率减慢,
2
原因是 __。
【解析】Na与H O反应的产物是NaOH和H ,反应速率很快,并放出大量的热,Na
2 2
的用量多,容易发生爆炸。由于ρ(煤油)<ρ(钠)<ρ(水),故钠块放入后将落在
煤油和水的界面上。钠与水反应,有氢气生成,氢气推动钠块上浮,当氢气逸出后,钠块又下沉到煤油与水的界面上与H O发生反应,重复发生上述现象,减慢了
2
Na与H O反应生成氢气的速率。
2
答案:(1)2Na+2H O 2NaOH+H ↑
2 2
(2)钠与水反应放出大量的热,使试管内H 与O 的混合气体点燃而爆炸
2 2
(3)钠比水轻,比煤油重,落在煤油与水的交界处。钠与H O反应产生的H 使钠浮
2 2
起,脱离水面,反应停止;当钠表面的H 逸出,钠又回落,与水反应,如此反复,减
2
慢了Na与H O的反应速率
2
一、选择题(本题包括1小题,共6分)
8.钠的化学性质非常活泼。下列关于金属钠的叙述错误的是 ( )
A.金属钠可以保存在煤油中
B.钠元素只能以化合态形式存在于自然界中
C.实验室取用金属钠需要镊子、滤纸、小刀3种用品
D.钠元素在自然界中主要以NaCl的形式存在
【解析】选C。实验室取用金属钠时,需要用镊子夹取钠,用滤纸吸干煤油,用小
刀切割,用玻璃皿盛放,所以所需的用品至少有4种,C项错误。
【补偿训练】在烧杯中加入水和苯(密度为0.88 g·cm-3,与水互不相溶,且不与钠反应)
各50 mL,将一小粒金属钠(密度为0.97 g·cm-3)投入烧杯中,观察到的现象可
能为 ( )
A.钠在水层中反应并四处游动
B.钠停留在苯层中不发生反应
C.钠在苯的液面上反应并四处游动
D.钠在苯与水的界面处反应并可能上浮下沉
【解析】选D。苯与水互不相溶,且钠的密度处于苯和水之间,加入钠后,钠处在
苯与水的中间。由于钠能与水反应,且钠与水反应放出氢气,所以会使钠在苯和
水的界面处反应并可能上下跳动。
二、非选择题(本题包括1小题,共10分)
9.现用金属钠和空气制备纯度较高的Na O ,可利用的装置如图所示。回答下列
2 2
问题[已知Na O 易与空气中CO 、H O(g)反应]:
2 2 2 2
(1)装置Ⅳ中盛放的试剂是____________,其作用是_______________ __。(2)若规定气体的气流方向从左到右,则组合实验装置时各件仪器的正确连接顺
序为(按从左到右顺序写明仪器的编号Ⅰ、Ⅱ……)________________,各仪器
接口的标号字母(a、b……)顺序是空气进入________________,
________________接________,________接________,________接________。
(3)装置Ⅱ的作用是_____________________________。
(4)操作中通空气和加热的顺序为________________________________。
【解析】用金属钠和空气制备纯度较高的Na O ,要避免生成的Na O 与空气中的
2 2 2 2
水分和二氧化碳发生反应,在制取过程中要除去这两种杂质,且要防止外界空气
中的水分和二氧化碳倒吸进入装置。
(1)由上述分析可知,应该除去空气中的CO ,故Ⅳ中的试剂为氢氧化钠溶液。
2
(2)由上述分析可知,实验的顺序为除CO →除水蒸气→与钠反应→避免CO 、水
2 2
蒸气进入反应装置,故装置顺序为Ⅳ→Ⅲ→Ⅰ→Ⅱ,接口顺序为hgfeabc或
hgfebac。
(3)装置Ⅱ的作用是避免空气中的CO 、水蒸气进入反应装置Ⅰ。
2
(4)为防止Na O 与CO 、水蒸气反应,应先排尽空气,再加热金属钠。
2 2 2
答案:(1)氢氧化钠溶液 吸收导入空气中的二氧化碳(2)Ⅳ、Ⅲ、Ⅰ、Ⅱ h g f e a(或b) b(或a) c
(3)防止空气中的水分和二氧化碳进入装置Ⅰ
(4)先通一段时间的空气,再加热Ⅰ装置