文档内容
原子结构与元素周期表(2)
重难点 题型 分值
1. 元素周期表的编排及结构
重点 2. 描述元素在周期表中的位置
3. 原子核外电子的排布规律 选择与填空 8-12分
难点 原子核外电子的排布规律
核心知识点一:
一、元素周期表
1. 元素周期表的发展历程
1869年,俄国化学家门捷列夫制出第一张元素周期表,将元素按照相对分子质量由小
到大依次排列,并将化学性质相似的元素放在一个纵列。
2. 元素周期表的编排原则
第1页3. 元素周期表的结构
注意:①元素所在周期序数=原子的电子层数;所在主族序数=原子的最外层电子数
②元素周期表中从第Ⅲ族到第Ⅱ族,其中包括了第Ⅷ族,共10个纵列,全部是金属元
素,统称为过渡元素。
③为了使元素周期表的结构美观,分别将第六、七周期的各15种元素统称为镧系元素
(57-71号)、锕系元素(89-103号),镧系元素和锕系元素各占一格,并在元素周期表
的下方单独列出。
④常见族的别称
族 别名
第ⅠA族(除氢
碱金属元素
外)
第ⅦA 卤族元素
0族 稀有气体元素
4.元素周期表中各方格内的信息
核心知识点二:
一、原子核外电子排布规律的应用
1. 推断元素的性质
元素 最 外 层 电 得失电子能力 化学性质 主要化合价
第2页子数
较稳定,一般
稀有气体 8 ( He 为 一般不易得失
不参与化学反 -
元素 2) 电子
应
金属元素 <4 易失电子 金属性 只有正价,一般是+1→+3
非金属元
≥4 易得电子 非金属性 既有正价又有负价
素
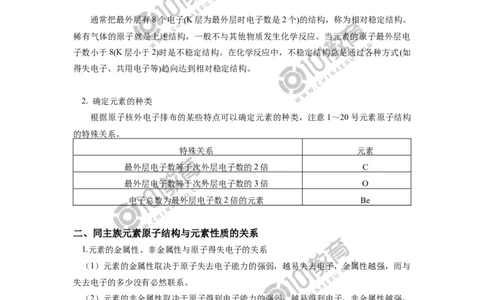
通常把最外层有8个电子K层为最外层时电子数是2个的结构,称为相对稳定结构。
稀有气体的原子就是上述结构,一般不与其他物质发生化学反应。当元素的原子最外层电
子数小于8K层小于2时是不稳定结构。在化学反应中,不稳定结构总是通过各种方式如
得失电子、共用电子等趋向达到相对稳定结构。
2. 确定元素的种类
根据原子核外电子排布的某些特点可以确定元素的种类,注意1~20号元素原子结构
的特殊关系。
特殊关系 元素
最外层电子数等于次外层电子数的2倍 C
最外层电子数等于次外层电子数的3倍 O
电子总数为最外层电子数2倍的元素 Be
二、同主族元素原子结构与元素性质的关系
1.元素的金属性、非金属性与原子得失电子的关系
(1)元素的金属性取决于原子失去电子能力的强弱,越易失去电子,金属性越强,而与
失去电子的多少没有必然联系。
(2)元素的非金属性取决于原子得到电子能力的强弱,越易得到电子,非金属性越强,
而与得到电子的多少没有必然联系。
(3)同主族元素从上到下,原子半径逐渐增大,失电子能力逐渐增强,而得电子能力逐
渐减弱,故金属性逐渐增强,非金属性逐渐减弱
2.元素金属性、非金属性强弱的判断方法
(1)元素金属性强弱的判断方法
依据 方法
根据与水(或酸)反应置换出氢气的难易程度 越易者金属性越强
第3页根据最高价氧化物对应水化物的碱性强弱 碱性越强者金属性越强
根据金属单质之间的置换反应 活动性强的能够置换出活动性弱的
(2)元素的非金属性强弱的判断方法
依据 方法
越易与氢气化合,氢化物越稳定者
根据与氢气化合的难易程度或生成氢化物的稳定性 非金属性越强
根据最高价氧化物对应水化物的碱性强弱
酸性越强者非金属性越强
非金属性强的能够置换出非金属性
根据非金属单质之间的置换反应
弱的
核心知识点一:
1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在
联系,成为化学史上的重要里程碑之一。下列有关元素周期表的说法正确的是( )
A. 元素周期表含元素最多的族是第ⅢB族
B. 元素周期表有18个族
C. 第ⅠA族的元素全部是金属元素
D. 短周期是指第一、二、三、四周期
【答案】A
【解析】第ⅢB族中包含锕系与镧系元素,共有32种元素,A项正确;元素周期表中
共有18个纵列,16个族,B项错误;第ⅠA族中H为非金属元素,C项错误;短周期包括
第一、二、三周期,D项错误。
【考点】元素周期表的结构
已知X、Y、Z三种主族元素在周期表中的位置如图所示,设X的原子序数为a。则下
第4页列说法不正确的是( )
Y
X
Z
A. Y与Z的原子序数之和可能为2a
B. Y的原子序数可能为a-17
C. Z的原子序数可能为a+31
D. X、Y、Z一定为短周期元素
【答案】D
【解析】X、Y、Z为主族元素,Y一定不在第一周期,则X、Y、Z均可能为长周期
元素,D项错误;若X、Y、Z分别位于第三、四、五周期的右边,则Y的原子序数为a-
17;Y与Z的原子序数之和可能为2a;若X、Y、Z分别位于第四、五、六周期的右边,Z
的原子序数可能为a+31。
【考点】元素周期表和原子序数的位置关系
核心知识点二:
A、B两种原子,A的M电子层比B的M电子层少3个电子,B的L电子层电子数恰
为A的L电子层电子数的2倍。A和B分别是( )
A. 硅原子和钠原子 B. 硼原子和氦原子
C. 氯原子和碳原子 D. 碳原子和铝原子
【答案】D
【解析】A的M电子层比B的M电子层少3个电子,B的L电子层电子数恰为A的L
电子层电子数的2倍,说明A、B为第二、第三周期元素;L电子层最多排8个电子,B的
L电子层电子数恰为A的L电子层电子数的2倍,说明B的L电子层有8个电子,A的L
电子层有4个电子,故A是碳原子;A的M电子层比B的M电子层少3个电子,故B为铝
原子。
【考点】元素金属性和非金属性强弱的判断方法
下列不能说明氯元素的非金属性比硫元素强的事实是( )
①HCl比HS稳定
2
②HClO氧化性比HSO 强
2 4
第5页③ HClO 酸性比HSO 强
4 2 4
④Cl 能与HS反应生成S
2 2
⑤氯原子最外层有7个电子,硫原子最外层有6个电子
A. ② ⑤ B. ① ② C. ① ② ④ D. ① ③ ⑤
【答案】A
【解析】元素的氢化物越稳定,最高价氧化物对应水化物的酸性越强,其非金属性越
强。
【考点】原子结构与元素之间的关系①③能够说明;含氧酸的氧化性不能作为判断元
素非金属性强弱的依据,②不能够说明;非金属单质间的置换反应Cl+HS=2HCl+S↓,说
2 2
明氯的非金属性比硫强,④能够说明;最外层电子数多,元素的非金属性不一定强,如非
金属性O﹥Cl,但最外层电子数:O﹤Cl,⑤不能够说明
(答题时间:25分钟)
选择题:本题包括12小题,每小题4分,共48分。
1. 下列说法正确的是( )
A. 常用元素周期表中元素排序的依据是原子的核电荷数
B. 元素周期表有十六个纵列,也就是十六个族
C. 原子的最外层电子数相同的元素,一定属于同一族
D. 电子层数相同的粒子,对应元素一定属于同一周期
2. 下列各图若为元素周期表的一部分(表中数字代表原子序数),其中合理的是 (
)
A B C D
3. 俄罗斯科学家用含20个质子的钙的一种原子轰击含95个质子的镅原子,结果4次成
功合成4个第115号元素的原子。这4个原子生成数微秒后衰变成第113号元素。下列有关
叙述正确的是( )
A. 115号元素在第六周期
B. 113号元素在第七周期ⅢA族
C. 115号和113号元素都是非金属元素
D. 镅元素和115号元素不在同一周期
第6页4. 核电荷数小于或等于18的元素中,原子的最外层电子数是其余电子总数一半的元素
种类有( )
A. 1种 B. 2种
C. 3种 D. 4种
5. 下图微粒的结构示意图,正确的是( )
6. (1)某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该
元素的原子结构示意图是________。
(2)已知某粒子的结构示意图为 ,试回答:
①当x-y=10时,该粒子为________(填“原子”“阳离子”或“阴离子”)。
②当y=8时,粒子可能为(填名称)________、________、________、________、
________。
第7页1. 【答案】A
【解析】元素周期表中有18个纵列,16个族,第Ⅷ族占三个纵列;Be和He的最外层
电子数都是2,但不属于同一族;Ne和Na+的电子层数都是2,但不属于同一周期。
2. 【答案】D
【解析】本题要求熟记周期表的结构,知道1~18号元素在周期表中的具体位置。解
题时可根据稀有气体2号、10号元素应在周期表的最右端和3号元素在周期表的最左端排
除A、B、C三项。
3. 【答案】B
【解析】95号元素镅、115号元素、113号元素,原子序数都大于86而小于118,所
以都在第七周期;115号比118号原子序数少3,应在第ⅤA族,113号元素在第ⅢA族;
113号元素和115号元素都是金属元素。
4. 【答案】B
【解析】在1号~18号元素中,符合题给要求的元素是Li和P。
5. 【答案】A
【解析】B 中微粒结构示意图是 Cl-而不是 Cl,C 中 Ar 的原子结构示意图应为
,D中K的原子结构示意图应为 。
6. 【答案】(1) (2)①原子 ②氩原子 氯离子 硫离子 钾离子 钙
离子
【解析】(1)设:核电荷数=质子数=a,元素原子的电子层数为x,最外层电子数
为y,依题意:a=5x,a=3y,则5x=3y,x=3y/5。因原子的最外层电子数不超过8,即y
为1~8的正整数,故仅当y=5,x=3合理,该元素的核电荷数为15。
(2)①当x-y=10时,x=10+y,说明核电荷数等于核外电子数,所以该粒子应为
原子;
②当y=8时,应有18个电子的粒子,所以可能为氩原子、氯离子、硫离子、钾离子、
钙离子。
第8页