文档内容
上学期期末试卷
(答题时间:90分钟满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 S 32 Cl 35. 5 Cu
64
一、选择题(本题包括20个小题,1-15题每小题2分,16-20每小题3分,共45分。在每
小题给出的四个选项中,只有一项是符合题目要求的。)
1. 焰火“脚印””“笑脸”“五环”,让北京奥运会开幕式更加辉煌、浪漫,这与高中
化学中“焰色试验”知识相关。下列说法中正确的是( )
A. 焰色试验是化学变化
B. 用稀盐酸清洗做焰色试验的铂丝(镍丝或铁丝)
C. 焰色试验均应透过蓝色钴玻璃观察
D. 利用焰色试验可区分NaCl与NaCO 固体
2 3
2. 下列化学反应中水作氧化剂的是
A. Cl +H O=HCl+HClO B. 2F+2H O=4HF+O
2 2 2 2 2
C. 2Na+2H O=2NaOH+H ↑ D. CaO+H O=Ca(OH)
2 2 2 2
3. 下列关于胶体的说法,正确的是
A. 向稀的NaOH溶液中逐滴加入5~6滴FeCl 饱和溶液,即可制得Fe(OH) 胶体
3 3
B. 胶体的分散质能通过滤纸孔隙,而浊液的分散质则不能
C. 丁达尔效应是胶体不同于溶液的本质区别
D. Fe(OH);胶体的电泳实验说明了Fe(OH) 胶体带电
3 3
4. 下列说法不正确的是( )
A. 纯碱和烧碱熔化时克服的化学键类型相同
B. 加热蒸发氯化钾水溶液的过程中有分子间作用力被破坏
C. H和F、O、N形成的共价键称为氢键
D. 钠与氧气反应的过程中,存在离子键的形成
5. 下列有关气体体积的叙述中,正确的是( )
A. 一定温度和压强下,各种气态物质的体积大小,由构成气体的分子大小决定
B. 一定温度和压强下,各种气态物质的体积大小由构成气体的分子数决定
C. 不同的气体,若体积不同,则它们所含的分子数也不同
D. 气体摩尔体积指1mol任何气体所占的体积约为22. 4L
6. 新制氯水中存在多种分子和离子,可通过实验的方法加以确定。下列有关新制氯水中
存在的粒子的说法错误的是( )
A. 加入含有硫酸氢钠的红色石蕊溶液红色褪去,说明有Cl 存在
2
B. 加入有色布条,有色布条褪色,说明有HClO存在
第1页C. 新制氯水呈浅黄绿色,且有刺激性气味,说明有Cl 存在
2
D. 加入硝酸酸化的硝酸银溶液产生白色沉淀,说明有Cl-存在
7. 用N 表示阿伏伽德罗常数的值,下列说法正确的是
A
A. 28g氮气含有的原子数是N
A
B. 标准状况下,22. 4L水的分子数是N
A
C. 2L0. 5mol/L的稀硫酸中含有HSO 分子数是N
2 4 A
D. 钠与水反应,生成2gH,则转移的电子数是2N
2 A
8. 下列反应的离子方程式书写正确的是( )
A. 稀硫酸滴在铜片上:Cu+2H+===Cu2++H↑
2
B. 稀硫酸与氢氧化钡溶液混合:SO 2-+Ba2+===BaSO ↓
4 4
C. 稀硝酸滴在大理石上:CaCO +2H+===Ca2++HCO
3 2 3
D. 氧化铁与稀盐酸混合:Fe O+6H+===2Fe3++3HO
2 3 2
9. 能在下列溶液中大量共存的离子组是
A. 含有大量Al3+的溶液:Na+、SO 2-、Cl-
4
B. 能使酚酞变红的溶液:Na+、Ca2+、CO2-
3
C. 含有大量Fe3+的溶液:OH-、Mg2+、Cl-
D. 含有大量HCO -的溶液:H+、SO 2-、Cl-
3 4
10. 短周期元素X、Y、Z所在的周期数依次增大,它们的原子序数之和为20,且Y2-与
Z+核外电子层的结构相同。下列化合物中同时存在极性键和非极性键的是( )
A. Z Y B. XY
2 2 2
C. Z Y D. ZYX
2 2
11. 下列实验操作能够制取Fe(OH) 并能较长时间观察到白色沉淀的是( )
2
12. 下列叙述不正确的是( )
选项 被提纯物质 杂质 除杂试剂或方法
A FeCl 溶液 FeCl 通入适量Cl
3 2 2
B FeCl 溶液 FeCl 加入过量铁粉并过滤
2 3
C 铜粉 铁粉 加入过量盐酸并过滤
D Fe(OH) Fe(OH) 在空气中灼烧
3 2
13. 现有下列几个离子反应:
2−
①Cr O7 +14H++6Cl-===2Cr3++3Cl↑+7HO
2 2 2
第2页②2Fe2++Br ===2Fe3++2Br-
2
2−
③2Fe3++SO +2HO===2Fe2++SO4 +4H+
2 2
下列有关性质的比较正确的是( )
2− 2−
A. 氧化性:Cr O7 >Cl>Fe3+ B. 氧化性:Cl>Br >Cr O7
2 2 2 2 2
C. 还原性:SO Cr3+>Fe2+
2
14. 将铁粉、铜粉、FeCl 溶液和CuCl 溶液混合在试管中充分反应,若过滤后滤渣能被
3 2
磁铁吸引,则下列有关叙述正确的是( )
A. 溶液中肯定不存在的离子只有Cu2+
B. Fe3+和Cu2+均完全被铁粉还原
C. 滤液中滴加KSCN溶液显红色
D. 滤渣中肯定不含有铜
15. 如图模拟“侯氏制碱法”制取NaHCO 的部分装置。下列操作正确的是( )
3
A. a先通入CO,然后b通入NH ,c中放碱石灰
2 3
B. b先通入NH ,然后a通入CO,c中放碱石灰
3 2
C. a先通入NH ,然后b通入CO,c中放蘸有稀硫酸的脱脂棉
3 2
D. b先通入CO,然后a通入NH ,c中放蘸有稀硫酸的脱脂棉
2 3
16. X、Y、Z、M、W为五种短周期元素。X原子的质子数与电子层数相同,W原子核
外电子数是M原子最外层电子数的2倍,Y、Z、M、W在周期表中的相对位置如图所示。
下列说法不正确的是( )
Y Z M
W
A. 原子半径:W>Y>Z>M>X
B. 热稳定性:XM>X Z;沸点:XZ>YX
2 2 3
C. 仅由X、Y、Z三种元素形成的化合物中不可能含离子键
D. YM 、WM 分子中每个原子最外层均达到8电子稳定结构
3 4
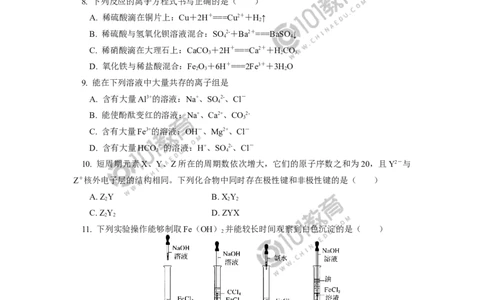
17. 利用下列装置可以制备无水氯化铁。下列有关说法正确的是( )
第3页A. 烧瓶B中制备氯气的反应物为二氧化锰和稀盐酸
B. 装置C、D中分别盛有浓硫酸、饱和食盐水
C. 装置E和装置F之间需要增加一个干燥装置,才能制得无水氯化铁
D. 装置F的作用是检验有无氯气逸出
18. 有下列结论:①微粒半径:S2->Cl>S>F;②氢化物的稳定性:HF>HCl>HS>
2
HSe;③离子的还原性:S2->Cl->Br->I-;④氧化性:Cl >S>Se>Te;⑤酸性:
2 2
HSO >HClO>HSeO;⑥非金属性:F>Cl>S>Se。其中正确的是( )
2 4 4 2 4
A. ②④⑥ B. ①③④
C. ①②⑤ D. ③⑤⑥
19. 废水脱氮工艺中有一种方法是在废水中加入过量NaClO使NH +完全转化为N,该反
4 2
应可表示为2NH + + 3C1O- = N ↑+3Cl-+2H+ + 3H O。下列说法中,不正确的是( )
4 2 2
A. 还原性NH +> Cl-
4
B. 经此法处理过的废水可以直接排放
C. 反应中氮元素被氧化,氯元素被还原
D. 反应中每生成1mol N,转移6mol电子
2
20. NaC1是一种化工原料,可以制备一系列物质(如图所示)。下列说法正确的是(
)
A. 25℃时,NaHCO 在水中的溶解度比NaCO 的大
3 2 3
B. 石灰乳与Cl 的反应中,Cl 既是氧化剂,又是还原剂
2 2
第4页C. 常温下,干燥的C1 能用钢瓶贮存,所以Cl 不与铁反应
2 2
D. 如图所示的转化反应都是氧化还原反应
二、非选择题(本题包括5个大题,共55分)
21.(11分) 已知A为常见的金属单质,根据如下所示的转化关系回答下列问题:
(1)写出下列物质的化学式:
A____________,B__________,C___________,D____________,E__________。
(2)反应③的离子方程式为_______________________________;
反应④的离子方程式为____________________________________;
反应⑦的化学方程式为_______________________________。
22.(9分)常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E
都含X元素,其转化关系如图所示:
(1)请分别写出下列物质的化学式(如为溶液请填溶质的化学式):
A________、B________、D________。
(2)写出下列反应的化学方程式或离子方程式(请注明反应条件):
A+HO(离子方程式):___________________________________;
2
A+NaOH(离子方程式):__________________________________;
D―→A(化学方程式):____________________________________。
23.(13分)下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化
学式回答下列问题:
第5页(1)表中元素,化学性质最不活泼的是________,只有负价而无正价的元素是
________。
(2)C元素在元素周期表中的位置是第三周期第________族。
(3)最高价氧化物的水化物酸性最强的是________,呈两性的是________。
( 4 ) A 分 别 与 E 、 G 、 H 形 成 的 化 合 物 中 , 最 稳 定 的 是
_____________________________。
(5)在B、C、E、F中,原子半径最大的是________。
(6)B、H两种元素所形成的化合物所含的化学键类型为________________。
(7)写出C的最高价氧化物与H的氢化物之间反应的离子方程式:_______________。
(8)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:
______________________________。
24.(10分)实验室有化学纯的浓硫酸,其试剂瓶标签上的部分内容如下图:
硫酸 化学纯(CP)
(500 mL)
品名:硫酸
化学式:HSO
2 4
相对分子质量:98
密度:1. 84 g·cm-3
质量分数:98%
请回答下列问题:
(1)配制溶液时,一般可以分为以下几个主要步骤:
①量取 ②计算 ③溶解 ④定容 ⑤转移 ⑥洗涤 ⑦装瓶,其正确的操作顺序为
________(填序号)。
(2)实验室只有 100mL、250mL、500mL三种规格的容量瓶,但要配制 480mL0.
50mol·L-1的稀硫酸,需取该浓硫酸________mL。
(3)接下来完成此实验将用到的仪器有20mL量筒、烧杯、玻璃棒、________。
(4)要从所配溶液中取出50mL盛装于试剂瓶中,给它贴上标签,则标签的内容是
__________________________;若再从中取出10mL溶液稀释至20mL,则稀释后溶液的物
质的量浓度为________。
(5)下列操作会使所配溶液浓度偏低的是____(填字母)。
A. 用量筒量取浓硫酸,读数时仰视刻度线
B. 转移溶液时未洗涤烧杯
C. 容量瓶用蒸馏水洗净后仍残留有蒸馏水
D. 定容时俯视容量瓶的刻度线
E. 定容摇匀后,发现液面低于刻度线,再加水至刻度线
25. (12分)某研究小组为探究元素周期表中元素性质的递变规律,设计了如下实验;
第6页I. (1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结
果:_________(填物质名称)与盐酸反应最剧烈。
(2)向NaS溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离
2
子方程式为____________________________________。
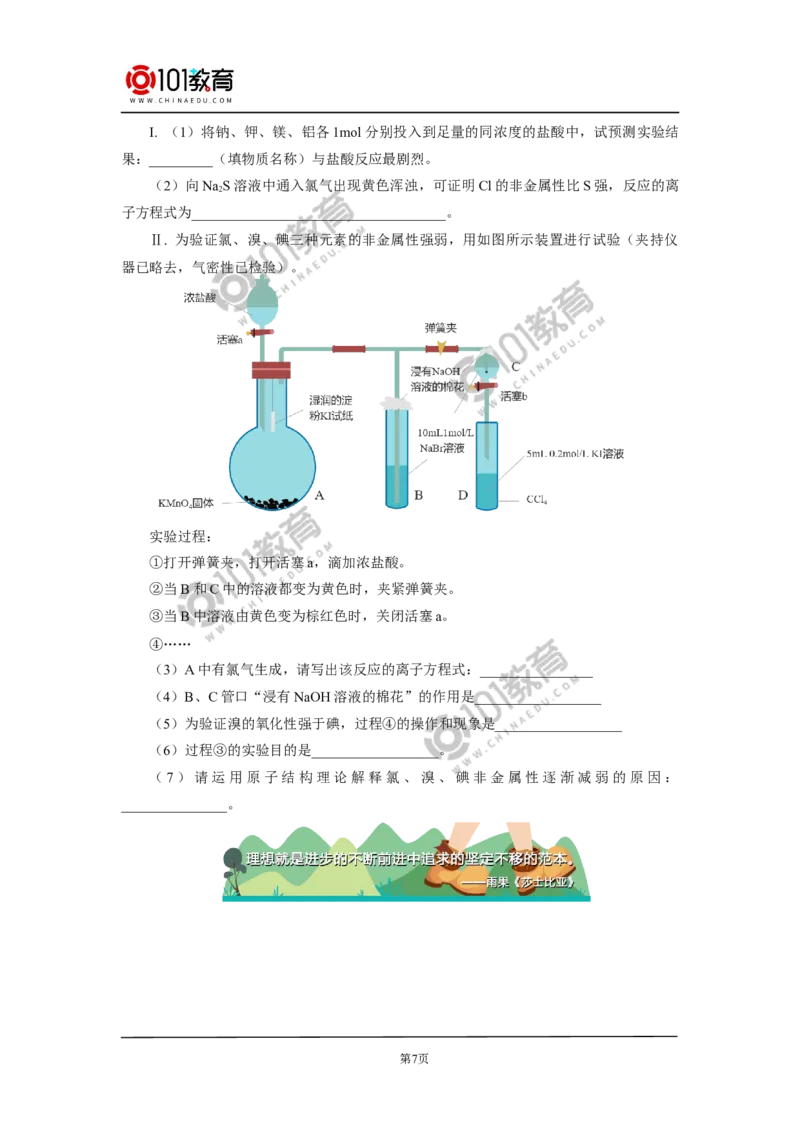
Ⅱ. 为验证氯、溴、碘三种元素的非金属性强弱,用如图所示装置进行试验(夹持仪
器已略去,气密性已检验)。
实验过程:
①打开弹簧夹,打开活塞a,滴加浓盐酸。
②当B和C中的溶液都变为黄色时,夹紧弹簧夹。
③当B中溶液由黄色变为棕红色时,关闭活塞a。
④……
(3)A中有氯气生成,请写出该反应的离子方程式:________________
(4)B、C管口“浸有NaOH溶液的棉花”的作用是__________________
(5)为验证溴的氧化性强于碘,过程④的操作和现象是__________________
(6)过程③的实验目的是__________________。
(7)请运用原子结构理论解释氯、溴、碘非金属性逐渐减弱的原因:
_______________。
第7页上学期期末试卷参考答案
1. B 【解析】焰色试验是物理变化,不是化学变化,A错误;盐酸可以溶解杂质,且易
挥发,不会残留痕迹,B正确;K的焰色试验需透过蓝色的钴玻璃观察,避免钠的焰色对
钾的焰色的干扰,其他元素不需要透过蓝色钴玻璃观察,C错误;焰色试验是金属元素的
性质,NaCl与NaCO 固体的焰色都为黄色,无法利用焰色试验来区分,D错误。
2 3
【考点】焰色反应
2. C 【解析】氯气和水的反应中氯气既做氧化剂又做还原剂,A错误;氟和水反应水做
还原剂,B错误;钠和水的反应中水做氧化剂,C正确;D为非氧化还原反应反应。
考点:氧化还原反应
3. B 【解析】A项,把饱和的三氯化铁溶液滴加到沸水中,继续加热至溶液呈现红褐
色停止加热,即得到Fe(OH) 胶体,NaOH溶液中逐滴加入少量饱和FeCl 溶液得到的是
3 3
氯氧化铁沉淀,故A错误;B项、胶体微粒直径小于100mm,能通过滤纸,浊液中分散质
粒子直径大于100mm能通过滤纸,故B正确;C项、胶体区别于其它分散系的本质是胶体
分散质微粒直径的大小,不是有丁达尔效应,故C错误;D项、氢氧化铁胶体微粒带正电,
Fe(OH) 胶体的电泳实验说明了Fe(OH) 胶粒带电,故D错误。故选B。
3 3
【考点】胶体的制备及其性质
4. C 【解析】纯碱(NaCO )和烧碱(NaOH)都是离子化合物,熔化时都需要克服离
2 3
子键,则纯碱和烧碱熔化时克服的化学键类型相同,故A正确;水分子间存在分子间作用
力,加热蒸发氯化钾水溶液的过程中水由液态变为气态,有分子间作用力被破坏,故 B正
确;H与F、O. N等原子间以一种特殊的分子间作用力结合的键,称为氢键,氢键不属于
共价键,故C错误;Na与O 反应生成NaO或NaO,存在离子键的形成,故D正确。
2 2 2 2
【考点】化学键
5. B 【解析】对于气体物质,在一定温度和压强下,分子间的距离远大于分子本身的
大小,因此其体积的大小主要由分子数的多少来决定,故A错误,B正确;气体的体积随
温度和压强的变化而变化,体积不同的气体,在不同的条件下,其分子数可能相同,也可
能不同,C错误;气体摩尔体积会随着温度、压强的变化而变化,22. 4L·mol-1是标准状况
下的气体摩尔体积,故D错误。
【考点】阿伏伽德罗定律
6. A 【解析】氯气与水反应生成盐酸(强酸)和次氯酸(弱酸),反应后的溶液中含
有氯气分子(新制氯水为浅黄绿色)、次氯酸分子(使石蕊溶液褪色,具有漂白性)、氢
离子、氯离子(与硝酸银溶液产生白色沉淀)、次氯酸根离子等粒子。
【考点】氯水的性质
7. D 【解析】28g氮气含有的原子数是2N ,A错误;标准状况下水不是气体,B错误;
A
第8页硫酸在水溶液中会完全电离成氢离子和硫酸根离子,不存在硫酸分子,C错误
【考点】阿伏伽德罗常数
8. D 【解析】选项A中铜与稀硫酸不反应;选项B中H+与OH-参加反应生成水;选
项C中反应生成的碳酸不稳定,可分解成二氧化碳和水。
【考点】离子反应方程式
9. 【解析】A 在B中Ca2+与CO2-不共存,C是含有Fe3+的溶液,所以是酸性溶液里面
3
含有大量氢离子,因此和氢氧根离子不共存,D中HCO -与H+不共存
3
【考点】离子共存
10. B 【解析】由题中信息可知X、Y、Z分别为第一、二、三周期元素,结合Y2-与Z
+核外电子层结构相同可知Y、Z分别为O、Na,再结合X、Y、Z的原子序数之和为20可
知X为H。A项,NaO中只含离子键;B项,HO 中O—H键是极性键;O—O键是非极
2 2 2
2−
性键;C项,NaO 中存在非极性键(O—O键)和离子键(Na+与O 之间);D项,
2 2
NaOH中存在离子键(Na+与OH-之间)和极性键(O—H键)。
【解析】化学键的认识
11. D 【解析】B项中CCl 密度大,应在下层,不能长时间观察到白色沉淀;D项中的
4
操作可防止氧气氧化Fe(OH),能较长时间观察到白色沉淀。
2
【考点】氢氧化亚铁的性质
12. D 【解析】FeCl 与Cl 反应生成FeCl ,FeCl 与Fe粉反应生成FeCl ,A、B都正确
2 2 3 3 2
Fe(OH)、Fe(OH) 受热都易分解,D错误。
3 2
【考点】实验除杂类问题
13. A 【解析】根据氧化剂的氧化性大于氧化产物的氧化性,还原剂的还原性大于还原
产物的还原性,并结合卤素单质及阴离子的性质递变规律可推知,氧化性强弱顺序为Cr O
2
2− 2−
7 >Cl>Br >Fe3+>SO4 ;还原性强弱顺序为SO >Fe2+>Br->Cl->Cr3+。
2 2 2
【考点】氧化还原反应的规律
14. B 【解析】若过滤后滤渣能被磁铁吸引,说明固体含有铁,溶液中的Fe3+、Cu2+全
部 参 加 反 应 生 成 Fe2+ 和 Cu , 反 应 的 反 应 方 程 式 为 : 2FeCl +Fe=3FeCl 、
3 2
CuCl +Fe=Cu+FeCl ,所以溶液中一定没有Fe3+、Cu2+,一定含有Fe2+,所以B选项是正确
2 2
的。
【考点】金属及其化合物性质
15. C 【解析】NH 的溶解度较大,为防止倒吸,b管通CO ,a管通NH ,要在食盐水
3 2 3
中先通NH 然后再通CO ,否则CO 通入后会从水中逸出,得到的产品也很少;尾气主要
3 2 2
是CO 和NH ,其中NH 对环境影响较大,要吸收,而NH 是碱性气体,所以在c装置中
2 3 3 3
要装酸性物质,据此可知A、B项错误,C项正确,D项错误。
【考点】侯氏制碱法
第9页16. C 【解析】X、Y、Z、M、W为五种短周期元素,由元素在周期表中的相对位置可
知,Y、Z、M处于第二周期,而W处于第三周期,W原子核外电子数是M原子最外层电
子数的2倍,设W最外层电子数为x,则2+8+x=2(x+3),解得x=4,则W为Si,Y为N,
Z为O,M为F。X的质子数与电子层数相同,则X为H。同周期从左到右原子半径逐渐减
小,同主族自上而下原子半径逐渐增大,五种元素中 H 原子半径最小,故原子半径
Si>N>O>F>H,故A正确;XM为HF,XZ为HO,非金属性F>O,故氢化物热稳定性
2 2
HF>H O,YX 为NH ,常温下水为液态,而NH 为气态,故沸点HO>NH ,故B正确;H、
2 3 3 3 2 3
N、O三种元素形成的化合物可以是NH NO ,NH NO 中既有离子键又有共价键,故C错
4 3 4 3
误;YM 为NF ,WM 为SiF ,分子中N、Si、F原子最外层均达到8电子稳定结构,故D
3 3 4 4
正确。
【考点】元素周期规律
17. C 【解析】干燥装置应在除杂装置后,装置C、D中分别盛有饱和食盐水、浓硫酸;
装置F中挥发出的水蒸气易逆行进入装置E,需在装置E、F之间增加干燥装置;装置F是
尾气吸收装置。
【考点】氯化铁的制备
18. A 【解析】微粒半径:S2->S>Cl>F,①错误;得电子能力:F>Cl>S>Se,②、
⑥正确;元素的非金属性:Cl>Br>I>S,则离子的还原性:S2->I->Br->Cl-,③错误;
由非金属性:Cl>S>Se>Te,故单质的氧化性:Cl >S>Se>Te,得电子能力:Cl>S>
2
Se,则酸性:HClO>HSO >HSeO,④正确,⑤错误。
4 2 4 2 4
【考点】元素周期规律的应用
19. B 【解析】标出反应前后元素的化合价,N元素化合价由-3升高到0,NH +才是还
4
原剂;Cl元素化合价从+l降低到-1,ClO-是氧化剂。根据同一氧化还原反应中,还原剂的
还原性强于还原产物的还原性可知,还原性NH +>Cl-,A说法正确;经过此法处理过的溶
4
液呈强酸性,不能直接排放,B说法错误;根据以上分析知,反应中N元素被氧化,Cl元
素被还原,C说法正确;根据化合价变化情况可判断,D说法正确。
【考点】氧化还原反应的规律
20. B 【解析】相同温度下,NaCO 的溶解度大于NaHCO 的,A项错误;石灰乳与
2 3 3
Cl 的反应方程式为2C1 +2Ca(OH) =CaCl +Ca(ClO) +2H O,从化合价变化的角度判
2 2 2 2 2 2
断,氧化剂、还原剂都是C1 ,B项正确;在加热条件下,Fe与Cl 反应生成FeCl ,C项
2 2 3
错误;NaCl与NH 、CO 、HO反应生成NaHCO ,NaHCO 受热分解转化为NaCO 的过
3 2 2 3 3 2 3
程发生的都是非氧化还原反应,D项错误。
【考点】元素及其化合物的性质
21.【答案】(1)Fe FeCl FeCl Fe(OH) Fe(OH)
2 3 2 3
(2)2Fe2++Cl===2Fe3++2Cl-(其他合理答案也可) 2Fe3++Fe===3Fe2+(其他合
2
第10页理答案也可)
4Fe(OH)+O+2HO===4Fe(OH)
2 2 2 3
【解析】
【考点】铁及其化合物的转化
22.【答案】(1)Cl HClO HCl
2
(2)Cl+HO===H++Cl-+HClO
2 2
Cl+2OH-===Cl-+ClO-+HO
2 2
4HCl(浓)+MnO =====MnCl +Cl↑+2HO
2 2 2 2
【解析】由题意可知A为氯气,B为次氯酸,D为氯化氢,C为氯化钠,E为次氯酸钠。
【考点】氯及其化合物之间的转化
23.【答案】(1)Ar F (2)ⅢA (3)HClO Al(OH)
4 3
(4)HF (5)Na (6)离子键
(7)Al O+6H+===2Al3++3HO
2 3 2
(8)Al(OH)+NaOH===NaAlO +2HO
3 2 2
【解析】依据元素周期表A~J分别为H、Na、Al、C、N、P、F、Cl、Ar、Si。
【考点】元素周期表的性质
24. 【答案】(1)②①③⑤⑥④⑦ (2)13. 6 (3)500mL 容量瓶、胶头滴管
(4) 0. 50mol·L-1HSO (aq) 0. 25mol·L-1 (5)BE
2 4
【解析】(2)实验室没有480mL的容量瓶,因此需要用500mL的容量瓶来配制。利
1000ρω
M
用图中数据可求出浓硫酸的物质的量浓度c = =18. 4mol·L-1。依据稀释前后硫
2
酸的物质的量不变,即cV=cV,可解得V≈13. 6mL。
1 1 2 2 2
(4)从所配溶液中取出50mL溶液,标签应写上溶液名称和物质的量浓度;cV =
1 1
cV,将c=0. 50mol·L-1,V=0. 01L,V=0. 02L代入可求得c=0. 25mol·L-1。
2 2 1 1 2 2
(5)A项,用量筒量取浓硫酸,读数时仰视刻度线导致量取的浓硫酸物质的量偏大,
所配溶液的浓度偏高;B项,转移溶液时未洗涤烧杯,烧杯中有残余的硫酸,导致所配溶
液浓度偏低;C项,容量瓶用蒸馏水洗净后仍残留有蒸馏水,对溶液所配浓度没有影响;
D项,定容时俯视容量瓶的刻度线,导致所配溶液体积偏小,浓度偏高;E项,定容摇匀
后,发现液面低于刻度线,再加水至刻度线,导致所配溶液体积偏大,浓度偏低。会使所
配溶液浓度偏低的是BE。
第11页【考点】一定物质的量浓度溶液的配置
25.【答案】Ⅰ.(1)钾 (2)S2- + Cl = S↓ + 2Cl-
2
Ⅱ.(3)2MnO - + 16H+ +10Cl- =2Mn2++5Cl↑+8H O(4)吸收氯气,防止污染环境
4 2 2
(5)打开活塞b,将少量C中溶液滴入D中,关闭活赛b,取下D,振高、静置后CCl 层
4
溶液变为紫红色(6)确认C的黄色溶液中无Cl ,排除C1 对验证溴的氧化性强于碘的实
2 2
验的干扰(7)同主族元素从上到下,原子半径逐渐增大,得电子能力逐渐减弱
【解析】1. (1)金属活波性顺序为钾>钠>镁>铝,所以相同条件下与盐酸反应最剧烈
的是钾,反应速率最慢的是铝。(2)氯气的氧化性孩于硫单质,所以氯气能够与硫离子反
应生成硫单质,反应的离子方程式为S2- + Cl = S↓ + 2Cl-。Ⅱ. (3)A中高锰酸钾和浓盐
2
酸发生氧化还原反应有氯气生成,反应的化学方程式为 2KMnO +16HCl(浓)=5Cl↑ +
4 2
2MnCl + 2KCl + 8H O,反应的离子方程式为2MnO - + 16H+ +10Cl- =2Mn2++5Cl↑+8H O。
2 2 4 2 2
(4)B、C管口“浸有NaOH溶液的棉花”的作用是吸收氯气,防止污染环境。(5)为验
证溴的氧化性强于碘,应将C中生成的溴加入到盛有KI溶液的D中,如发生氧化还原反
应,则静置后CC1 层溶液变为紫红色,故操作步骤及现象为打开活塞b,将少量C中溶液
4
滴入D中,关闭活塞b,取下D,振荡、静置后CCl 层溶液变为紫红色。(6)为验证溴的
4
氧化性强于碘,实验时应避免氯气的干扰,当B中溶液由黄色变为棕红色时,说明有大量
的溴生成,则C的黄色溶液中无Cl,可以排除Cl 对实验的干扰。(7)同主族元素从上到
2 2
下,电子层数依次增多,原于半径逐渐增大,得电子能力逐渐减弱,元素的非金属性逐渐
减弱。
【考点】氧化还原
第12页