文档内容
第一章 原子结构与性质
第二节 原子结构与元素的性质
第二课时 元素周期律
基础达标
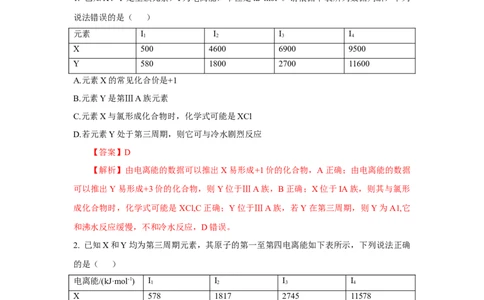
1. 已知X、Y是主族元素,I为电离能,单位是kJ·mol-1。请根据下表所列数据判断,下列
说法错误的是( )
元素 I I I I
1 2 3 4
X 500 4600 6900 9500
Y 580 1800 2700 11600
A.元素X的常见化合价是+1
B.元素Y是第ⅢA族元素
C.元素X与氯形成化合物时,化学式可能是XCl
D.若元素Y处于第三周期,则它可与冷水剧烈反应
【答案】D
【解析】由电离能的数据可以推出X易形成+1价的化合物,A正确;由电离能的数据
可以推出Y易形成+3价的化合物,则Y位于ⅢA族,B正确;X位于IA族,则其与氯形
成化合物时,化学式可能是XCl,C正确;Y位于ⅢA族,若Y在第三周期,则Y为A1,它
和沸水反应缓慢,不和冷水反应,D错误。
2. 已知X和Y均为第三周期元素,其原子的第一至第四电离能如下表所示,下列说法正确
的是( )
电离能/(kJ·mol-1) I I I I
1 2 3 4
X 578 1817 2745 11578
Y 738 1451 7733 10540
A.X通常显+3价,Y通常显+1价
B.X的第一电离能大于Y的第一电离能
C.X、Y的最高价氧化物的水化物都不能与氢氧化钠反应
D.工业上制取X采用的是电解熔融的X的氧化物,制取Y采取的是电解熔融的Y的氯化物
【答案】D
【解析】X的第四电离能突然增大,X最外层有3个电子,X是A1元素,铝通常显+3价;Y的第三电离能突然增大,Y最外层有2个电子,Y是Mg元素,镁通常显+2价,A
错误;根据表格数据,X的第一电离能小于Y的第一电离能,B错误;氢氧化铝能与氢氧
化钠反应生成偏铝酸钠,C错误;工业上采用的是电解熔融的氧化铝冶炼金属铝,电解熔
融的氯化镁冶炼金属镁,D正确。
3.下列有关电离能的说法,正确的是( )
A.第一电离能越大的原子失电子的能力越强
B.第一电离能是元素的原子失去核外第一个电子需要的能量
C.同一周期中,主族元素原子第一电离能从左到右越来越大
D.同主族元素,随原子序数的递增,第一电离能逐渐减小
【答案】D
【解析】A错,元素原子的第一电离能越大,表示该元素的原子越难失去电子;B错,
第一电离能是气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量
C错,从总的变化趋势上看,同一周期中,主族元素的第一电离能从左到右逐渐增大,但
有反常,如I(N)>I (O)。
1 1
4. 下列说法中正确的是( )
①元素电负性越大表示该元素的金属性越强②元素电负性越大表示该元素的非金属性越强
③元素电负性很小表示该元素的单质不发生化学反应④元素电负性很大表示该元素的单质
在发生化学反应时一般易得到电子
A.①③ B.①④ C.②③ D.②④
【答案】D
【解析】①元素电负性越大,原子对键合电子的吸引力越大,则元素的金属性越弱,
故错误;②元素电负性越大,原子对键合电子吸引力越大,则元素的非金属性越强,故正
确;③元素电负性很小表示该元素的单质易发生氧化反应,故错误;④元素电负性越大表
示该元素对键合电子的吸引力越大,单质在发生化学反应时一般易得到电子,故正确。
5. 不能说明X的电负性比Y大的是( )
A.与H 化合时X单质比Y单质容易
2
B.X的最高价氧化物的水化物的酸性比Y的最高价氧化物的水化物的酸性强
C.X原子的最外层电子数比Y原子的最外层电子数多
D.X单质可以把Y从其氢化物中置换出来
【答案】C
【解析】A项,与H 化合时X单质比Y单质容易,则X的非金属性强于Y,元素非金
2属性越强电负性越大,能说明X的电负性比Y大;B项,X的最高价氧化物的水化物的酸
性比Y的最高价氧化物的水化物的酸性强,则X的非金属性强于Y,元素非金属性越强电负
性越大,能说明X的电负性比Y大;C项,X原子的最外层电子数比Y原子的最外层电子
数多不能说明X的电负性比Y大,如Si的电负性比H小;D项,X单质可以把Y从其氢化
物中置换出来,则X的非金属性强于Y,元素非金属性越强电负性越大,能说明X的电负性
比Y大。
6. 下列说法不正确的是( )
A.同族元素在性质上的相似性,取决于原子价电子排布的相似性
B.同周期元素的原子半径越小,电负性越大
C.元素的电负性越大,表示其原子在化合物中吸引电子的能力越强
D.电负性大的元素易呈现正价,电负性小的元素易呈现负价
【答案】D
【解析】元素原子的电负性越大,对键合电子的吸引力越大,故在化合物中,电负性
大的元素易呈现负价,电负性小的元素易呈现正价。
7. 下列说法中正确的是( )
A.铝的第一电离能比镁的第一电离能大
B.同一主族元素从上到下,电负性逐渐变大
C.镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态
D.最外层电子数是核外电子总数1/5的原子和最外层电子排布式为4s24p3的原子是同种元素
原子
【答案】D
【解析】镁原子的3s能级电子的能量低于Al原子的3p能级电子的能量,第一电离能比
Al元素高,A错误;同一主族元素从上到下,金属性逐渐增强,电负性依次减弱,B错误;
基态Mg的电子排布式为1s22s22p63s2,能量处于最低状态,当变为1s22s22p63p2时,电子发生
跃迁,需要吸收能量,变为激发态,C错误;最外层电子数是核外电子总数的1/5的原子是
Br,核外电子排布式为1s22s22p63s23p63d104s24p5,最外层电子排布式为4s24p5,两者是同种元素
原子,D正确。
8.下列物质组成元素间电负性差值可能大于1.8的化合物是( )
A. CH B. CO C. NO D. Na O
4 2 2
【答案】D
【解析】一般来说,元素的电负性的差值大于1.7时,原子间形成离子键,元素的电负性的差值小于1.7时,原子间形成共价键,所以组成元素间电负性差值可能大于1.8的化合
物应是离子化合物,D符合。
9.若成键的两原子所对应的元素的电负性之差为 0,则这两种原子之间一定不能形成的化学
键是( )
A.共价键 B.离子键 C.非极性键 D.极性键
【答案】B
【解析】经验规律告诉我们当成键的两原子相应元素电负性的差值△X>1.7时,一般为
离子键,当△X<1.7时,一般为共价键。所以若成键的两原子所对应的元素的电负性之差
为0,两种原子之间形成共价键,一定不可能是离子键。
能力提升
10. 短周期主族元素X、Y在同一周期,且电负性X>Y,下列说法不正确的是( )
A.X与Y形成化合物时,X显负价,Y显正价
B.第一电离能Y小于X
C.原子半径:X小于Y
D.气态氢化物的稳定性:H Y弱于HX
m n
【答案】B
【解析】因为电负性X>Y,所以X和Y形成化合物时,X显负价,Y显正价,A正确;
一般非金属性越强,第一电离能越大,若Y的最外层电子为半满或全满稳定结构,则第一
电离能Y大于X,B错误;因短周期主族元素X、Y在同一周期,且电负性X>Y,所以原子半
径:XY,所以非金属性X>Y,气态氢化物的稳
定性:H Y弱于HX,D正确。
m n
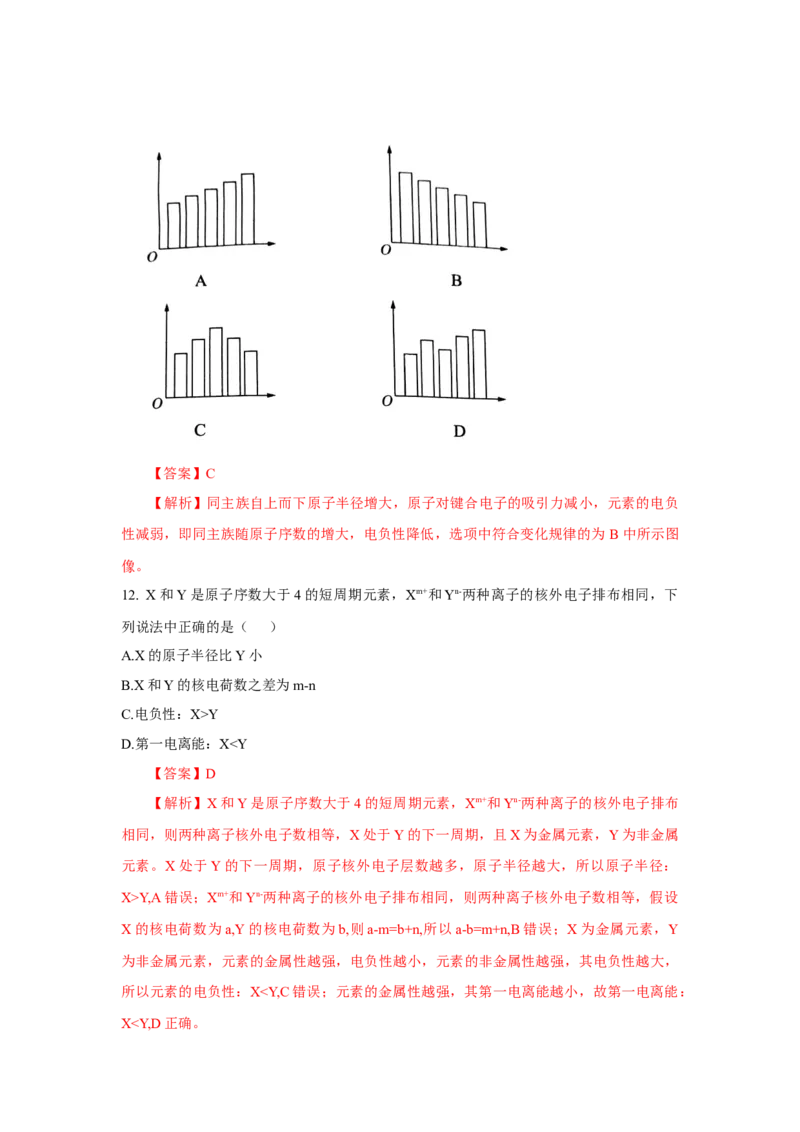
11.下列图示中横坐标表示元素的电负性数值,纵坐标表示同一主族的五种元素的原子序数
的是( )【答案】C
【解析】同主族自上而下原子半径增大,原子对键合电子的吸引力减小,元素的电负
性减弱,即同主族随原子序数的增大,电负性降低,选项中符合变化规律的为 B中所示图
像。
12. X和Y是原子序数大于4的短周期元素,Xm+和Yn-两种离子的核外电子排布相同,下
列说法中正确的是( )
A.X的原子半径比Y小
B.X和Y的核电荷数之差为m-n
C.电负性:X>Y
D.第一电离能:XY,A错误;Xm+和Yn-两种离子的核外电子排布相同,则两种离子核外电子数相等,假设
X的核电荷数为a,Y的核电荷数为b,则a-m=b+n,所以a-b=m+n,B错误;X为金属元素,Y
为非金属元素,元素的金属性越强,电负性越小,元素的非金属性越强,其电负性越大,
所以元素的电负性:XD,A
的原子结构示意图为 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对
电子,E对应的单质是目前用量最大的金属。回答下列问题:
(1)写出下列元素的符号:A ,B ,C ,D
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是 ,碱性最
强的是
(3)用元素符号表示D所在周期第一电离能最大的元素是
(4)E原子价电子排布式是 ,E元素在周期表中的位置是 。
已知元素周期表可按电子排布分为s区、p区等,则E元素在 区。
(5)写出D元素原子构成单质的电子式
【答案】(1)Si Na P N (2)HNO , NaOH (3)Ne (4)3d64s2 第四周期第Ⅷ族 d
3
(5)
【解析】
(1)A、B、C、D、E是前四周期元素,A的原子结构示意图为 ,K层最多排列2个电子,所以x=2,则A原子核内有14个电子,为Si元素;A、B、C同周期,B是同周期第一
电离能最小的元素,则B是Na元素;C的最外层有三个未成对电子,则C为P元素;C、
D同主族且原子半径C>D,D属于短周期元素,则D为N元素;E对应的单质是目前用量最
大的金属,则E是Fe元素。
(2)元素的非金属性越强,其最高价氧化物对应的水化物酸性越强,元素的金属性越强,其
最高价氧化物对应的水化物碱性越强,这几种元素中,非金属性最强的是N元素,所以
HNO 的酸性最强,金属性最强的是Na元素,所以NaOH的碱性最强。
3
(3)同一周期,元素的第一电离能随着原子序数增大而呈增大趋势,但第ⅡA族、第VA族
元素第一电离能大于其相邻元素,D是N元素,位于第二周期,第二周期第一电离能最大
的是Ne元素。
(4)E是Fe元素,Fe元素的价电子排布式为3d64s2,核外电子数是26,Fe元素在周期表中的位
置是第四周期第Ⅷ族,第Ⅷ族元素属于d区。
(5)D是N元素,其单质为氮气,氮气分子中含有1个三键,其电子式为
15.下表是某些短周期元素的电负性(X)值:
元 素 Li Be B C O F Na Al Si P S Cl
符号
X值 1.0 1.5 2.0 2.5 3.5 4.0 0.9 1.5 1.8 2.1 2.5 3.0
(1)根据表中数据归纳元素的电负性与原子吸引电子的能力的关系是
(2)通过分析X值变化规律,确定N、Mg最接近的X值范围: 1.7时,它们之间通
常形成离子键;△X<1.7时,通常形成共价键。结合以上问题分析AlBr 中的化学键类型是
3
【答案】(1)元素的电负性越大,原子吸引电子的能力越强 (2)0.9 1.5 2.5 3.5
(3)原子半径越大,X值越小 周期性 (4)共价键
【解析】
(1)由表中数据可知,电负性越大的元素,其非金属性越强,在反应中越易得到电子。
(2)确定X值的范围应注意取同周期递变和同主族递变的交集。
(3)分析同周期和同主族元素X值的递变,均可得出X值随原子半径的增大而减小。
(4)Cl与Al的△X为3.0-1.5=1.5<1.7,Br的X值小于Cl的X值,故AIBr 中成键的两原子相
3应元素的△X<1.7,为共价键。