文档内容
第二章 分子结构与性质
第二节 分子的空间结构
2.2.1 分子结构的测定与多样性 价层电子对互斥模型
一.选择题
1. 价层电子对互斥理论 是关于分子几何构型的经验规律,该理论认为,分子的稳定结
构应使中心原子价层电子对之间的斥力最小,且不同价层电子对之间排斥力相对大小满足:孤
对电子 孤对电子 孤对电子 键对电子 键对电子 键对电子。如 分子中
下列推断不合理的是
A. 分子中
B. 键角 小于 键角
C. 已知 分子为正四面体, 中的 小于 中的
D. 离子中 小于 分子中
【答案】D
【解析】
A. 分子中N原子有一对孤电子对,根据孤对电子 键对电子 键对电子 键对电子,故
,故A正确;
B. 中O有两对孤电子对,而 中O有一对孤电子对,故H 中键角 小于
键角 ,故B正确;
C.已知 分子为正四面体, 中P有孤电子对, 中P无孤电子对,故 中的
小于 中的 ,故C正确;
D. 离子中 大于 分子中 ,故D错误。
2. 下列各组微粒的空间构型相同的是和 和 和 和
和 和 和
A. 全部 B. 除 以外 C. D.
【答案】C
【解析】
中价层电子对个数 且含有一个孤电子对,所以为三角锥形,
中价层电子对个数 且含有两个孤电子对,所以为V形结构,二者空间构型
不同,故 错误;
中价层电子对个数是4且不含孤电子对,为正四面体形结构; 中O原子价层电子对
个数 且含有一个孤电子对,所以为三角锥形结构,二者空间构型不
同,故 错误;
为三角锥形结构、 中O原子价层电子对个数 且含有
一个孤电子对,所以为三角锥形结构,所以二者空间构型相同,故 正确;
、 中价层电子对个数都是3且都含有一对孤电子对,所以分子空间构型都是V形,故
正确;
分子中价层电子对 ,所以二氧化碳是直线型结构, 中Be
价层电子对 ,是sp杂化,是直线型结构,二者空间构型相同,故 正
确;
和 中价层电子对个数都是4且不含孤电子对,所以空间构型都是正四面体结构,所
以空间构型相同,故 正确;
中B原子杂化轨道数 ,所以分子构型为平面正三角形,气态氯化铝通常以二聚分子形式存在, 结构 ,Al采用 杂化轨道成键,为正四面体结构,
二者空间构型不同,故 错误。
故选C。
3. 通常状况下, 是一种油状液体,下列对 的有关叙述正确的是
A. 中 键键长比 中 键键长短
B. 分子中的N原子无孤电子对
C. 分子的空间构型为三角锥型
D. 稳定性弱于 ,因为 的键能比 的键能大
【答案】C
【解析】
A. 中 键键长比 中 键键长长,故A错误;
B.N原子最外层有5个电子, 分子中N原子的价层电子对数为4,孤对电子数为1,故B错
误;
C. 分子中N原子的价层电子对数为4,孤对电子数为1,空间构型为三角锥型,故C正确;
D.因为 的键能比 的键能小, 稳定性弱于 ,故D错误。
故选C。
4. 下列化学用语表示或描述不正确的是
A. Ca的电子排布式是
B. 的VSEPR的模型名称是平面三角形
C. 中心原子N上的孤电子对数为0
D. 在 里, 的氮原子给出孤电子对,形成配位键
【答案】A
【解析】
A.Ca原子最外层电子为4s能级上2个电子,Ca原子的电子排布式是 或,故A错误;
B. 中B原子价层电子对个数 ,所以 的VSEPR的模型名称是平面三角
形,故B正确;
C. 中心原子N上的孤电子对数 ,故C正确;
D.配离子中含有孤电子对的原子提供孤电子对、含有空轨道的原子提供空轨道形成配位键,
的氮原子含有孤电子对而提供孤电子对,铜离子提供空轨道而形成配位键,故D正确;
故选:A。
5. 下列分子或离子中,VSEPR模型与粒子的立体构型一致的是
A. B. HCHO C. D.
【答案】B
【解析】
分子中S原子孤电子对数 , 键电子对为2,价层电子对个数
,S原子采取 杂化,VSEPR模型为平面三角形结构,含有1个孤电子对,空间构型为V形,故
A错误;
B.当中心原子没有孤电子对时,VSEPR模型与分子的立体构型就是一致的,故B正确;
C. 中N原子孤电子对数 ,价层电子对数为 ,VSEPR模型为四面体,而
微粒空间构型为三角锥形,故C错误;
D. 价层电子对个数 且含有1个孤电子对,所以VSEPR模型是
四面体结构,实际空间构型为三角锥形,故D错误。
6. 下列关于价层电子对互斥模型 VSEPR模型 的叙述中错误的是
A. VSEPR模型可用来预测分子的立体结构
B. 分子中价电子对相互排斥决定了分子的空间结构
C. 中心原子上的孤电子对不参与互相排斥
D. 分子中键角越大,价电子对相互排斥力越小【答案】C
【解析】
模型可用来预测分子的立体构型,注意实际空间构型要考虑孤电子对,故A正确;
B.分子的空间结构与价电子对相互排斥有关,分子中价电子对相互排斥决定了分子的空间结构,故
B正确;
C.中心原子上的孤电子对参与互相排斥,故C错误;
D.分子中键角越大,价电子对相互排斥力越小,故D正确;
故选:C。
7. 用VSEPR模型预测下列分子或离子的立体结构,其中不正确的是
A. 为正四面体形 B. 为直线形
C. HCN为V形 D. 为三角锥形
【答案】C
【解析】
A. 中N原子的价层电子对个数 且不含有孤电子对,所以其空间
构型为正四面体结构,故A正确;
B. 分子中价层电子对个数 且不含有孤电子对,所以为直线形结构,
故B正确;
C.HCN的结构为 ,C原子的价层电子对数为2,不含有孤电子对,为直线形,故C错
误;
D. 分子中P原子的价层电子对个数 且含一个孤电子对,所以其空间
构型为三角锥形,故D正确。
故选C。
8. 根据价层电子对互斥模型,判断下列分子或者离子的空间构型不是三角锥形的是
A. B. C. HCHO D.
【答案】C
【解析】根据价层电子对互斥理论确定其空间构型,价层电子对数 键个数 ,a指中心原子价
电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数,据此分析解答。
A.三氯化磷分子中,P原子价层电子对数 ,且含有一个孤电子对,所以其
空间构型是三角锥形,不符合,故A错误;
B.水合氢离子中,O原子价层电子对数 ,且含有一个孤电子对,所以
其空间构型是三角锥形,不符合,故B错误;
C.HCHO中,C原子价层电子对数 ,且不含孤电子对,所以其空
间构型是平面三角形,故C正确;
D. 分子中,P原子价层电子对数 ,且含有一个孤电子对,所以其空
间构型是三角锥形,不符合,故D错误。
故选C。
9. 下列关于 的说法中不正确的是
A. 1个 中有3个 键
B. 中心原子上有1对孤对电子
C. 的立体构型是三角锥形
D. 键之间的夹角:
【答案】D
【解析】
对于 ,根据VSEPR理论,中心O原子的配位原子数为3,孤电子对数为 ,
则价电子对数为 ,根据杂化轨道理论,中心O原子为 杂化,
A. 中中心O为 杂化,有4个 杂化轨道,而成键是3根键,还有一对孤电子对,则1个中有3个 键,故A正确;
B.中心O上存在一对孤电子对,占据正四面体形的一个顶点,故B正确;
C. 杂化的粒子的理论空间构型为正四面体形,由于 中存在一对孤电子对占据正四面体形
的一个顶点,因此粒子的立体构型为三角锥形,故C正确;
D. 中含有1对孤电子对, 中含有2对孤电子对,由于孤电子对斥力大于键合电子对斥
力,孤电子对数目越多,键角越小,因此 键之间的夹角: ,故D错误。
故选D。
10. 下列关于价层电子对互斥模型 模型 的叙述中不正确的是
A. VSEPR模型可用来预测分子的立体构型
B. 分子中价电子对相互排斥决定了分子的立体构型
C. 中心原子上的孤电子对也要占据中心原子周围的空间并参与互相排斥
D. 分子中键角越大,价电子对相互排斥力越大,分子越稳定
【答案】D
【解析】
A.VSEPR模型可用来预测分子的立体构型,注意实际空间构型要去掉孤电子对,故A正确;
B.立体构型与价电子对相互排斥有关,所以分子中价电子对相互排斥决定了分子的立体构型,故B
正确;
C.中心原子上的孤对电子也要占据中心原子周围的空间并参与互相排斥,且孤电子对间排斥力 孤
电子对和成对电子对间的排斥力,故C正确;
D.分子的稳定性与键角没有关系,故D错误;
故选:D。
11. 用价层电子对互斥理论判断 的分子构型为
A. 正四面体形 B. V形 C. 三角锥形 D. 平面三角形
【答案】 D
【解析】
三氧化硫分子中,中心原子硫原子最外层6个电子,价层电子对数 键个数 孤电子对个数,且不含孤电子对,所以三氧化硫分子为平面三角形结构。故D正确。
12. 下列离子的VSEPR模型与离子的空间立体构型一致的是
A. B. C. D.
【答案】B
【解析】
A. 中价层电子对个数 且含有一对孤电子对,所以VSEPR模型
为四面体结构,离子的空间立体构型为三角锥形结构,故A错误;
B. 中价层电子对个数 且不含孤电子对,所以离子的VSEPR模
型与离子的空间立体构型一致都是四面体结构,故B正确;
C. 中价层电子对个数 且含有一对孤电子对,所以其VSEPR模型
是平面三角形,离子的空间立体构型为V形,故C错误;
D. 中价层电子对个数 且含有一对孤电子对,所以VSEPR模型
是四面体结构,离子的空间立体构型为三角锥形,故D错误。
故选B。
13. 用价层电子对互斥理论可以预测许多分子或离子的空间构型,也可推测键角大小,下列判断正
确的是
A. 是V形分子 B. 键角大于
C. 是三角锥形分子 D. 键角等于
【答案】D
【解析】
A. 中中心原子价层电子对个数 ,为直线形结构,故A错误;
B. 中中心原子价层电子对个数 且含有一对孤电子对,为V形结构,孤电子对与成键电子对之间的排斥力大于成键电子对之间的排斥力,所以 键角小于
,故B错误;
C. 中中心原子价层电子对个数 ,为平面三角形结构,故B错误;
D. 中中心原子价层电子对个数 ,为正四面体结构,所以
键角等于 ,故D正确;
故选D。
14. 下列分子中的中心原子 点“ ”的原子为中心原子 的价层电子对数正确的是
A. N B. C C. B D. S
【答案】A
【解析】
根据价电子对互斥理论确定微粒的空间构型和原子的杂化方式,价层电子对个数 键个数 孤电
子对个数. 键个数 配原子个数,孤电子对个数 ,a指中心原子价电子个数,x指配
原子个数,b指配原子形成稳定结构需要的电子个数,据此解答。
A. 中N原子价层电子对数 ;故A正确;
B. 中C原子价层电子对数 ,故B错误;
C. 中B原子的价层电子对数 ,故C错误;
D. 中S原子价层电子对个数 ,故D错误。
故选A。
15. 在白磷 分子中,4个P原子分别处在正四面体的四个顶点,结合有关P原子的成键特点,
下列有关白磷的说法正确的是
A. 白磷分子的键角为 B. 分子中共有4对共用电子对
C. 白磷分子的键角为 D. 分子中有6对孤电子对【答案】C
【解析】
A.白磷分子无中心原子,根据共价键的方向性和饱和性,每个磷原子都以3个共价键与其他3个磷
原子结合形成共价键,从而形成正四面体结构,所以键角为 ,故A错误;
B.白磷总共有6个共价单键,6对共用电子,故B错误;
C.白磷分子无中心原子,根据共价键的方向性和饱和性,每个磷原子都以3个共价键与其他3个磷
原子结合形成共价键,从而形成正四面体结构,所以键角为 ,
故C正确;
D. 键角为 ,总共有6个共价单键,每个磷原子含有一对孤对电子,总计有4对孤对电子,故D
错误;
故选C。
二、填空题
16. 是有机合成中常用的还原剂, 中的阴离子空间构型是_______,中心原子的
杂化形式为_______。
根据价层电子对互斥理论, 、 、 的气态分子中,中心原子价层电子对数不同
于其他分子的是_______。
中华本草 等中医典籍中,记载了炉甘石 入药,可用于治疗皮肤炎症或表面创
伤。 中,阴离子空间构型为_______,C原子的杂化形式为_______。
射线衍射测定等发现, 中存在 离子, 离子的几何构型为_______,中心原子
的杂化形式为_______。
【答案】 正四面体 ;
平面三角形;
V形 ;
【解析】中的阴离子是 ,中心原子铝原子的价层电子对数是4,且不存在孤电子对,所以其
空间构型是正四面体;中心原子的杂化轨道类型是 杂化;
根据价层电子对互斥模型可知, 、 、 的气态分子中,中心原子价层电子对数分别
是 、 、 ,因此中心原子价层电子对数不同于其他分子
的是 ;
碳酸锌中的阴离子为 ,根据价层电子对互斥模型,其中心 C原子的价层电子对数为
,不含孤电子对,所以其空间构型为平面三角形,C原子为 杂化;
的中心I原子形成2个 键,孤电子对数为 ,即中心I原子形成2个 键,还
有2个孤电子对,故 的几何构型为V形;中心I原子采取 杂化。
17. 有下列分子或离子: , , , , , , ,
。
粒子的立体构型为直线形的有________;粒子的立体构型为V形的有________;粒子的立体构
型为平面三角形的有________;粒子的立体构型为三角锥形的有________;粒子的立体构型为
正四面体形的有________。
【答案】 ; ; ; ;
【解析】
, 键电子对数为2,孤电子对数为0,空间构型为直线形;
, 键电子对数为3,孤电子对数为1,空间构型为三角锥形;
, 键电子对数为2,孤电子对数为2,空间构型为V形;
, 键电子对数为3,孤电子对数为0,空间构型为平面三角形;
, 键电子对数为3,孤电子对数为1,空间构型为三角锥形;
, 建电子对数为4,孤电子对数为0,空间构型为正四面体形;, 键电子对数为3,孤电子对数为0,空间构型为平面三角形;
, 键电子对数为2,孤电子对数为1,空间构型为V形;
故答案为: ; ; ; ; 。
18. 通入稀NaOH溶液中可生成 , 分子构型为________,
其中氧原子的杂化方式为__________。 常用作 转化为
的催化剂。 分子中S原子价层电子对数是________对,分子的立体构型为________;
气态为单分子,该分子中S原子的杂化轨道类型为________; 的三聚体环状结构如图
所示,该结构中S原子的杂化轨道类型为________;该分子中含有________个 键。
【答案】 形;
;V形; 杂化; 杂化;12。
【解析】
分子的中心原子的价层电子对数为 ,中心原子还有2个孤电子对,故其
分子的空间构型为V形,其中氧原子的杂化方式为 ,故答案为:V形; ;
分子中S原子形成2个 键,孤电子对数为 , 分子中S原子价层电子对
数是3,为V形结构; 气态为单分子,该分子中S原子形成3个 键,没有孤对电子,则为
杂化, 的三聚体中S原子形成4个 键,为 杂化; 的三聚体中含有 键数目为
,故答案为:3;V形; 杂化; 杂化;12。
19. N、O、S、Cl、Cu五种元素的单质及其化合物在现代工业生产中有着广泛应用。请回答下列
问题:
第一电离能:N________ 填“ ”或“ ”,下同 ,电负性:S________Cl。
前四周期元素中,未成对电子数为5的元素符号是 ______ ;的空间构型是________,分子中的大 键可用符号 表示,其中m代表参与形成的
大 键原子数,n代表参与形成大 键的电子数 如苯分子中的大 键可表示为 ,则
中的大 键应表示为________。
亚硒酸根离子 的VSEPR模型为 ______ ;
与 互为等电子体的微粒有________ 任写两种
【答案】 ; ;
;
平面正三角形; ;
四面体形;
; 合理即可 。
【解析】
、O位于同一周期相邻位置,N原子的2p能级电子数达到了半满结构,比较稳定,则第一电
离能 ,元素的电负性与非金属性有关,非金属性越强,电负性越大,则电负性 ;
前四周期元素中,未成对电子数为5的元素的外围电子构型为 ,元素符号为Mn;
的中心原子为S原子,形成3个 键,孤电子对为 ,则空间构型为平面正
三角形, 中S原子形成3个 键,还有3个电子,3个氧原子有3个电子,形成4原子6电子的
大 键,应表示为 ;亚硒酸根离子 的中心原子为Se,形成3个 键,孤电子对为 ,则
VSEPR模型为四面体形;
为四个原子的离子,价电子总数为24,互为等电子体的是 、 。
20. 利用VSEPR模型推断分子或离子的立体构型。
____________; ____________; ____________。
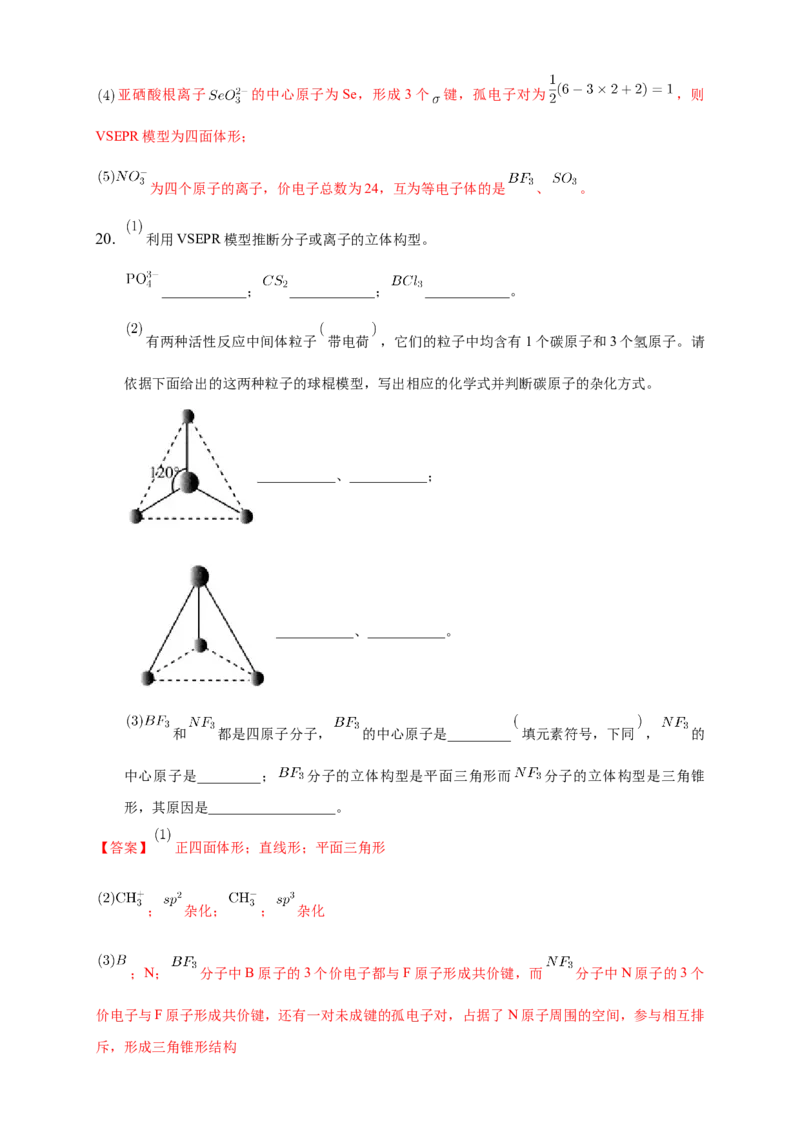
有两种活性反应中间体粒子 带电荷 ,它们的粒子中均含有1个碳原子和3个氢原子。请
依据下面给出的这两种粒子的球棍模型,写出相应的化学式并判断碳原子的杂化方式。
___________、___________;
___________、___________。
和 都是四原子分子, 的中心原子是_________ 填元素符号,下同 , 的
中心原子是_________; 分子的立体构型是平面三角形而 分子的立体构型是三角锥
形,其原因是__________________。
【答案】 正四面体形;直线形;平面三角形
; 杂化; ; 杂化
;N; 分子中B原子的3个价电子都与F原子形成共价键,而 分子中N原子的3个
价电子与F原子形成共价键,还有一对未成键的孤电子对,占据了N原子周围的空间,参与相互排
斥,形成三角锥形结构【解析】
属于 型,成键电子对数是4,孤电子对数为0,呈正四面体形; 属于 型,成
键电子对数是2,孤电子对数为0,呈直线形; 属于 型,成键电子对数是3,孤电子对数
为0,呈平面三角形;
对于 型分子,若中心原子无孤电子对,呈平面三角形;若有一对孤电子对,则呈三角锥
形,所以题中两种模型表示的物质的化学式及碳原子的杂化方式分别是 、 杂化和 、
杂化;
根据 和 的组成可知二者的中心原子分别为B和N;由于 分子中B原子的3个价电
子都与F原子形成共价键,而 分子中N原子的3个价电子与F原子形成共价键,还有一对未成
键的孤电子对,占据了N原子周围的空间,参与相互排斥,所以前者形成平面三角形结构而后者形
成三角锥形结构。