文档内容
第二节 分子的空间结构
一、分子结构的测定
1.早年的科学家主要靠对物质的化学性质进行系统总结得出规律后推测分
子的结构。如今,科学家应用红外光谱、晶体 X射线衍射等现代仪器和方法测
定分子的结构。
2.红外光谱工作原理
(1)原理:分子中的原子不是固定不动的,而是不断震动的。红外线透过分
子时,分子会吸收跟它的某些化学键的振动频率相同的红外线,再记录到谱图
上呈现吸收峰。通过和已有谱图库比对,或通过量子化学计算,可以得知分子
中含有何种化学键或官能团的信息。
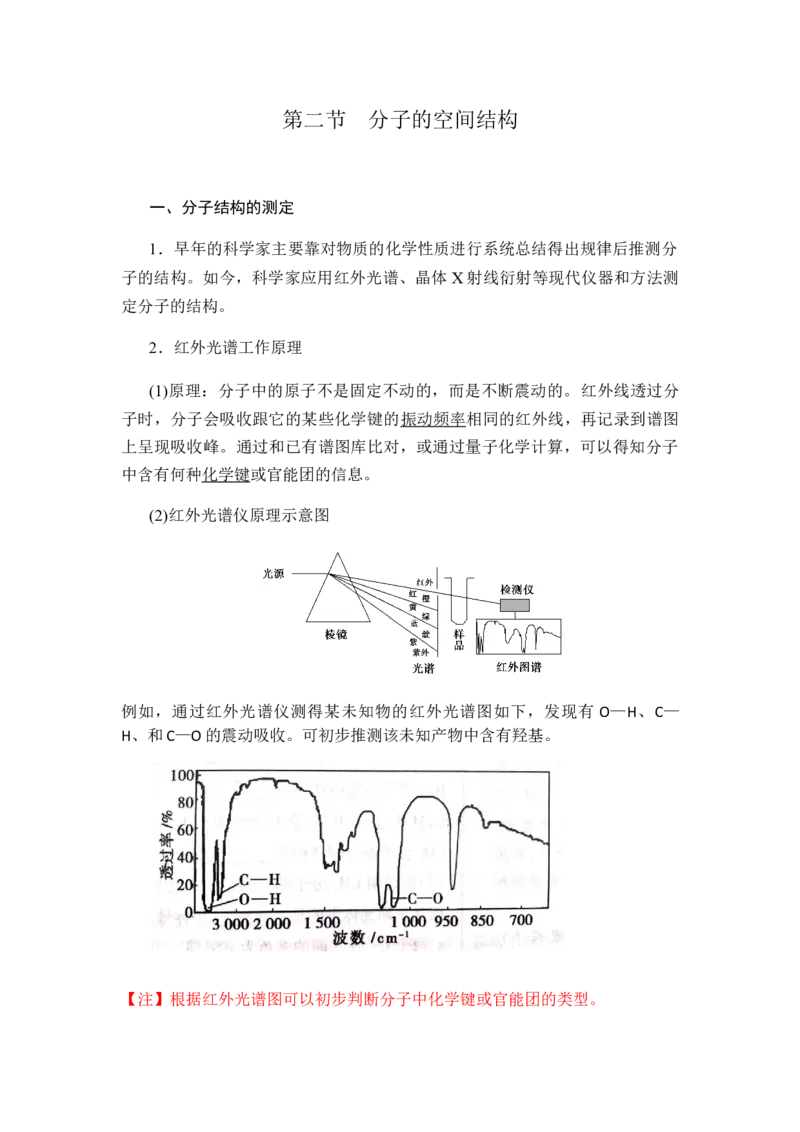
(2)红外光谱仪原理示意图
例如,通过红外光谱仪测得某未知物的红外光谱图如下,发现有 O—H、C—
H、和C—O的震动吸收。可初步推测该未知产物中含有羟基。
【注】根据红外光谱图可以初步判断分子中化学键或官能团的类型。二、多样的分子空间结构
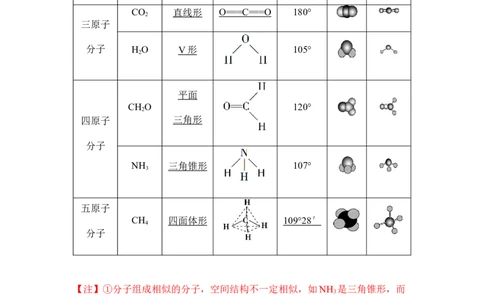
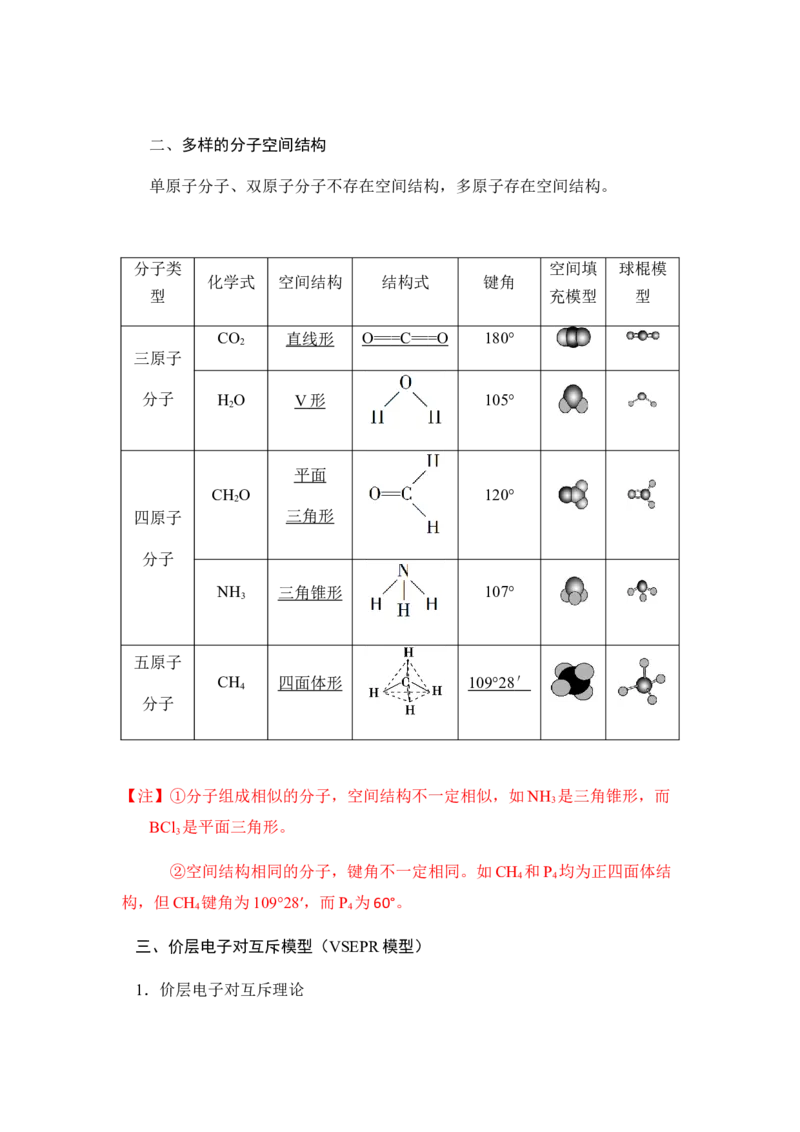
单原子分子、双原子分子不存在空间结构,多原子存在空间结构。
分子类 空间填 球棍模
化学式 空间结构 结构式 键角
型 充模型 型
CO 直线形 O == = C == = O 180°
2
三原子
分子 H O V 形 105°
2
平面
CH O 120°
2
四原子 三角形
分子
NH 三角锥形 107°
3
五原子
CH 四面体形 109°28 ′
4
分子
【注】①分子组成相似的分子,空间结构不一定相似,如NH 是三角锥形,而
3
BCl 是平面三角形。
3
②空间结构相同的分子,键角不一定相同。如CH 和P 均为正四面体结
4 4
构,但CH 键角为109°28′,而P 为60°。
4 4
三、价层电子对互斥模型(VSEPR模型)
1.价层电子对互斥理论分子的空间结构是中心原子周围的“价层电子对”相互排斥的结果。
VSEPR的“价层电子对”是指分子中的中心原子与结合原子间的 σ键电子
对和中心原子的孤电子对。
2.中心原子上价层电子对的计算
(1)价层电子对
(2)计算
①σ键电子对的计算
由分子式确定,即中心原子形成几个 σ键,就有几对σ键电子对。如H O
2
分子中,O有2 对σ键电子对,NH 分子中,N有3 对σ键电子对。
3
②中心原子上的孤电子对的计算
中心原子上的孤电子对数=(a-xb)
a.a表示中心原子的价电子数。
对于主族元素:a=原子的最外层电子数。
对于阳离子:a=中心原子的价电子数-离子的电荷数。
对于阴离子:a=中心原子的价电子数+ 离子的电荷数 ( 绝对值 )。
b.x表示与中心原子结合的原子数。
c.b表示与中心原子结合的原子最多能接受的电子数,氢为1,其他原子
= 8 -该原子的价电子数 。
(3)VSEPR模型与分子或离子的空间结构
σ 键电子对数+孤电子对数=价层电子对数 ―――――→VSEPR 模
型――――――→分子或离子的空间结构。
VSEPR 分子或离子
分子或离子 孤电子对数 价层电子对数
模型名称 的空间结构名称CO 、BeCl 0 2 直线形 直线形
2 2
SO 、PbCl 1 3 平面三角形 V形
2 2
CO、BF 0 3 平面三角形 平面三角形
3
H O、H S 2 4 四面体形 V形
2 2
NH 、NF 1 4 四面体形 三角锥形
3 3
CH 、CCl 0 4 正四面体形 正四面体形
4 4
(4)价层电子对之间的斥力
①电子对间夹角越小,斥力越大。
②分子中电子对之间的斥力大小顺序:孤电子对—孤电子对 > 孤电子对—
成键电子对 > 成键电子对—成键电子对。
③由于三键、双键比单键包含的电子多,所以斥力大小顺序:三键 > 双键
>单键。
【注】①孤电子对对成键电子对的排斥作用会挤压周围的化学键,使键与键之
间的键角变小,如H O的键角105°,NH 的键角107°。
2 3
②中心原子的价层电子都用于形成共价键分子,其空间结构与VSEPR模
型相同,如CO 、CH 。
2 4
③中心原子上有孤电子对时,分子的空间结构与VSEPR模型不同,如
SO 、NH 。
2 3
④价层电子对互斥模型对分子的空间结构的预测少有事物,但它不能预测
以过渡金属为原子的分子。
例1.若AB 分子的中心原子A上没有未用于形成共价键的孤电子对,根据
n
价层电子对互斥理论,下列说法正确的是( )A.若n=2,则分子的空间结构为V形
B.若n=3,则分子的空间结构为三角锥形
C.若n=4,则分子的空间结构为正四面体形
D.以上说法都不正确
【答案】 C [若中心原子A上没有未用于成键的孤电子对,则根据斥力
最小的原则,当n=2时,分子的空间结构为直线形;当 n=3时,分子的空间
结构为平面三角形;当n=4时,分子的空间结构为正四面体形。]
2.用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的空间结构,
有时也能用来推测键角大小,下列判断错误的是( )
A.SO 、CS 、HI都是直线形的分子
2 2
B.BF 键角为120°
3
C.BF 、SO 都是平面三角形的分子
3 3
D.PCl 、NH 都是三角锥形的分子
3 3
【答案】 A [A.SO 中价层电子对数=2+×(6-2×2)=3且含有1对孤
2
电子对,所以SO 为V形结构,CS 、HI为直线形结构,故A错误;B.BF 中价
2 2 3
层电子对数=3+×(3-3×1)=3,为平面三角形结构,所以BF 键角为120°,
3
故B正确;C.BF 、SO 中中心原子价层电子对数都是3且不含孤电子对,所以
3 3
这两种分子都是平面三角形结构,故C正确;D.PCl 、NH 中价层电子对数=3
3 3
+×(5-3×1)=4,且含有1对孤电子对,所以PCl 、NH 均为三角锥形结构,
3 3
故D正确。]
例3. 下列叙述正确的是( )
A.NH 分子中N原子处在3个H原子所组成的三角形的中心
3
B.CCl 分子中C原子处在4个Cl原子所组成的正方形的中心
4
C.H O分子中O原子处在2个H原子所组成的直线的中央
2D.CO 是非极性分子,分子中C原子处在2个O原子所连接的直线的中央
2
【答案】 D [NH 分子为三角锥形分子,N原子位于锥顶,A错误;CCl
3 4
分子为正四面体形分子,B错误;H O分子为V形结构,C错误;CO 分子为直
2 2
线形,C原子位于两个O原子连线的中央,D正确。]
四、杂化轨道理论简介
1.用杂化轨道理论解释甲烷分子的形成
在形成CH 分子时,碳原子的一个 2s 轨道和三个2p 轨道发生混杂,形成4
4
个能量相等的 sp 3 杂化轨道。4个 sp 3 杂化轨道分别与4个H原子的1s轨道重叠
形成4个C—Hσ 键,所以4个C—H键是等同的。
2.杂化轨道的形成及其特点
【注】①原子轨道的杂化只有在形成分子的过程中才会发生,孤立的原子
不可能发生杂化。
②只有能量相近的轨道才能发生杂化。
③杂化后原子轨道数目不变,且杂化轨道的能量相同。
④杂化后轨道的伸展发向、形状发生改变,使原子形成的共价键更牢
固。但相同杂化形式的杂化轨道形状完全相同。
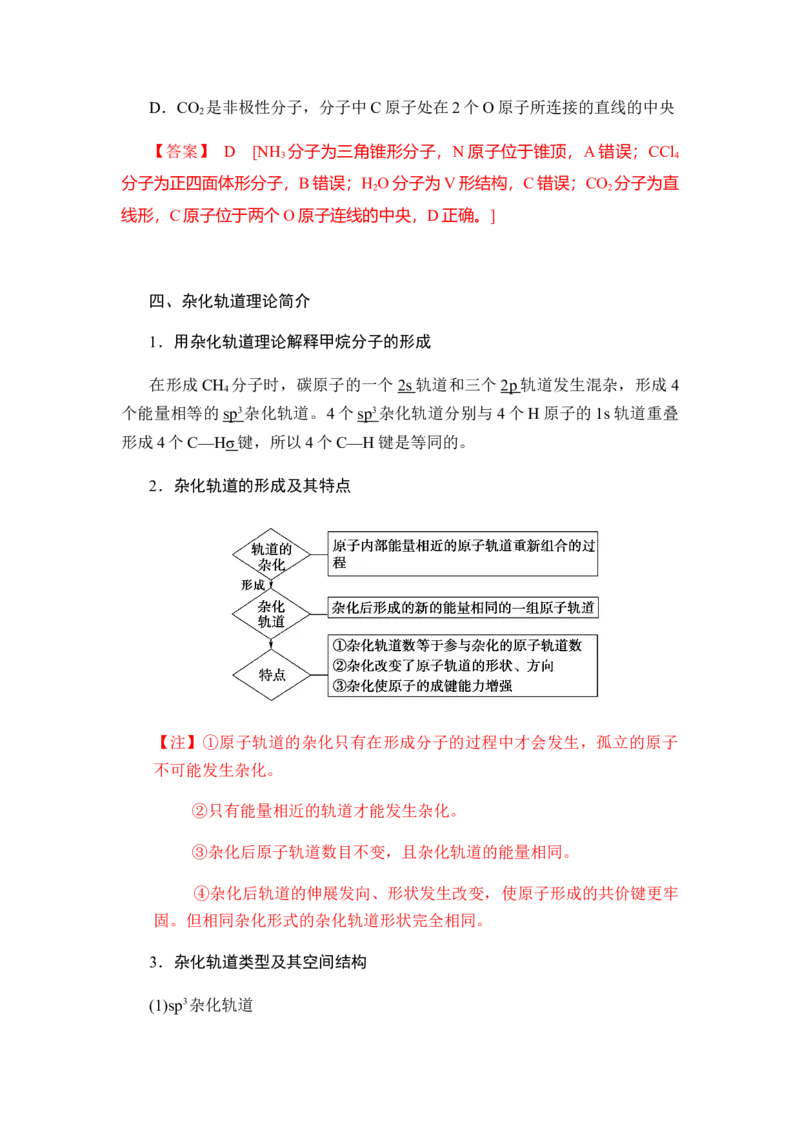
3.杂化轨道类型及其空间结构
(1)sp3杂化轨道sp3杂化轨道是由1 个s轨道和3 个p轨道杂化形成的。sp3杂化轨道间的夹
角是109°28′,空间结构为正四面体形(如下图所示)。
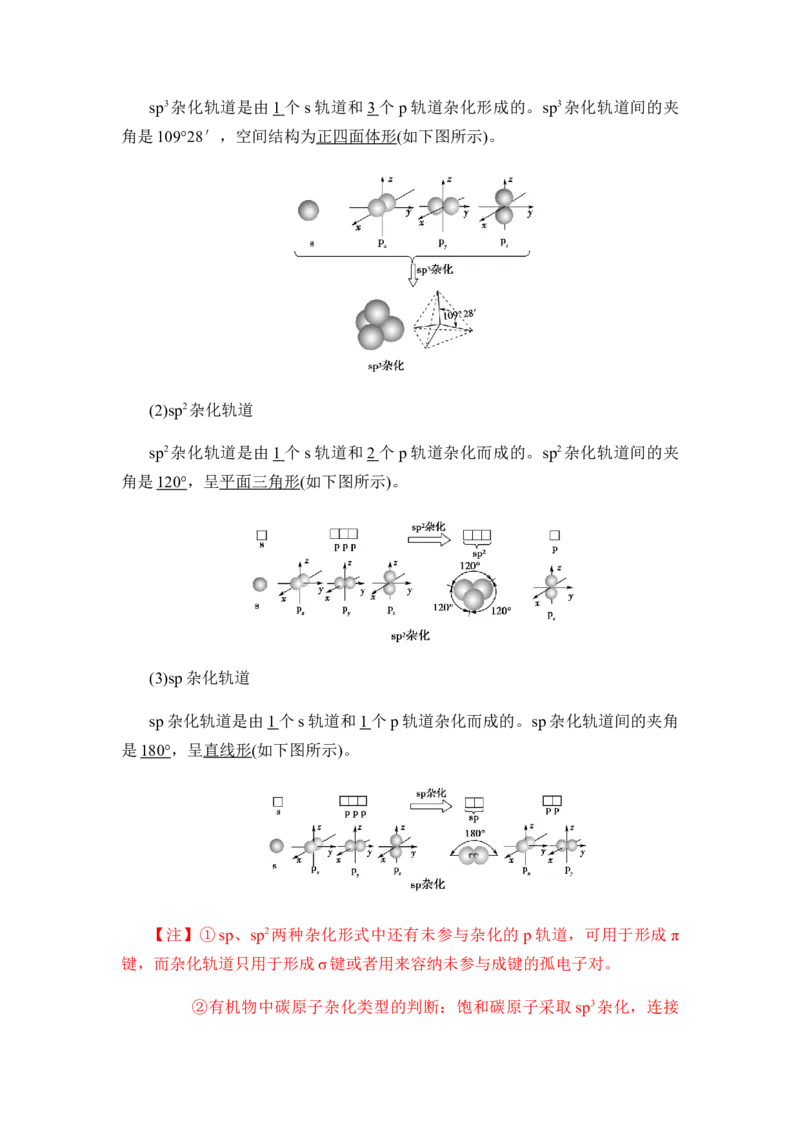
(2)sp2杂化轨道
sp2杂化轨道是由1 个s轨道和2 个p轨道杂化而成的。sp2杂化轨道间的夹
角是120°,呈平面三角形(如下图所示)。
(3)sp杂化轨道
sp杂化轨道是由1 个s轨道和1 个p轨道杂化而成的。sp杂化轨道间的夹角
是180°,呈直线形(如下图所示)。
【注】①sp、sp2两种杂化形式中还有未参与杂化的 p轨道,可用于形成 π
键,而杂化轨道只用于形成σ键或者用来容纳未参与成键的孤电子对。
②有机物中碳原子杂化类型的判断:饱和碳原子采取 sp3杂化,连接双键的碳原子采取sp2杂化,连接三键的碳原子采取sp杂化。
4.VSEPR模型与中心原子的杂化轨道类型
杂化轨道类型 VSEPR模型 典型分子 空间结构
sp CO 直线形
2
sp2 SO V形
2
sp3 H O V形
2
sp2 SO 平面三角形
3
sp3 NH 三角锥形
3
五、杂化轨道类型的判断方法
1. 根据杂化轨道数目判断
对于AB 型分子(或离子),中心原子A的价层电子对数为其杂化轨
m
道数。可先确定分子或离子的VSEPR模型,然后确定中心原子的杂化轨道类型。
如ClO -、ClO 的价层电子对数为4,则杂化轨道数均为4。
3 4-
2. 根据杂化轨道之间的夹角判断:
若杂化轨道之间的夹角为109°28′,则中心原子发生sp3杂化;
若杂化轨道之间的夹角为120°,则中心原子发生sp2杂化;
若杂化轨道之间的夹角为180°,则中心原子发生sp杂化。
3.根据共价键类型判断
没有形成π键,为sp3杂化:CH
4形成一个π键,为sp2杂化:CH ==CH
2 2
形成两个π键,为sp杂化:CH≡CH、O==C==O
4. 有机物中碳原子杂化类型的判断:
饱和碳原子采取sp3杂化,连接双键的碳原子采取sp2杂化,连接三键的碳
原子采取sp杂化。
5.取代法
(1)如(CH ) N可看作三个甲基取代了NH 分子中的三个氢原子而得,
3 3 3
所以其分子中氮原子采用采取sp3杂化。
(2)CH CH==CH 分子可以看作乙烯基取代了CH 分子中的一个氢原子
3 2 4
而得,则甲基中碳原子为sp3杂化,也可看作甲基取代了CH ==CH 分子中的一
2 2
个氢原子而得,故两个不饱和碳为sp2杂化。
例4.下列分子中中心原子的杂化方式和分子的空间结构均正确的是( )
A.C H :sp2、直线形 B.SO:sp3、三角锥形
2 2
C.H O+:sp3、V形 D.BF :sp2、平面三角形
3 3
【答案】D [乙炔的结构式为H—C≡C—H,每个碳原子价层电子对个数
是2且不含孤电子对,所以 C原子采用sp杂化,为直线形结构;SO中硫原子
的价层电子对数=4,孤电子对数为0,采取sp3杂化,为正四面体形;H O+中
3
氧原子的价层电子对数=3+1=4,所以中心原子原子轨道为sp3杂化,该离子
中含有一个孤电子对,所以其空间结构为三角锥形;BF 分子中硼原子价层电
3
子对数=3+0=3,杂化轨道数为3,孤电子对数为0,所以其空间结构为平面
三角形。]
例5.下列说法中正确的是( )
A.NCl 分子呈三角锥形,这是氮原子采取sp2杂化的结果
3
B.sp3杂化轨道是由任意的1个s轨道和3个p轨道混合形成的4个sp3杂化轨道
C.中心原子采取sp3杂化的分子,其空间结构可能是四面体形或三角锥形
或V形
D.AB 型的分子空间结构必为平面三角形
3
【答案】C [NCl 分子中心氮原子上的价层电子对数=σ键电子对数+孤电
3
子对数=3+=4,因此NCl 分子中氮原子以sp3杂化,选项A错误;sp3杂化轨
3
道是原子最外电子层上的s轨道和3个p轨道“混杂”起来,形成能量相等、成
分相同的4个轨道,选项B错误;一般中心原子采取sp3杂化的分子所得到的空
间结构为四面体形,如甲烷分子,但如果有杂化轨道被中心原子上的孤电子对
占据,则空间结构发生变化,如NH 、PCl 分子是三角锥形,选项D错误,选
3 3
项C正确。 ]