文档内容
2.3.2 物质的量浓度
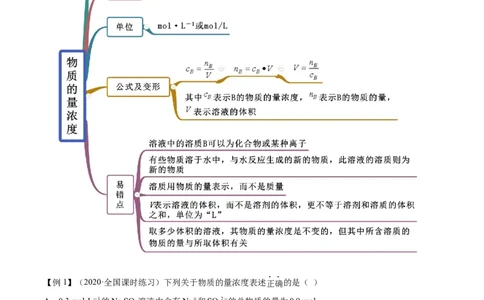
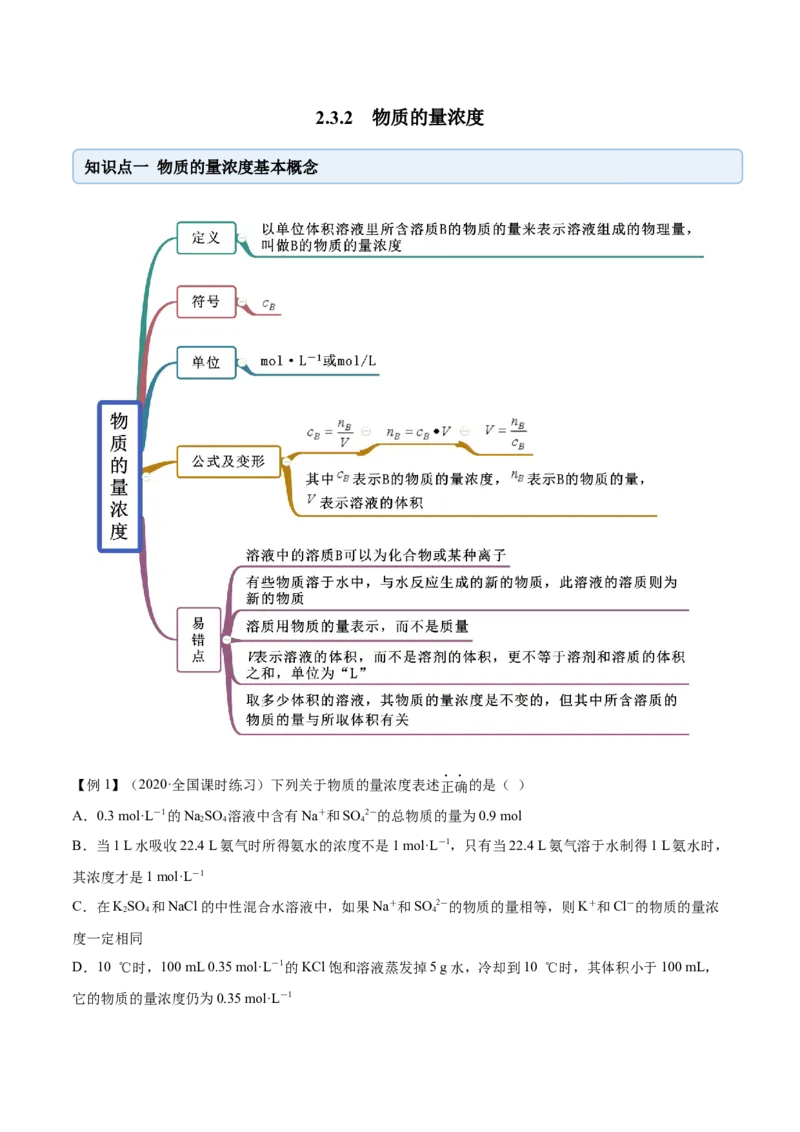
知识点一 物质的量浓度基本概念
【例1】(2020·全国课时练习)下列关于物质的量浓度表述正确的是( )
A.0.3 mol·L-1的NaSO 溶液中含有Na+和SO 2-的总物质的量为0.9 mol
2 4 4
B.当1 L水吸收22.4 L氨气时所得氨水的浓度不是1 mol·L-1,只有当22.4 L氨气溶于水制得1 L氨水时,
其浓度才是1 mol·L-1
C.在KSO 和NaCl的中性混合水溶液中,如果Na+和SO 2-的物质的量相等,则K+和Cl-的物质的量浓
2 4 4
度一定相同
D.10 ℃时,100 mL 0.35 mol·L-1的KCl饱和溶液蒸发掉5 g水,冷却到10 ℃时,其体积小于100 mL,
它的物质的量浓度仍为0.35 mol·L-1【一隅三反】
1.(2020·小店·山西大附中月考)下列溶液中物质的量浓度为1 mol/L的是( )
A.将40 g NaOH固体溶解于1 L水中 B.将22.4 L氯化氢气体溶于水配成1 L溶液
C.将1 L 10 mol/L的浓盐酸与9 L水混合 D.10 g NaOH固体溶解在水中配成250 mL溶液
2.(2020·全国课时练习)下列溶液中Cl﹣浓度由大到小的顺序是( )
①200mL 2mol/L MgCl 溶液②1000mL 2.5mol/L NaCl溶液
2
③300mL 5mol/L KCl溶液④250mL 1mol/L FeCl 溶液。
3
A.③①④② B.④①②③ C.③②①④ D.②③①④
3.(2020·全国课时练习)下列各溶液中n(Na+)与100 mL 0.1 mol/L Na SO 溶液中n(Na+)相同的是
2 4
( )
A.100 mL 0.1 mol/L NaCl 溶液 B.50 mL 0.2 mol/L NaNO 溶液
3
C.100 mL 0.1 mol/L NaHSO 溶液 D.200mL 0.2mol/L HCl溶液与100 mL 0.2 mol/L NaHCO 溶液混合
4 3
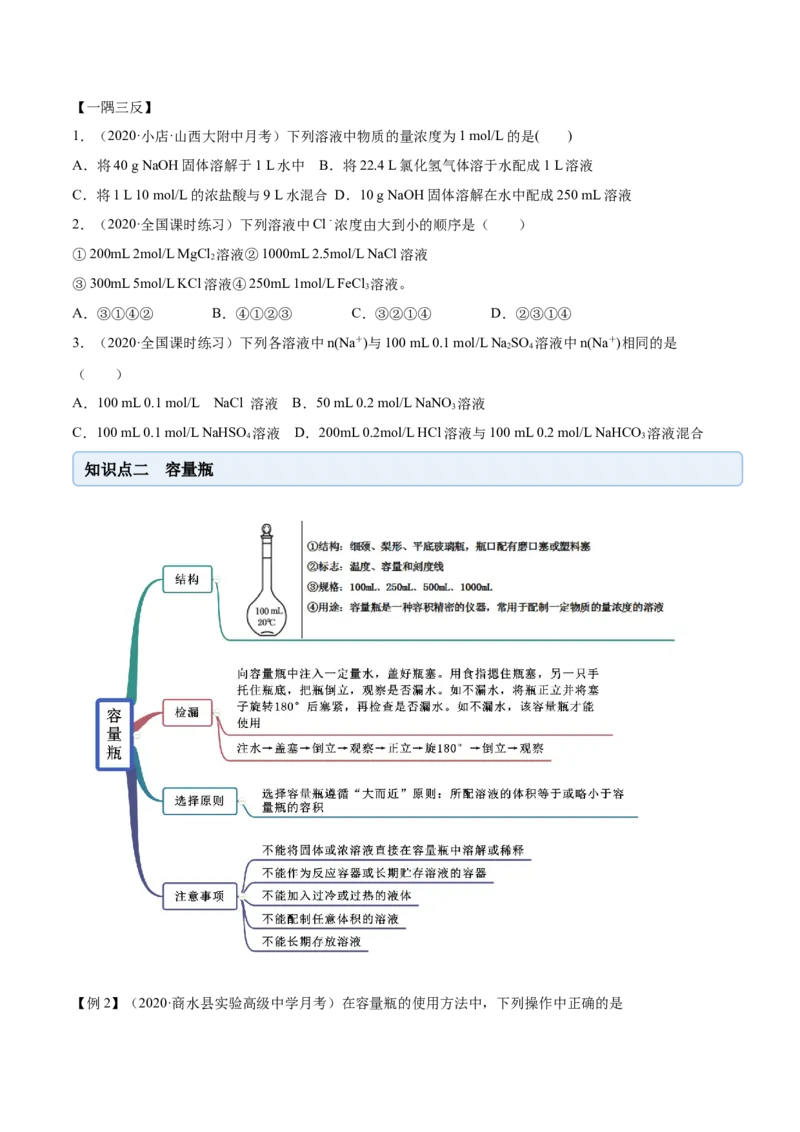
知识点二 容量瓶
【例2】(2020·商水县实验高级中学月考)在容量瓶的使用方法中,下列操作中正确的是A.容量瓶用蒸馏水洗净后,再用待配液润洗
B.使用容量瓶前检查它是否漏水
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近刻度
线2﹣3cm处,用滴管滴加蒸馏水到刻度线
D.配制溶液时,如果试样是液体,用量筒量取试样后直接到入容量瓶中,缓慢加入蒸馏水到接近刻度线2
﹣3cm处,用滴管加蒸馏水到刻度线
【一隅三反】
1.(2020·四川邻水实验学校月考)在容量瓶上没有标记的是( )
A.刻度线 B.温度
C.浓度 D.容量
2.(2020·西华县第一高级中学月考)下列实验中所选用的仪器合理的是
①用50 mL量筒量取5.2 mL稀硫酸
②用托盘天平称量11.70g氯化钠晶体
③配制一定物质的量浓度的溶液,定容时俯视刻度线会导致所配溶液浓度偏高
④用250 mL容量瓶配制250 mL 0.2 mol/L的NaOH溶液
A.①② B.②③
C.①③ D.③④
3.(2020·全国课时练习)实验室中需要 的 溶液450mL,配制时应选用的容量瓶的规
格和称取胆矾的质量分别是( )
A.500mL 25.0g B.450mL 22.5g
C.450mL 14.4g D.500mL 16.0g
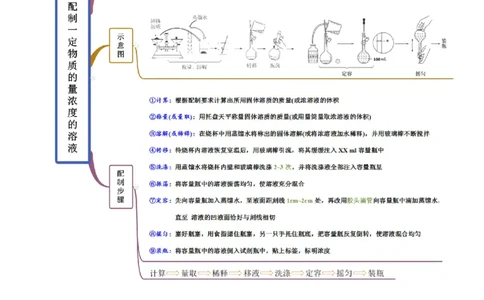
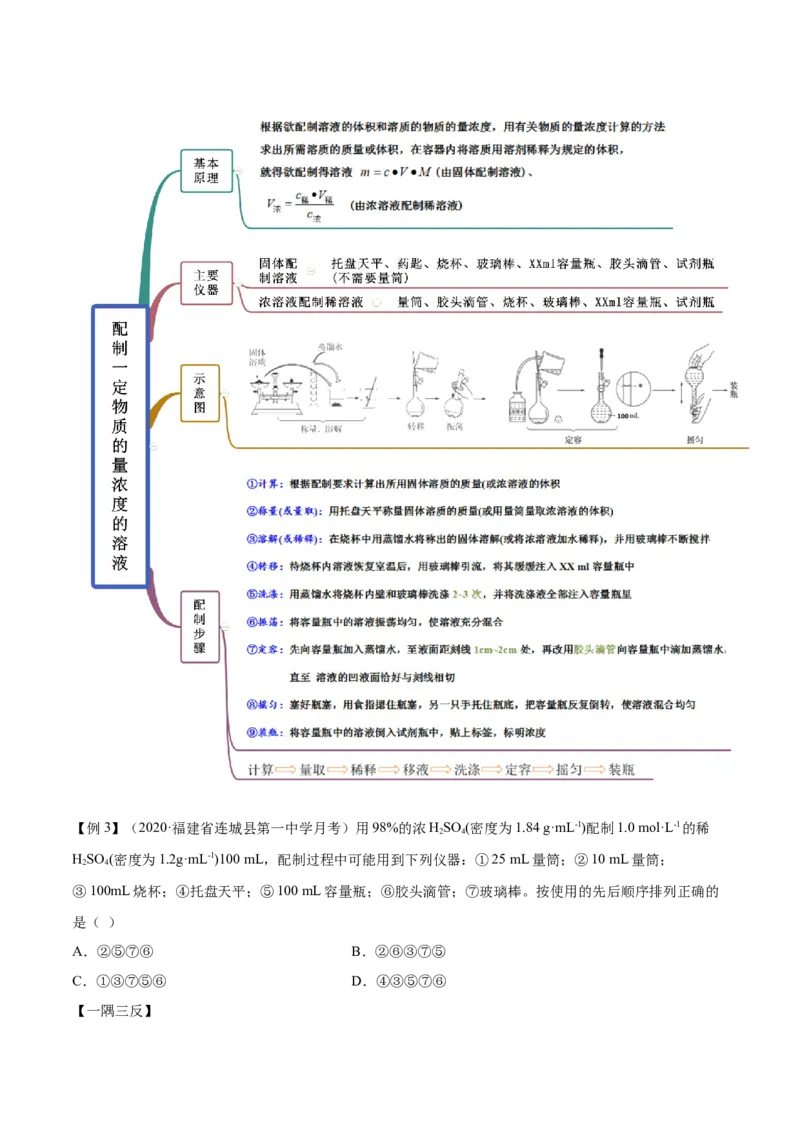
知识点三 配制一定物质的量浓度溶液的配制过程【例3】(2020·福建省连城县第一中学月考)用98%的浓HSO (密度为1.84 g·mL-1)配制1.0 mol·L-1的稀
2 4
HSO (密度为1.2g·mL-1)100 mL,配制过程中可能用到下列仪器:①25 mL量筒;②10 mL量筒;
2 4
③100mL烧杯;④托盘天平;⑤100 mL容量瓶;⑥胶头滴管;⑦玻璃棒。按使用的先后顺序排列正确的
是( )
A.②⑤⑦⑥ B.②⑥③⑦⑤
C.①③⑦⑤⑥ D.④③⑤⑦⑥
【一隅三反】1.(2020·西华县第一高级中学月考)配制100mL1.0mol/LNa CO 溶液,下列操作正确的是
2 3
A.称取10.6g无水碳酸钠,加入100mL容量瓶中,加水溶解、定容
B.称取10.6g无水碳酸钠,加入100mL蒸馏水,搅拌、溶解
C.转移NaCO 溶液时,未用玻璃棒引流,直接倒入容量瓶中
2 3
D.定容后,塞好瓶塞,反复倒转、摇匀
2.(2020·全国课时练习)下列有关溶液配制的说法正确的是( )
A.在50mL量筒中配制0.1000 mol/L NaCl溶液
B.配制一定物质的量浓度的溶液,定容时仰视刻度线
C.配制240 mL 0.1000 mol/ 溶液需用250mL容量瓶
D.定容时蒸馏水加多了,可用胶头滴管吸出多余的液体
3.(2020·全国课时练习)配制100 mL 1 mol/L的NaCl溶液时,下列做法不正确的是
A.选择容积100 mL的容量瓶
B.在容量瓶中溶解NaCl固体
C.转移NaCl溶液时用玻璃棒引流
D.定容时向容量瓶中滴加蒸馏水至液面与刻度线相切
知识点四 配制溶液的误差分析【例3】(2020·全国课时练习)实验室需要480 mL 1mol/L NaOH溶液,根据溶液配制情况回答下列问题:
(1)实验中除需要托盘天平(带砝码)、药匙、量筒、烧杯、玻璃棒、试剂瓶外,还需要的玻璃仪器有
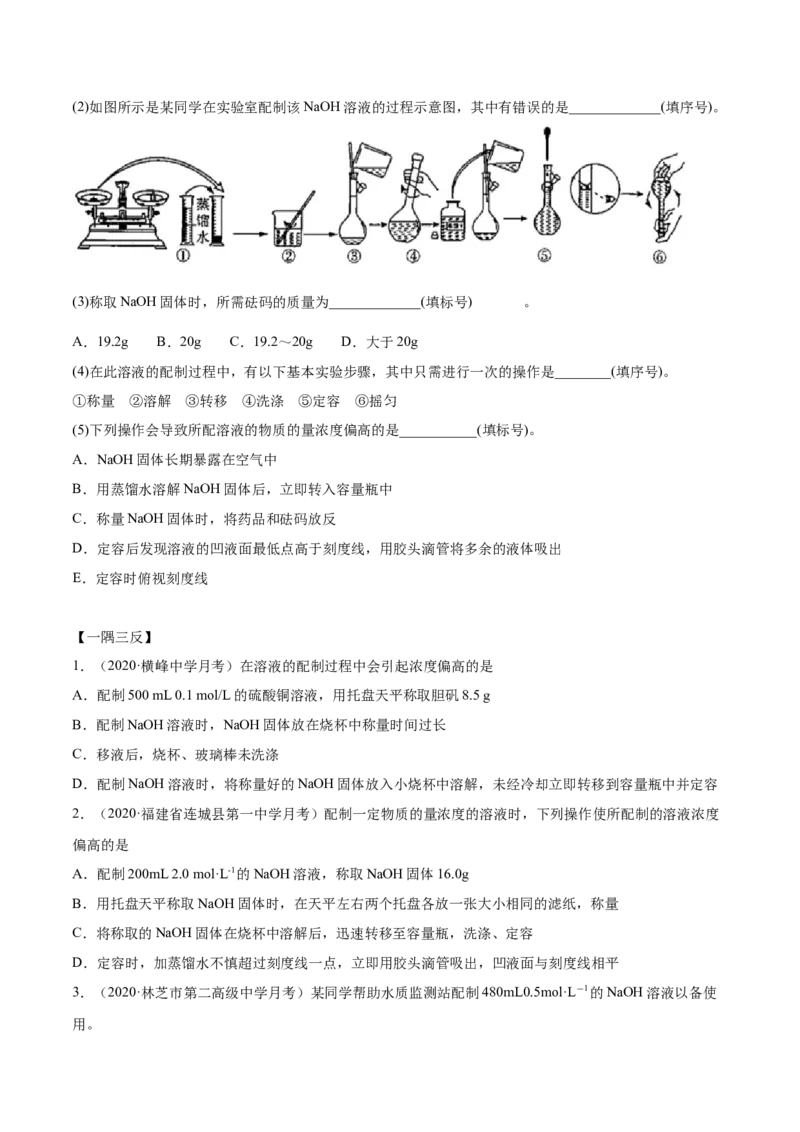
____________________。(2)如图所示是某同学在实验室配制该NaOH溶液的过程示意图,其中有错误的是_____________(填序号)。
(3)称取NaOH固体时,所需砝码的质量为_____________(填标号) 。
A.19.2g B.20g C.19.2~20g D.大于20g
(4)在此溶液的配制过程中,有以下基本实验步骤,其中只需进行一次的操作是________(填序号)。
①称量 ②溶解 ③转移 ④洗涤 ⑤定容 ⑥摇匀
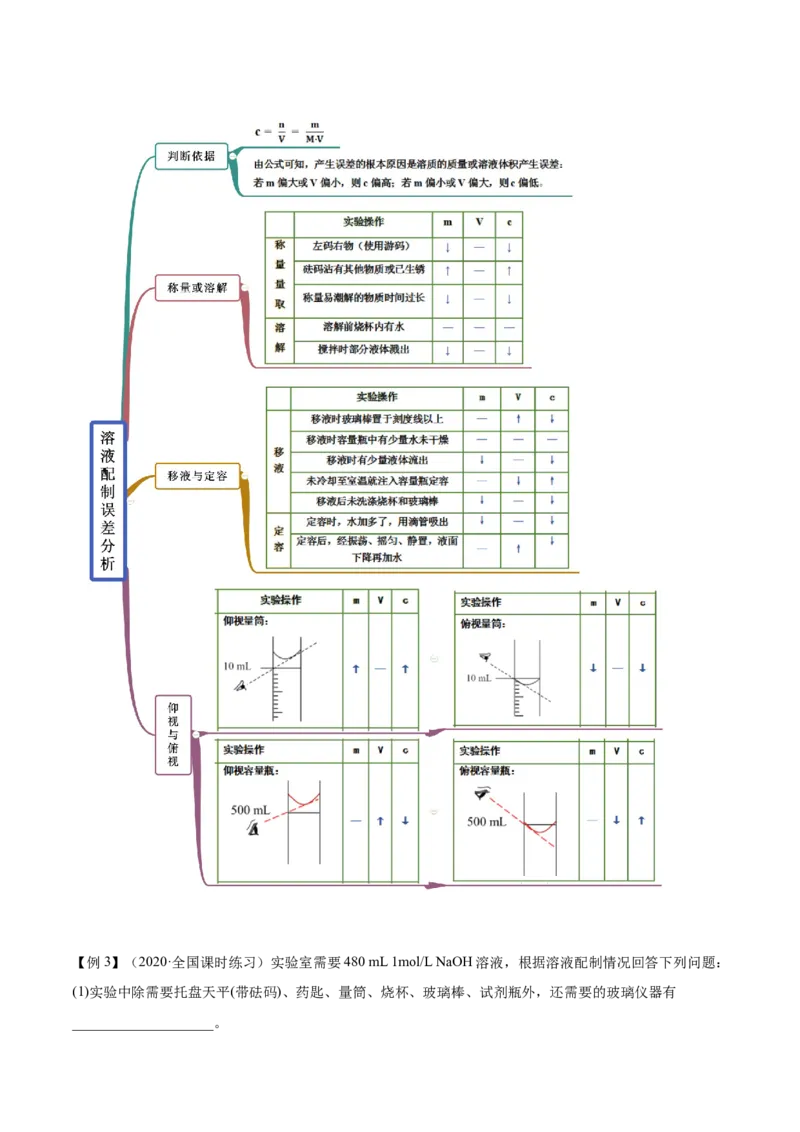
(5)下列操作会导致所配溶液的物质的量浓度偏高的是___________(填标号)。
A.NaOH固体长期暴露在空气中
B.用蒸馏水溶解NaOH固体后,立即转入容量瓶中
C.称量NaOH固体时,将药品和砝码放反
D.定容后发现溶液的凹液面最低点高于刻度线,用胶头滴管将多余的液体吸出
E.定容时俯视刻度线
【一隅三反】
1.(2020·横峰中学月考)在溶液的配制过程中会引起浓度偏高的是
A.配制500 mL 0.1 mol/L的硫酸铜溶液,用托盘天平称取胆矾8.5 g
B.配制NaOH溶液时,NaOH固体放在烧杯中称量时间过长
C.移液后,烧杯、玻璃棒未洗涤
D.配制NaOH溶液时,将称量好的NaOH固体放入小烧杯中溶解,未经冷却立即转移到容量瓶中并定容
2.(2020·福建省连城县第一中学月考)配制一定物质的量浓度的溶液时,下列操作使所配制的溶液浓度
偏高的是
A.配制200mL 2.0 mol·L-1的NaOH溶液,称取NaOH固体16.0g
B.用托盘天平称取NaOH固体时,在天平左右两个托盘各放一张大小相同的滤纸,称量
C.将称取的NaOH固体在烧杯中溶解后,迅速转移至容量瓶,洗涤、定容
D.定容时,加蒸馏水不慎超过刻度线一点,立即用胶头滴管吸出,凹液面与刻度线相平
3.(2020·林芝市第二高级中学月考)某同学帮助水质监测站配制480mL0.5mol·L-1的NaOH溶液以备使
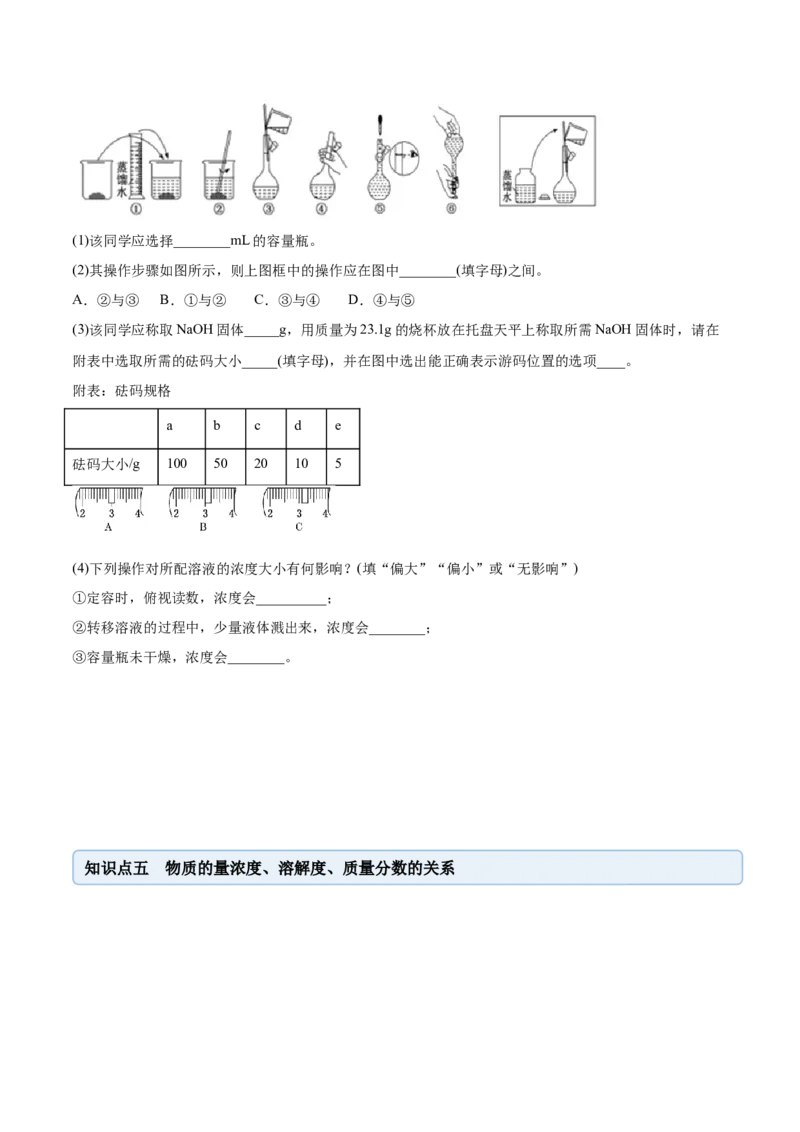
用。(1)该同学应选择________mL的容量瓶。
(2)其操作步骤如图所示,则上图框中的操作应在图中________(填字母)之间。
A.②与③ B.①与② C.③与④ D.④与⑤
(3)该同学应称取NaOH固体_____g,用质量为23.1g的烧杯放在托盘天平上称取所需NaOH固体时,请在
附表中选取所需的砝码大小_____(填字母),并在图中选出能正确表示游码位置的选项____。
附表:砝码规格
a b c d e
砝码大小/g 100 50 20 10 5
(4)下列操作对所配溶液的浓度大小有何影响?(填“偏大”“偏小”或“无影响”)
①定容时,俯视读数,浓度会__________;
②转移溶液的过程中,少量液体溅出来,浓度会________;
③容量瓶未干燥,浓度会________。
知识点五 物质的量浓度、溶解度、质量分数的关系【例5】(2019·东北育才学校月考)下列有关溶质的质量分数和物质的量浓度的计算结果错误的是( )
A.有KSO 和Al (SO ) 的混合溶液,已如其中Al3+的物质的量浓度为0.4mol/L, SO 的物质的量浓
2 4 2 4 3
度为0.7mol/L,则此溶液中K+的物质的量浓度为0.2mol/L
B.将5mol/L的Mg(NO ) 溶液a mL稀释至b mL,稀释后溶液中NO 的物质的量浓变为 mol/L
3 2
C.将标准状况下,将VLA气体(摩尔质量为Mg/mol)溶于0.1L水中,所得溶液密度为ρg/cm3,则此溶
液的物质的量浓度为. mol/LD.密度为0.91g/cm3的氨水,质量分数为25%。该氨水用等体积的水稀释后,所得溶液中溶质的质量分数
等于12.5%
利用好公式:c=n/V,ρ=m/V,ω=m(溶质)/m(溶液),注意溶液体积单位的变化,否则计算结果相差1000倍。
【一隅三反】
1.(2020·江西上高二中月考)将标准状况下,将VLA气体(摩尔质量为Mg/mol)溶于0.1L水中,所得溶液
密度为ρg/cm3,则此溶液的物质的量浓度(mol/L)为( )
A. B.
C. D.
2.(2020·全国课时练习)从500mL1.0mol·L-1NaCl溶液中取出100mL溶液的叙述正确的是( )
A.物质的量的浓度为1.0mol·L-1
B.溶液中含有1molNaCl
C.溶液中含有29.25gNaCl
D.物质的量的浓度为0.2mol·L-1
3.(2019·江西丰城九中期中)某结晶水合物的化学式为R·nHO,其相对分子质量为M。25 ℃时,a g该
2
晶体能够溶于b g水中形成
V mL溶液,下列关系中不正确的是
A.该溶液中溶质的质量分数为w= %
B.该溶液的物质的量浓度为c= mol·L-1
C.该溶液中溶剂与溶质的质量比为m(水)∶m(溶质)=( +b)∶(a- )
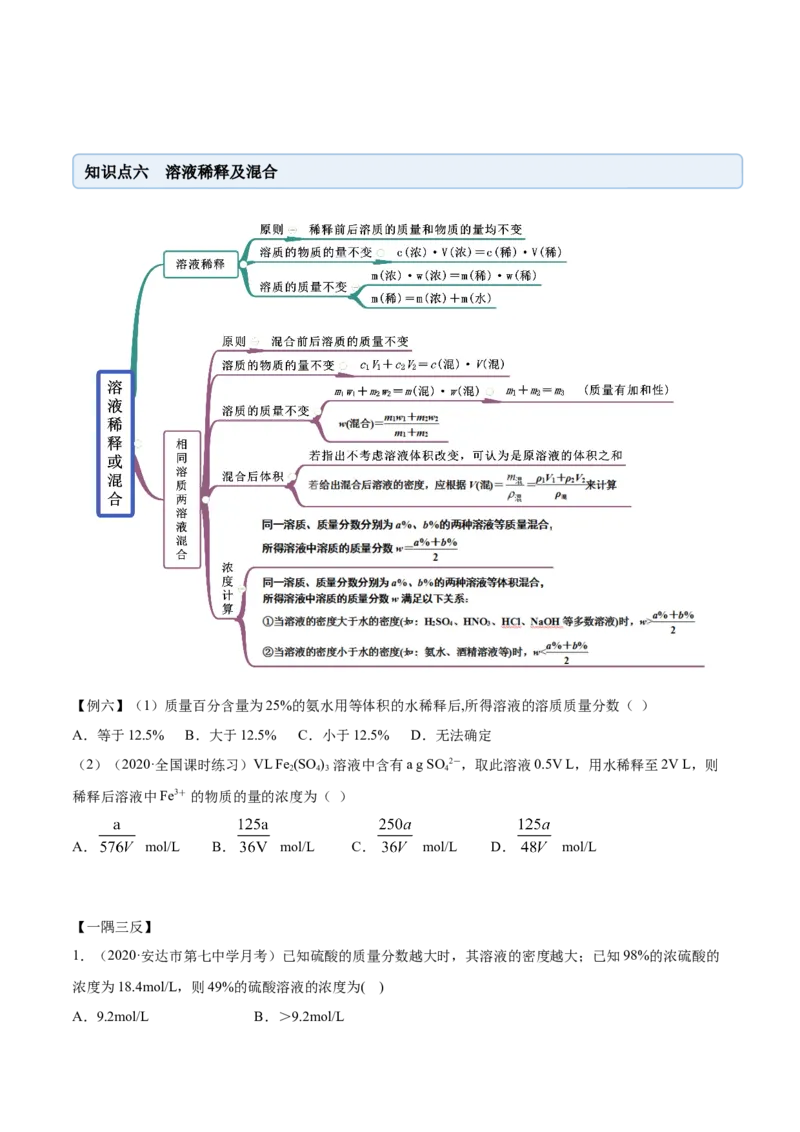
D.该溶液的密度为ρ= g·L-1知识点六 溶液稀释及混合
【例六】(1)质量百分含量为25%的氨水用等体积的水稀释后,所得溶液的溶质质量分数( )
A.等于12.5% B.大于12.5% C.小于12.5% D.无法确定
(2)(2020·全国课时练习)VL Fe (SO ) 溶液中含有a g SO2-,取此溶液0.5V L,用水稀释至2V L,则
2 4 3 4
稀释后溶液中Fe3+ 的物质的量的浓度为( )
A. mol/L B. mol/L C. mol/L D. mol/L
【一隅三反】
1.(2020·安达市第七中学月考)已知硫酸的质量分数越大时,其溶液的密度越大;已知98%的浓硫酸的
浓度为18.4mol/L,则49%的硫酸溶液的浓度为( )
A.9.2mol/L B.>9.2mol/LC.<9.2 mol/L D.无法确定
2.(2020·全国课时练习)两种硫酸溶液,一种硫酸溶液的物质的量浓度为 ,密度为 ;另一种硫酸溶液的
物质的量浓度为c,密度为 ,将它们等体积混合后,所得溶液的密度为 ,则混合后硫酸的物质的量浓度为(
2
)
A. B. C. D.
3.(2020·全国高一课时练习)把5%的碳酸钠溶液蒸发掉64.3 g水后,溶液变为31 mL,浓度变为14%,
没有晶体析出,则浓缩后碳酸钠溶液的物质的量浓度为( )
A.8.52 mol·L-1 B.4.26 mol·L-1
C.1.52 mol·L-1 D.3.04 mol·L-1
4.(2020·小店·山西大附中月考)体积为VmL,密度为ρg/mL的含有相对分子质量为M的某物质的溶液,
其中溶质为mg,其物质的量浓度为cmol/L,溶质的质量分数为ω,则下列表达式错误的是( )
A.c= B.m=V×ρ×ω
C.ω= % D.c=