文档内容
第一节 铁及其化合物
第2课时 铁的氧化物、氢氧化物单质
基础巩固
1.(2022·全国·高一)火星被称为“红色的星球”,这是因为它的岩石和土壤中含有丰富的
A.FeO B.Fe O C.Fe O D.Fe
3 4 2 3
【答案】C
【解析】A.氧化亚铁为黑色,与火星被称为“红色的星球”无关,A错误;
B.四氧化三铁为黑色,与火星被称为“红色的星球”无关,B错误;
C.Fe O 是一种红棕色粉末,俗称“铁红”,是赤铁矿的主要成分,所以火星岩石和土壤中含有丰富的
2 3
Fe O ,C正确;
2 3
D.铁单质为银白色,与火星被称为“红色的星球”无关,D错误;
故答案选C。
2.许多富脂糕点的包装盒内都装有一小包黑色的活性铁粉,长时间放置的糕点,其包装盒内的活性铁粉
往往会变成红棕色。下列说法正确的是
A.富脂食品长时间放置易被还原
B.红棕色固体的主要成分是
C.活性铁粉变成红棕色的过程中铁粉发生了氧化反应
D.如果在包装盒内放入氧化钙,也可起到与铁粉同样的作用
【答案】C
【解析】A.富脂食品长时间放置容易被空气中的氧气氧化,A错误;
B.铁粉在空气中被氧化成氧化铁,B错误;
C.铁粉变成氧化铁发生了氧化反应,C正确;
D.氧化钙是干燥剂,不具有还原性,与铁粉作用不同同,D错误;
故选C。
3.(2021·全国·高一课时练习)下列说法正确的是
A.赤铁矿的主要成分是Fe O
3 4
B.Fe O 为碱性氧化物,可与水反应生成Fe(OH)
2 3 3
C.铁锈的主要成分是Fe O·xHO
2 3 2
D.Fe O 中铁元素有+2价和+3价,故Fe O 是混合物
3 4 3 4
【答案】C
【解析】A.赤铁矿的主要成分是Fe O,故A错误;
2 3
B.Fe O 为碱性氧化物,不能与水反应,但可以与酸反应生成盐和水,故B错误;
2 3
C.铁锈的主要成分是Fe O·xHO,故C正确;
2 3 2
D.Fe O 中铁元素有+2价和+3价,但是Fe O 是化合物不是混合物,故D错误;
3 4 3 4
故答案为C。
学科网(北京)股份有限公司4.(2021·全国·高一课时练习)铁有+2价和+3价两种价态,下列有关反应中不涉及铁元素价态变化的是
A.铁与稀硫酸反应
B.铁在氧气中燃烧,其产物溶于盐酸中可得到两种盐
C.氢氧化亚铁是白色固体,在空气中迅速变成灰绿色,最终变成红褐色
D.氢氧化铁受热分解
【答案】D
【解析】A.Fe与稀硫酸反应生成FeSO 和H,铁元素的化合价由0价升至+2价;涉及铁元素价态变化,
4 2
A不符合题意。
B.Fe在氧气中燃烧生成Fe O,铁元素的化合价发生变化;B不符合题意。
3 4
C.白色氢氧化亚铁固体在空气中迅速变成灰绿色,最终变成红褐色,发生反应:
4Fe(OH) +O +2H O=4Fe(OH) ,铁元素的化合价由+2价升至+3价;C不符合题意。
2 2 2 3
D.氢氧化铁受热分解生成Fe O 和水,反应前后铁元素的化合价均为+3价;不涉及铁元素价态变化,D符
2 3
合题意。
故选D。
5.(2022·上海·高一专题练习)如图是CO还原Fe O 的实验装置图,下列说法中错误的是
2 3
A.a装置中现象是管中黑色固体变为红棕色
B.CO有毒应加尾气处理装置
C.b装置中澄清石灰水变浑浊
D.此反应可体现CO的还原性
【答案】A
【解析】CO与Fe O 在高温下反应产生CO 、Fe,反应方程式为3CO+Fe O 3CO +2Fe,然后根据物质
2 3 2 2 3 2
的性质及反应现象分析、判断。
A.CO还原Fe O ,生成Fe和CO ,Fe O 是红棕色固体,单质铁是灰黑色的,因此反应后看到硬质玻璃管
2 3 2 2 3
中固体由红棕色固体变为灰黑色,A错误;
B.CO是有毒气体,应加尾气处理装置,以防止大气污染,B正确;
C.该反应产生了CO ,CO 与Ca(OH) 反应产生难溶于水的CaCO ,而使装置b中的澄清石灰水变浑浊,C
2 2 2 3
正确;
D.在该反应中C元素化合价由反应前CO中的+2价变为反应后CO 中的+4价,化合价升高,失去电子被
2
氧化,因此CO作还原剂,表现还原性,D正确;
故合理选项是A。
学科网(北京)股份有限公司6.下列离子方程式中,正确的是
A.铁钉放入硫酸铜溶液中:Fe + SO = FeSO
4
B.氧化铁和稀硫酸反应:Fe O + 6H+ = 2Fe2+ + 3H O
2 3 2
C.向Ba(OH) 溶液中滴加H SO 溶液至恰好为中性:Ba2+ + OH-+ H+ + SO = BaSO ↓+H O
2 2 4 4 2
D.氢氧化铁与盐酸反应:Fe (OH) + 3H+ = Fe3+ + 3H O
3 2
【答案】D
【解析】A.发生置换反应生成Cu单质,离子反应为 ,A项错误;
B.电荷不守恒,离子反应为Fe O + 6H+ = 2Fe3+ + 3H O,B项错误;
2 3 2
C.当溶液显中性时,Ba(OH) 溶液中的OH-恰好反应完全,离子反应为Ba2+ +2OH-+2H++ =
2
BaSO ↓+2H O,C项错误;
4 2
D.该反应符合离子反应的书写规则,D项正确
7.如图所示装置,可用以制取和观察 在空气中被氧化时颜色的变化。下列说法错误的是
A.实验前,应事先煮沸溶液除去溶解氧
B.装置Ⅰ可制取 溶液并排尽装置内空气
C.关闭止水夹可观察到装置Ⅱ中溶液进入装置Ⅰ中
D.取下装置Ⅱ的橡皮塞可观察沉淀颜色变化
【答案】C
【解析】
氢氧化钠溶液中有少量氧气,需要加热煮沸除去氧气;打开止水夹,铁屑和稀硫酸反应生成硫酸亚铁和
氢气,利用反应产生的氢气排装置内的空气,然后关闭止水夹,试管Ⅰ形成密闭体系,利用反应产生的氢
气的压强作用,把硫酸亚铁溶液压入到装置Ⅱ中,产生氢氧化亚铁白色沉淀,氢氧化亚铁遇到空气后,变
为灰绿色,最后变为红褐色。
A.氢氧化钠溶液中有少量氧气,氢氧化亚铁易被氧气氧化,所以实验前,应事先煮沸溶液除去溶解氧,
故A正确;
B.结合以上分析可知,装置Ⅰ可制取 溶液并排尽装置内空气,故B正确;
C.结合以上分析可知,关闭止水夹可观察到装置Ⅰ中溶液进入装置Ⅱ中,故C错误;
D.结合以上分析可知,氢氧化亚铁具有强还原性,能够被氧气氧化,颜色发生变化,所以取下装置Ⅱ的
橡皮塞可观察沉淀颜色变化,故D正确;
故选C。
8.下列说法正确的是
学科网(北京)股份有限公司A.Fe O 与HCl反应生成FeCl 、FeCl ,所以Fe O 是碱性氧化物
3 4 2 3 3 4
B.Na O 与盐酸反应生成盐和水,所以Na O 是碱性氧化物
2 2 2 2
C.FeO、Fe O 与硫酸反应只生成盐和水,所以都是碱性氧化物
2 3
D.NaHSO 在水中能电离出氢离子溶液显酸性,所以NaHSO 是酸
4 4
【答案】C
【解析】
A.Fe O 与HCl反应生成FeCl 、FeCl 和水,生成两种盐,所以Fe O 不是碱性氧化物,A错误;
3 4 2 3 3 4
B.Na O 与盐酸反应生成盐和水、O ,所以Na O 不是碱性氧化物,B错误;
2 2 2 2 2
C.FeO、Fe O 与硫酸反应生成盐和水,所以都是碱性氧化物,C正确;
2 3
D.NaHSO 能电离出H+,同时产生金属阳离子Na+及酸根离子 ,所以NaHSO 是盐,D错误;
4 4
选C。
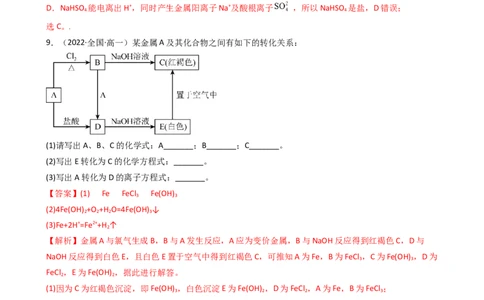
9.(2022·全国·高一)某金属A及其化合物之间有如下的转化关系:
(1)请写出A、B、C的化学式:A_______;B_______;C_______。
(2)写出E转化为C的化学方程式:_______。
(3)写出A转化为D的离子方程式:_______。
【答案】(1) Fe FeCl Fe(OH)
3 3
(2)4Fe(OH) +O +H O=4Fe(OH) ↓
2 2 2 3
(3)Fe+2H+=Fe2++H ↑
2
【解析】金属A与氯气生成B,B与A发生反应,A应为变价金属,B与NaOH反应得到红褐色C,D与
NaOH反应得到白色E,且白色E置于空气中得到红褐色C,可推知A为Fe,B为FeCl ,C为Fe(OH) ,D为
3 3
FeCl ,E为Fe(OH) ,据此进行解答。
2 2
(1)因为C为红褐色沉淀,即Fe(OH) ,白色沉淀E为Fe(OH) ,D为FeCl ,A为Fe,B为FeCl ;
3 2 2 3
(2)Fe(OH) 被空气中的氧气氧化成Fe(OH) ,反应的化学方程式为4Fe(OH) +O +H O 4Fe(OH) ↓;
2 3 2 2 2 3
(3)铁和盐酸反应生成FeCl 和H ,反应的离子方程式为Fe+2H+=Fe2++H ↑。
2 2 2
10.(2021·湖北·南漳县第二中学高一月考)Fe O 又称铁红,请根据要求完成下列问题。
2 3
(1)Fe O 固体(红棕色)属于___________(填“纯净物”或“混合物”)。将其加入适量盐酸中,反应的离子化
2 3
学方程式:___________。
(2)用上述所得溶液进行下列实验:取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀
产生,反应的离子化学方程式:___________。
(3)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向烧杯中加入几滴FeCl 饱和溶液,继续煮沸至出现
3
___________色,即可制得Fe(OH) 胶体。
3
学科网(北京)股份有限公司(4)另取一小烧杯也加入20 mL蒸馏水,向烧杯中加入1 mL FeCl 溶液,振荡摇匀后,将此烧杯(编号甲)
3
与盛有Fe(OH) 胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到
3
___________烧杯的液体中产生了丁达尔效应。
【答案】
(1) 纯净物 Fe O +6H+=2Fe3++3H O
2 3 2
(2)Fe3++3OH-=Fe(OH) ↓
3
(3)红褐
(4)乙
【解析】(1)Fe O 固体(红棕色)中只含有一种物质,属于纯净物,将其加入适量盐酸中的反应方程式为:
2 3
Fe O +6HCl=2FeCl +3H O,该反应的离子化学方程式为:Fe O +6H+=2Fe3++3H O,故答案为:纯净物;
2 3 3 2 2 3 2
Fe O +6H+=2Fe3++3H O;
2 3 2
(2)取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀产生,即FeCl 与NaOH反应生成
3
Fe(OH) 沉淀,该反应的离子化学方程式:Fe3++3OH-=Fe(OH) ↓,故答案为:Fe3++3OH-=Fe(OH) ↓;
3 3 3
(3)由课本中制备Fe(OH) 胶体的方法可知,在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向烧杯中加
3
入几滴FeCl 饱和溶液,继续煮沸至出现红褐色,即可制得Fe(OH) 胶体,故答案为:红褐;
3 3
(4)胶体能够产生丁达尔效应,而溶液不能,故另取一小烧杯也加入20 mL蒸馏水,向烧杯中加入1 mL
FeCl 溶液,振荡摇匀后,将此烧杯(编号甲)与盛有Fe(OH) 胶体的烧杯(编号乙)一起放置于暗处,分别用激
3 3
光笔照射烧杯中的液体,可以看到乙烧杯的液体中产生了丁达尔效应,故答案为:乙。
能力提升
11.(2022·全国·高一)元素的“价-类”二维图是我们学习元素及其化合物相关知识的重要模型和工具,
它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图。下图为铁元素的“价-
类”二维图,其中的箭头表示部分物质间的转化关系,下列说法正确的是
A.铁与高温水蒸气的反应可实现上述转化①
B.加热Fe(OH) 发生转化⑥,Fe O 加水溶解可转化为Fe(OH)
3 2 3 3
C.由图可预测:高铁酸盐(FeO )具有强氧化性,可用于饮用水的消毒
D.FeO是一种黑色粉末,只能用作还原剂
【答案】C
【解析】A.铁与高温水蒸气反应生成四氧化三铁和氢气,不能实现上述转化①,故A错误;
学科网(北京)股份有限公司B.加热Fe(OH) 发生转化⑥分解生成氧化铁,Fe O 不溶于水,加水不溶解,不可实现转化③,故B错误;
3 2 3
C.高铁酸盐(FeO )具有强氧化性,与水反应生成Fe(OH) 胶体,其中Fe元素化合价由+6价变为+3价,
3
则O元素化合价由-2价变为0价,即有氧气生成,可用于消毒,则反应的离子方程式为4FeO
+10H O=4Fe(OH) (胶体)+3O ↑+8OH-,生成的氢氧化铁胶体具有较大表面积,吸附悬浮杂质可以作净水剂,
2 3 2
故C正确;
D.FeO是一种黑色粉末,其中Fe元素显+2价既可作氧化剂又可作还原剂,故D错误;
故答案为C
12.(2022·江苏南通·高一期中)一种以铁粉、硫酸亚铁溶液为原料制取氧化铁黑的原理如图所示。下列
说法正确的是
A.转化I、Ⅱ均为置换反应
B.图中转化仅涉及Fe、O元素的化合价发生变化
C.转化Ⅱ反应的离子方程式为6Fe2++6H O+O =2Fe O +12H+
2 2 3 4
D.转化Ⅱ中所需O 可由通入过量的空气来实现
2
【答案】C
【解析】
A.转化I为置换反应,而反应Ⅱ中某一单质生成,不是置换反应,A错误;
B.I中氢元素化合价降低,B错误;
C.根据转化关系图可判断转化Ⅱ反应的离子方程式为6Fe2++6H O+O =2Fe O +12H+,C正确;
2 2 3 4
D.转化Ⅱ中若通入过量的空气,则氧气将会继续氧化四氧化三铁中的亚铁,属于不能通入过量的空气,
D错误;
答案选C。
13.用CO还原2.40g氧化铁,当固体质量变成2.28g时,测得此固体中只存在2种氧化物。则此固体成分
和它们的物质的量之比可能的是
A.n(FeO):n(Fe O )=1∶1 B.n(Fe O ):n(FeO)=2∶1
3 4 2 3
C.n(Fe O ):n(FeO)=1∶1 D.n(Fe O ):n(Fe O )=1∶1
2 3 2 3 3 4
【答案】A
【解析】
固体减少的质量为CO获得的氧原子的质量,根据固体质量差,可知减少氧原子的质量为
2.40g-2.28g=0.12g,则减少氧原子的物质的量为 ,氧化铁的物质的量为
,则反应后氧化物中的O的物质的量为
,反应中Fe原子的物质的量不变,则反应后氧化物中Fe、O
学科网(北京)股份有限公司原子数目之比为: ,据此分析解答。
A.当n(FeO):n(Fe O )=1∶1时,Fe、O原子数目之比为: ,故选A;
3 4
B.当n(Fe O ):n(FeO)=2∶1时,Fe、O原子数目之比为: ,故B不选;
2 3
C.当n(Fe O ):n(FeO)=1∶1时,Fe、O原子数目之比为: ,故C不选;
2 3
D.当n(Fe O ):n(Fe O )=1∶1时,Fe、O原子数目之比为: ,故D不选。
2 3 3 4
答案选A。
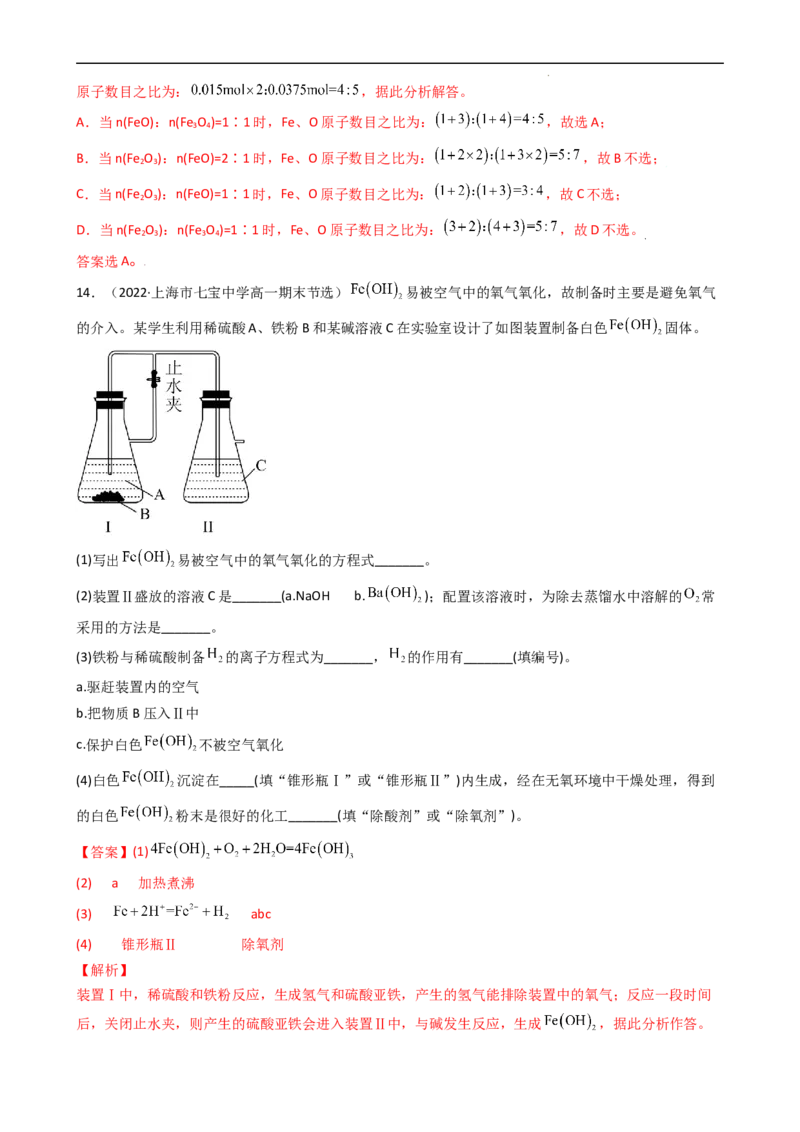
14.(2022·上海市七宝中学高一期末节选) 易被空气中的氧气氧化,故制备时主要是避免氧气
的介入。某学生利用稀硫酸A、铁粉B和某碱溶液C在实验室设计了如图装置制备白色 固体。
(1)写出 易被空气中的氧气氧化的方程式_______。
(2)装置Ⅱ盛放的溶液C是_______(a.NaOH b. );配置该溶液时,为除去蒸馏水中溶解的 常
采用的方法是_______。
(3)铁粉与稀硫酸制备 的离子方程式为_______, 的作用有_______(填编号)。
a.驱赶装置内的空气
b.把物质B压入Ⅱ中
c.保护白色 不被空气氧化
(4)白色 沉淀在_____(填“锥形瓶Ⅰ”或“锥形瓶Ⅱ”)内生成,经在无氧环境中干燥处理,得到
的白色 粉末是很好的化工_______(填“除酸剂”或“除氧剂”)。
【答案】(1)
(2) a 加热煮沸
(3) abc
(4) 锥形瓶Ⅱ 除氧剂
【解析】
装置Ⅰ中,稀硫酸和铁粉反应,生成氢气和硫酸亚铁,产生的氢气能排除装置中的氧气;反应一段时间
后,关闭止水夹,则产生的硫酸亚铁会进入装置Ⅱ中,与碱发生反应,生成 ,据此分析作答。
学科网(北京)股份有限公司(1) 易被空气中的氧气氧化,生成氢氧化铁,化学方程式为: ,
故答案为: ;
(2)硫酸亚铁会进入装置Ⅱ中,与碱发生反应,生成 ,可知该碱为NaOH;配置该溶液时,为除去
蒸馏水中溶解的 常采用的方法是加热煮沸,故答案为:a;加热煮沸;
(3)稀硫酸和铁粉反应,生成氢气和硫酸亚铁,离子方程式为 ;产生的氢气能驱赶装置
内的空气、关闭止水夹,能把物质B压入Ⅱ中、同时防止空气进入装置Ⅱ,保护白色 不被空气
氧化,故答案为: ;abc;
(4)由分析可知,白色 沉淀在锥形瓶Ⅱ内生成; 易被空气中的氧气氧化,经在无氧环境
中干燥处理,得到的白色 粉末是很好的化工除氧剂,故答案为:锥形瓶Ⅱ;除氧剂。
学科网(北京)股份有限公司学科网(北京)股份有限公司