文档内容
3.2 金属材料
【题组一 合金、铁合金、铝合金】
1.(2019·江西丰城九中期中)中国传统文化对人类文明贡献巨大。下列古代文献涉及的化学研究成果,对
其说明不合理的是( )
A.《抱朴子·黄白》中“曾青涂铁,铁赤色如铜”主要发生了置换反应
B.《本草纲目》中“用浓酒和糟入甑,蒸令气上,用器承滴露”,利用到蒸馏
C.《天工开物•五金》中记载:“若造熟铁,则生铁流出时,相连数尺内……众人柳棍疾搅,即时炒成熟
铁。”炒铁是为了降低铁水中的碳含量,且熟铁比生铁质地更硬,延展性稍差
D.《梦溪笔谈》中“以剂钢为刃,柔铁为茎干,不尔则多断折”中的剂钢是指铁的合金
2.(2020·全国高一课时练习)铁和不锈钢(铁合金)都是生活中常见的材料,下列说法中不正确的是(
)
A.铁和不锈钢都能与盐酸反应 B.铁是纯净物,不锈钢是混合物
C.铁和不锈钢都只含有金属元素 D.不锈钢比铁更耐腐蚀
3.(2020·运城市景胜中学高一开学考试)铁是一种应用广泛的金属。下列有关铁的叙述正确的是
A.铁是地壳中含量最多的金属 B.铁丝在氧气中燃烧生成氧化铁
C.用铁可以回收硝酸银废液中的银 D.炼铁就是把铁矿石变成纯净的氧化铁
4.(2020·福建省福州格致中学期末)我国高铁列车的车厢大部分采用铝合金材料,其原因是铝合金( )
A.化学性质活泼
B.比纯铝熔点高,耐高温
C.质量轻、强度大、有较好的抗腐蚀能力
D.在自然界的含量丰富,容易获得
5.(2020·全国课时练习)下列说法不正确的是
A.铝合金的硬度和强度均比铝单质的大
B.铝制器皿可长期盛放酸梅汤和碱水等
C.铝合金可用于制造汽车车轮的骨架等
D.硬铝是含有Al、Cu、Mg、Si、Mn等元素的铝合金
6.(2020·全国课时练习)下列说法错误的是
A.铝合金大量用于高铁建设
B.“玉兔二号”钛合金筛网轮的主要成分是非金属材料
C.制饭勺、饭盒,高压锅等的不锈钢是合金
D.商代后期铸造出工艺精湛的后(司)母戊鼎,该鼎属于铜合金制品
7.(2020·全国)下列有关金属及其合金的说法不正确的是( )
A.目前我国流通的硬币是由合金材料制成的
B.镁在空气中燃烧发出耀眼的白光,可用于制作照明弹
C.日用铝制品表面覆盖着氧化膜,对内部金属起保护作用
D.生铁、普通钢和不锈钢中的碳含量依次增加
8.(2020·全国高一课时练习)日常生活中常用铝制炊具,它质轻且坚固耐用,其原因是
A.铝制品表面涂有一层油,可以保护铝不受腐蚀
B.铝很不活泼,不易与其他物质反应C.铝制品表面有一层致密的氧化物薄膜,起保护作用
D.铝虽然很活泼,但只有在高温下才能反应
9.(2020·全国高一课时练习)镁铝合金质优体轻,又不易锈蚀,大量用于航空工业、造船工业、日用化
工等领域。下列关于镁铝合金性质的叙述中,不正确的是
A.此合金的熔点比镁和铝的熔点都低
B.此合金能全部溶解于足量稀盐酸中
C.此合金能全部溶解于足量氢氧化钠溶液中
D.此合金的硬度比镁和铝的硬度都大
10.(2020·长春市第二十九中学高一期末)铝制品具有较强的抗腐蚀性,主要是因为( )
A.铝的化学性质稳定
B.铝在常温时与氧气不反应
C.铝具有金属性,也具有非金属性
D.铝与氧气反应生成一层致密的氧化物薄膜
【题组二 铝及化合物】
1.(2020·全国课时练习)下列关于金属铝及氧化铝的说法不正确的是( )
A.铝是地壳中含量最多的元素
B.铝在自然界中通常以化合态形式存在
C.金属铝在空气中有良好的抗腐蚀性
D .氧化铝是一种高硬度﹑高熔沸点的化合物,红宝石、蓝宝石的主要成分均是氧化铝
2.(2020·临颍县南街高级中学月考)铝箔在空气中加热,金属熔化而不滴落的原因是( )
A.熔化的金属铝非常黏稠 B.铝的密度小,所受重力也小
C.大部分铝已经被氧化 D.氧化膜的熔点比铝高,兜住了熔化的铝
3.(2020·浙江高三月考)下列有关铝的说法正确的是( )
A.铝制品表面虽然有致密的氧化膜,但若遇到酸、碱及氯化钠溶液均会发生反应而被腐蚀
B.利用铝热反应可以焊接钢轨,也可以用于冶炼各种活泼金属
C.铝元素在人体中积累可使人慢性中毒,因此要严禁明使矾用于食物膨化剂中
D.将一块铝投入到硫酸铜溶液中, 一段时间内无明显现象, 说明铝不能与硫酸铜溶液反应
4.(2020·深圳市龙岗区科城实验学校高一月考)下列关于铝的叙述中,不正确的是( )
A.铝是地壳里含量最多的金属元素 B.铝是一种比较活泼的金属
C.在常温下,铝不能与氧气反应 D.在化学反应中,铝易失去电子,是还原剂
5.(2020·全国课时练习)下列关于铝及其化合物说法,不正确的是
A.明矾可用作净水剂和消毒剂 B. 熔点高,可用作耐高温材料
C.铝可用作包装材料和建筑材料 D.氢氧化铝可用作治疗胃酸过多的药物
6.(2020·北京师范大学珠海分校附属外国语学校高一期末)铝在空气中能够稳定存在的原因是
A.铝的活泼性差 B.铝的还原性差
C.铝与氧气不反应 D.铝表面有氧化膜
7.(2020·四川郫都·)利用金属活动性的不同,可以采取不同的方法冶炼金属,其中上述过程中的②就可
以用铝热法炼铁,下图中所示装置为铝热反应的实验装置,请回答下列问题:(1)该实验中还缺____;所缺实验用品的作用是____;引发铝热反应的操作为_____。
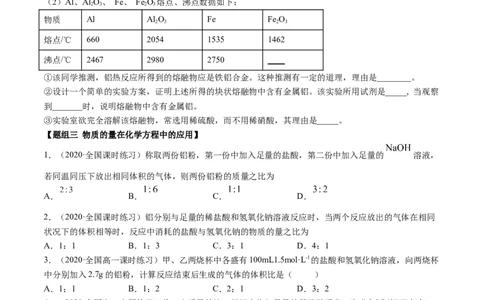
(2)Al、Al O、 Fe、 Fe O 熔点、沸点数据如下:
2 3 2 3
物质 Al Al O Fe Fe O
2 3 2 3
熔点/℃ 660 2054 1535 1462
沸点/℃ 2467 2980 2750 ____
①该同学推测,铝热反应所得到的熔融物应是铁铝合金。这种推测有一定的道理,理由是________。
②设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是_____, 当观察
到_______时,说明熔融物中含有金属铝。
③实验室欲完全溶解该熔融物,常选用稀硫酸,而不用稀硝酸,其理由是_____。
【题组三 物质的量在化学方程中的应用】
1.(2020·全国课时练习)称取两份铝粉,第一份中加入足量的盐酸,第二份中加入足量的 溶液,
若同温同压下放出相同体积的气体,则两份铝粉的质量之比为
A. B. C. D.
2.(2020·全国课时练习)铝分别与足量的稀盐酸和氢氧化钠溶液反应时,当两个反应放出的气体在相同
状况下的体积相等时,反应中消耗的盐酸与氢氧化钠的物质的量之比为
A.1:1 B.1:3 C.3:1 D.4:1
3.(2020·全国高一课时练习)甲、乙两烧杯中各盛有100mL1.5mol·L-1的盐酸和氢氧化钠溶液,向两烧杯
中分别加入2.7g的铝粉,计算反应结束后生成的气体的体积比是( )
A.1:1 B.1:2 C.2:1 D.3:2
4.(2020·全国高一专题练习)将一定质量的锌、铝混合物与足量的稀硫酸反应,生成2.8 L(标况)氢气,
原混合物的质量可能是( )
A.2 g B.1 g C.8 g D.10 g
5.(2020·全国高一课时练习)分别向盛有等物质的量浓度的稀硫酸和氢氧化钠溶液的烧杯中加入足量的
铝,反应后放出的气体体积在标准状况下为1︰2,则所取稀硫酸和氢氧化钠溶液的体积比为
A.1︰2 B.3︰4 C.3︰2 D.6︰1
6.(2020·福建省福州格致中学期末)设N 为阿伏加德罗常数,下列有关说法正确的是( )
A
A.100mL12mol/L浓盐酸与足量的MnO 加热充分反应生成Cl 分子数为0.3N
2 2 A
B.5.4g铝粉与足量的氢氧化钠溶液充分反应生成H 分子数为0.3N
2 AC.向FeI 溶液中通入适量Cl,当有1 mol Fe2+被氧化时,转移的电子的数目为N
2 2 A
D.18gHO在标准状况下所占体积约为22.4L
2
7.(2019·全国高一课时练习)将四份相同的铝镁合金粉末分别放入下列四种过量的溶液中充分反应,放
出氢气最多的是( )
A.2mol•L-1HSO 溶液 B.18mol•L-1HSO 溶液
2 4 2 4
C.6mol•L-1NaOH溶液 D.3mol•L-1BaCl 溶液
2
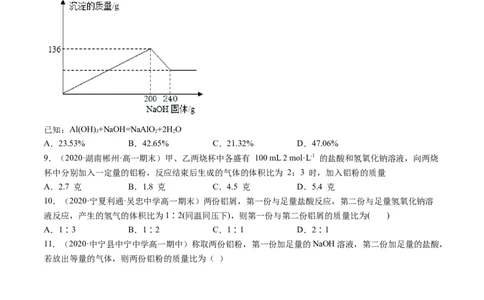
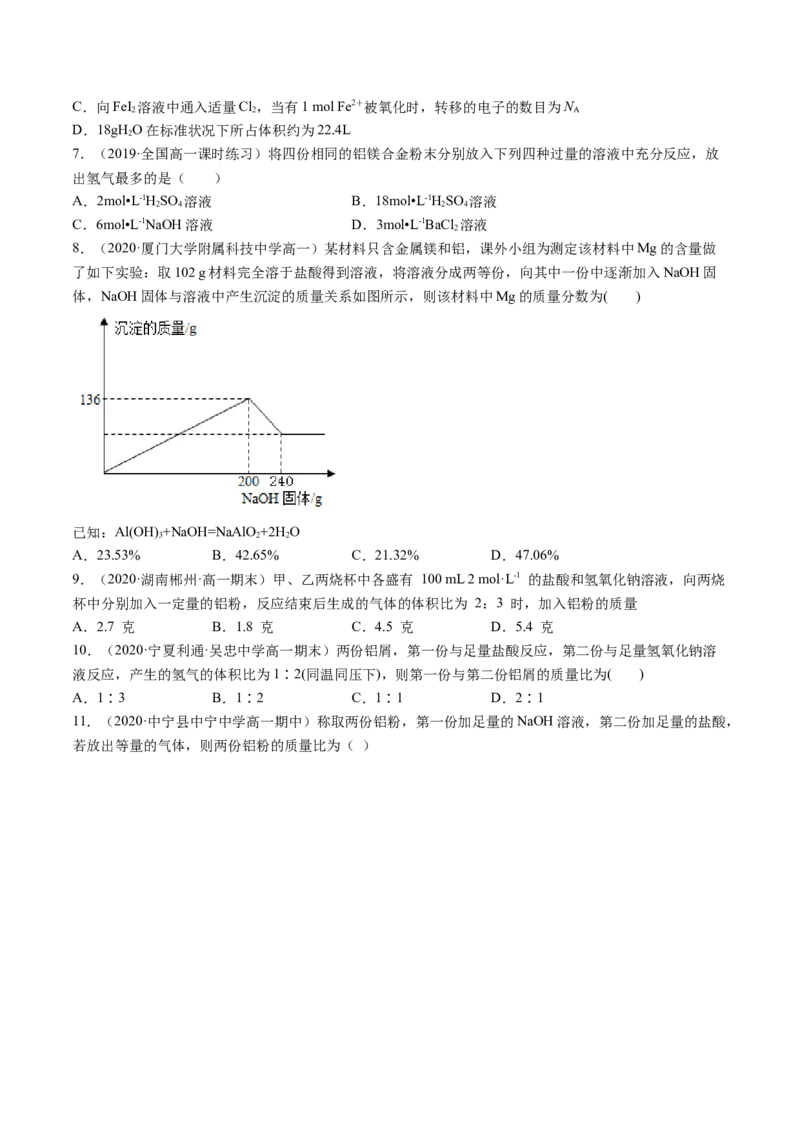
8.(2020·厦门大学附属科技中学高一)某材料只含金属镁和铝,课外小组为测定该材料中Mg的含量做
了如下实验:取102 g材料完全溶于盐酸得到溶液,将溶液分成两等份,向其中一份中逐渐加入NaOH固
体,NaOH固体与溶液中产生沉淀的质量关系如图所示,则该材料中Mg的质量分数为( )
已知:Al(OH) +NaOH=NaAlO +2H O
3 2 2
A.23.53% B.42.65% C.21.32% D.47.06%
9.(2020·湖南郴州·高一期末)甲、乙两烧杯中各盛有 100 mL 2 mol·L-1 的盐酸和氢氧化钠溶液,向两烧
杯中分别加入一定量的铝粉,反应结束后生成的气体的体积比为 2:3 时,加入铝粉的质量
A.2.7 克 B.1.8 克 C.4.5 克 D.5.4 克
10.(2020·宁夏利通·吴忠中学高一期末)两份铝屑,第一份与足量盐酸反应,第二份与足量氢氧化钠溶
液反应,产生的氢气的体积比为1∶2(同温同压下),则第一份与第二份铝屑的质量比为( )
A.1∶3 B.1∶2 C.1∶1 D.2∶1
11.(2020·中宁县中宁中学高一期中)称取两份铝粉,第一份加足量的NaOH溶液,第二份加足量的盐酸,
若放出等量的气体,则两份铝粉的质量比为( )